PTC颈部中央区淋巴结转移与超声征象的相关性分析
2020-12-29刘灵川陈斌朱张茜徐琦
刘灵川 陈斌 朱张茜 徐琦
近年来,甲状腺癌发病率逐年上升,增加的病例几乎为甲状腺乳头状癌(PTC)[1]。发病原因包括性别、辐射暴露史、家族史等,由于病理学的发展对PTC分类的理解[2],以及高分辨超声和FNA的精确诊断[3]。虽然PTC恶性程度相对较低,但也可侵犯甲状腺包膜及周围组织,易发生颈部中央区淋巴结转移(CLNM)甚至远处转移[4]。PTC颈部淋巴结转移影响患者的手术方式和预后,以及患者的10年生存率[5]。术前彩色多普勒超声检查可以了解淋巴结转移位置、大小及区域,具有较高的应用价值,但该检查方式特异性及敏感性较低[6]。因此,在术前通过PTC的超声影像预测其颈部中央区淋巴结转移,对患者的治疗方案与预后具有重要意义。本文探讨PTC颈部中央区淋巴结转移的危险因素,及其与超声影像的相关性。
1 资料与方法
1.1 临床资料 选取本院2014年1月至2018年6月195例PTC患者资料。所有病例均具有完整超声影像图(灰阶图、大小三径测量图、彩色多普勒血流图),常规行颈部VI区淋巴结清扫,经术后病理证实为单发PTC。其中男57例,女138例,男女比例1∶2.4;年龄21~77岁,平均年龄(47.06±11.39)岁。其中颈部中央区淋巴结转移患者58例(男19例,女39例),纳入淋巴结转移组,无颈部中央区淋巴结转移的患者137例(男38例,女99例),纳入淋巴结无转移组。排除标准:(1)合并其他部位肿瘤伴发转移的患者;(2)存在头颈部放射治疗史的患者;(3)合并其他内分泌系统及代谢性疾病的患者;(4)信息不完全的患者;(5)多灶性PTC的患者;(6)曾有甲状腺手术史的患者。
1.2 方法 根据超声影像图,以甲状腺TI-RDAS 分级白皮书[7]为参考标准,依次记录病灶部位,边界(不清/清晰)、边缘(成角/光整)、形态(垂直位/水平位)、是否突向甲状腺包膜、内部回声(极低/低/中/高)、内部是否存在钙化(微钙化/粗钙化)、病灶后方回声是否存在衰减,病灶左右径、上下径、前后径,其中PTC病灶与甲状腺包膜的距离≤1mm或突出甲状腺包膜轮廓外;病灶处甲状腺包膜回声连续并向腺体外突出;病灶处甲状腺包膜回声中断并被病灶侵占;视为甲状腺乳头状突向甲状腺包膜。见图1。
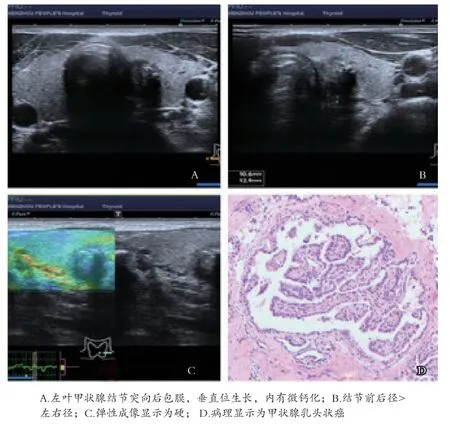
图1 PTC超声影像及病理显示
1.3 统计学方法 采用SPSS 23.0 统计软件。计数资料两组间比较采用χ2检验,计量资料两组间比较采用t检验。多因素分析采用Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 影响PTC颈部中央区淋巴结转移的单因素分析 单因素分析显示PTC突向包膜、病灶形态、病灶内部存在微钙化、病灶的左右径、上下径、前后径是PTC颈部中央区淋巴结转移的危险因素,差异均有统计学意义(P<0.05)。见表1。
表1 颈部中央区淋巴结转移的单因素分析(±s)
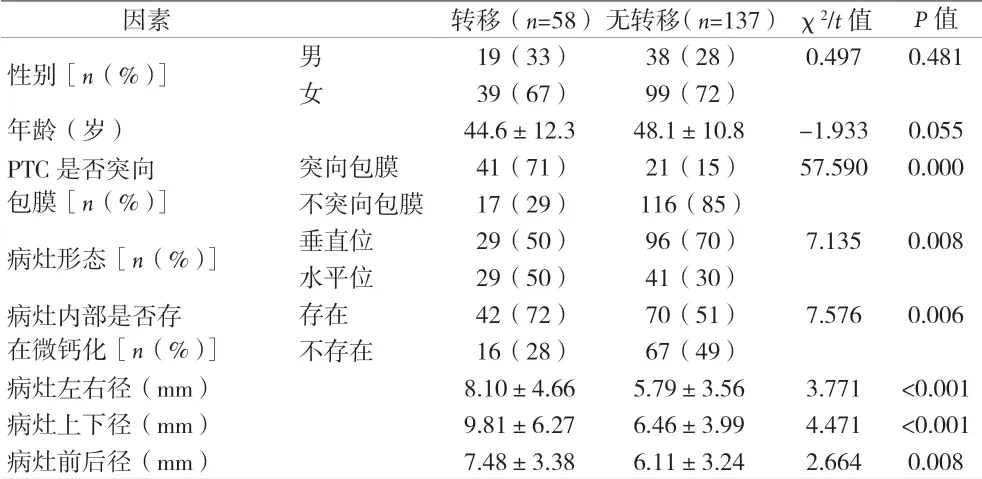
表1 颈部中央区淋巴结转移的单因素分析(±s)
因素 转移(n=58)无转移(n=137)χ2/t值 P值性别[n(%)] 男 19(33) 38(28) 0.497 0.481女39(67) 99(72)年龄(岁) 44.6±12.3 48.1±10.8 -1.933 0.055 PTC是否突向包膜[n(%)]突向包膜 41(71) 21(15) 57.590 0.000不突向包膜 17(29) 116(85)病灶形态[n(%)] 垂直位 29(50) 96(70) 7.135 0.008水平位 29(50) 41(30)病灶内部是否存在微钙化[n(%)]存在 42(72) 70(51) 7.576 0.006不存在 16(28) 67(49)病灶左右径(mm) 8.10±4.66 5.79±3.56 3.771 <0.001病灶上下径(mm) 9.81±6.27 6.46±3.99 4.471 <0.001病灶前后径(mm) 7.48±3.38 6.11±3.24 2.664 0.008
2.2 影响PTC颈部中央区淋巴结转移多因素分析 将单因素分析差异有统计学意义的因素纳入二元Logistic回归分析,结果显示PTC突向甲状腺包膜是PTC颈部中央区淋巴结转移的独立危险因素(P<0.001),而病灶形态、病灶内部存在微钙化、病灶的左右径、上下径、前后径与颈部中央区淋巴结转移均无相关关(P>0.05),见表2。
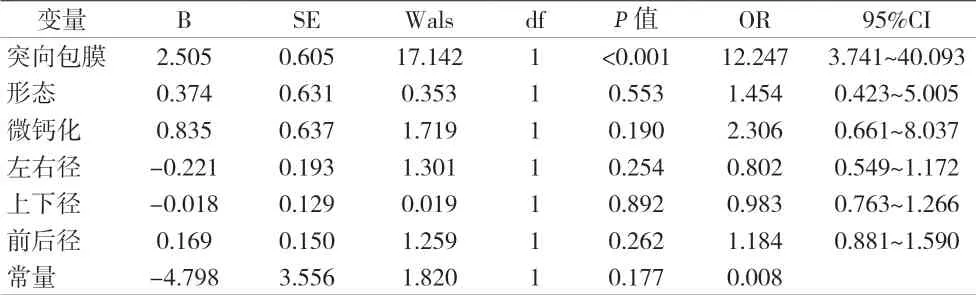
表2 颈部中央区淋巴结转移的多因素分析
3 讨论
PTC是最常见的甲状腺癌之一,近10年来发病率不断上升[8]。而PTC的10年生存率>90%,其中颈部淋巴结转移率50%~80%,而颈部淋巴结中又以中央区转移为多[9]。颈部淋巴结是否转移关系患者手术方式以及预后。因此,通过术前超声检查所获得PTC的超声影象,预测其颈部中央区淋巴结转移,具有重要意义,可以为临床治疗方案以及手术方式的选择,提供可靠的参考依据。
研究表明,PTC中,多发病灶与颈侧区淋巴结转移有关,而单发病灶与中央区淋巴结在转移有关[10]。因此,本研究选取病例均为单发灶的PTC。研究表明,年龄与性别均为PTC颈部中央区淋巴结转移的危险因素[11]。本资料结果显示,年龄与性别的P值接近临界值(0.055、0.481),考虑为样本量不足。
恶性肿瘤的生长依靠肿瘤内的新生血管生成,生长速度越快,癌灶增长幅度越大,增长越迅速,颈部淋巴结转移的发生几率也会随之增加[12]。本资料中,转移组病灶的左右径、上下径、前后径均大于与无转移组,表明病灶的大小可以影响其颈部中央区淋巴结转移,是PTC颈部中央区淋巴结转移的危险因素。本资料显示,PTC呈垂直位生长,病灶内部有微钙化,为颈部中央区淋巴结转移的危险因素,而非独立危险因素,与较多文献报道相符合[13],如将更多甲状腺癌病理类型纳入研究,则上述危险因素可与恶性相关[14]。
PTC由于其恶性的生物学特点,浸润性生长是其基本的生长方式,癌灶的生长会引起癌灶周围甲状腺组织、被膜及被膜周围软组织的侵犯,从而引起淋巴结转移。本资料将PTC病灶与包膜的距离≤1mm或突出于甲状腺包膜轮廓外;病灶处甲状腺包膜回声连续并向腺体外突出;病灶处甲状腺包膜回声中断并被病灶侵占;视为甲状腺乳头状突向甲状腺包膜。多因素分析显示PTC病灶突向甲状腺包膜为颈部中央区淋巴结转移独立危险因素,与多数文献符合[15-16]。
综上所述,PTC的超声征象可以用来预测颈部中央区淋巴结转移,能为临床手术方式的选择提供一定影像学依据。
