帕米膦酸二钠治疗累及股骨近端多发性纤维结构不良的 24 例报告
2014-02-14徐明许宋锋于秀淳
徐明 许宋锋 于秀淳
帕米膦酸二钠治疗累及股骨近端多发性纤维结构不良的 24 例报告
徐明 许宋锋 于秀淳
目的探讨帕米膦酸二钠对不同程度病情的累及股骨近端多发性纤维结构不良的治疗方法及临床疗效。方法2009 年 6 月至 2012 年 1 月,我院收治的累及股骨近端的多发性纤维结构不良者 24 例,其中男 14 例,女 10 例,年龄 8~61( 平均 24 )岁。手术+术后帕米膦酸二钠治疗组 11 例,其中肿瘤刮除植骨内固定术 8 例,不刮除病灶单纯行内固定者 3 例;单纯应用帕米膦酸二钠治疗组 13 例。术后或第一次治疗后,每 3 个月按疗程应用帕米膦酸二钠,共 2 年。所有病例于治疗前及每次给予帕米膦酸二钠前检测骨代谢指标骨钙素和 I 型胶原 C 端肽,并行影像学检查。采用 VAS 评分系统评价治疗前后的疼痛变化,Harris 髋关节评分系统评价髋关节功能。观察有无药物不良反应。结果本组 24 例共接受了 205 次帕米膦酸二钠治疗。所有病例均获 24~55 个月的随访,中位随访时间 42 个月。治疗后第 2 年血清骨钙素水平( 80.195±64.75 )μg / L较治疗前( 147.198±104.86 )μg / L 明显降低,差异有统计学意义( P=0.000 ),血清 I 型胶原 C 端肽水平( 0.672±0.61 )μg / L 较治疗前( 1.396±0.6 )μg / L 也明显降低,差异有统计学意义( P=0.000 )。手术+术后应用帕米膦酸二钠的 11 例中仅有 1 例出现病情恶化,再次骨折,其余 10 例内固定均牢靠,7 例骨量增加,3 例病情无变化。单纯应用帕米膦酸二钠治疗的 13 例仅有 1 例病情恶化,其余 12 例均有不同程度的骨量增加、溶骨区减少、骨皮质增厚。所有病例治疗后疼痛逐渐减轻,末次随访 VAS 评分平均为优,手术+药物治疗组:末次随访 VAS 评分( 1.33±1.1 )明显小于治疗前 VAS 评分( 7.25±1.7 );单纯药物治疗组:末次随访 VAS评分( 1.17±1.5 )小于治疗前 VAS 评分( 5.83±1.3 ),差异均有统计学意义( P=0.002 )。所有病例髋关节功能明显恢复,末次随访 Harris 评分平均为良,手术+药物治疗组:末次随访 Harris 评分( 79.58±5.2 )大于治疗前 Harris 评分( 43.67±31.8 );单纯药物治疗组:末次随访 Harris 评分( 79.17±8.4 )大于治疗前 Harris 评分( 69.75±7.9 ),差异均有统计学意义( P=0.002 )。除 5 例在首次静滴帕米膦酸二钠后次日发热外,24 例均未见其它不良反应。结论帕米膦酸二钠治疗累及股骨近端多发性纤维结构不良疗效确切,能减少溶骨性破坏、预防骨折风险、缓解疼痛、改善髋关节功能,不良反应轻微、短暂。对无症状的 PFD、MAS 无须手术治疗,可直接应用帕米膦酸二钠治疗;对病变范围局限、溶骨性破坏者须行刮除植骨内固定术,对于股骨近端病变范围大、骨强度不佳者可单纯内固定,二者术后均须应用帕米膦酸二钠治疗,以防止植骨吸收及病情恶化。
骨纤维发育不良;股骨;修复外科手术;内固定器;帕米膦酸二钠
骨的纤维结构不良( fibrous dysplasia,FD )又称骨纤维异常增殖症,是一种少见的良性骨肿瘤。该病的特点是在正常骨髓腔内纤维组织及不成熟的编织骨异常增殖,导致骨质脆弱、畸形并易发生骨折。临床上分为单发性( monostotic fibrous dysplasia,MFD )、多发性( polyostotic fibrous dysplasia,PFD )、McCune-Albright 综合征( PFD 伴有内分泌系统疾病,MAS )。MFD 与 PFD 病变的自然病程截然不同[1]。MFD 病变局限,在骨骼发育停止后一般停止发展。而 PFD 和 MAS 病变可持续增大,且病变范围可累及整块骨骼,容易出现病理骨折和畸形,治疗难度大。股骨近端是纤维结构不良最容易累及的部位,Ippolito 等[2]报道,在多发性病例中有 92% 累及股骨。股骨近端因应力高度集中容易出现骨折、畸形,成为 FD 治疗中的难点。对于多发性病变的治疗,可以分为两个方向,一是针对病变本身的治疗,一是针对病变引起的骨折及畸形的治疗。目前基础研究证实,FD 病变组织中,破骨细胞被激活并造成骨质破坏[3]。因此抑制破骨细胞是治疗该疾病的靶点,二膦酸盐类药是目前临床上一组最重要的可用于治疗由破骨细胞介导以骨吸收为特点的药物[4]。国外报道帕米膦酸二钠治疗 FD 有效[5],国内尚无报道。2009 年 6 月至 2012 年 1 月,我们采用手术+静滴帕米膦酸二钠或单纯应用帕米膦酸二钠两种方法治疗 24 例累及股骨近端多发性纤维结构不良的患者,现将其治疗策略和临床疗效报道如下。
资料与方法
一、一般资料
本组共 24 例( 其中 2 例为 MAS ),男 14 例,女10 例;年龄 8~61 岁,平均 24 岁。12 例行手术治疗,经病理确诊;另 12 例经穿刺活检确诊。累及股骨和胫骨 14 例,其中有 4 例另外分别累及髋臼、腓骨、肱骨、髂骨;双侧股骨 4 例,其中 1 例同时累及双侧耻骨及坐骨;股骨和腓骨 3 例,其中 1 例同时累及颅骨;累及股骨和髋臼 2 例;累及股骨和肱骨 1 例。
二、治疗方法
1. 治疗策略:手术+术后药物治疗:对于股骨近端病理骨折、濒临骨折或畸形较重的 11 例入院后采用手术+术后应用帕米膦酸二钠治疗。其中对病变范围局限、溶骨性破坏者行刮除植骨内固定术,对于病变范围广、骨强度不佳者行单纯内固定术。术后每隔 3 个月按疗程应用帕米膦酸二钠药物,共2 年。
单纯药物治疗:对于股骨近端无骨折、无濒临骨折或畸形的 10 例及对于股骨近端畸形严重,无法行手术治疗的 3 例,每 3 个月单纯应用帕米膦酸二钠药物治疗,共 2 年。
2. 帕米膦酸二钠的应用:本组所有病例静滴帕米膦酸二钠。根据国外文献用药方案[6]:成人 1 次静滴 60 mg,1 天 1 次,连续 3 天;儿童 1 次静滴1 mg / kg,1 天 1 次,连续 3 天;每隔 3 个月用药连续 3 天,根据病情发展,常规用药 2 年。
3. 手术及术后处理:刮除病灶的手术方式:肿瘤刮除植骨内固定术,应用于病变相对局限、刮除肿瘤后骨皮质强度允许并有充足骨量植骨的 8 例。于骨折处或开窗直视下刮除病变组织,电刀烧灼瘤壁,植入自体髂骨或人工骨。其中 2 例病变位于股骨颈濒临骨折及 1 例股骨粗隆间病理性骨折应用动力髋内固定;病变位于小转子远端、股骨近端 1 / 3处的 5 例中有 3 例儿童为防止破坏股骨头处骨骺应用钢板内固定,2 例应用髓内针内固定。
不刮除病灶的手术方式:( 1 )截骨矫形带锁髓内针内固定术:应用于髋内翻畸形合并病理性骨折 2 例,病变范围广,侵及股骨近端 1 / 2。于转子下区股骨骨折处外侧楔形外翻截骨,常规置入髓内针,穿过截骨段以恢复颈干角及下肢力线,均不刮除髓腔内肿瘤组织。其中 1 例由于第 1 次行股骨近端刮除植骨、截骨矫形钢板内固定,术后应用 9 次帕米膦酸二钠后病情恶化,第 2 次再行截骨矫形带锁髓内钉内固定且不刮除病灶。( 2 )单纯带锁髓内针内固定术:应用于侵及股骨颈、粗隆间及股骨近端 1 / 3 者 2 例,濒临骨折但无畸形。单纯给予带锁髓内针内固定,不行肿瘤刮除植骨。( 3 )单纯植骨、钢板内固定术:应用于 10 岁儿童 1 例。该病例给予 8 次帕米膦酸二钠后,病情恶化,给予预防性内固定,病灶内植入异体骨并应用钢板螺钉内固定,不刮除病灶。
术后处理:术后 24 h 行股四头肌等长收缩锻炼及髋、膝关节被动活动。术后 2 周扶拐不负重下地活动,2~3 个月后部分负重。术后 3 个月按疗程应用帕米膦酸二钠。分别于术后 3、6、12、24 个月,在每次给予帕米膦酸二钠治疗前行手术部位 X 射线片正侧位检查,根据 X 射线片评估骨愈合情况,指导负重行走和功能锻炼。
三、疗效观察
1. 骨代谢指标:骨钙素( osteocalcin,OC )反应骨吸收程度。采用放射免疫法检测 OC 值。正常参考值:女性绝经前( 11~43 )μg / L,女性绝经后( 15~46 )μg / L;男性 18~30 岁( 24~70 )μg / L,男性 31~50 岁( 14~42 )μg / L,男性 51~70 岁( 14~46 )μg / L。
I 型胶原 C 端肽( β isomerized type I collagen C-telopeptides,β-CTx )反应骨吸收的敏感指标。采用放射免疫法检测 OC 值。正常参考值:女性绝经前:( 0.068~-0.68 )μg / L,女性绝经后:( 0.131~-0.9 )μg / L;男性:( 0.043~-0.783 )μg / L。
于治疗前及每次给予帕米膦酸二钠前检测 24 例的骨代谢指标。
2. 影像学变化、疼痛情况、功能情况及不良反应的随访:患者需要每隔 3 个月住院应用帕米膦酸二钠治疗,共 2 年。每次入院后复查病变部位,所有病例每次给予帕米膦酸二钠治疗前均行 X 线及CT 冠状位扫描+容积重建,观察髓腔内病变是否进展、颈干角和股骨内翻角度变化以及手术患者骨质愈合情况。对帕米膦酸二钠治疗前后患者的疼痛情况、髋关节功能及不良反应进行随访( 包括用帕米膦酸二钠治疗的 2 年 )。采用 VAS 评分评价治疗前后疼痛变化[7]。采用 Harris 髋关节评分系统评价髋关节功能[8]。
四、统计学方法
术前、术后的骨代谢指标、影像学变化、疼痛VAS 评分及 Harris 评分数据均使用 SPSS 20.0 软件进行统计处理,以( x-±s )的形式表示,采用配对符号秩和检验( Wilcoxon ),P<0.05 表示差异有统计学意义。
结 果
所有病例均获 24~55 个月的随访,中位随访时间 42 个月。帕米膦酸二钠药物治疗方案为每隔 3 个月应用药治疗,每次连续 3 天,持续 2 年。本组中15 例接受全部 9 次治疗;7 例因疼痛明显缓解,接受了 8 次治疗;2 例接受了 7 次治疗。全部 24 例共接受了 205 次帕米膦酸二钠治疗。
一、骨代谢指标变化
基础研究证实,骨纤维异常增殖症患者的组织中,破骨细胞被激活并造成骨质破坏,本组病例均为多发性骨纤维结构不良,骨质溶骨性破坏较重,检测骨代谢指标发现有些患者异常增高。
本组 24 例治疗后血清 OC 值均有不同程度地降低。治疗前血清 OC 平均值( 147.198±104.86 )μg / L;治疗后第 1 年( 第 3、6、9、12 个月 )平均值( 111.092±86.24 )μg / L,较治疗前血清 OC 值平均值小,差异有统计学意义( P=0.000 );治疗后第 2 年( 第 15、18、21、24 个月 )平均值( 80.195±64.75 )μg / L,明显小于治疗前 OC 平均值,且差异有统计学意义( P=0.000 )。
本组 24 例治疗后血清 β-CTx 值均有不同程度地降低。治疗前 β-CTx 平均值( 1.396±0.6 )μg / L;治疗后第 1 年( 第 3、6、9、12 个月 )平均值( 0.971±0.73 )μg / L;较治疗前 β-CTx 平均值小,差异有统计学意义( P=0.000 );治疗后第 2 年( 第 15、18、21、24 个月 )平均值为( 0.672±0.61 )μg / L,明显小于治疗前 β-CTx 平均值,差异有统计学意义( P=0.000 )。
二、影像学变化
手术+术后药物治疗组,共 11 例。骨折患者平均术后 4( 3~6 )个月 X 线片显示骨折线模糊、骨皮质连续,骨折均一期愈合。7 例药物治疗后平均15( 2~25 )个月 X 线片及 CT 显示均有不同程度的骨量增加、溶骨区减少、骨皮质增厚( 图1 )。3 例治疗后平均 13( 6~20 )个月 X 线片及 CT 均显示平均13 个月出现植骨部分吸收,给予帕米膦酸二钠治疗后,吸收范围稳定没有变化。1 例 8 岁患者行股骨近端截骨矫形钢板内固定术后应用 9 次帕米膦酸二钠后病情恶化,钢板远端股骨溶骨性破坏,摔伤后骨折。给予取出钢板,带锁髓内钉内固定,术后 4 个月骨折愈合。
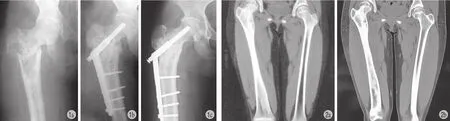
图1 病例 5,男,31 岁。右股骨粗隆间纤维结构不良并病理性骨折行刮除植骨动力髋钢板内固定术 a:术前股骨粗隆间溶骨性破坏,病理性骨折;b:行肿瘤刮除自体腓骨移植、动力髋钢板内固定术,术后 7 天 X 线片;c:术后 3 年随访,应用 7 次帕米膦酸二钠,见植骨愈合、内固定牢靠图2 病例 14,女,10 岁。右股骨、胫骨多发性纤维结构不良应用帕米膦酸二钠治疗 a:治疗前,CT 冠状位重建示股骨髓腔内“磨砂玻璃样”改变,无畸形及濒临骨折;b:应用 9 次帕米膦酸二钠后,骨量增加Fig.1 A 31-year-old male patient with right femoral intertrochanteric fbrous dysplasia and pathological fractures underwent curettage and bone graft with dynamic hip screw internal fxation a: Femoral intertrochanteric osteolytic destruction and pathological fractures were noticed before the operation; b: The X-ray at 7 days after the operation showed curettage and fbular graft with dynamic hip plate internal fxation; c: The patient was followed up for 3 years and received 7 times of pamidronate disodium injection, with the results of bone union and frm internal fxationFig.2 A 10-year-old female patient with polyostotic fibrous dysplasia in the right femur and tibia received pamidronate disodium injection a: Before the treatment, the CT coronal reconstruction showed frosted glass-like changes in the femoral marrow cavity, without deformities or on the verge of fractures; b: After the injection of pamidronate disodium for 9 times, bone mass was increased
单纯药物治疗组,共 13 例。6 例药物治疗后平均 7.5( 6~9 )个月 X 线片及 CT 显示均有不同程度的骨量增加、溶骨区减少、骨皮质增厚( 图2 )。6 例治疗后平均 22.5( 21~24 )个月 X 线片及 CT 均显示病情无变化,影像学无明显变化。1 例 10 岁患者应用 8 次帕米膦酸二钠后病情恶化,股骨近端髓腔内由“磨砂玻璃”样改变逐渐呈“空壳”样溶骨性改变,皮质破坏>50%,病理骨折可能性增大,及时给予预防性钢板内固定治疗。
三、疼痛情况
所有病例治疗前均存在与纤维结构不良病灶相关的疼痛,治疗后疼痛逐渐减轻,末次随访 VAS 评分平均为优( 0~2 )。手术+药物治疗组:末次随访 VAS 评分( 1.33±1.1 )明显小于治疗前 VAS 评分( 7.25±1.7 ),差异有统计学意义( P=0.002 )。单纯药物治疗组:末次随访 VAS 评分( 1.17±1.5 )小于治疗前疼痛 VAS 评分( 5.83±1.3 ),差异有统计学意义( P=0.002 )。
四、功能情况
所有病例治疗后髋关节功能明显恢复,末次随访 Harris 髋关节功能评分平均为良( 70~80 )。手术+药物治疗组:末次随访 Harris 评分( 79.58±5.2 )大于治疗前 Harris 评分( 43.67±31.8 ),差异有统计学意义( P=0.002 )。单纯药物治疗组:末次随访Harris 评分( 79.17±8.4 )大于治疗前疼痛 Harris 评分( 69.75±7.9 ),差异有统计学意义( P=0.002 )。
五、帕米膦酸二钠不良反应
5 例在首次静滴帕米膦酸二钠后次日发热,体温 37.3 ℃~38.5 ℃,给予地塞米松注射液 5 mg+0.9% 生理盐水 500 ml 静滴后发热逐渐消退。24 例用药前后检查肝功、血生化以及外周血白细胞、红细胞和血小板计数,均未见异常。
讨 论
一、帕米膦酸二钠治疗多发性纤维结构不良的有效性和安全性
自 1994 年 Liens 等[5]首先报告静脉滴注帕米膦酸二钠治疗纤维结构不良获得确切效果后,二膦酸盐类药物得到广泛应用。国外报道,使用帕米膦酸二钠能使多发性纤维结构不良患者疼痛明显减轻、骨折发生率降低、病变区皮质增厚、骨化增加[9-11]。本组 24 例共接受了 205 次帕米膦酸二钠治疗,治疗后末次随访疼痛明显减轻,髋关节功能明显好转。治疗后第 1、2 年骨代谢指标血清 OC、β-CTx 均较治疗前明显降低。OC 是由成骨细胞产生和分泌的一种非胶原蛋白,大部分沉积在骨基质中,小部分进入血液循环。当骨基质降解时,其中的 OC 进入循环中。因此测定血中 OC,一方面能反映成骨细胞的活性,但在更大程度上反映的是骨吸收的程度。Zacharin 等[12]对 8 例多发性纤维结构不良患者静脉滴注帕米膦酸二钠 1 mg / kg / 天,共 3 天,每半年 1 次,共 2 年。骨钙素从( 35.5± 5.6 )μg / L 降到( 28.4±4.1 )μg / L,差异有统计学意义( P<0.05 )。β-CTx 是 I 型胶原的降解产物,在I 型胶原降解过程中,该肽段被完整的释放入血清。在骨骼破坏加快的情况下,β-CTx 浓度会升高,是反映骨吸收的敏感指标。Chapurlat 等[13]对 20 例纤维结构不良患者静脉滴注帕米膦酸二钠 30 mg /天,共 3 天,每半年 1 次,共 8 次。通过检测尿的β-CTx,发现治疗后尿的 β-CTx 水平下降 71%( P=0.002 )。本研究治疗后第 1、2 年血清 OC 及 β-CTx明显降低,说明应用帕米膦酸二钠能有效抑制多发性纤维结构不良患者的骨吸收。
本组 24 例行定期影像学检查,其中 13 例应用帕米膦酸二钠治疗后平均 15( 2~25 )个月 X 线片及CT 显示均有不同程度的骨量增加、溶骨区减少、骨皮质增厚。9 例治疗后病情无变化,影像学无明显变化。Chapurlat 等[9]对 50 例有 X 线检查的 FD 患者进行随访,发现有 27 例( 54% )应用帕米膦酸二钠后影像学明显改善,表明应用帕米膦酸二钠能抑制骨吸收,增加骨量,降低骨折风险。但是对于多发病变的儿童患者,帕米膦酸二钠治疗病变本身的能力受到了质疑。本组有 2 例儿童在行帕米膦酸二钠治疗的 2 年内病情恶化,病灶范围扩大,呈溶骨性破坏,1 例出现病理性骨折,1 例濒临骨折并给予带锁髓内针内固定。Plotkin 等[14]对 13 例应用帕米膦酸二钠治疗的多发性纤维结构不良的儿童进行影像学评估,没有发现溶骨区内有骨质的再填充,反而发现病变宽度的增大。作者认为儿童较成人病变发展迅速,药物治疗很难控制。虽然帕米膦酸二钠治疗儿童多发性纤维结构不良安全性良好,可缓解骨痛,但是没有证据表明帕米膦酸二钠能治疗病变本身。因此对于儿童多发病变者,在应用帕米膦酸二钠过程中要密切随访,如出现溶骨区扩大、畸形加重、濒临骨折,须及时手术干预。本组 24 例随访时常规行病变部位 CT 冠状位容积重建,通过重建,可以清楚地观察到髓腔内溶骨区的范围,骨皮质破坏的程度,可以早期评估出现病理性骨折的风险。
国外研究未发现应用帕米膦酸二钠有严重不良反应。Chapurlat 等[9]报道 23 例( 39% )在首次应用帕米膦酸二钠后出现轻到中度的一过性发热,3 例出现静脉刺激症状。本组有 5 例出现了一过性发热,应用地塞米松后缓解,所有患者无肝肾功能损害,无下颌骨坏死等严重不良反应。
二、多发性纤维结构不良的手术适应证及手术方式的选择
纤维结构不良病变本身并不是手术的指征,原则上不须进行预防性的刮除植骨,手术治疗的适应证为病变引起的骨折或畸形[1]。股骨近端是纤维结构不良最容易累及的部位,由于应力的高度集中容易出现骨折、畸形。当主诉髋部疼痛加重,须评估骨折的可能性。影像学检查尤其是 CT 冠状位容积重建显示应力骨折、囊性变或畸形加重,是选择内固定手术的指征。但对于濒临骨折的患者,评估病理性骨折的风险具有很大的主观性和不确定性,需要临床医生的经验。目前还没有相关的临床评分系统,李涛等[15]认为对于病变范围大( 病变区波及髓腔直径≥50%,骨皮质完整 )或骨强度不佳( 病变侵及骨皮质厚度≥50% )者,需要手术并应用内固定治疗。
病灶刮除植入自体骨或异体骨是治疗股骨近端纤维结构不良的常用方法,但对于病变广泛、骨强度不佳的患者效果较差。Ennecking 等[16]总结发现,25 例股骨近端纤维结构不良接受刮除松质骨植骨,13 例出现局部的吸收及病变复发。Guille 等[17]对 13 例股骨近端纤维结构不良进行了共计 24 次刮除自体松质骨和( 或 )皮质骨植骨,随访 2.5~41.3 年发现,所有的植骨在 X 线片上都出现了吸收,病变没有消失或减小。本组 8 例行刮除植骨内固定术,3 例出现植骨部分吸收,给予帕米膦酸二钠治疗后,吸收范围稳定没有变化。为了解决植骨吸收的问题,Ennecking 通过试验发现皮质骨相对于松质骨更难被吸收及爬行替代,提出了使用自体皮质骨植入的方法,对 15 例股骨近端纤维结构不良者不刮除病灶,直接植入腓骨或胫骨条,平均随访 6 年,只有 2 例出现了局部吸收。Stephenson等[18]建议有效地切开复位内固定而不处理病灶,这种方式虽然没有去除病变组织,但直接加强了局部的骨骼强度而有助于避免局部骨折或畸形等并发症的出现,报道中有 86%( 19 / 22 )的病变通过这种方法获得了平均 10 年的稳定。由于本组中有 1 例做了两次手术,第 1 次行股骨近端截骨矫形钢板内固定,术后应用 9 次帕米膦酸二钠后病情恶化,第2 次行带锁髓内钉内固定且不刮除病灶,故本组共5 例采用内固定术而不刮除病灶。其中 1 例植入异体皮质骨板,1 例植入异体骨粒,术后均给予常规帕米膦酸二钠治疗,随访 15~18 个月,5 例均无骨折及畸形的发生,病情无变化。因此我们认为,对于病变范围局限、溶骨性破坏的病灶,可行刮除植骨内固定术;对于病变范围广、骨强度不佳的患者,可以采用单纯内固定术而不处理病灶,如有溶骨性破坏范围较大,可植入皮质骨,术后应用帕米膦酸二钠治疗,防止植骨吸收及病情恶化。
三、内固定的应用及选择
由于股骨近端应力高度集中,通过内固定可以大大提高局部稳定性,Stephenson 等[18]对<18 岁的多发纤维结构不良的 14 例行单纯刮除植骨术,有13 例再次出现病理骨折;对另一组 15 例行切开复位内固定术,有 13 例疗效满意。本组共 12 例应用内固定治疗,仅有 1 例钢板远端股骨溶骨性破坏、病理性骨折。因此对于股骨近端病变范围广、骨质强度差或伴有髋内翻畸形行截骨矫形者,必须采用坚强内固定治疗。
使用何种内固定器械,目前尚无统一标准,主要取决于病灶范围和骨的质量。髓内钉系统总体上优于单纯螺钉系统、钉板系统。李伟栩等[19]对12 例多发骨纤维结构不良并髋内翻畸形者采用楔形截骨、动力髋或动力髁内固定,1 例髋螺钉滑动、1 例钢板远端股骨干骨折。欧洲小儿骨科协会对累及整个股骨近端并病理骨折的 8 例 PFD 患者使用钢板螺钉固定,结果均出现钉板断裂和松动,畸形加重。该协会对病变范围大、波及整个股骨近端的12 例 PFD 患者采用了髓内针内固定技术,随访时间超过 10 年,疗效满意[2]。加上进行了两次手术的1 例,本组共 6 例应用髓内针治疗,没有出现畸形加重或骨折。我们认为选用的内固定一定要超过病变本身,髓内针才能提供长期有效的稳定性,防止骨折和严重畸形的出现。
四、本研究的不足及局限性
手术时机及内固定的选择主观性较强,尚未得出统一的标准。报道的病例数较少,随访时间短,未设随机对照组等,未来还须经过多中心、大样本量的研究加以验证。
综上所述,( 1 )帕米膦酸二钠治疗 PFD、MAS疗效确切,能减少溶骨性破坏、预防骨折风险、缓解疼痛、改善髋关节功能,不良反应轻微、短暂,尤其适合病变范围广及多发性病变的患者,但对儿童病例要密切随访;( 2 )对无症状的 PFD、MAS 患者不需要手术治疗,可直接应用帕米膦酸二钠治疗;( 3 )对病变范围局限、溶骨性破坏的 PFD、MAS 须行刮除植骨内固定术,对于股骨近端病变范围大、骨强度不佳者可单纯内固定,二者术后均须应用帕米膦酸二钠治疗,防止植骨吸收及病情恶化。
[1] DiCaprio MR, Enneking WF. Fibrous dysplasia. Pathophysiology, evaluation, and treatment. J Bone Joint Surg Am, 2005, 87(8):1848-1864.
[2] Ippolito E, Bray EW, Corsi A, et al. Natural history and treatment of fibrous dysplasia of bone: a multicenter clinicopathologic study promoted by the European Pediatric Orthopaedic Society. J Pediatr Orthop B, 2003, 12(3):155-177.
[3] Riminucci M, Saggio I, Robey PG, et al. Fibrous dysplasia as a stem cell disease. J Bone Miner Res, 2006, 21(2):125-131.
[4] Morris CD, Einhorn TA. Bisphosphonates in orthopaedic surgery. J Bone Joint Surg Am, 2005, 87(7):1609-1618.
[5] Liens D, Delmas PD, Meunier PJ. Long-term effects of intravenous pamidronate in fbrous dysplasia of bone. Lancet, 1994, 343(8903):953-954.
[6] Lane JM, Khan SN, O’Connor WJ, et al. Bisphosphonate therapy in fibrous dysplasia. Clin Orthop Relat Res, 2001, (382):6-12.
[7] Johnson EW. Visual analog scale (VAS). Am J Phys Med Rehabil, 2001, 80(10):717.
[8] Mahomed NN, Arndt DC, McGrory BJ, et al. The Harris hip score: comparison of patient self-report with surgeon assessment. J Arthroplasty, 2001, 16(5):575-580.
[9] Chapurlat RD, Hugueny P, Delmas PD, et al. Treatment of fbrous dysplasia of bone with intravenous pamidronate: longterm effectiveness and evaluation of predictors of response to treatment. Bone, 2004, 35(1):235-242.
[10] Parisi MS, Oliveri B. Long-term pamidronate treatment of polyostotic fibrous dysplasia of bone: A case series in young adults. Curr Ther Res Clin Exp, 2009, 70(2):161-172.
[11] Isaia GC, Lala R, Deflippi C, et al. Bone turnover in children and adolescents with McCune-Albright syndrome treated with pamidronate for bone fbrous dysplasia. Calcif Tissue Int, 2002, 71(2):121-128.
[12] Zacharin M, O’Sullivan M. Intravenous pamidronate treatment of polyostotic fibrous dysplasia associated with the McCune Albright syndrome. J Pediatr, 2000, 137(3):403-409.
[13] Chapurlat RD, Delmas PD, Liens D, et al. Long-term effects of intravenous pamidronate in fbrous dysplasia of bone. J Bone Miner Res, 1997, 12(10):1746-1752.
[14] Plotkin H, Rauch F, Zeitlin L, et al. Effect of pamidronate treatment in children with polyostotic fbrous dysplasia of bone. J Clin Endocrinol Metab, 2003, 88(10):4569-4575.
[15] 李涛, 行斌斌, 段宏, 等. 股骨近端骨纤维结构不良的外科治疗. 中国修复重建外科杂志, 2009, 3:261-263.
[16] Enneking WF, Gearen PF. Fibrous dysplasia of the femoral neck. Treatment by cortical bone-grafting. J Bone Joint Surg Am, 1986, 68(9):1415-1422.
[17] Guille JT, Kumar SJ, MacEwen GD. Fibrous dysplasia of the proximal part of the femur. Long-term results of curettage and bone-grafting and mechanical realignment. J Bone Joint Surg Am, 1998, 80(5):648-658.
[18] Stephenson RB, London MD, Hankin FM, et al. Fibrous dysplasia. An analysis of options for treatment. J Bone Joint Surg Am, 1987, 69(3):400-409.
[19] 李伟栩, 叶招明, 林, 等. 截骨矫形钢板固定治疗股骨近段纤维结构不良伴髋内翻畸形. 中华骨科杂志, 2011, 31(6): 577-581.
( 本文编辑:代琴 )
关于投稿请提供伦理委员会批准文件及受试对象知情同意书
本刊要求,当论文的主体是以人为研究对象的试验时,作者应该说明其遵循的程序是否符合负责人体试验的委员会( 单位性的、地区性的或国家性的 )所制定的伦理学标准,并提供该委员会的批准文件,及受试对象的知情同意书。
Pamidronate disodium for polyostotic fbrous dysplasia in the proximal femur: twenty-four cases report
XU Ming, XU Song-feng, YU Xiu-chun. Orthopedic Department, the General Hospital of Jinan Military Commanding Region, Jinan, Shandong, 250031, PRC
ObjectiveTo investigate the therapeutic methods and clinical effects of pamidronate disodium for polyostotic fbrous dysplasia in the proximal femur in different degrees.MethodsFrom June 2009 to January 2012, 24 patients with polyostotic fbrous dysplasia in the proximal femur were adopted and treated. There were 14 males and 10 females, whose average age was 24 years old( range; 8-61 years ). A combination of surgery and postoperative pamidronate disodium was performed on 11 patients, curettage, bone graft and internal fxation on 8 patients, simple internal fixation on 3 patients and only pamidronate disodium on 13 patients. Pamidronate disodium was taken every 3 months after the operation or after the frst treatment, and the duration was 2 years. Before the treatment or before pamidronate disodium injection, bone metabolic markers were detected and the imaging examination was performed in all the patients, including osteocalcin( OC )and C-terminal telopeptides of type I collagen( CTX-I ).The Visual Analogue Scale( VAS )was used to evaluate the preoperative and postoperative pain. The hip function was systematically assessed based on the Harris hip score. The adverse effects were observed.ResultsA total of 205 times of pamidronate disodium injection were received. All the patients were followed up for 24-55 months, and the median follow-up time was 42 months. At the 2nd year after the treatment, the level of OC in the serum was( 80.195±64.75 )μg/L, which was obviously reduced when compared with the level of( 147.198±104.86 )μg/L before the treatment. The differences between them were statistically signifcant( P=0.000 ). At the 2nd year after the treatment, the level of CTX-I in the serum was( 0.672±0.61 )μg/L, which was also obviously reduced when compared with the level of( 1.396±0.6 )μg/L before the treatment. The differences between them were statistically signifcant( P=0.000 ). In the group of a combination of surgery and postoperative pamidronate disodium, disease progression of fracture again was noticed only in 1 case and frm internal fxation in the other 10 cases, including 7 cases of increased bone mass and 3 cases of no disease progression. In the group of only pamidronate disodium, disease progression was noticed only in 1 case and increased bone mass, reduced osteolysis and cortical thickening of bone in different degrees in the other 12 cases. Pain was gradually relieved after the treatment in all the patients, with excellent VAS scores on average in the latest follow-up. In the group of a combination of surgery and pamidronate disodium, the VAS score was( 1.33±1.1 )points in the latest follow-up, which was obviously reduced when compared with the preoperative VAS score of( 7.25±1.7 )points. The differences between them were statistically signifcant( P=0.002 ). In the group of only pamidronate disodium, the VAS score was( 1.17±1.5 )points in the latest follow-up, which was reduced when compared with the preoperative VAS score of( 5.83±1.3 )points. The differences between them were statistically signifcant( P=0.002 ). The hip function was well restored in all the patients, with good Harris hip scores in the latest follow-up. In the group of a combination of surgery and pamidronate disodium, the Harris hip score was( 79.58±5.2 )points in the latest follow-up, which was greater than the preoperative Harris hip score of( 43.67±31.8 )points. The differences between them were statistically signifcant( P=0.002 ). In the group of only pamidronate disodium, the Harris hip score was( 79.17±8.4 )points in the latest follow-up, which was greater than the preoperative Harris hip score of( 69.75±7.9 )points. The differences between them were statistically signifcant( P=0.002 ). Except that fever was noticed in 5 patients at the 2nd day after the frst intravenous drip infusion of pamidronate disodium, no adverse reactions were found in the 24 patients.ConclusionsPamidronate disodium is effective in the treatment of polyostotic fibrous dysplasia in the proximal femur, with the advantages of inhibiting osteolytic bone destruction, preventing the risk of bone fractures, relieving pain, improving the hip function, reducing adverse reactions and minimizing the treatment time. For the patients with asymptomatic polyostotic fibrous dysplasia or McCune-Albright syndrome, surgery is unnecessary and pamidronate disodium is a good choice. Curettage, bone graft and internal fxation should be performed on the patients with limited extent of lesions and osteolytic bone destruction. Simple internal fxation should be performed on the patients with extensive lesions in the proximal femur, pathological fractures or severe deformities or on the verge of fractures. Both kinds of patients above should receive pamidronate disodium injection after the operation, so as to prevent bone absorption and disease progression.
Fibrous dysplasia of bone; Femur; Reconstructive surgical procedures; Internal fixators; Pamidronate disodium
10.3969/j.issn.2095-252X.2014.05.013
R738.1
250031 济南军区总医院骨病科
于秀淳,Email: yxch48@vip.sina.com
2014-04-07 )
