经导管主动脉瓣置换术术后永久起搏器植入的预测因素Meta分析
2021-12-17李瑞锋韩克张勇王小可吴岳袁祖贻
李瑞锋 韩克 张勇 王小可 吴岳 袁祖贻
经导管主动脉瓣置换术(transcatheter aortic valve replacement, TAVR)的开展为不能行外科手术及高危主动脉瓣重度狭窄患者提供了新的有效治疗策略。指南中指出,对于中低危(胸外科医师学会评分<8分)患者,TAVR与外科主动脉瓣置换术相比无劣效性,可进一步根据患者年龄和患者意愿来选择TAVR[1]。随着TAVR越来越多地被研究及临床应用,现已成为心血管介入领域的热点技术。然而,TAVR术后常伴发高级房室传导阻滞和新出现的左束支传导阻滞(left bundle branch block,LBBB)而需要永久起搏器植入(permanent pacemaker implantation,PPI)。有回顾性分析显示TAVR术后PPI并没有随着时间的推移而减少,比例在13.2%~18.8%[2]。有研究显示TAVR术后PPI增加住院费用,并且与更高的心脏死亡率及1年内因心力衰竭再住院治疗相关[3-4]。因此分析TAVR术后PPI的危险因素对于实施风险分层和患者管理有重要的临床意义。既往研究多从患者基本特征、基础心电图改变、心脏结构差异、瓣膜类型及手术相关操作等方面评估TAVR术后PPI的预测因素,并试图通过对高危人群调整手术策略来降低PPI的风险[5-6]。然而,现在并没有完备的研究捕获所有潜在的危险因素。并且,受限于样本量等因素,研究中不同危险因素预测效能的差异及各研究间结果的矛盾性可能会阻碍指导原则的推广。
因此,本研究回顾既往发表的真实世界研究或病例对照研究并进行荟萃分析,旨在系统性识别和总结TAVR术后PPI的危险因素。
1 对象与方法
1. 1 检索策略
本研究对截至2020年12月1日发表在PubMed、EMBASE上的文献进行了全面检索。用以下检索词进行研究筛选: “transcatheter aortic valve replacement OR transcatheter aortic valve implantation OR(TAVR)OR (TAVI) AND pacemaker”。另外,为了获得潜在符合条件的研究,本研究组对检索文献的参考文献列表进行了回顾并手动筛选了其他相关研究。考虑数据分析的准确性,我们仅关注已发表的文章。
1. 2 文献纳入与排除标准
纳入标准: (1)真实世界研究、病例对照研究;(2)参与者为接受TAVR治疗的患者,不受性别和地理位置的限制;(3)研究的主要目的为TAVR术后传导异常及PPI发生并报道了危险因素或预测因子;(4)研究可提供各项指标的数值及比例(二分类变量),或均数及标准差(连续型变量)。当研究涉及同一中心或同一注册研究不同时间、不同人群分析时,选择覆盖范围最广、病例数据最全的研究。排除标准: (1)病例报告、综述及会议摘要;(2)重复数据;(3)缺乏详细的数据支持及不完整结果的数据;(4)分析瓣中瓣(valve-invalve)技术的研究;(5)单独分析已退市的Lotus瓣膜的研究;(6)研究样本量小于100例。
1. 3 研究变量
定义TAVR术后PPI为研究终点。根据近期发表综述中提及[7]以及各入选文献报道,确定以下有预测意义的临床指标为研究变量,包括(1)患者基本特征:年龄、性别、Euroscore评分;(2)心电图:是否存在心房颤动、各类型传导阻滞及PR间期、QRS波宽度;(3)影像学:瓣口面积、瓣环直径、流出道内径、左心室舒张末期内径、室间隔厚度、左冠状动脉瓣钙化积分、右冠状动脉瓣钙化积分及是否存在二瓣化、瓷化主动脉瓣、重度钙化;(4)手术操作:置入深度、膜部长度、是否存在预扩张或后扩张、瓣膜尺寸超出程度;(5)瓣膜类型及型号:自膨胀瓣膜包括Corevalve(Medtronic,Minneapolis,MN)、Evolute(Medtronic, Minneapolis,MN)、Portico(St.Jude Medical,St Paul, MN)及其他;球囊扩张瓣膜包括Cribier、Sapien、Sapien XT、Sapien 3(Edwards Lifesciences,Irvine, CA)。
1. 4 数据提取与质量评估
两位研究者分别按照标准化格式提取数据。在数据提取方面的任何差异通过讨论和咨询第三位研究者以达成共识来解决。提取的信息主要包括(1)研究信息:数据来源(单中心、多中心或注册研究)、患者所在区域、研究时间和样本量;(2)上述确定的有预测意义的临床指标。
本研究采用循证护理中心(Joanna Briggs Institute,JBI)文献质量评价标准对纳入研究进行偏倚风险评价。0分为不符合要求,1分为提到但没有详尽叙述,2分为详尽全面叙述。JBI评价标准包括10项,满分20分。得分>总分70%可认为偏倚风险较低。低质量的研究不纳入Meta分析。
1. 5 统计学分析
各研究利用漏斗图来进行发表偏倚分析,如漏斗图不对称或不完整,则提示可能存在发表偏倚,经过进一步研究检索仍不能降低偏倚,便予以舍弃。各变量如涉及的研究数目小于5篇,则予以舍弃。
PPI比例采用事件数/样本量的方法进行计算。二分类变量计算比值比(odds ratios,OR)及95%置信区间(conf idence interval,CI)以评估各研究变量与TAVR术后PPI的关系,连续变量通过计算平均差(mean difference,MD)及95%CI以评估TAVR术后PPI与无PPI两组变量的差异,结果以森林图形式进行展示。各研究间的异质性用CochranQ检验及I2指数进行量化,P<0.05,I2<31%,则认为各研究是同质的,采用固定效应模型;P<0.05,I2>56%,则提示各研究间存在较大的异质性,采用随机效应模型。P<0.05,I2为31%~56%不能排除异质性,亦采用随机效应模型。
分层分析不同类型瓣膜术后PPI相关危险因素时,纳入研究为仅包含同一类型瓣膜的研究。GRADE证据评级用于对危险因素的质量评价[8],极低证据质量(+)的危险因素考虑真实性极可能与估计值大不相同,不予进一步分析。敏感性分析:将JBI评分<17分的研究剔除后再次计算各变量OR/MD值及95%CI,对比剔除前后结果差异。使用Revman 5.4软件进行数据分析。统计学检验采用双尾检验,以P<0.05为差异有统计学意义。
2 结果
2. 1 研究筛选
根据检索策略从数据库中初步检索到4048篇研究,通过去重及去除摘要或会议论文,筛选出1416篇研究。进一步审查题目及摘要,筛选出840篇TAVR相关报道。通过全文检索确定了80篇报告了TAVR术后PPI预测因子分析的研究,根据最初拟定的纳入及排除标准最终确定涉及23 934例患者的30项研究以供进一步荟萃分析[6,9-37](图1)。
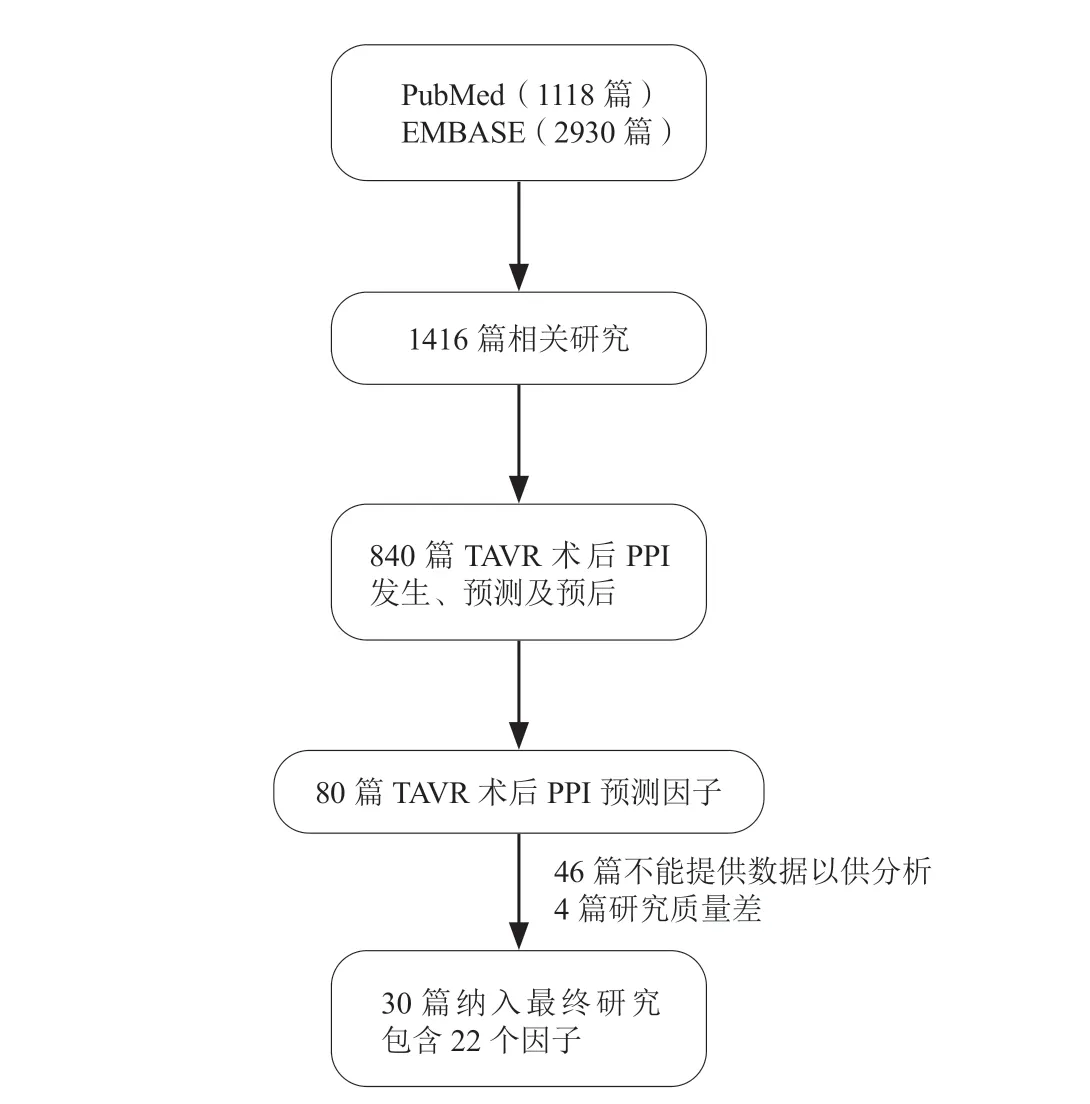
图1 研究筛选
2. 2 研究特征
符合条件的30项研究的基线信息列于表1。所有研究均为2005年1月至2019年8月进行的真实世界研究,其中20项为单中心研究,10项为多中心研究,样本量从106例到9785例不等。纳入人群所在区域包含欧洲、亚洲、大洋洲、南北美洲,欧洲研究最多为16项,北美洲9项,亚洲3项,南美洲1项,大洋洲1项。另外,7项研究仅涉及自体膨胀瓣膜,9项研究仅涉及球囊扩张瓣膜,其余14项研究以上两种类型瓣膜均有涉及。JBI文献质量评分为15~20分,17分以上22篇。
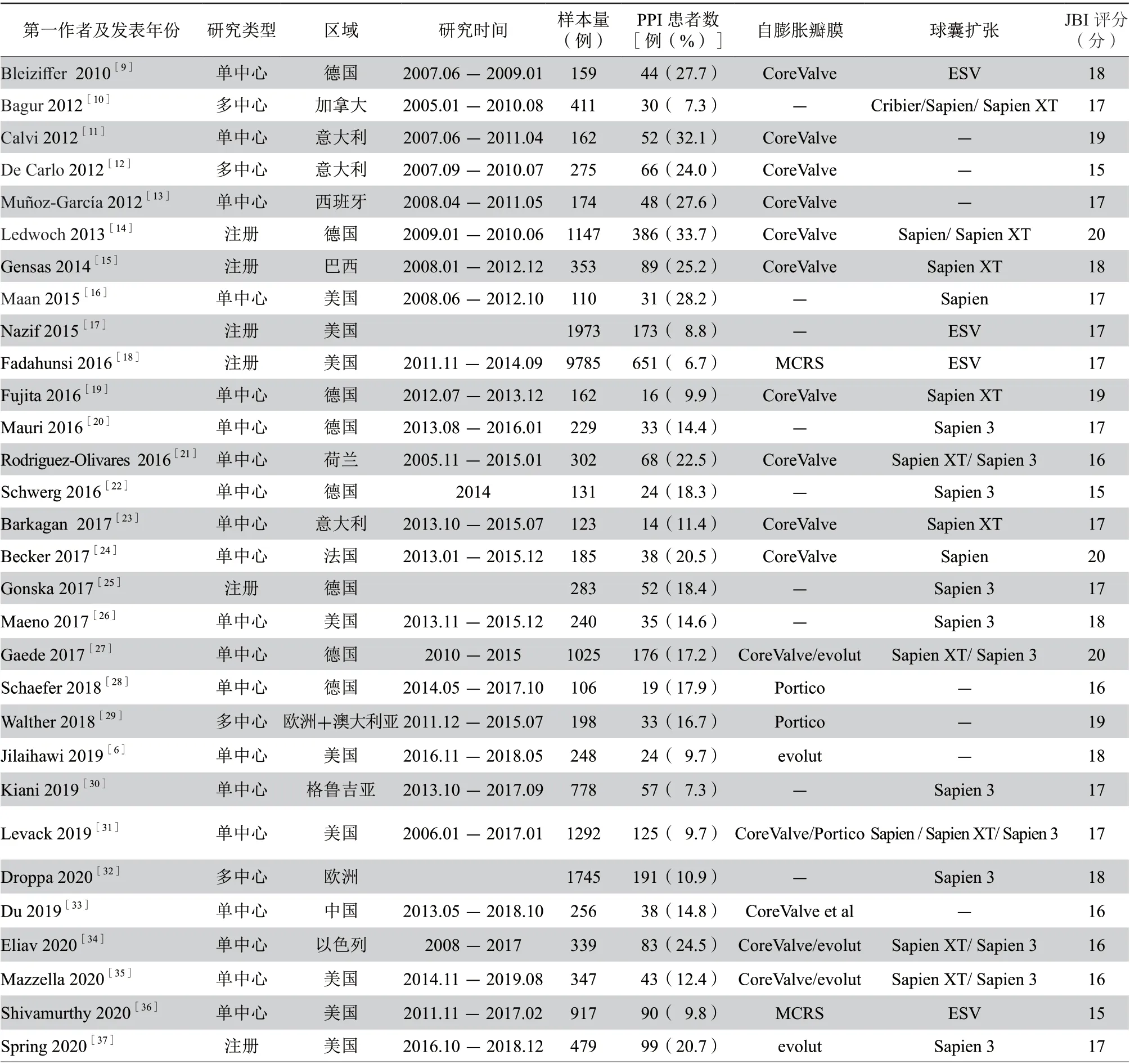
表1 研究特征
2. 3 危险因素指标
经过综合及偏倚性分析后,留下供总体分析的预测指标有20个,其中二分类变量9个:性别、心房颤动、左前分支传导阻滞(left anterior fascicular block,LAFB)、LBBB、右束支传导阻滞(right bundle branch block,RBBB)、一度房室传导阻滞(atrioventricular block,AVB)、预扩张、后扩张、瓣膜类型;连续性变量11个:年龄、Euroscore评分、PR间期、QRS波宽度、瓣口面积、瓣环直径、流出道内径、左心室舒张末期内径、室间隔厚度、置入深度、瓣膜尺寸超出程度。进行分层分析时:自膨胀瓣膜可供分析的预测指标有7个,分别为:年龄、性别、心房颤动、LBBB、RBBB、瓣环内径、置入深度;球囊扩张瓣膜可供分析的预测指标有8个:年龄、性别、Euroscore评分、心房颤动、LBBB、RBBB、一度AVB、QRS波宽度。
2. 4 数据结果
2. 4. 1 PPI比例 总研究患者数23 934例,其中PPI 2828例(11.8%)。应用自膨胀瓣膜行TAVR患者5243例,术后PPI 1360例(25.9%,1360/5243);应用球囊扩张瓣膜行TAVR患者17 067例,术后PPI 1280例(7.5%,1280/17 067),球囊扩张瓣膜中Sapien/Sapien XT术后PPI比例为6.0%,Sapien 3术后PPI比例为12.1%(表2)。
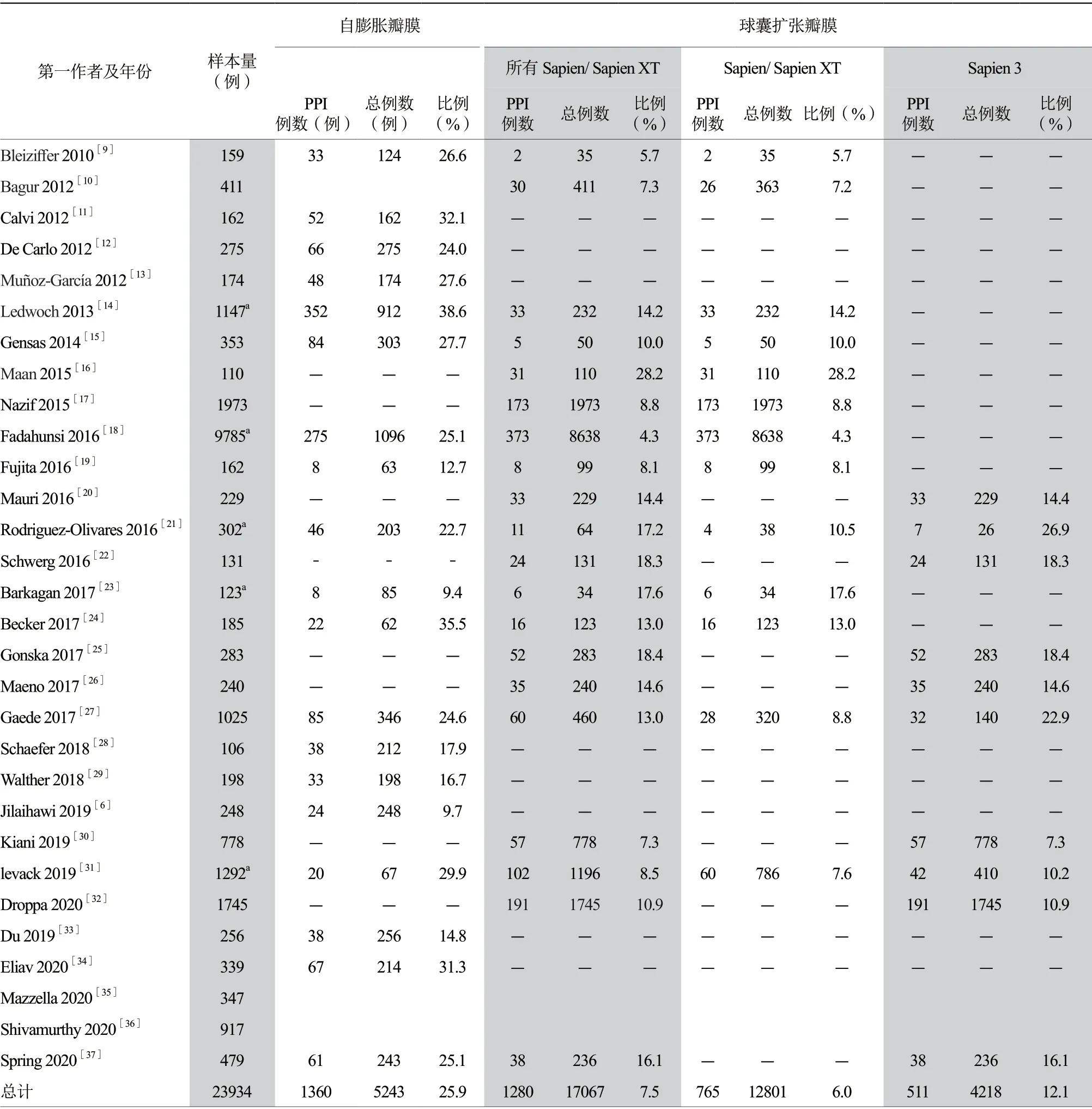
表2 瓣膜类型与TAVR 术后PPI
2. 4. 2 危险因素分析 本研究对20种潜在的TAVR术后PPI危险因素校正后进行Meta分析(表3)。结果显示,RBBB(OR5.39,95%CI4.73~6.14,证据级别++++)、自膨胀瓣膜较球囊扩张瓣膜(OR3.86,95%CI3.38~4.40,证据级别+++)与TAVR术后PPI风险显著相关;一度AVB(OR1.86,95%CI1.54~2.24,证据级别++)、男性较女性(OR1.17,95%CI1.07~1.28,证据级别++)亦增加TAVR后PPI风险。心房颤动、左前分支传导阻滞与TAVR术后PPI风险增加亦存在相关,但证据级别极低。术后PPI患者年龄较大(MD0.35,95%CI0.12~0.58,证据级别+)、PR间期较长(MD12.13,95%CI8.09~16.18,证据级别++)、基础QRS波较宽(MD6.59,95%CI5.40~7.77,证据级别++)、瓣口面积较大(MD0.03,95%CI0.02~0.04,证据级别+)、瓣环内径较大(MD0.86,95%CI0.79~0.93,证据级别+)、左心室舒张末期内径较大(MD1.6,95%CI1.57~1.64,证据级别+)、置入深度较深(MD1.29,95%CI0.99~1.58,证据级别++)。
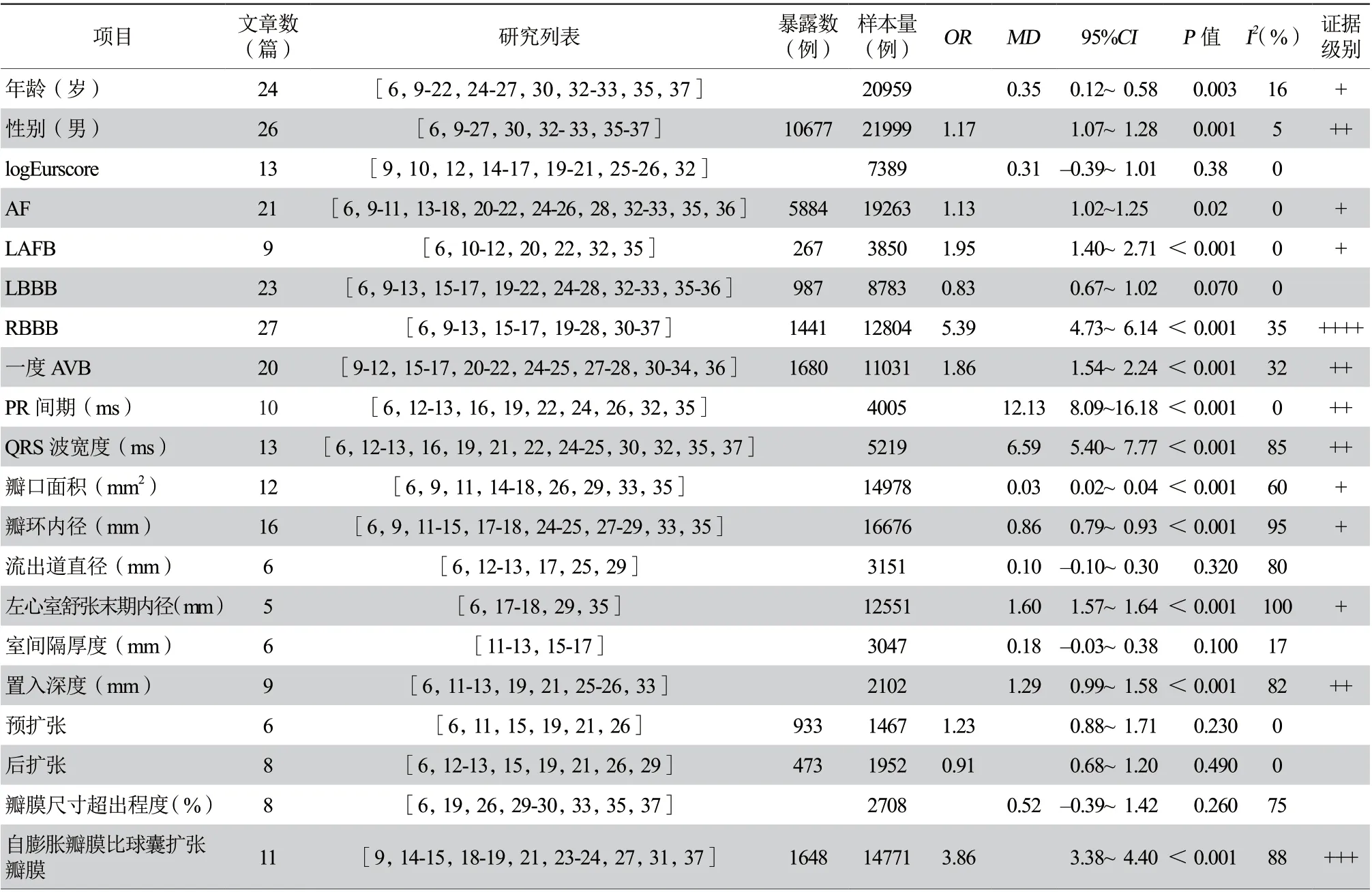
表3 TAVR 术后PPI 危险因素的Meta 分析及GRADE 证据分级
2. 4. 3 敏感性分析 剔除JBI评分<17分的8项研究后,对上述阳性指标进行Meta分析,并对比剔除前后结论差异(表4)。剔除后分析,男性较女性(OR1.18,95%CI1.05~1.32,证据级别+)、RBBB(OR5.27,95%CI4.50~6.16,证据级别++++)、一度AVB(OR1.87,95%CI1.44~2.43,证据级别++)、自膨胀瓣膜较球囊扩张瓣膜(OR4.01,95%CI3.51~4.59,证据级别+++)与TAVR术后PPI风险显著相关(图2 A)。同样术后PPI的患者PR间期较长、QRS波宽度较宽、置入深度较深(图2B)。
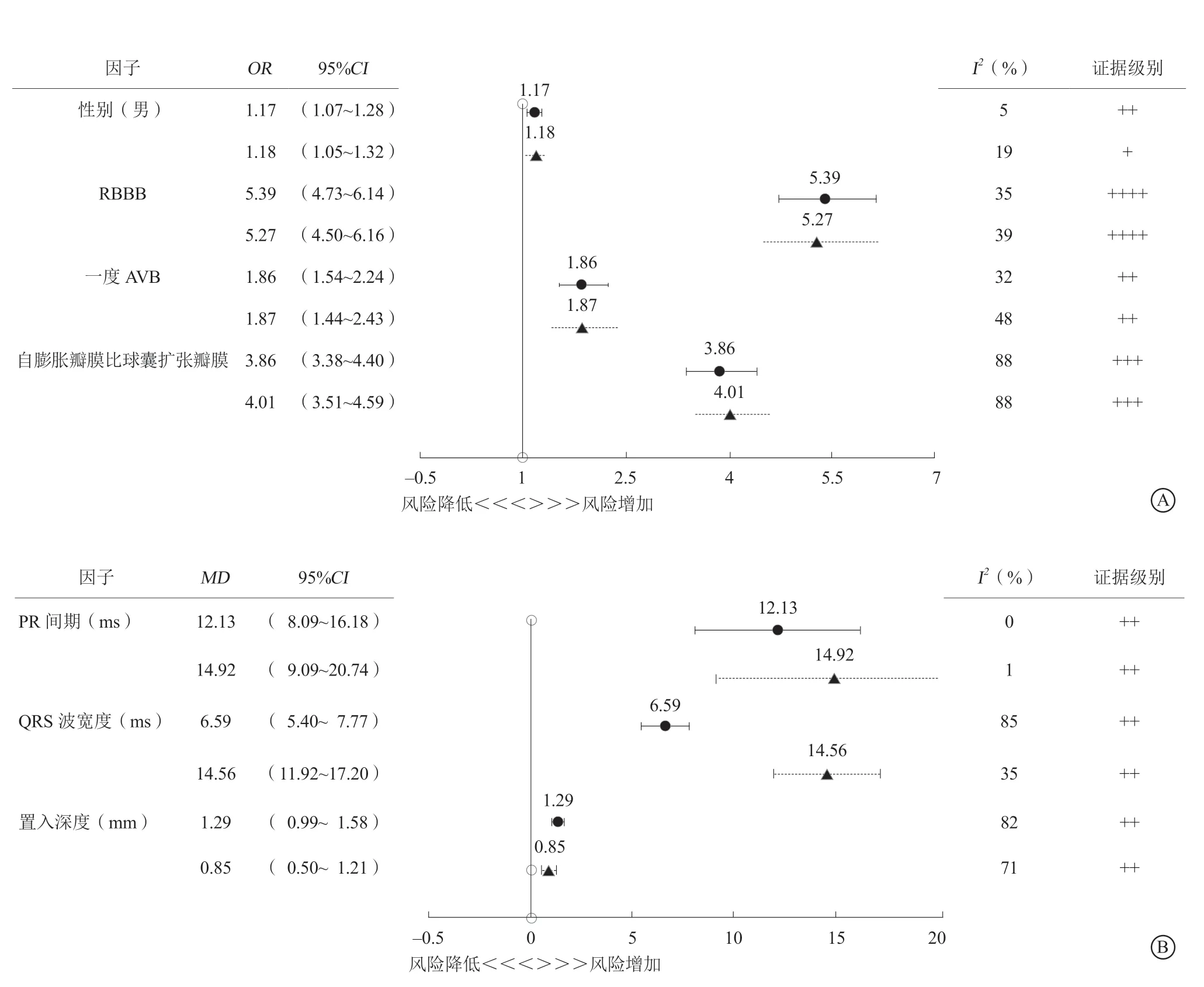
图2 TAVR术后敏感性分析森林图,所有研究分析阳性危险因素结果(黑点),剔除JBI评分<17分的研究后分析结果(三角) A. 二分类变量危险因素结果 ;B. 连续变量危险因素结果
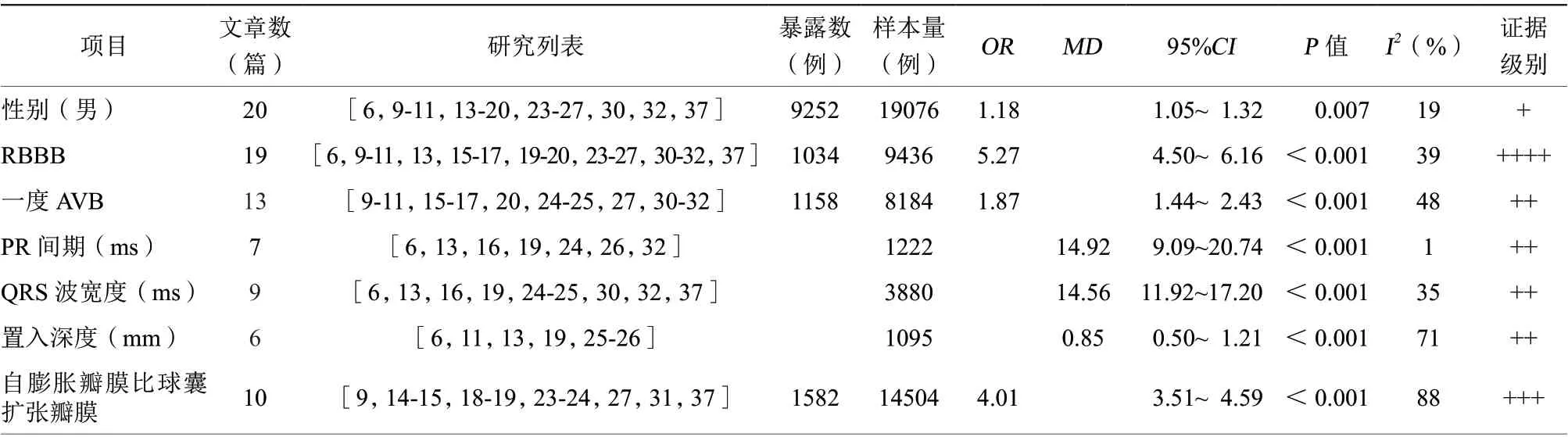
表4 TAVR 术后PPI 危险因素Meta 分析结论的敏感性分析
2. 4. 4 分层分析 进一步根据瓣膜类型分层校正进行Meta分析(表5),在应用自膨胀瓣膜行TAVR术患者中,RBBB(OR5.53,95%CI3.37~8.11,证据级别+++)与TAVR术后PPI风险增加显著相关,PPI组患者瓣环直径更大(MD0.49,95%CI0.20~0.78,证据级别+)、置入深度更深(MD1.60,95%CI1.20~2.01,证据级别++)。而在应用球囊扩张瓣膜行TAVR术患者中,RBBB(OR7.08,95%CI5.46~9.18,证据级别++++)与TAVR术后PPI风险增加显著相关,一度AVB(OR1.71,95%CI1.38~2.12,证据级别++)与TAVR术后PPI风险增加相关,而LBBB(OR0.64,95%CI0.46~0.89,证据级别++)与TAVR术后PPI风险增加负相关。PPI患者年龄较大(MD0.13,95%CI0.05~0.21,证据级别+)、QRS波较宽(MD15.45,95%CI12.26~18.65,证据级别++),见图3。
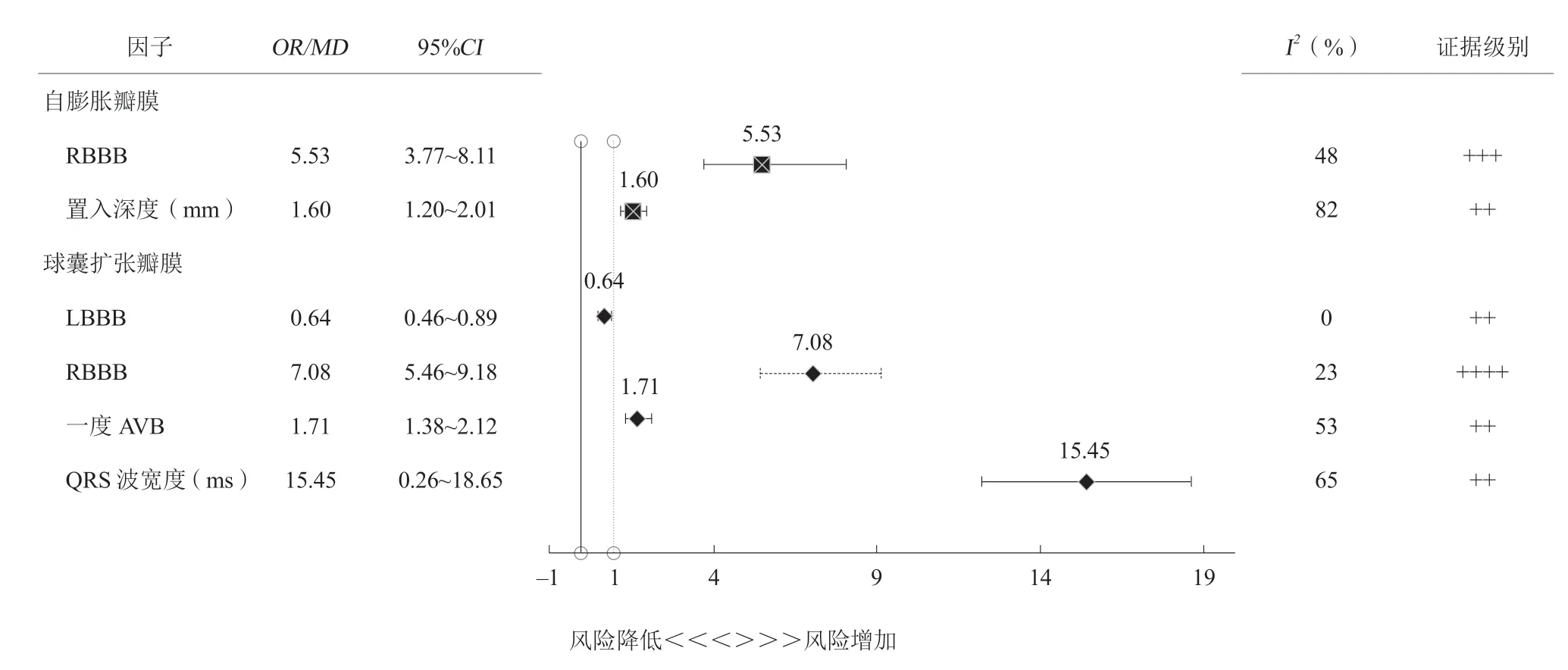
图3 不同类型瓣膜TAVR术后PPI危险因素Meta分析森林图
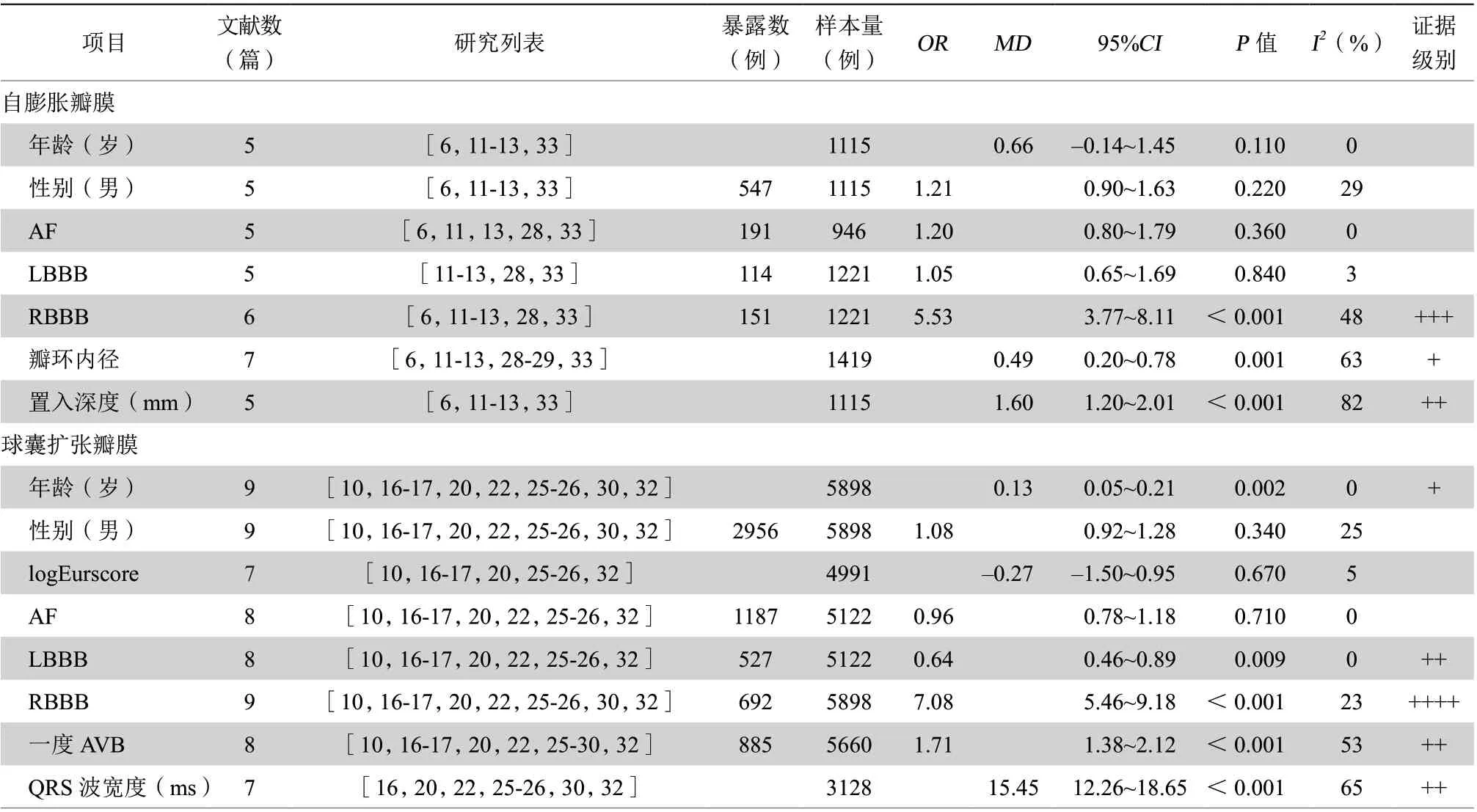
表5 不同类型瓣膜TAVR 术后PPI 危险因素的Meta 分析及GRADE 证据分级
3 讨论
本研究结果显示:(1)总体而言,PPI是TAVR术后一个比较常见的并发症,男性、基础存在心房颤动、LAFB、RBBB、一度AVB可能是TAVR术后PPI的预测因子;(2)无论何种瓣膜类型,PPI患者RBBB、一度AVB均有较高的风险;(3)自膨胀瓣膜较球囊扩张瓣膜在术后更容易导致PPI的发生,但新一代球囊扩张瓣膜Sapien 3术后PPI的发生率亦较上代瓣膜增加,自膨胀瓣膜与Sapien 3术后PPI的差异不如之前显著。
因固有主动脉瓣与房室传导系统的解剖学邻近,术中操作可能造成Koch三角区房室结区水肿或损伤,可能导致传导系统的异常或原有异常的加重。TAVR术后球囊扩张或瓣膜扩张过程中存在直接损伤房室结或左束支的可能,这是导致TAVR术后无论何种瓣膜都存在较高PPI风险的机制。球囊扩张瓣膜因其较少的瓣膜支撑结构而PPI风险相对较低,而Sapien 3瓣膜为减少瓣周漏的发生而设计带有袖部,这一设计导致其术后PPI的风险相对升高。但本研究提示Sapien 3相较于上代Sapien XT术后PPI风险的差异并无统计学意义。自膨胀瓣膜存在较长的瓣膜支撑部分进入左心室流出道,进而导致对传导系统造成损伤,故其在术后PPI风险明显要高于球囊扩张瓣膜。自膨胀瓣膜因其材质问题术后仍存在残余的膨胀,亦可能导致延迟的传导阻滞[38]。
完全性RBBB是目前公认的预测TAVR术后PPI的因素[39],一度AVB也在一些研究中显示出与TAVR术后PPI存在较高的相关关系[24-25,32],这也与上述解剖关系明确相关。希氏(His)束紧邻室间隔膜性,特别是左束支靠近位于右侧和非冠状瓣之间的叶间三角的基部,故瓣膜置入有可能损伤左束支,进而导致房室传导的进一步加重。在既往研究中,包括室间隔膜部长度[26,40]、置入深度[12-13]、左心室流出道厚度[21]等均与术后新发LBBB及PPI相关。而钙化分布不均[40]或左冠状瓣钙化[19]的加重有可能增加瓣膜释放后对对侧(即室间隔膜部侧)的挤压,进而导致传导阻滞的发生。本研究亦提示PPI组患者存在瓣膜置入深度更深、左冠状动脉瓣钙化积分(left coronary cusp calcium volume,LCC)更高,但并未得出两组左心室流出道厚度的差异,这可能与临床上瓣膜尺寸选择策略相关。
心房颤动也与TAVR术后PPI相关。Mazzella等[35]的研究指出,心房颤动/心房扑动与早期PPI无明显相关,但对于晚期PPI还是存在差异,这可能与引起心房颤动的本身窦房结功能不全或持续性心房颤动房室结功能减退有关。
本研究仍发现男性的PPI风险增加。这在TAVR患者预后性别差异的研究中被提到,女性患者年龄更高且合并症较多,但术后PPI的风险要比男性低30%[41]。Amgai等[42]的研究也指出,女性相对男性PPI的风险要低60%,研究者考虑是因为女性患者左心室流出道、瓣环及瓣口面积相对要小,所以导致根据结构选择瓣膜尺寸时比较保守相关。
本研究存在以下局限:(1)所有纳入的研究均为横断面研究,使本研究结果有一定的局限性;(2)存在较高的估计异质性,这可能与不同的设计、研究区域和研究人群有关;(3)部分潜在预测因素因数据不足未进行荟萃分析,如室间隔膜部长度与置入差值、二瓣化主动脉瓣、瓣环因素、着陆区钙化、S状室间隔(局限性间隔沙丘状增厚,男性>13 mm,女性>12 mm,较室间隔中段增厚超过50%)[43]等。综上所述,临床结论需要结合其他指标进行综合评价,需要增加更多的样本量和研究来验证我们的结果。
本研究结果表明,TAVR术后PPI的比例平均为11.8%,自膨胀瓣膜TAVR术后PPI比例平均为25.9%,球囊扩张瓣膜为7.5%。RBBB、瓣膜类型、一度AVB、性别、基础PR间期、QRS波宽度及瓣膜置入深度可作为TAVR术后PPI的预测因子。进一步可设计预测评分系统来协助临床术后PPI风险的判断。亦可以协同术后快速起搏观察有无文氏型房室传导阻滞现象来协助评估术后PPI的风险[44]。还需大规模和前瞻性的研究来进行验证。
利益冲突 所有作者均声明不存在利益冲突
