反相高效液相色谱法测定枯草杆菌二联活菌颗粒中甜菊糖苷的含量
2016-06-20孙菲孙欣
孙 菲 孙 欣
反相高效液相色谱法测定枯草杆菌二联活菌颗粒中甜菊糖苷的含量
孙 菲 孙 欣
【摘要】目的 建立反相高效液相色谱(RP-HPLC)法测定枯草杆菌二联活菌颗粒中甜菊糖苷的含量。方法 选用AgiLent Zobax SB-C18(250 mm×4.6 mm,5 μm)为色谱柱,线性梯度洗脱,流动相为乙腈-0.002 mol/L磷酸溶液;检测波长为210 nm;流速1.0 ml/min;进样量10 μl;柱温30 ℃。结果 甜菊糖苷的线性范围为5.160~103.2 g/ml(r=0.9999,n=7);提取回收率为99.04%(RSD为0.6%,n=6)。结论 本法操作简便、准确,可用于枯草杆菌二联活菌颗粒的质量控制。
【关键词】枯草杆菌二联活菌颗粒;含量测定;甜菊糖苷;反相高效液相色谱法
鸡西市食品药品检验检测中心,黑龙江鸡西 158100
甜菊素又称甜菊糖或甜菊糖苷,是一种天然的甜味剂,文献[1-5]报道其高甜度、低热量、稳定性好、安全性高,且具有降血糖、抑菌等特性,被广泛应用于各类食品、饮料、医药、日化工业,作为药用辅料收载在《中国药典》中。枯草杆菌二联活菌颗粒为儿童专用药品,适用于因肠道菌群失调引起的腹泻、便秘、胀气、消化不良等。甜菊素作为枯草杆菌二联活菌颗粒辅料中的甜味剂,现行标准未对其含量进行质量控制,反相高效液相色谱(RP-HPLC)法排除了其他成分的干扰,可以准确地检测出枯草杆菌二联活菌颗粒中甜菊糖苷的含量,为药物质量控制提供依据。
1 仪器与试药
1.1 仪器 HP1100高效液相色谱仪(安捷伦公司),HP1100工作站(自动进样,紫外检测器),METTLER TOLEDO电子天平(XSE 205),JAC-40型超声波清洗器(功率:300 W,频率:40 KHz,济宁市奥波超声电器有限公司),UV-2550紫外-可见分光光度计(苏州岛津)。
1.2 试药 甜菊糖苷对照品(20150701,含量98.0%,曲阜圣仁制药有限公司),市售枯草杆菌二联活菌颗粒3批(北京韩美药品有限公司,批号:20150531、20150419、20150509),水为娃哈哈纯净水,乙腈(TEDIA)色谱纯,甲醇(科密欧)色谱纯,磷酸(天津市恒兴化学试剂制造有限公司)分析纯。
2 方法与结果
2.1 色谱条件与系统适用性实验 选用AgiLent Zobax SB-C18(250 mm×4.6 mm,5 μm)为色谱柱,流动相以乙腈(A)-0.002 mol/L磷酸溶液(B),按照表1比例,进行线性梯度洗脱;流速1.0 ml/min;检测波长为210 nm;进样量10 μl;柱温30 ℃。理论板数以甜菊糖苷计不低于7000,甜菊糖苷与相邻峰的分离度均符合要求。
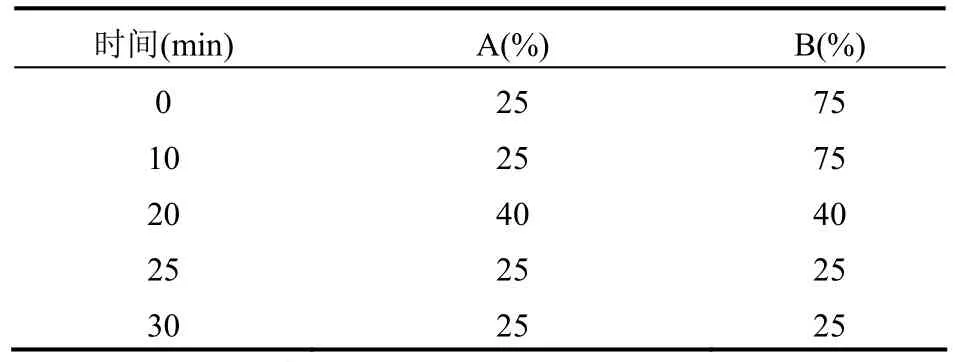
表1 线性梯度洗脱程序
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取甜菊糖苷对照品21.06 mg(含量98.0%)置20 ml量瓶中,加乙腈-0.002 mol/L磷酸溶液(25:75)适量,超声使其溶解,加上述溶液稀释至刻度,作为对照品溶液。
2.2.2 供试品溶液的制备 精密称取样品适量(约1 g)置100 ml量瓶中,加乙腈-0.002 mol/L磷酸溶液(25:75)40 ml,超声提取10 min(功率:300 W,频率:40 KHz),放置至室温,加上述溶液稀释至刻度,摇匀,滤过,精密量取续滤液1.0 ml置20 ml量瓶中,加上述溶液稀释至刻度,摇匀,作为供试品溶液。
2.2.3 阴性对照溶液的制备 按枯草杆菌二联活菌颗粒的处方,不加甜菊素,依法制备阴性样品,按2.2.2项下供试品溶液制备的方法制备阴性对照溶液。分别取对照溶液、供试品溶液、阴性对照溶液,微孔滤膜滤过,按上述色谱条件,分别进样,色谱图见图1。
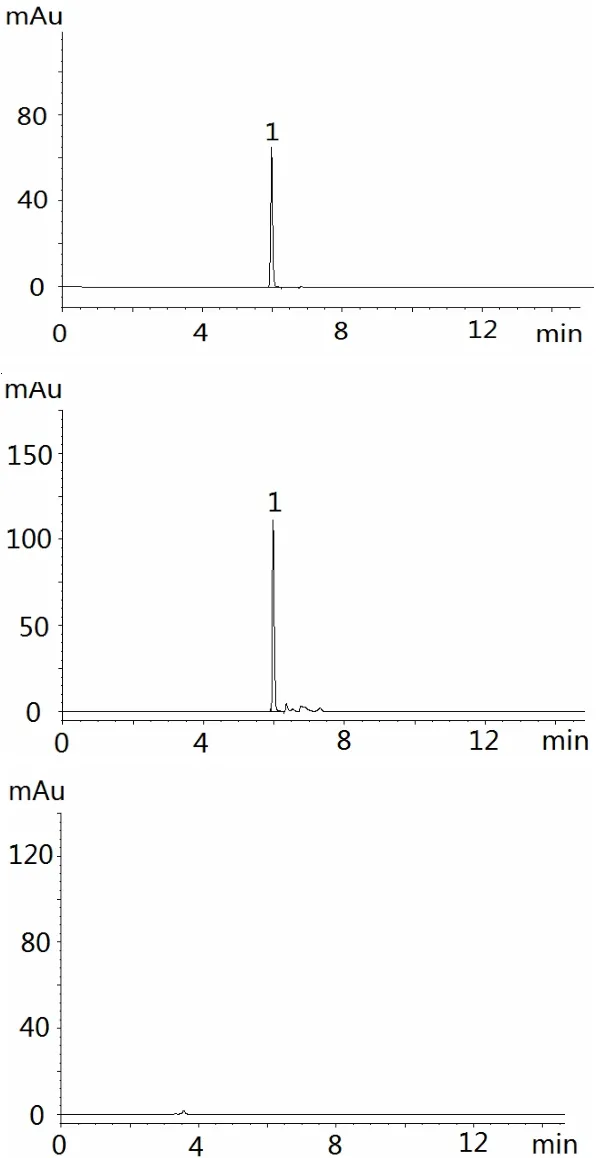
图1 对照品溶液、供试品溶液和阴性对照溶液HPLC色谱图(1为甜菊糖苷)
2.3 线性关系考察 精密量取2.2.1项下的对照品溶液0.1、0.2、0.4、0.5、0.8、1.0、2.0 ml置20 ml量瓶中,按上述色谱条件,分别进样10 μl,以色谱峰面积Y对应进样浓度X(μg/ml)进行回归分析,可得:甜菊糖苷回归方程Y=29.27X-2.562,r=0.9999 (n=7),甜菊糖苷在5.160~103.2 μg/ml浓度范围内线性良好。
2.4 精密度实验 精密量取2.2.1项下的对照品溶液0.5 ml置20 ml量瓶中,加乙腈-0.002 mol/L磷酸溶液(25:75)至刻度,得浓度为25.80 μg/ml对照品溶液。摇匀,微孔滤膜滤过,连续重复进样5次,每次10 μl,记录色谱图峰面积,测得甜菊糖苷峰面积值的RSD为0.4%(n=5),实验结果表明仪器精密度良好。
2.5 稳定性实验 精密称取样品适量(约1 g),按2.2.2项下方法制备成供试品溶液,分别在供试品溶液配制后的0、2、4、8、12、16、24 h,按上述色谱条件,分别进样10 μl,记录色谱图峰面积,测得甜菊糖苷峰面积的RSD为0.5%(n=7),实验结果表明甜菊糖苷在24 h内稳定。
2.6 重复性实验 分别精密称取同一批号供试品(批号:20150531)5份,按2.2.2项下的方法制备供试品溶液,按上述色谱条件,分别进样10 μl,记录色谱图峰面积,测量甜菊糖苷的平均含量为39.28 mg/袋,RSD为0.8%(n=5),实验结果表明方法重复性较好。
2.7 回收率实验 精密称取已知含量的样品(批号:20150531)约0.5 g,6份,分别置100 ml量瓶中,另精密称取甜菊糖苷对照品相当于甜菊糖苷纯品20 mg,6份,分别置上述100 ml量瓶中,按2.2.2项下的方法制备溶液,用微孔滤膜滤过,进样10 μl,结果甜菊糖苷平均回收率为99.04%(RSD=0.6%,n=6),见表2。
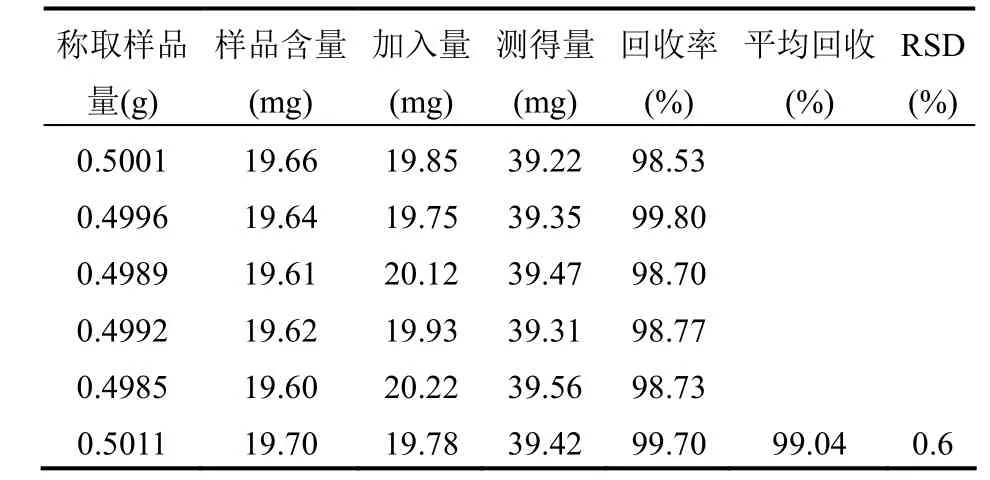
表2 甜菊糖苷回收率实验测定结果
2.8 样品含量测定 取本品6袋,精密称定,混匀,研细,精密称取本品适量(约相当于1 g)按2.2.2项下的方法制备供试品溶液,每一批号平行制备3份供试品溶液,按上述色谱条件,分别进样10 μl,记录色谱图峰面积,根据峰面积外标法计算3批市售样品中甜菊糖苷的含量,结果见表3。
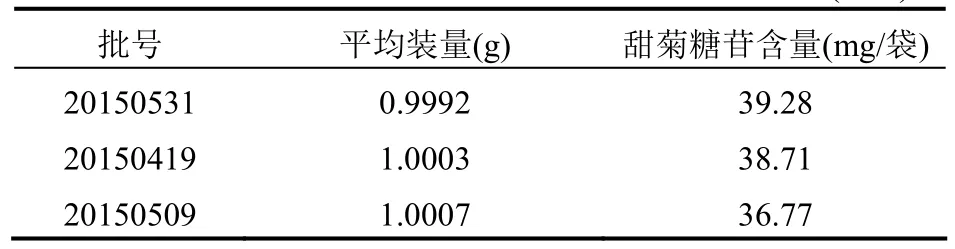
表3 市售枯草杆菌二联活菌颗粒含量测定结果(n=3)
3 讨论
3.1 检测波长的选择 取对照品溶液在190~500 nm波长范围内进行紫外扫描,在210 nm波长处有最大吸收,故检测波长设为250 nm,实验图谱基线平稳,效果较好。
3.2 色谱选择 实验过程中分别考察了AgiLent Zobax SB-C18(250 mm×4.6 mm,5 μm)和AgiLent Zobax SB-C18(150 mm×4.6 mm,5 μm)两种色谱柱。实验结果表明,150 mm短柱柱效较250 mm长柱低,且甜菊糖苷保留时间过短,甜菊糖苷色谱峰和相邻色谱峰不能有效分离,选用250 mm长柱取得了较好的分离效果。
3.3 流动相的考察 实验过程中分别考察了以甲醇-水、乙腈-水、乙腈-0.002 mol/L磷酸溶液为流动相,结果表明乙腈-0.002 mol/L磷酸溶液为流动相,甜菊糖苷色谱峰形最好,且保留时间适宜。
3.4 文献[6]报道了容量法和RP-HPLC法测定甜菊糖苷含量的比较,表明RP-HPLC法能有效排除干扰,更加客观准确。待测物质甜菊糖苷分离出后,采用梯度洗脱能快速洗脱其他物质,排除实验干扰,有效提高分离效率,充分体现RP-HPLC法的高效、准确、便利等特性。
3.5 甜菊糖苷具有“天然、绿色、安全、保健”等诸多优点,文献[7-8]探讨了甜菊素代替蔗糖在中药制剂中应用,在未来的医药发展中甜菊素作为甜味剂应用将更加广泛。药用辅料质量对药品的体内溶出、释放、代谢都起着重要作用,随着药品质量标准的不断提高和完善,药品辅料逐渐增加到标准中,因此本法的建立是对现行标准的有效补充和提高。
参考文献
[1] 王飞生,叶荣飞,闵建.甜菊糖苷的特性及应用[J].中国调味品,2009,34(10):91-95.
[2] 朱焕铃,刘景彬,谢印芝.甜菊糖甙的性质及在食品中的应用[J].食品研究与开发,2011,32(11):189-192.
[3] 王贵民,董振红,郝再彬.甜叶菊糖苷的应用和安全性的研究进展[J].中国食品添加剂,2007(6):65-69.
[4] 娄力行.甜菊糖及其衍生物的研究进展[J].中国糖料,2008(2):70-72.
[5] 曹芳,冯文静,陈明,等.甜菊糖苷降糖作用研究[J].中国药物与临床,2009,9(2):127-127.
[6] 刘景彬,刘安军,战虎,等.容量法与HPLC法测定甜菊糖甙含量结果的比较[J].食品科技,2009,9(2):127-127.
[7] 钱丽明.关于中药制剂用甜菊苷替代蔗糖的探讨[J].时珍国医国药,2005,16(2):139-139.
[8] 元新峰,张树红.浅谈甜菊甙在中药制剂中的应用[J].中国医药前沿,2008,13(3):103-103.
Determination of Steviosin in Combine Bacillus Subtilis and Enterococcus Faecium Granules with Multivitamines,live By RP-HPLC
Sun Fei Sun Xin
【Abstract】Objective To establish RP-HPLC method for determination of Steviosin in Combine Bacillus Subtilis and Enterococcus Faecium Granules with Multivitamines,live.Methods Using a column packed with AgiLent Zobax SB-C18(250 mm×4.6 mm,5 μm);The mobile phase was acetonitrile-0.002 mol/L H3pO4by gradient elution and the detection wavelength was 210 nm;the flow rate was 1.0ml/min,the injection volume was 10 μl,the column temperature was 30 ℃.Results The Linear response of Steviosin range from 5.160~103.2 μg/ml r=0.9999(n=7);The average recovery of Steviosin was 99.04%,RSD= 0.6%(n=6).Conclusion The method is convenient and accurate and can be used for the quality control of Combine Bacillus Subtilis and Enterococcus Faecium Granules with Multivitamines,live.
【Key words】Combine Bacillus Subtilis and Enterococcus Faecium Granules with Multivitamines,live;Determination;Steviosin;RP-HPLC
【中图分类号】R927.2
【文献标志码】A 【DOI】10.12010/j.issn.1673-5846.2016.06.004
作者简介:孙菲(1981.12-),副主任药师。研究方向:药品检验。E-mail:chenlizhu1980@163.com
