肝硬化门静脉高压症腹腔镜与开腹治疗的临床对照研究
2016-05-25张安澎向俊西刘鹏张谞丰吕毅刘学民
张安澎 向俊西 刘鹏 张谞丰 吕毅 刘学民
·论 著·(门静脉高压症外科专题)
肝硬化门静脉高压症腹腔镜与开腹治疗的临床对照研究
张安澎 向俊西 刘鹏 张谞丰 吕毅 刘学民
目的 比较腹腔镜与开腹脾切除加贲门周围血管离断术治疗门静脉高压症的临床效果及安全性,探讨腹腔镜脾切除是否增加了门静脉血栓形成的发生率。方法 自2013年1月到2015年12月,有204例病人因诊断为门静脉高压症行腹腔镜或开腹脾切除术。详细收集临床资料并进行回顾性分析,评估临床疗效,并对血栓形成的可能危险因素进行单因素及多因素回归分析。结果 84例病人采用腹腔镜手术,其中18例中转开腹,120例施行开腹手术。完全腹腔镜组(66例)和开腹组(120例)比较,手术时间、术中出血量及输血率相似,腹腔镜组与开腹组术后平均住院时间差异有统计学意义[(11.0±4.0) d比(12.6±5.4) d,P=0.032],两组间术后门静脉血栓形成差异无统计学意义[19例(28.8%)比32例(26.7%),P=0.756)。脾脏长径≥20 cm、术后住院时间>10 d是门静脉血栓形成的独立危险因素(P<0.05)。结论 腹腔镜脾切除术的近期疗效优于传统开腹手术,相对于开腹脾切除术,前者并未增加门静脉血栓的发生率。
腹腔镜;脾切除术;门静脉高压症;门静脉系统血栓形成
肝炎后肝硬化所致的门静脉高压症,常伴有食管胃底静脉曲张及脾功能亢进,存在上消化道出血的风险,具有较高的死亡率。脾切除加贲门周围血管离断术(esophagogastric devascularization,ED)是治疗门静脉高压症的一种有效的外科手术[1],可以同时解决上消化道出血及脾功能亢进的问题。随着腔镜外科手术技术的不断发展成熟,以及新型止血器械的发明和进步,腹腔镜脾切除术(laparoscopic splenectomy,LS)已得到越来越多地临床推广应用[2]。近年来,脾切除术后门静脉血栓的发生越来越受到重视,严重的门静脉血栓明显增加了肝硬化病人行肝移植手术的术中风险,影响了移植病人的预后。相比于开腹脾切除术,腹腔镜脾切除是否增加了血栓发生率值得关注。本研究比较了LS与传统开腹脾切除手术(open splenectomy,OS)的临床效果及安全性,统计分析了本中心行LS和OS共204 例的临床资料,现报告如下。
资料与方法
一、临床资料
2013年1月至2015年12月,我院收治门静脉高压症行脾切除术的病人共204例,其中男性110例,女性94例,有上消化道出血史者102例(50.0%),LS 84例,OS 120例。纳入手术的指征[3]为:①经反复多次内镜治疗后仍有出血的病人;②食管静脉曲张部位广泛,程度严重,迂曲粗大,尤其是伴有胃底静脉曲张者;③伴有明显脾肿大及脾功能亢进;④18~70岁,一般状况及重要脏器功能满足手术的指征,并能耐受CO2气腹者。排除标准包括:胰腺肿瘤行胰体尾联合脾切除者、胃癌扩大根治联合脾切除术者、恶性肿瘤脾脏转移联合脾切除者、合并免疫缺陷疾病、长期激素治疗史。详细记录人口学资料、原发疾病、手术史、出血史、术前检查、手术方式、手术指标、术后住院日、腹腔引流时间、术后并发症等情况,并进行回顾性分析。
LS组(66例,余18例中转开腹)和OS组(120例)的临床资料比较,两组病人在年龄、性别、既往腹部手术史、上消化道出血史等术前手术条件上差异无统计学意义,具有可比性(表1)。
二、手术方法
1.LS+ED 全身麻醉,气管内插管,常规留置胃管及尿管。头高足低约15°~30°仰卧位,左侧酌情抬高10°~20°。CO2气腹压力约12~15 mmHg,脐下置入10 mm Trocar作为观测孔,直视下分别于左锁骨中线脐水平、左腋前线脾下极下方、脐与剑突连线中点处分别设置主操作孔及辅助操作孔,根据脾脏情况进行调节以保证良好的操作空间。仔细探查腹腔及肝脾情况,打开胃结肠韧带,暴露脾动脉,两枚血管夹双重夹闭并离断。应用LigaSure血管闭合器离断脾结肠韧带、脾肾韧带,紧靠胃大弯侧切断脾胃韧带。打开脾蒂前层游离脾蒂,紧靠脾脏仔细分离二级脾蒂血管,对直径小于5 mm的血管用LigaSure紧贴脾门直接离断,对直径大于5 mm的血管,可用Hem-o-lok夹闭后离断。如此逐渐向脾上极分离。如术中脾蒂不易游离,则采用直线型切割闭合器逐步切断脾蒂,彻底游离脾脏。大部分门静脉高压症病人需同时行贲门周围血管离断术,根据术中情况,用超声刀或LigaSure分离胃周围组织及韧带,打开小网膜,离断食管下段约5~7 cm、胃上半部分周围血管及其分支,并充分游离。将脾脏装入标本袋中夹碎,经延长的刺口处取出。冲洗腹腔,检查脾窝及术野无活动性出血后,脾窝留置腹腔引流管,缝合切口。
2.OS+ED 全身麻醉,气管插管,采用左上腹部“L”形切口。主要操作过程与LS类似,约半数病人先予结扎脾动脉,再切断脾周围韧带,分次结扎和切断脾蒂血管,切除脾脏。同时离断胃短静脉,完全离断胃冠状静脉的胃支、食管支、高位食管支或存在的异位高位食管支;结扎离断胃后静脉及左膈下静脉。同时结扎离断与上述静脉伴行的同名动脉,阻断门奇静脉之间的反常血流。常规脾窝处放置引流管,逐层关腹。术中主要以传统的手术器械给予结扎或缝合。

表1 两组病人术前一般临床资料对比±s)
三、统计学处理

结 果
LS组中有18例病人中转开腹,中转率为21.4%。主动中转11例,主要原因是空间狭小,操作困难,预计有大出血可能;被动中转7例,因术中出血较多,难以有效止血。中转开腹直接原因包括:脾周严重粘连致操作困难3例(16.7%),巨脾脾门显露困难3例(16.7%),脾动脉显示不清、脾门结构复杂4例(22.2%),胃冠状静脉重度曲张预计出血1例(5.6%),游离时脾及血管破裂出血6例(33.3%),胰腺尾部活动性出血,延长取脾切口1例(5.6%)。
两组病人脾脏长径及食管胃底静脉曲张差异有统计学意义,详见表1。
LS组有44例联合行断流术,占66.7%;OS组有104例,占86.7%。LS组与OS组比较,平均手术时间、术中出血量、术中输血量、门静脉血栓形成发生率差异均无统计学意义。LS组术后脾窝引流管引流时间较OS组更短(P=0.041),LS组术后住院时间也较OS组更短(P=0.032),差异有统计学意义(表2)。
对可能影响术后门静脉血栓形成的危险因素进行单因素分析,结果提示,脾脏长径≥20 cm及术后住院时间>10 d是术后门静脉血栓形成的危险因素,而腹腔镜手术并不是其危险因素,详见表3。
进一步将门静脉血栓是否形成作为因变量,脾脏长径、术中是否输注红细胞及术后住院时间作为自变量进行非条件性二元多因素Logistic回归分析,结果提示(表4),脾脏长径≥20 cm、术后住院时间>10 d是门静脉血栓形成的独立危险因素(P<0.05)。
讨 论
在我国,肝硬化门静脉高压症和继发性脾功能亢进是常见病,其中部分病人需手术治疗,传统上行OS+ED,创伤较大,术后腹腔粘连严重,增加了后续的肝移植手术的难度。随着腹腔镜技术的发展和超声刀、LigaSure等的应用[4],肝硬化门静脉高压症和继发性脾功能亢进病人行LS已成为常规术式。LS中充分利用30°腹腔镜,可以多角度、多方位调整手术视野,更容易暴露狭窄的空间,3~5倍放大的图片使视野清晰,超声刀或LigaSure设备极少产生烟雾和焦痂,同时可以完全阻断食管和胃底周围的曲张血管[5],避免了由于结扎滑脱引起的术后出血。
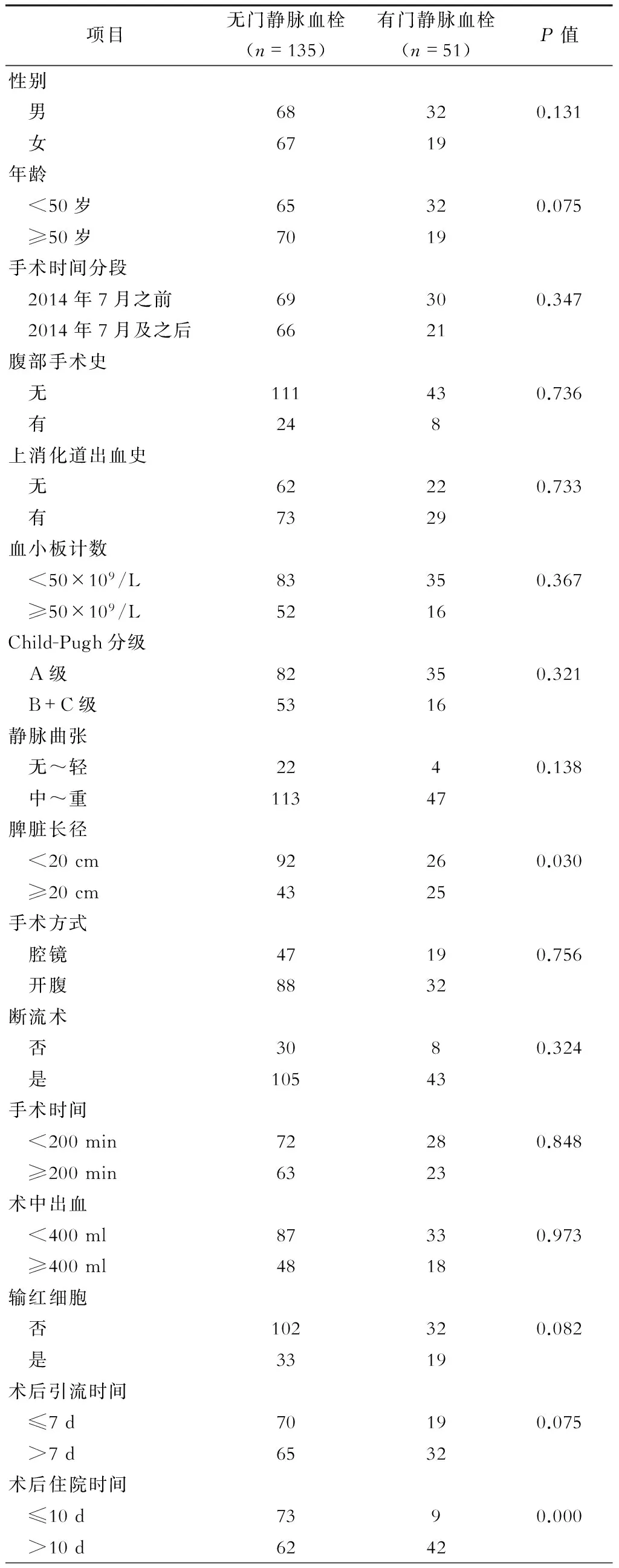
表3 门静脉血栓形成危险因素单因素分析(例)

表2 手术效果对比±s)

表4 门静脉血栓形成危险因素Logistic回归分析
在本研究中,LS和OS手术组有相同的纳入、排除标准,相同的操作步骤(即先结扎脾动脉,其次是充分游离脾脏,然后解剖结扎脾门,并最终离断贲门周围血管)。这两者之间的唯一区别是手术路径。但术者处于早期学习期时技术不够熟练,脾脏长径较大和静脉曲张较严重的病人多选择开腹手术治疗,而随着手术技术熟练和临床经验的积累,术者更倾向于完成难度大的腔镜手术。
LS组病人的手术时间与OS组比较差异无统计学意义,且术中出血及输血量的差异也无统计学意义。但腹腔镜下手术视野被放大,且视野清晰,可转换视角,变相地增加手术空间,联合使用腹腔镜器械(如超声刀、LigaSure等)更快更方便,对小血管不需要结扎或缝合,同时节省了开腹及关腹时间。根据一些腹腔镜手术的学习曲线,手术时间在不同的中心明显不同,主要取决于经验和技能[6]。随着术者经验技术的积累,腹腔镜手术器械的改进和完善,相信LS的手术时间会逐渐缩短,并能降低LS的中转开腹率[7]。
微创手术对机体免疫及细胞因子水平影响较小,创伤反应弱,有助于肝硬化病人术后肝功能的恢复[8],同时避免了开腹手术中应用纱布垫对小肠、结肠的包裹,减少了对肠道浆膜的刺激;也避免腹腔脏器同空气和空气中的细菌尘埃的接触和污染[9],可以减少术后脾窝引流管引流时间。术中腹腔引流管放置依手术情况而定,本中心常规放置脾窝引流管,有利于排出术野的积液和积血,并检测是否有腹腔出血和胰漏发生,可以防止感染形成及扩散,有助于避免发生腹膜炎和二次手术,对于少量胰漏,经过持续引流可治愈。如引流无异常,尽早拔除腹腔引流管,以减少其引起的疼痛,方便病人术后早期下床活动,有助于早期康复。早期下床活动可加快肠蠕动,提高肺活量,增强抗病能力,加快体质恢复,同时加速切口部位血液循环,促进切口愈合及下肢静脉回流,预防术后深静脉血栓形成[10],并能降低门静脉血栓的发生率。
脾脏手术相对较大,且术中联合行贲门周围血管离断术,会对胃及食管的功能造成损伤,术后胃肠道恢复较慢,因此多在通气后嘱病人进流食,并逐渐过渡为普食。与开腹手术相比,腔镜手术对腹腔器官创伤更小,病人术后胃肠功能恢复更快,通气时间更早[11]。早期进食不仅促进肠蠕动恢复,维护肠黏膜功能,而且可以促进切口愈合,增加内脏血流量,减轻病人疲劳感,利于术后病人的康复[12],并缩短术后住院时间。
门静脉系统血栓(portal venous system thrombosis,PVST)是脾切除术后的常见并发症。由于大量的肝硬化病人在终末期阶段需行肝移植手术延长病人的生命,而严重的PVST明显增加了术中的风险并影响近远期预后,是肝移植手术的相对禁忌证。因此OS或LS+ED在术后PVST形成和发展中的作用值得研究。有些研究表明手术方式对PVST的发病率没有影响[13],PVST形成的主要原因是术后门静脉系统血流动力学的改变,血管内皮的损伤以及血液凝固性的改变[14]。在既往的回顾研究中,我们发现近年来LS的PVST发生率呈上升趋势,这可能和术后门静脉系统的影像学检查成为常规有关。而该发生率升高的原因是否与腹腔镜手术增多有关尚不清楚。在本研究中,我们证实同一时期内LS组的PVST形成与OS组[19例(28.8%)比32例(26.7%),P=0.756]差异无统计学意义,LS并不是PVST的危险因素。门静脉血栓形成危险因素的Logistic回归分析结果表明,脾脏长径≥20 cm,术后住院时间>10 d是PVST形成的独立危险因素(P<0.05),考虑与术前脾功能亢进的程度及术后早期活动锻炼有关,脾脏长径长短能间接地反映脾功能亢进的程度,而术后住院时间也能间接反映病人术后的早期活动锻炼。尽管还有研究表明术前食管胃底静脉曲张程度、术中大量出血等是PVST的独立危险因素[7],但结论并不完全一致,这可能与病例的选择、统计方法等有关。究其根本原因,可能还是与门静脉高压引起的血流动力学紊乱程度相关。脾脏切除术后,病人会经历血小板急剧增加的过程,血液由低凝变为高凝状态,可能也是PVST发生的重要原因[15],但本研究中术前血小板的数量不是门静脉血栓形成的危险因素。术后住院时间>10 d的病人机体功能恢复较慢,导致长期卧床,下地活动量少,血液循环不畅,导致PVST形成。
本研究中,LS组中转开腹率为21.4%,高于其他报告的3%~18%[16-18]。可能的原因包括:①纳入病例肝功能较差,有4例入院时肝功能为Child-Pugh C级,但经保肝治疗后,术前肝功能检查尚可,肝功能可达到Child-Pugh B级;②既往上腹部手术史,腹腔粘连严重不易暴露;③有些病人脾肿大达盆腔,严重限制了手术视野;④脾动脉与胰腺关系紧密,无法分离;⑤术者的腹腔镜手术操作不够熟练或倾向于完成难度较大的手术。因此,术者应严格把握腔镜手术的适应证,并掌握正确的游离、暴露方法和腹腔镜下常规操作技术,能够妥善应对局部粘连、术中出血等突发状况[19],在此基础上选择合适病例完成足够数量的LS训练,能够逐步降低中转开腹率。
同时,本研究还存在一些局限之处和值得继续深入研究的问题。首先,回顾性研究难以避免选择偏倚,腔镜组和开腹组在术前基线水平上有所差异,可能影响到观察结果。尽管如此,我们在危险因素分析中又对脾脏长径和食管胃底静脉曲张进行了分析,证明了脾脏长径≥20 cm是术后血栓形成的独立危险因素。其次,单中心病例数量有限,多名外科医生完成本组手术病例可能影响观察结果。最后,本组病例缺乏长期随访数据,对于病人的长期预后没有进行分析探讨。因此,进一步多中心大样本的前瞻性临床试验仍然有待进行。
总而言之,LS是可行的、安全的。运用熟练、细致的手术操作和先进的器械,可以有效地治疗门静脉高压症引起的脾功能亢进、食管胃底静脉曲张。LS与OS比较,手术步骤基本一致,但LS体表创伤小,可以早期下床活动,减少脾窝引流时间,术后恢复快,缩短住院时间。同时LS并不会增加脾切术后血栓发生率。
1 Feng LS, Chen XP. Combined splenocaval or mesocaval C shunt and portoazygous devascularization in the treatment of portal hypertension: Analysis of 150 cases. Hepatobiliary Pancreat Dis Int, 2006,5:70-73.
2 Gamme G, Birch DW, Karmali S. Minimally invasive splenectomy: An update and review. Can J Surg, 2013,56:280-285.
3 中华医学会消化内镜学分会. 食管胃静脉曲张内镜下诊断和治疗规范试行方案(2003年). 中华消化内镜杂志, 2004,21:149-151. DOI:10.3760/cma.j.issn.1007-5232.2004.03.001.
4 刘清波, 王卫东, 吴志强, 等. LigaSure血管闭合系统在腹腔镜脾功能亢进脾切除术中的应用(附28例报告). 腹腔镜外科杂志, 2010,15:286-288.
5 Machado NO, Al Kindy N, Chopra PJ. Laparoscopic splenectomy using LigaSure. JSLS, 2010,14:547-552. DOI:10.4293/108680810X12924466008286.
6 Peters MJ, Camacho D, Ojeda H, et al. Defining the learning curve for laparoscopic splenectomy for immune thrombocytopenia purpura. Am J Surg, 2004,188:522-525. DOI:10.1016/j.amjsurg.2004.07.026.
7 向俊西, 刘学民, 刘鹏, 等. 腹腔镜脾切除术门静脉系统血栓形成和中转开腹的危险因素分析. 腹部外科,2015,28:389-393. DOI:10.3969/j.issn.1003-5591.2015.06.004.
8 冯泽荣, 贺孝文, 廖轲. 手助腹腔镜与开腹脾切除加门奇断流术对机体免疫功能和创伤反应影响临床研究. 中国内镜杂志, 2003,9:39-41. DOI:10.3969/j.issn.1007-1989.2003.07.015.
9 毕永辉, 孙绍伟, 林鑫星. 腹腔镜脾切除术与开腹脾切除术的疗效观察. 中华普通外科学文献:电子版, 2014,8:399-401. DOI:10.3877/cma.j.issn.1674-0793.2014.05.014.
10 赵泽文, 仲小舟, 赵至成. 快速康复外科理念在腹腔镜胆囊切除术围手术期管理中的临床价值.中华消化外科杂志,2014,13:461-463. DOI:10.3760/cma.j.issn.1673-9752.2014.06.012.
11 Zhe C, Jian-wei L, Jian C,et al.Laparoscopic versus open splenectomy and esophagogastric devascularization for bleeding varices or severe hypersplenism: A comparative study. J Gastrointest Surg, 2013,17:654-659. DOI:10.1007/s11605-013-2150-4.
12 赵艳, 陈中, 倪家连. 加速康复外科理念在腹部外科围手术期护理的应用现状.实用医药杂志,2011,28:939-941. DOI:10.3969/j.issn.1671-4008.2011.10.057.
13 Harris W, Marcaccio M. Incidence of portal vein thrombosis after laparoscopic splenectomy. Can J Surg, 2005,48:352-354.
14 Winslow ER, Brunt LM, Drebin JA, et al. Portal vein thrombosis after splenectomy. Am J Surg,2002,184:631-636.
15 林栋栋,刘晋宁,卢实春,等.门静脉高压症脾切除断流术后血流动力学变化及其临床意义.中国实用外科杂志,2007,27:644-645. DOI:10.3321/j.issn:1005-2208.2007.08.024.
16 Pomp A, Gagner M, Salky B, et al. Laparoscopic splenectomy: A selected retrospective review. Surg Laparosc Endosc Percutan Tech, 2005,15:139-143.
17 Patel AG, Parker JE, Wallwork B, et al. Massive splenomegaly is associated with significant morbidity after laparoscopic splenectomy. Ann Surg, 2003,238:235-240. DOI:10.1097/01.sla.0000080826.97026.d8.
18 Casaccia M, Torelli P, Pasa A, et al. Putative predictive parameters for the outcome of laparoscopic splenectomy: A multicenter analysis performed on the Italian Registry of Laparoscopic Surgery of the Spleen. Ann Surg, 2010,251:287-291. DOI:10.1097/SLA.0b013e3181bfda59.
19 Marte G, Scuderi V, Rocca A, et al. Laparoscopic splenectomy: A single center experience. Unusual cases and expanded inclusion criteria for laparoscopic approach. Updates Surg, 2013,65:115-119. DOI:10.1007/s13304-013-0197-0.
Comparative study on laparoscopic splenectomy vs. open splenectomy for liver cirrhosis with portal hypertension
ZhangAnpeng,XiangJunxi,LiuPeng,ZhangXufeng,LyuYi,LiuXuemin.
DepartmentofHepatobiliarySurgery,TheFirstAffiliatedHospitalofXi'anJiaotongUniversity,Xi'an710061,China
LiuXuemin,Email:a1090224@163.com
Objective To compare the clinical outcomes and safety of laparoscopic splenectomy plus esophagogastric devascularization vs. open splenectomy plus esophagogastric devascularization for portal hypertension and to explore whether laparoscopic splenectomy increases the incidence of portal venous system thrombosis. Methods From January 2013 to December 2015, 204 patients were diagnosed as having portal hypertension and serious gastroesophageal varices in our institute. The clinical data were collected and analyzed retrospectively. The clinical outcomes were assessed, and the risk factors of portal vein system thrombosis were analyzed by single factor analysis and Logistic regression. Results Eighty-four patients were subjected to laparoscopic splenectomy and esophagogastric devascularization, and 120 patients underwent the open procedure. Eighteen patients were converted to laparotomy in the laparoscopic group. There was no significant difference in operating time, blood loss and transfusions between two groups. The postoperative hospital stay was significantly shorter in the laparoscopic group than in the open surgery group [(11.0±4.0) days vs. (12.6±5.4) days,P=0.032]. There was no significant difference in the incidence of postoperative portal vein thrombosis between two groups (28.8% vs. 26.7%,P=0.756). Spleen major diameter ≥ 20 cm and the hospital stays >10 days were independent risk factors of portal vein system thrombosis (P<0.05). Conclusions The short-term effect of laparoscopic splenectomy and esophagogastric devascularization was better than that of open surgery. And laparoscopic splenectomy would not increase the incidence of portal venous system thrombosis.
Laparoscope; Splenectomy; Portal hypertension; Portal vein system thrombosis
教育部创新团队发展计划(IRT 1279);国家自然科学基金(81501608)
710061 西安,西安交通大学第一附属医院肝胆外科
刘学民,Email:a1090224@163.com
R657.6
A
10.3969/j.issn.1003-5591.2016.03.006
2016-05-04)
