肾移植术后重症肺部感染患者死亡危险因素分析
2016-04-19张朋朋明英姿叶啟发
张朋朋 明英姿 叶啟发, 2
·论著·
肾移植术后重症肺部感染患者死亡危险因素分析
张朋朋1明英姿1叶啟发1, 2
目的 探讨肾移植术后重症肺部感染患者死亡危险因素,为临床诊治提供对策。方法 对2003年1月至2015年5月中南大学湘雅三医院器官移植中心收治的99例肾移植术后重症肺部感染患者进行回顾性研究,分析其死亡独立危险因素。将99例患者根据治疗结果分为治愈组和死亡组,比较两组供者类型、免疫抑制方案、术后重症肺部感染发生时间、是否合并败血症及休克、ARDS分型等指标。采用Logistic回归进行多因素分析,P<0.05为差异有统计学意义。结果 82例重症肺部感染发生在肾移植术后6个月内,17例发生在肾移植术后6个月后。58例患者治愈,41例死亡。99例患者共检出病原体167例次,感染病原体以细菌为主(126/167)。多因素分析可知供者类型、合并败血症、合并休克、免疫抑制方案、经济状况、ARDS分型是肾移植术后重症肺部感染患者死亡的独立危险因素(OR=12.041、0.225、0.074、0.143、0.093、0.124,P均<0.05)。结论 肾移植术后重症肺部感染患者的死亡与供者类型、是否合并败血症及休克、经济状况、免疫抑制方案及ARDS分型有关,针对以上因素采取预防措施,指导临床治疗,可降低肾移植术后重症肺部感染的病死率。
肾移植; 肺部感染; 急性呼吸窘迫综合征; 死亡; 危险因素
肾移植是治疗终末期肾衰竭最有效的方法,然而由于围手术期供、受者不可控因素众多,肾移植术后易发生肺部感染。据不完全统计,肾移植术后肺部感染发生率可达9%~16%,且肺部感染进展迅速,易发生急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS),严重威胁患者生命[1]。肾移植术后肺部感染是引起受者死亡的常见原因之一[2]。 Candan等[3]报道肾移植术后发生肺部感染的患者与其他患者相比,死亡率明显升高(66.6%和26.6%),而重症肺部感染死亡率更高。导致肾移植术后重症肺部感染患者死亡的因素众多,积极有效的预防和干预具有重要的临床意义[4-5]。本研究通过回顾性分析中南大学湘雅三医院器官移植中心肾移植受者临床资料,探讨肾移植术后重症肺部感染患者死亡危险因素。
1 资料与方法
1.1 一般资料
研究纳入2003年1月至2015年5月我中心收治的99例肾移植术后重症肺部感染患者。肾移植术后均接受他克莫司/环孢素+吗替麦考酚酯(mycophenolate mofetil,MMF)+泼尼松三联免疫抑制方案,监测他克莫司和环孢素血药浓度以调整免疫抑制剂方案,他克莫司血药浓度谷值维持在8~12 ng/mL(术后3个月内)、6~8 ng/mL(3~6个月)、5~8 ng/mL(6个月后);环孢素血药浓度谷值维持在250~350 ng/mL(术后3个月内)、200~300 ng/mL(3~6个月)、150~200 ng/mL(6个月后)。
1.2 重症肺部感染的诊断和治疗
重症肺部感染根据美国胸科学会的诊断标准[6]。主要标准:(1)需要有创机械通气;(2)感染性休克需要血管收缩剂治疗。次要标准:(1)呼吸频率≥30次/min;(2)低氧血症,氧合指数≤250 mmHg(1 mmHg=0.133 kPa,下同);(3)胸片示多肺叶浸润或入院后48 h内病变范围扩大超过50%;(4)低体温(<36 ℃);(5)白细胞减少(<4×109/L);(6)血小板减少(<10×109/L);(7)低血压,需要强力的液体复苏;(8)意识障碍/定向障碍;(9)氮质血症(血清尿素氮>20 mg/dL)。符合1项主要标准或3项次要标准以上者可诊断为重症肺炎。
ARDS分型根据柏林定义[7],按氧合指数水平分为轻度(200 mmHg<氧合指数≤300 mmHg)、中度(100 mmHg<氧合指数≤200 mmHg)和重度(<100 mmHg)。
所有病例常规进行痰涂片查找病原体(晨起反复漱口后留取深部合格痰,即每低倍镜视野下白细胞>25个,上皮细胞<10个);部分病例在纤维支气管镜下取支气管分泌物行细菌及真菌培养,对检测到的细菌行药敏试验。行血清病毒抗体(IgG、IgM)及CMV-DNA检查。影像学检查包括胸部X线检查、肺部CT等。
根据患者临床症状和血气分析等检查结果确定治疗方案。所有患者均采用无创呼吸机或气管插管有创呼吸机辅助呼吸。抗感染方案多采用经验性的“降阶梯”治疗方案[8],同时将免疫抑制剂减量或停用,应用糖皮质激素改善症状,免疫球蛋白及胸腺肽α1提升免疫力,维持水、电解质、酸碱平衡,补充白蛋白,加强营养等支持、对症治疗。
1.3 分组与观察指标
将99例肾移植术后重症肺部感染患者根据治疗结果分为治愈组和死亡组,比较两组年龄、性别、供者类型、肾移植次数、有无糖尿病、是否在围手术期使用生物制剂、免疫抑制方案、术后有无肺部感染病史(不包括本次感染)、术后重症肺部感染发生时间、是否合并败血症及休克、是否使用胸腺肽α1、免疫球蛋白及更昔洛韦治疗、使用呼吸机辅助通气期间实验室数据(白细胞计数、血小板计数、淋巴细胞计数、血清肌酐及白蛋白水平)、经济状况(家庭年收入<5万元或≥5万元)、是否有HBV及HCV感染、ARDS分型。
1.4 统计学方法
采用SPSS 19.0统计软件进行数据处理。计量资料以均数±标准差表示,两组患者年龄采用t检验进行比较。计数资料以率或构成比表示,两组供者类型、有无糖尿病、免疫抑制方案等采用χ2检验或Fisher确切概率法进行比较。将单因素分析中有统计学差异的变量作为自变量,重症肺部感染患者的转归作为因变量,采用Logistic回归进行多因素分析。P<0.05为差异有统计学意义。
2 结 果
2.1 肾移植术后重症肺部感染患者临床特征
99例肾移植术后重症肺部感染的患者中,男性82例,女性17例,平均年龄为(40±11)岁。37例为亲属活体肾移植,62例为尸体肾移植。术后三联免疫抑制方案的选择上,70例患者应用他克莫司+MMF+泼尼松,29例应用环孢素+MMF+泼尼松。82例重症肺部感染发生在肾移植术后6个月内,17例发生在肾移植6个月后。58例患者治愈,41例死亡。58例治愈组患者中,男性48例,女性10例,平均年龄为(40±11)岁;41例死亡组患者中,男性34例,女性7例,平均年龄为(38±11)岁;两组患者年龄、性别差异无统计学意义(t=1.088,χ2=0.0005,P均>0.05)。
2.2 病原体分类结果
99例肾移植术后重症肺部感染患者共检出病原体167例次,其中细菌感染126例次,病毒感染30例次,真菌感染11例次。后期多出现混合感染,尚有部分患者未找到病原体。详见表1。

表1 99例肾移植术后重症肺部感染患者病原体分类及例次
2.3 肾移植术后重症肺部感染患者死亡危险因素单因素分析结果
治愈组与死亡组患者相比,供者类型、术后有无肺部感染病史(不包括本次)、免疫抑制方案、经济状况、术后重症肺部感染发生时间、是否合并败血症及休克、是否使用更昔洛韦、ARDS分型差异有统计学意义(P均<0.05),提示上述因素是肾移植术后重症肺部感染患者死亡危险因素。详见表2。
2.4 肾移植术后重症肺部感染患者死亡危险因素Logistic回归多因素分析结果
将单因素分析中有统计学意义的危险因素进行Logistic 分析,结果显示:供者类型、经济状况、免疫抑制方案、是否合并败血症及休克、ARDS分型是肾移植术后重症肺部感染患者死亡的独立危险因素,差异有统计学意义(P均<0.05)。详见表3。
3 讨 论
Rubin等[9]将肾移植术后感染分为三期:一期为术后1个月内,主要以移植前潜伏感染为主,如结核分枝杆菌、慢性细菌感染等[10];二期为术后1~6个月,此阶段机会性感染多见,主要以病毒感染为主,最常见的为CMV、肝炎病毒、单纯疱疹病毒感染,其次为耶氏肺孢子菌感染,寄生虫感染机会也会增加;三期为术后6个月后,大部分感染与一般人群类似,此时以社区获得性感染为主,肺炎链球菌、支原体、呼吸道病毒感染多见。肾移植术后早期(6个月内)机会性感染以肺部感染最为多见[11],严重时可导致患者死亡,是肾移植术后人/肾存活率降低的重要原因[12]。移植后免疫抑制最严重的时间为术后80~130 d,此时自身免疫功能最为低下,因此最容易发生肺部感染[13]。本研究中肺部感染发生在6个月内的患者占82.8%(82/99)。
本研究通过对肾移植术后重症肺部感染患者的病原学检测资料进行分析,发现细菌是主要病原体,共检出细菌感染126例次,以鲍曼不动杆菌和铜绿假单胞菌为主;病毒感染30例次,真菌感染11例次。后期多出现混合感染,有部分患者未找到病原体。这与国外报道的以病毒感染为主[14]差别较大。可以认为,革兰阴性菌是肾移植术后预防和治疗肺部感染的重点,感染后期要特别警惕细菌、真菌混合感染[15]。CMV对正常人影响较小,但当细胞免疫功能低下时,则可引起局部感染,甚至通过血液播散引起严重的感染症状[16]。此外,本研究中未发现肺结核感染,除样本量小的因素外,可能与随着生活质量的提高,肺结核的发病率逐渐降低有关。
本研究结果显示,供者类型对肾移植术后重症肺部感染的预后有明显影响。亲属活体供肾移植术后重症肺部感染患者的病死率明显低于尸体供肾患者(24.3%和51.6%),可能与亲属供者自身感染机率、术后发生排斥反应的风险以及激素和生物制剂的使用较尸体供肾患者明显减少有关。大剂量使用糖皮质激素,会抑制机体蛋白质和淋巴细胞DNA的合成,使巨噬细胞对抗原的处理作用减弱,抗体产生减少,更易发生肺部感染[17]。目前尸体供肾多以心脏死亡器官捐献(donation after cardiac death, DCD)供肾为主,供者长时间维持治疗过程中免疫力下降,引起体内机会性致病菌的大量生长,且部分供者使用呼吸机辅助呼吸,在此过程中可能会引起供者感染。维持治疗时间越长,DCD供者感染的可能性越大,即使应用抗生素预防和控制感染,仍然会有正常菌群的移位,通过移植手术到达受者体内,最终引起受者的感染。
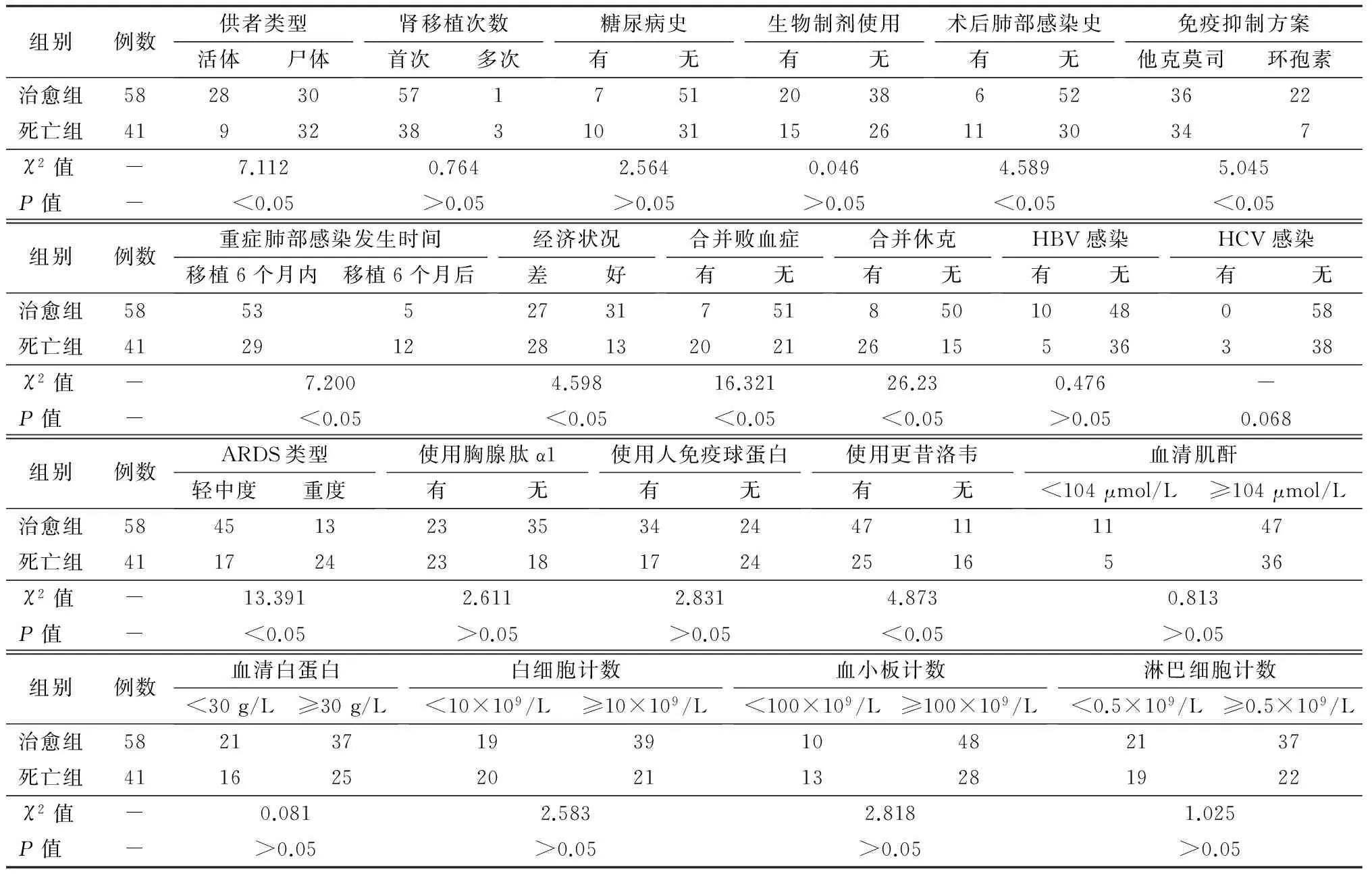
表2 肾移植术后重症肺部感染患者死亡危险因素单因素分析结果(例)
注: ARDS. 急性呼吸窘迫综合征;-. 无数据

表3 肾移植术后重症肺部感染患者死亡危险因素多因素分析结果
注: ARDS. 急性呼吸窘迫综合征
Jones等[18]研究了应用不同免疫抑制方案对小鼠肢体移植长期预后的影响,结果显示他克莫司组小鼠多于移植后273~334 d死于肺部感染,而环孢素组小鼠多死于排斥反应和其他并发症,证实应用他克莫司相比环孢素可导致肺部感染病死率升高。这一结论与本研究结果相同。但张彦选等[19]报道肾移植术后应用他克莫司或环孢素对术后肺部感染的发生率无明显影响,这可能与术后药物浓度的控制有关。
本研究多因素分析结果显示,经济状况也是引起肾移植术后重症肺部感染死亡的独立危险因素。Kutinova等[20]报道,肾移植术后1年或2年内发生肺部感染会平均增加38 400美元的额外治疗成本。本研究中肺部感染患者相关治疗花费在10万元左右,对于经济能力有限的低收入家庭,往往会选择放弃或无法积极治疗,其病死率明显增加。有研究表明,重度ARDS是使用呼吸机的恶性肿瘤患者死亡的独立危险因素[21],但目前尚未见肾移植术后重症肺部感染与该因素相关性的报道。本研究发现重度ARDS与肾移植术后重症肺部感染死亡相关。得出这一结果,考虑可能与重度ARDS患者氧合指数较低,细胞缺氧严重导致抵抗力下降有关。此外,本研究还证实,重症肺部感染患者合并败血症及休克是患者死亡的独立危险因素。Abbott等[22]报道肾移植术后细菌性败血症的发病率是普通人群的40倍。肾移植术后重症肺部感染患者免疫力更低,发生败血症的风险更高,更易出现感染性休克、循环功能衰竭,最终导致多器官功能衰竭、严重的水电解质平衡紊乱和机体免疫功能低下,死亡率明显升高。
肾移植术后肺部感染多发生在术后6个月内,若未及时有效控制,病情进展迅速,病死率极高;及时合理的综合治疗是改善预后、降低病死率的关键。因此,肾移植术后6个月内的预防治疗显得尤为重要。一般从术后2~4周开始应用更昔洛韦/缬更昔洛韦预防CMV感染,疗程为3个月。现有研究表明应用复方新诺明联合更昔洛韦预防肾移植术后肺部感染疗效更佳[23]。一旦发生肺部感染,在明确感染病原体之前根据经验给予“四联”疗法,遵循“降阶梯”治疗方案[8],以抗革兰阴性菌为主,待明确病原体后再根据药敏试验结果调整抗生素治疗方案。同时,适当调整免疫抑制方案,特别是应用他克莫司的患者,一旦发生严重肺部感染,应及时停用免疫抑制剂,同时给予丙种球蛋白及胸腺肽α1进行免疫调节治疗。对于肺功能受损严重的患者及时纠正缺氧,尽早应用机械通气,避免进展到重度ARDS。一旦患者出现败血症及休克,病死率明显增高,需定时行血培养监测,早期诊断,联合用药,尽早控制感染,降低重症肺部感染的病死率。
1 范连慧, 刘龙, 向军, 等. 187例肾移植受者死亡原因分析[J]. 中华器官移植杂志, 2005,26(8):461-463.
2 杨淑蓉, 贾会学, 李六亿. 肾移植术后肺部感染的调查与分析[J]. 中华医院感染血杂志, 2009,19(2):162-163.
3 Candan S, Pirat A, Varol G, et al. Respiratory problems in renal transplant recipients admitted to intensive care during long-term follow-up[J]. Transplant Proc, 2006,38(5):1354-1356.
4 桑林涛, 许静. 氨曲南联合更昔洛韦于治疗肾移植术后肺部感染的临床研究[J]. 中国农村卫生, 2012,z2:304-305.
5 朱琳, 曾昭全, 魏文树, 等. 我院1例肾移植术后肺部感染患者的药学监护[J]. 中国临床药理学与治疗学, 2011,16(11):1244-1247.
6 Niederman MS, Mandell LA, Anzueto A, et al. Guideline for the management of adults with community-acquired pneumonia. Diagnosis, assessment of severity, antimicrobial therapy, and prevention[J]. Am J Rrespir Crit Care Med, 2001,163(7):1730-1754.
7 ARDS Definition Task Force, Ranieri VM, Rubenfeld GD, et al. Acute respiratory distress syndrome: the Berlin Definition[J]. JAMA, 2012,307(23):2526-2533.
8 朱有华, 闵志廉, 齐隽, 等. 广义降阶梯治疗方案在肾移植后重症肺部感染患者中的应用[J]. 中华国际医学杂志, 2002,2(6):497-499.
9 Rubin RH, Wolfson JS, Cosimi AB, et al. Infection in the renal transplant recipient[J]. Am J Med, 1981,70(2):405-411.
10 Johnston RB Jr, Thareja S, Shenefelt PD. Disseminated histoplasmosis in a renal transplant patient[J]. Cutis, 2013,91(6):295-299.
11 张燕燕, 张晓东, 李瑛, 等. 肾移植术后患者肺部感染及预后因素分析[J]. 河北医学, 2013,35(7):1013-1015.
12 Sileri P, Pursell KJ, Coady NT, et al. A standardized protocol for the treatment of severe pneumonia in kidney transplant recipients[J]. Clin Transplant, 2002,16(6):450-454.
13 宋晓杰, 李丹, 刘伟, 等. 肾移植术后肺部感染诊治进展[J]. 中国老年学杂志, 2014,(8):2312-2314.
14 Durlik M, Siennicka J, Litwińska B, et al. Comparison of antigenemia (pp65) assay and polymerase chain reaction in diagnosis of cytomegalovirus infection in renal transplant recipients treated with ATG[J]. Transplant Proc, 2000,32(6):1350-1352.
15 郭鹏, 王瑜, 解志远, 等. 肾移植术后围手术期肺部感染分析[J]. 广东医学杂志, 2010,31(10):1090-1092.
16 Motta VN, Martins SL. Impairment of cytomegalovirus-specific cellular immune response as a risk factor for cytomegalovirus disease in transplant recipients[J]. Braz J Med Biol Res, 2008,41(1):5-11.
17 李壮江, 孙煦勇, 聂峰, 等. 肾移植术后肺部感染的诱因分析及对策[J]. 中华器官移植杂志, 2012,33(4):225-228.
18 Jones NF, Heberbrand D, Buttemever R, et al. Comparison of long-term immunosuppression for limb transplantation using cyclosporine, tacrolimus, and mycophenolate mofetil: implications for clinical composite tissue transplantation[J]. Plast Reconstr Surg, 2001,107(3):777-784.
19 张彦选, 于立新, 付绍杰, 等. 肾移植术后应用新型免疫抑制剂受者肺部感染的临床研究[J]. 南方医科大学学报, 2008,28(6):1037-1040.
20 Kutinova A, Woodward RS, Ricci JF, et al. The incidence and costs of sepsis and pneumonia before and after renal transplantation in the United States[J]. Am J Transplant, 2006,6(1): 129-139.
21 Azoulay E, Lemiale V, Mokart D, et al. Acute respiratory distress syndrome in patients with malignancies[J]. Intensive Care Med, 2014,40(8):1106-1114.
22 Abbott KC, Oliver JD 3rd, Hypolite I, et al. Hospitalizations for bacterial septicemia after renal transplantation in the United States[J]. Am J Nephrol, 2001,21(2):120-127.
23 瞿立辉, 吕蓉, 吴建永, 等. 复方新诺明联合更昔洛韦预防肾移植术后肺部感染[J]. 中华肾脏病杂志, 2008,24(3):158-161.
(本文编辑:鲍夏茜)
张朋朋, 明英姿, 叶啟发. 肾移植术后重症肺部感染患者死亡危险因素分析[J/CD]. 中华移植杂志:电子版, 2016,10(2):66-70.
Risk factors of mortality in recipients with severe pneumonia after renal transplantation
ZhangPengpeng1,MingYingzi1,YeQifa1, 2.
1DepartmentofTransplantSurgery,theThirdXiangyaHospital,CentralSouthUniversity,Changsha410013,China;2DepartmentofTransplantSurgery,ZhongnanHospital,WuhanUniversity,Wuhan430071,China
YeQifa,Email:yqf_china@163.com
Objective To investigate the risk factors of mortality in recipients with severe pneumonia after renal transplantation and to provide a strategy for the patients′ clinical diagnosis and treatment. Methods The clinical and laboratory data of 99 patients were retrospectively analyzed between January 2003 and May 2015 in Organ Transplantation Center of the Third Xiangya Hospital. All the patients were divided into cured group and death group according to the results of treatment and observation indexs included type of donor, type of immune inhibitor, the time between pneumonia and operation, combining with sepsis or shock, and ARDS classification. Univariate and multivariate logistic regression analysis were conducted to identify the independent risk factors associated with infection-related mortality (P<0.05). Results Eighty-two patients occurred pulmonary infection within 6 months after renal transplantation compared with 17 patients after 6 months. Fifty-eight patients were cured and 41 patients died. There were 167 cases of pathogens detected from 99 patients, and bacterial was the main infection types (126/167). The multivariate analysis showed that the risk factors associated with infection-related mortality were the type of donor, combining with sepsis or shock, type of immune inhibitor, economic level and ARDS classification (OR=12.041, 0.225, 0.074, 0.143, 0.093, 0.124, respectively,P<0.05). Conclusions The severe pneumonia-related mortality after renal transplantation was associated with the type of donor, combining with sepsis or shock, type of immune inhibitor, economic level and ARDS classification. In clinical, taking preventive measures in terms of the risk factors can reduce the patients′ mortality of severe pulmonary infection after renal transplantation.
Renal transplantation; Pulmonary infection; Acute respiratory distress syndrome; Death; Risk factors
10.3877/cma.j.issn.1674-3903.2016.02.004
410013 长沙, 中南大学湘雅三医院器官移植中心1; 430071 武汉大学中南医院移植医学中心2
叶啟发, Email: yqf_china@163.com
2015-10-13)
