卡培他滨单药二线治疗复发转移胃癌的临床研究
2012-04-29郑江虹王思本
郑江虹 王思本
[摘要]目的 观察卡培他滨单药二线治疗复发转移胃癌的近期疗效、毒副作用和临床获益。 方法45例初次治疗后区域复发或/和广泛转移的胃癌患者随机分为两组,观察组22例,用单药卡培他滨2 000 mg/(m2·d),第l~14天,停药7 d,21 d为1周期。对照组23例,采用DC(多西他赛+顺铂)方案,多西他赛60 mg/m2,d1;顺铂25 mg/(m2·d), 第1~3天,21 d为1周期。所有患者接受3~6个周期治疗,至少接受2周期后评价疗效及副作用。 结果 两组的近期有效率、中位生存时间和中位缓解期比较,差异均无统计学意义(P > 0.05)。两组患者的Ⅲ度以上毒副作用主要为血液学毒性和消化道反应。对照组Ⅲ度以上的血液学毒性、恶性呕吐及便秘的发生率显著高于观察组(P < 0.05),卡培他滨单药化疗的主要毒性作用是手足综合症。结论 单药卡培他滨口服二线治疗复发转移性胃癌疗效好,与DC方案无显著性差异,毒副作用较联合方案小。
[关键词] 胃癌;卡培他滨;疗效;毒副反应
[中图分类号] R735.2[文献标识码] B[文章编号] 1673-9701(2012)29-0067-03
世界范围内胃癌居肿瘤发病率的第四位、肿瘤相关死亡的第二位[1],中国更是胃癌的高发区,全球新发胃癌中42%的病例发生在中国[2]。早期胃癌诊断率低,临床确诊时大多数为进展型和晚期胃癌。手术治疗后两年内有50%~60%的患者出现复发和转移。目前认为化疗为主的综合治疗能提高复发转移性胃癌的生存率,但尚无明确的标准方案。本文对22例经手术及一线化疗后复发的胃癌以卡培他滨单药二线化疗为观察组,且用DC方案联合化疗为对照组,观察其近期疗效、进展时间、总生存率和耐受性,现报道如下。
1.资料与方法
1.1 一般资料
2008年6月~2011年7月我院收治的复发转移胃癌患者。病例大部分来源于“进展期胃癌根治术后Folfox4方案化疗联合同步放疗的治疗耐受性及疗效临床研究”资料。其中男30例,女15例。年龄29~74岁,中位年龄56岁。所有病例均经根治性手术,术后初次化疗方案包括FOLFOX4方案(奥沙利铂+ 5-氟尿嘧啶/亚叶酸钙持续泵入)30例,EOF方案(多柔比星/表柔比星 +奥沙利铂+ 5-氟尿嘧啶)10例,其他方案5例,除外一线方案中含有紫杉类或顺铂的病例。45例患者术后至确诊复发时间为3~34个月,东部协作肿瘤组(ECOG)评分为0~2分,预计生存时间>3个月。患者血常规及肝、肾功能均正常,无化疗禁忌证,化疗前均签署知情同意书。将45例患者随机分为观察组22例,对照组23例。两组在年龄、病理类型、术后分期、切缘情况、首次化疗方案、术后至复发时间等各项临床资料均无统计学意义。
1.2 治疗方法
观察组22例,卡培他滨2 000 mg/(m2·d)(罗氏公司,批号:H3206),第l~14天,停药7 d,21 d为1周期,口服化疗期间同时予口服胃黏膜保护剂或/和质子泵抑制剂。对照组23例,采用DC方案,多西他赛60 mg/m2,d1;顺铂25 mg/m2,第1~3天,21 d为1周期。静脉化疗前半小时常规予格拉司琼止吐,多西他赛前给地塞米松10 mg、苯海拉明50 mg预处理以防过敏。所有患者接受3~6个周期的治疗,至少接受2周期后评价疗效。治疗中出现Ⅲ度以上骨髓抑制者予以G-CSF支持或延迟治疗相应。
1.3 疗效及毒副作用评价
疗效评价疗效参照RECIST实体肿瘤客观疗效评定标准[3],分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(SD)。化疗期间每周1~2次血常规及肝肾功能检查,每1~2个月用CT或加B超、内镜等判定疗效。生存时间自接受化疗开始时计算,比较两组的中位生存时间与中位缓解时间。不良反应按照美国NCICTC3.0版的标准,分为0~IV度。
1.4 统计学处理
采用SPSS13.0统计学软件进行数据分析,计数资料以率(%)表示,组间比较采用χ2检验,生存时间用log-rank检验。P < 0.05为差异有统计学意义。
2 结果
2.1 近期疗效
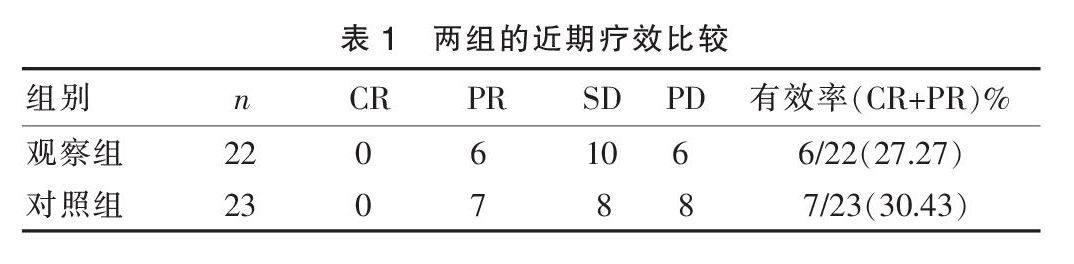
观察组CR+PR者6例(27.27%),对照组CR+PR者7例(30.43%),差异无统计学意义(χ2=0.08,P > 0.05)。两组的中位生存时间平均(9.6±0.3)个月vs(10.8±0.1)个月(t = 1.03,P > 0.05);中位缓解期平均(6.5±0.5)个月vs(7.1±0.3)个月(t = 0.85,P > 0.05),差异无统计学意义。见表1。
表1 两组的近期疗效比较
2.2 毒副反应
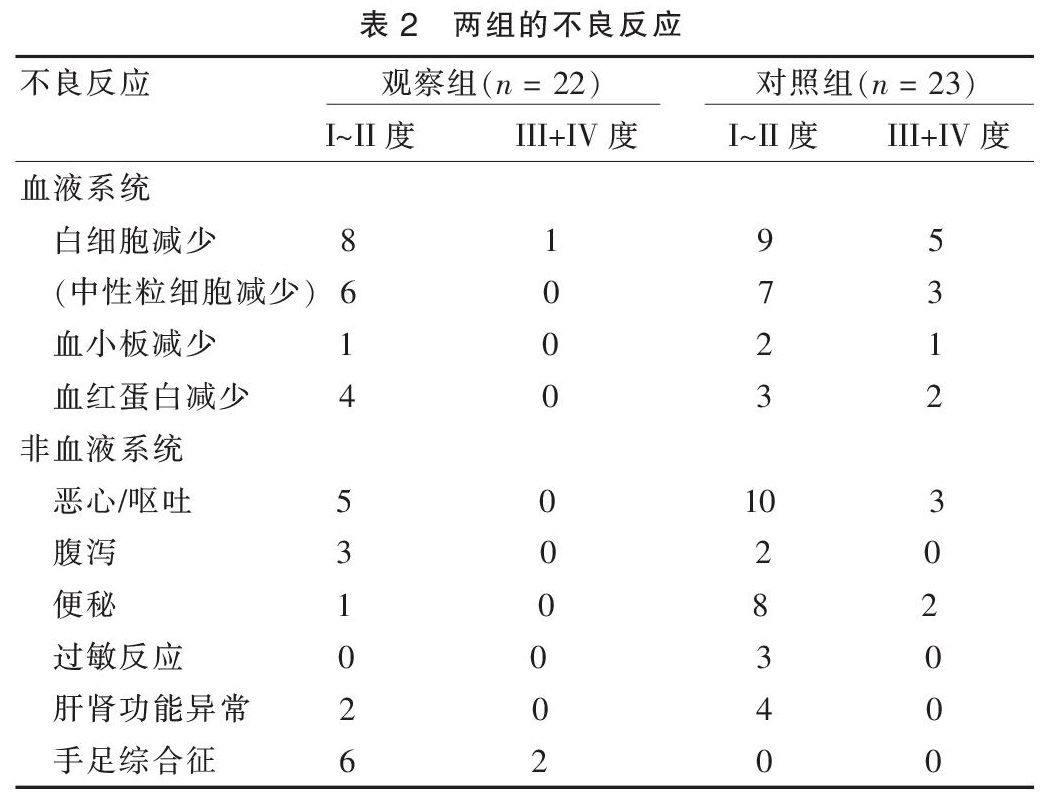
见表2。血液系统毒性反应分别为白细胞、血红蛋白及血小板降低。其中对照组血液系统III度以上不良反应发生率为8/23(34.78%),较观察组的1/22(4.55%)明显增加,两者间差异有统计学意义(χ2=4.53,P<0.05)。两组恶心呕吐发生率分别为5/22(22.7%)、13/23(56.52%),两者间差异有统计学意义(χ2=5.78,P < 0.05)。观察组仅1例出现便秘(1/22;4.55%),而对照组便秘发生率为10/23(43.48%),(χ2=7.24,P < 0.01)。观察组中有8例出现手足综合征,Ⅰ~Ⅱ度6例、Ⅲ度2例;对照组有3例出现Ⅰ~Ⅱ度的过敏反应。其他不良反应的发生率两组间均无统计学差异。对照组有4例患者因毒性反应而延长化疗间歇时间。所有不良反应经对症治疗或延迟化疗后得以控制,无化疗相关死亡。
表2 两组的不良反应
3 讨论
尽管早期诊断和根治性手术显著提高了胃癌的生存率,但胃癌的总体疗效仍不令人满意,半数以上的患者在胃癌根治术后复发死亡。转移或复发性胃癌的治疗以全身化疗为主,但晚期胃癌目前尚无一线的标准化疗方案[4,5],对转移或复发性胃癌的二线化疗结果更少有报道。近年来研究结果表明,含紫杉类、奥沙利铂和卡培他滨的第三代化疗方案对晚期胃癌更具优势,但预后仍很差,中位生存期一般不超过12个月[6]。本文对22例经手术及一线化疗后复发的胃癌以卡培他滨单药二线化疗为观察组,且用DC方案联合化疗为对照组,结果显示观察组CR+PR者6例(27.27%);对照组CR+PR者7例(30.43%);两组间差异比较无统计学意义。观察组与对照组的MST 及PFS 分别为9.6个月、6.5个月vs 10.8个月、7.1个月,两组间差异比较无统计学意义。与文献报道相比[6,7],近期有效率、MST及PFS相近。
晚期胃癌尤其是术后复发胃癌的治疗是姑息性的,因此临床在选择治疗方案时必须充分考虑化疗的毒副作用及患者的生活质量。在评价DCF方案(多西他赛75 mg/m2,d1;顺铂75 mg/m2;氟尿嘧啶750 mg/m2)在晚期胃癌治疗中作用时,Ilson[8]指出该方案在有限提高0.6个月生存期的同时明显增加了不良反应,代价太大。另外该方案不能改进生存质量和临床受益,而只是维持生活质量和临床受益不恶化。因而提出适当减少药物剂量或改为连续、每周、双周的给药方式。
卡培他滨属于5-Fu的前体药物,口服后生物利用度很高,可经小肠完整吸收,模拟持续性静脉输注5-Fu,同时避免胃肠外给药的屏障问题。卡培他滨能在肿瘤组织中选择性活化,提高了药物在癌细胞内的浓度和抗肿瘤作用,减少了全身的毒性作用,达到高效的靶向治疗。卡培他滨单药或联合用药在治疗胃癌中的作用已有多项研究证实[9,10]。Lee等[9]报告了一项Ⅱ期临床研究,采用卡培他滨对比S-1来治疗老年晚期胃癌91例。结果表明,希罗达组的PR29.5%、SD38.6%;S-1组的CR2.2%、PR 26.7%、SD 40.0%.两组的PFS分别为4.8个月和4.2个月,总生存期(OS)分别为10.0个月和7.9个月。该研究中卡培他滨的毒性反应轻,最常见不良反应是手足综合征,无Ⅲ度以上的血液系统及消化系统不良反应出现。结论是卡培他滨和S-1单药口服化疗均具有良好的疗效及耐受性。
本研究中入选的患者是初次治疗后区域复发或/和广泛转移的胃癌患者,一线化疗方案是近年临床常用的FOLFOX4方案和EOF方案,复发后二线治疗主要目的是改善生活质量和提高临床受益。单药口服卡培他滨可居家服用,在社区医疗点或门诊定期观察,符合肿瘤姑息治疗的趋势。本研究中对照组DC方案剂量也作了相应调整,减少了多西他赛的剂量,并将顺铂分连续3 d给予。结果表明,两组均取得了良好的近期治疗效果及中位生存时间,观察组中除其特有的手足综合症毒副作用发生率高于对照组外,血液系统及消化系统毒性均明显小于对照组。
总之,单药卡培他滨口服二线治疗复发转移性胃癌疗效有良好的疗效,与DC方案联合化疗对照组及文献相比在近期疗效、MST及PFS上无明显差异;毒性小且服用方便,更利于提高晚期患者的生活质量、节约医疗成本,值得进一步研究。
[参考文献]
[1]Kamangar F,Dores GM,Anderson WF. Patterns of cancer incidence,mortality,and prevalence across five continents:defining priorities to reduce cancer disparities in different geographic regions of the world[J]. J Clin Oncol,2006,24(14):2137-2150.
[2]Parkin DM,Bray F,Ferlay J,et al. Global cancer statistics 2002[J]. CA Cancer J Clin.,2005,55(2):74-108.
[3]Gehan EA,Tefft MC. Will there be resistance to the RECIST(Response evaluation criteria in solid tumors)[J]. J Natl Cancer Inst,2000,92(3):179–181.
[4]Wager AD,Grothe W,Haerting J,et al. Chemotherapy in advanced gastric cancer:a systematic review and meta-analysis based on aggregate data[J]. J Clin Oncol,2006,24(18):2903-2909.
[5]秦叔逵,刘秀峰,张华. 晚期胃癌三种一线化疗方案的临床比较研究[J]. 循证医学,2005,5(4):214-217.
[6]Roth AD,Fazio N,Stupp R,et al. Docetaxal,cisplatin,and fluorouracil;Docetaxal and cisplatin;and epirubicin,cisplatin,and fluorouracil as systemic treatment for advanced gastric cancinoma:A randomized phase II trial of the Swiss Group for Clinical Cancer Research[J]. J Clin Oncol,2007,25(22):3217-3223.
[7]Van Cutsem E,Moiseyenko VM,Tjulandin S,et al. Phase III study of docetaxel and cisplatin plus fluorouracil as first line therapy for advanced gastric cancer:A report of V325 study group[J]. J Clin Oncol,2006,24(31):4991-4997.
[8]Ilson DH. Docetaxel,cisplatin,and fluorouracil in gastric cancer: Dose the punishment fit the crime [J]. J Clin Oncol,2007,25(22):3188-3190.
[9]Lee J,Kang Y,Lee K,et al. A randomised multicentre phase II trial of capecitabine vs S-1 as first-line treatment in elderly patients with metastatic or recurrent unresectable gastric cancer[J]. Br J Cancer,2008,99(4):584-590
[10]Cunningham D,Starling N,Rao S,et al. Capecitabine and oxaliplatin for advanced esophagogastric cancer[J]. N Engl J Med,2008,358(1):36-46.
(收稿日期:2012-06-25)
