高海拔地区血液筛查核酸检测系统性能验证结果评价*
2023-12-02臧亮周磊多吉林豪白睿杨梅旦超范亚欣
臧亮 周磊 多吉 林豪 白睿 杨梅 旦超 范亚欣△
(1.大连市血液中心,辽宁 大连 116001;2.那曲市中心血站)
近年来,随着病毒核酸检测技术(nucleic acid testing,NAT)在血液筛查中的全面推行,大大降低了HBV/HCV/HIV 的输血传播风险[1-3]。 按照《血站质量管理规范》《血站实验室质量管理规范》和《血液技术操作规程(2019 版)》的要求[4-6],应对核酸检测系统进行性能验证,确认核酸检测系统能够满足实验室检测工作的要求,确保检测结果的准确性和可靠性。 目前现有的验证方案与方法均是参考低海拔地区实验室建立的,针对高海拔地区的验证方案与方法尚未见报道。 西藏那曲地区海拔约4 450 米,高寒缺氧,气压低、气候条件差,对核酸检测系统的性能验证指标的选择、验证方案的标准化以及验证结果的评价与低海拔地区的差异值得研究。 我们基于国家标准和行业标准,针对高海拔地区实验室检测模式和实际工作特点,选择分析灵敏度、特异性、重复性、符合率、检测系统比对等关键指标,建立适宜高海拔地区的性能验证方案,以保证血液检测过程的标准化和检测结果的准确性,提升高海拔地区的血液安全,同时也为其他高海拔地区的采供血机构顺利开展核酸检测工作提供参考。
1 材料与方法
1.1 标本来源 核酸检测系统性能验证血清盘由国家卫健委临检中心提供。 其中,NAT 血清盘C—G(分析灵敏度验证盘)共30 份标本,包括HBV C 型标本5 份(C2—C6),浓度为25、12、6、3、1.5 IU/mL;HCV 2a 型标本5 份(D2—D6),浓度为170、85、40、20、10 IU/mL;HIV CRF07_BC 型标本5 份(E2—E6),浓度为210、105、50、25、12.5 IU/mL;HCV 1b 型标本5 份(F2—F6),浓度为140、70、35、17、8.5 IU/mL;HCV 6a型标本5 份(G2—G6),浓度为220、110、55、27、13 IU/mL;阴性标准物质5 份。 血清盘A(单检检测策略评估)共46 份标本,每一编号3 支,每份标本3 mL。
1.2 试剂与仪器 HBV、HCV 和HIV-1 病毒核酸检测试剂盒(达安基因公司,批号:202201001);血液核酸筛查系统:DA3500S 全自动核酸提取仪(达安基因公司)、AGS4800 PCR扩增仪(杭州安誉公司)。
1.3 方法
1.3.1 灵敏度 采用国家卫健委临检中心提供的NAT 血清盘C—G 进行检测,标本浓度覆盖试剂说明书声明的最低检出限(HBV/HCV/HIV≤100 IU/mL),标本检测前置于室温复融,漩涡震荡30 s 或颠倒30 次充分混匀,为防止交叉污染,混匀后瞬时离心再打开盖子。 每个灵敏度验证盘分3 d进行检测,每天每个浓度检测≥6 次,3 d 检测每个浓度合计检测≥20 次。 汇总每种病毒的所有重复测试数据并采用SPSS 20.0 进行PROBIT 分析,评估该核酸检测系统的LOD和双侧95%置信区间。
1.3.2 重复性 采用国家卫健委临检中心提供的浓度≤3倍LOD 的HBV DNA、HCV RNA、HIV-1 RNA 标准物质以及阴性标准物质,重复单检20 次,汇总检测结果评价检测系统的重复性。
1.3.3 抗交叉污染 将分析灵敏度验证盘中的5 支阳性标准物质(C2—G2)与血清盘中配套的5 支阴性标准物质交叉放置于标本架,以单检模式进行检测,分析阳性与阴性标准物质的检测情况。
1.3.4 检测系统比对评估 采用国家卫健委临检中心提供的NAT 血清盘A 中46 份HBV DNA 低浓度标本进行核酸检测,标本检测前置于室温复融,漩涡震荡30 s 或颠倒30 次充分混匀,1 000~1 500×g 离心5 min。 所有标本均进行单样检测,初次检测仅检测1 次,第2 次检测为双孔复检。 汇总血清盘A 的标本的检测结果,与其他核酸检测系统的检测结果进行比较,分析该核酸检测系统在高海拔地区的检出能力,以评估当前检测策略。
2 结果
2.1 灵敏度验证结果 见表1~5。 分别对HBV DNA、HCV RNA、HIV-1 RNA 的重复检测数据进行PROBIT 分析,计算每种病毒的95%评估检测下限(95% LOD)和双侧95%置信区间,结果见表6。
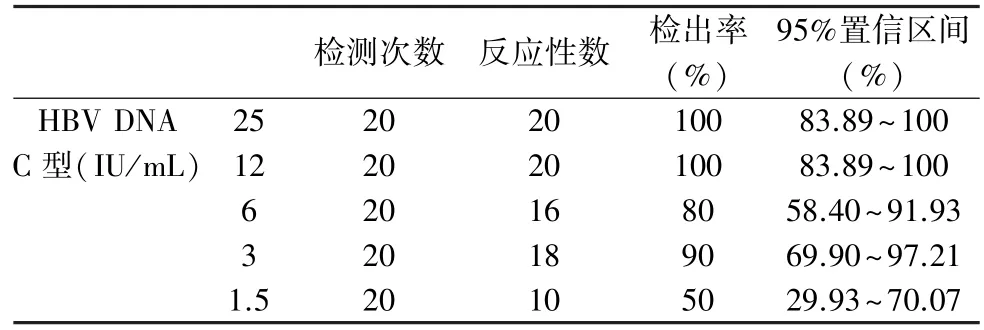
表1 HBV DNA C 型分析灵敏度验证结果
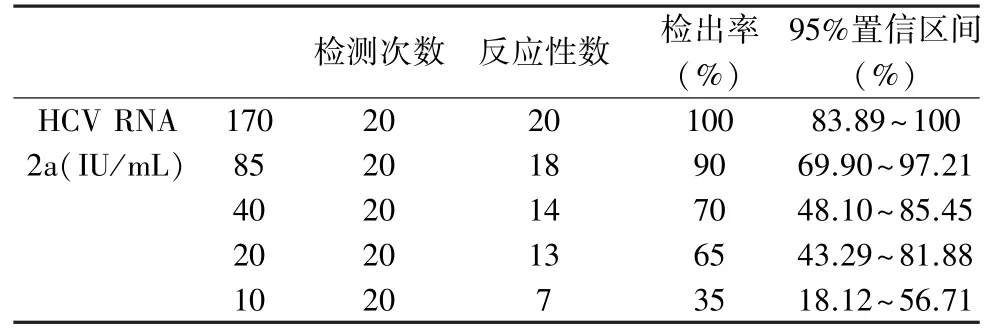
表2 HCV RNA 2a 型分析灵敏度验证结果
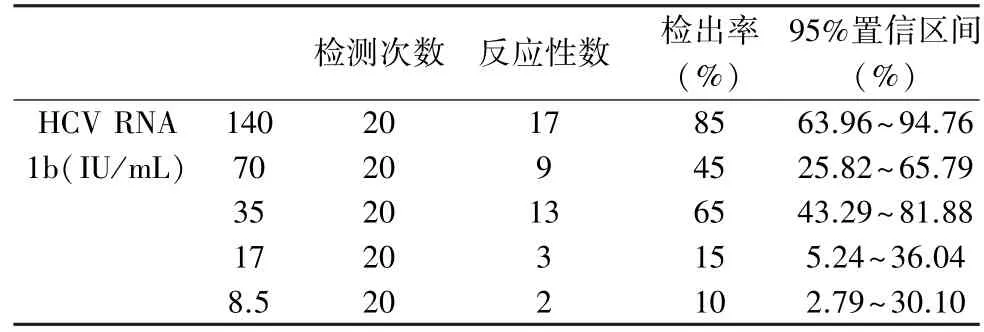
表3 HCV RNA 1b 型分析灵敏度验证结果
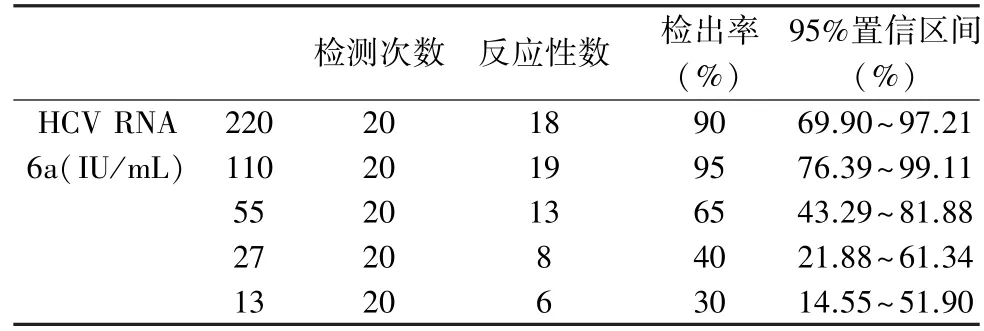
表4 HCV RNA 6a 型分析灵敏度验证结果
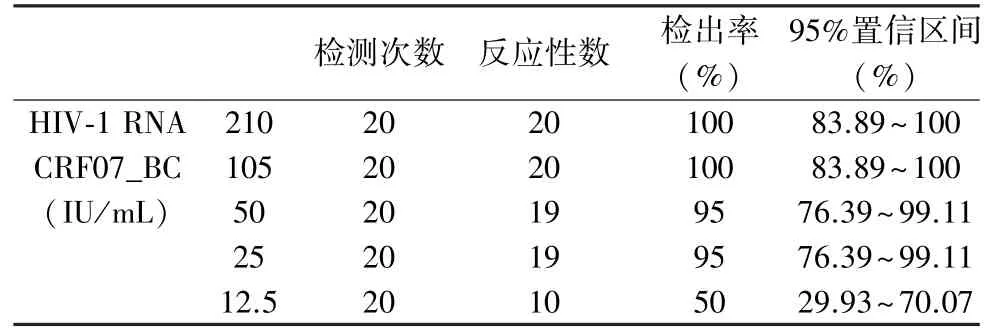
表5 HIV-1 RNA CRF07_BC 型分析灵敏度验证结果
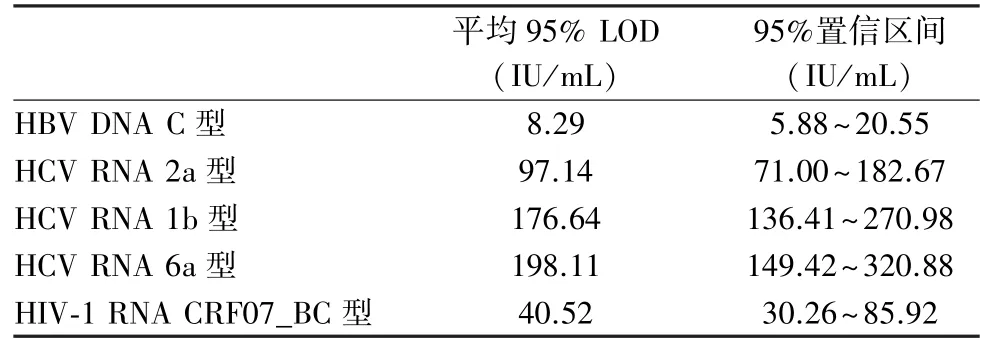
表6 不同病毒分析灵敏度的PROBIT 分析
2.2 重复性试验结果 见表7。
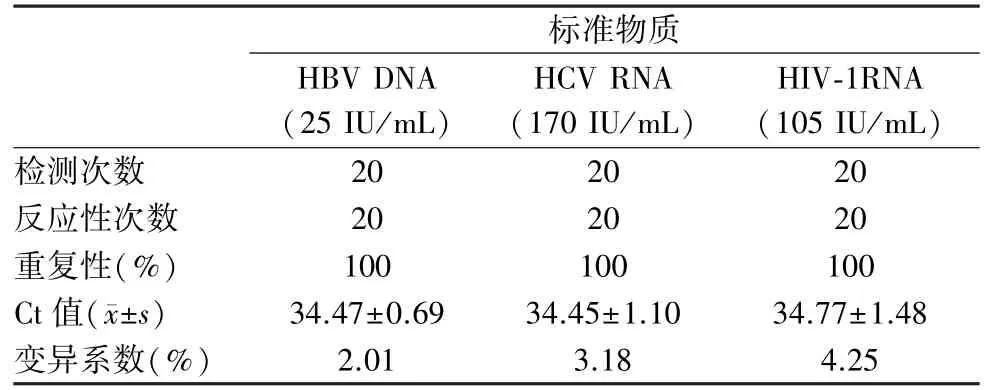
表7 核酸检测系统重复性验证结果
2.3 交叉污染试验检测结果 阴性标本和阳性标本交叉排列单检结果显示,5 个阳性标本(含HBV DNA、HCV RNA 和HIV RNA)的检测结果均为反应性,阳性符合率为100%;5个阴性标本的结果均为无反应性,阴性符合率为100%。 未出现检测标本之间的相互交叉污染情况。
2.4 检测系统比对评估 所有标本经化学发光法检测HBsAg,结果均为无反应性,临检中心确证为HBV DNA 低浓度标本,见表8。 其中,18 份经罗氏核酸检测系统检测结果为反应性的标本,在本站初筛检测结果为反应性的有8 份,初筛阳性符合率为44.44%,复测结果为反应性的有14 份,复检阳性符合率为77.78%;22 份经浩源核酸检测系统检测结果为反应性的标本,在本站初筛检测结果为反应性的有13份,初筛阳性符合率为59.09%,复测结果为反应性的有13份,复检阳性符合率为59.09%。 在血清学检测HBcAb 呈反应性的38 份标本中,本站初筛检出率为47.37%(18/38),复测检出率为68.57%(24/35),有3 份标本因标本量不足而未对其进行复测,结果按初筛结果判定。 在对NAT 血清盘A中所有的低浓度HBV DNA 标本的检测结果中,本站检测系统与低海拔地区检测结果的一致性分别为77.78%和77.27%,见表9。
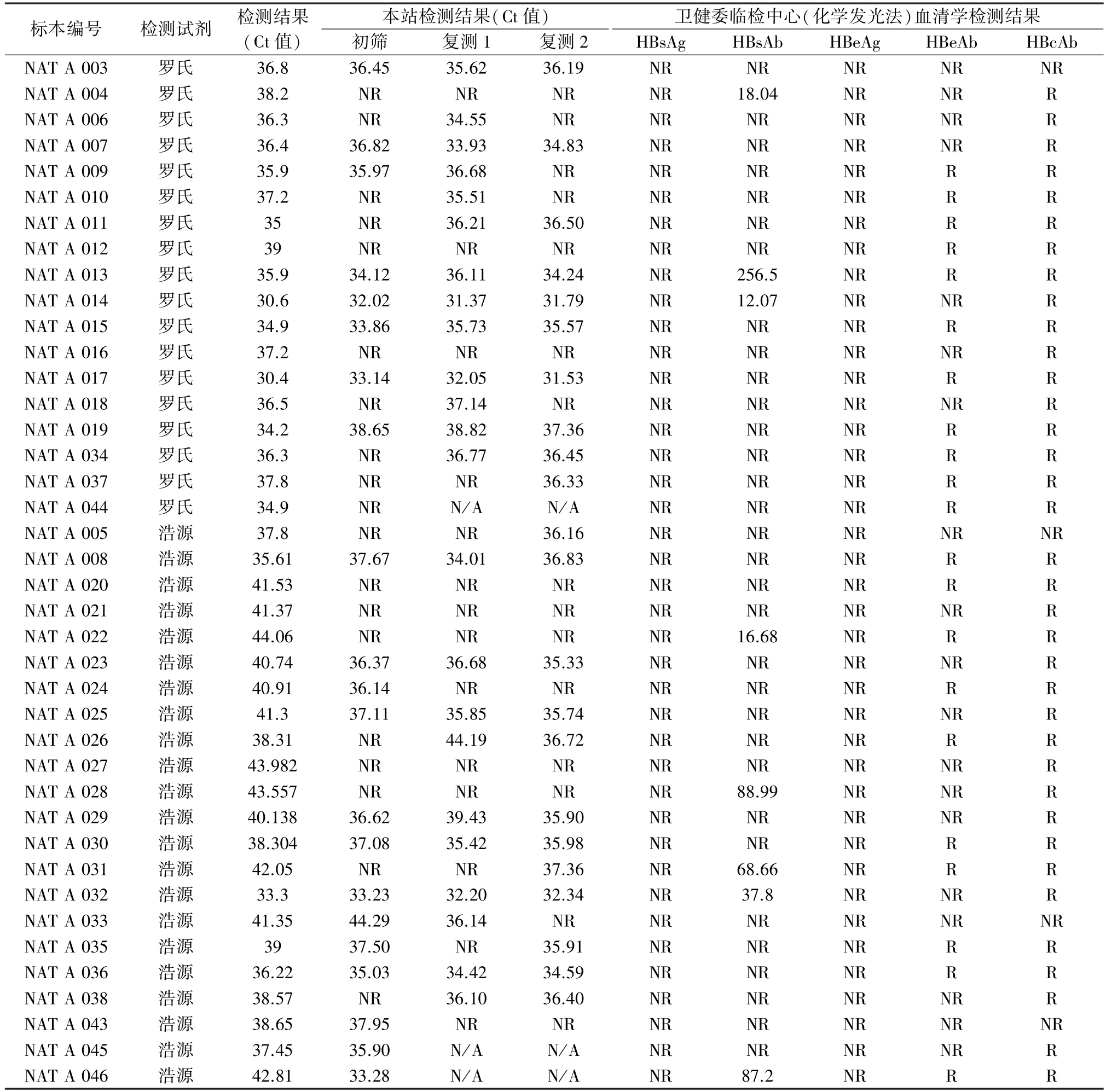
表8 HBV DNA 低浓度标本信息及在不同系统的检测结果

表9 HBV DNA 低浓度标本在不同海拔地区系统的检出情况
3 讨论
NAT 具有高灵敏度和高特异性,能够显著缩短血清学检测的“窗口期”,降低病毒经血传播风险,提升血液安全[1-3]。随着我国血液筛查核酸检测的基本全覆盖,如今NAT 已成为血液筛查实验室的重要检测手段[7]。 西藏那曲地区海拔在4 450 米以上,高寒缺氧,气候干燥,对国产的核酸检测系统是一个全新的挑战,因此其核酸检测过程的标准化要求也与低海拔地区具有明显差异[8]。 目前血液检测的标准化文件以及相关的法律法规,更多的是体现低海拔地区的特性,亟待建立符合高海拔地区特点的核酸检测系统技术指标和性能验证方法,以确保核酸检测工作的顺利进行,提升高海拔地区的血液安全[9-11]。 我们参考国家标准和行业标准,在国家卫生健康委临床检验中心的大力支持下,结合西藏那曲血站采供血特点和血液筛查实验室的工作实际,从多方面探索符合高海拔地区特点的核酸检测性能验证方案与方法。该研究选择在4 千米以上的海拔地区进行研究,再结合其他海拔高度的数据,如拉萨(海拔3 650 米)[18-19]等,可以得出该研究结果也适用于其他海拔高度的地区。
通过对分析灵敏度血清盘多浓度多基因型HBV DNA/HCV RNA/HIV-1 RNA 标本进行单人份检测,对HBV DNA和HIV-1 RNA 的高浓度标本的检出率均为100%,对中浓度标本的检出率均为90%以上;对检测结果进行分析灵敏度的PROBIT 分析显示,该系统对HBV DNA 的平均95% LOD 为8.29 IU/mL,HIV-1 RNA 的平均95% LOD 为40.52 IU/mL,远低于说明书声明的≤100 IU/mL。 由于该血清盘的标本量无法满足在低海拔地区再次检测的要求,因此本研究与低海拔地区的分析灵敏度的比较无法通过该血清盘的再次检测来实现,但通过相关报告[20]可以看出,使用该系统在低海拔地区进行性能验证的结果与高海拔地区没有差异。
该检测系统对HBV 和HIV 的检出能力均较好;HCV RNA 各基因型的检出率之间差异较大,这与检测系统对不同分型的HCV 检出存在一定的差异有关,不同的核酸检测系统之间对于HCV 片段的模板选择不一致,因此对于不同的分型检出能力就不一致[13-15];2 份220 IU/mL 的HCV RNA 6a 型高浓度标本未检出,均发生在同1 批检测中,原因可能与标本处理不当、病毒分布不均、提取过程受到抑制或操作过程中病毒核酸发生降解有关,这与高海拔地区的气压和空气密度的影响也有一定的关系,这就对实验室人员的操作提出了更高的要求,因此在进行核酸检测时的操作规范性就显得更为重要。 低浓度标本的检出在不同的检测系统的确存在一定的差距,但不同的检测系统在某种基因型上的检出能力上也的确可能各有不同。 从性能验证的数据看,与低海拔地区不存在明显的差异,因此低浓度标本的检出情况应该与低海拔地区没有明显的差异。 但系统本身在HCV 不同基因型的低浓度标本的检出上的确存在着较大的差异,这也与HCV 病毒本身的变异较大有关,不同的检测系统在模板的选择上存在着差异。 同时由于该血清盘标本的选择为其他系统检出的低浓度标本,因此使用在该系统进行检测本身就存在一定的客观影响,不能完全体现出该系统的检测性能。 从HBV DNA 以及HIV-1 RNA 在低浓度的检测数据来看,在性能上基本可以满足实验室检出性能的要求。 因此总体来看,该检测系统分析灵敏度基本能够满足实验室实际检测的需求。
重复性分析结果显示均为100%,且反应性标本的Ct 值变异系数波动范围较小,符合标准规定的≤5%,说明该系统检测的批内精密度较好,完全能够满足当地血站批量标本的检测要求。 交叉污染性能验证中,将阳性标本和阴性标本汇集交叉放置,按照日常检测模式进行检测,结果显示标本间没有发生交叉污染,说明该核酸检测系统具有良好的抗交叉污染的能力。
我国西藏地区是乙型肝炎的高发地区。 由于西藏地区的交通相对闭塞,医疗资源紧缺,因此对乙肝的防治开展较晚,献血人群中HBV 的感染率和漏检率都相对较高[12]。 为了减少HBV 的输血传播风险,在西藏自治区政府的支持下,血站与国家卫健委临检中心合作,对HBV DNA 低浓度标本进行多系统平行检测,以评估当前核酸检测实验室检测系统与其他系统之间的差异性[16]。 结果显示,该核酸检测系统对HBV 的检测能力较好,虽然实验室检测条件与低海拔地区具有一定的差异,但对弱阳性标本的总体阳性检出率也达到80%左右,复测阳性符合率为59.09%—77.78%,这与检测的次数有一定的关系,检测次数越多,检出的概率也越高[17]。 高海拔地区的采供血量相对较少,单检模式的筛查策略既能够在更大程度上减少HBV 低浓度标本的漏检率,也符合高海拔地区核酸实验室的日常检测要求。
根据国家卫健委关于做好“组团式” 对口支援西藏采供血工作的有关部署,大连市血液中心对口支援那曲市中心血站,以充分发挥优质医疗卫生资源作用。 那曲市海拔4 450米,其高海拔、低含氧量、低气压等特点对实验室检测设备、检测技术以及检测策略方面有不同程度的影响,与低海拔地区有着较大的差异[18-19]。 检测设备在高海拔地区的性能验证与低海拔地区的差异化评价是保证检测结果准确的重要手段,针对不同的检测系统进行性能验证,能够有效保证检测过程标准化以及检测结果的准确性。 本研究通过对核酸检测系统的分析灵敏度、重复性、防交叉污染等多项关键指标进行验证,对检测策略进行评估,结果达到预期要求,可满足高海拔地区实际检测的工作需要,填补了高海拔地区血液筛查核酸检测系统性能验证的空白,有助于确保高海拔地区血液检测过程的标准化,提高检测结果的准确性和可靠性,从而提升高海拔地区的血液安全水平,有利于提升高海拔地区的血液安全。 同时,本文提出的高海拔地区性能验证方案和方法也能为其他高海拔地区的采供血机构开展核酸检测工作提供了参考。 在不同的高海拔地区,可以根据本研究的方案和方法进行适当的调整和优化,以确保核酸检测系统在各地的准确性和可靠性。
利益冲突:所有作者均声明不存在利益冲突。
