颈动脉体瘤围手术期颅神经损伤症状评估专家共识△
2023-09-16中国微循环学会周围血管疾病专业委员会
中国微循环学会周围血管疾病专业委员会
颈动脉体瘤(carotid body tumor,CBT)是起源于颈动脉分叉处外膜的一种副神经节瘤,是较为罕见的头颈部肿瘤。多数情况下,CBT是生长缓慢的良性肿瘤,常以无痛性颈部肿块偶然被发现。增大的瘤体可压迫神经,使患者出现头晕、头痛、吞咽困难、声音嘶哑等症状。目前,手术切除仍是治疗CBT的主要方式。由于CBT的解剖位置复杂,病变常累及颅神经及颈部血管,手术致颅神经损伤(cranial nerve injury,CNI)的风险也较高。研究证实,手术所致的CNI是CBT患者术后最常见的并发症之一[1]。虽然大部分CNI患者的症状是暂时性的,但其对患者生活质量的影响很大,因此,早期识别CNI是尽早干预的首要及关键环节。开展CBT患者围手术期CNI的管理虽然已逐渐受到重视,但现阶段仍缺乏系统性的量化评估方法和指导方案。为此,中国微循环学会周围血管疾病专业委员会通过成立专项课题组,组织全国24所医院的CBT医疗、护理、康复方面的专家,以循证为基础,结合中国临床实践,总结多年临床经验,广泛征求专家组意见,经充分讨论后制定《颈动脉体瘤围手术期颅神经损伤症状评估专家共识》(以下简称《共识》),旨在为CBT患者围手术期CNI的量化评估提供指引,提高CBT患者CNI症状的评估及管理质量。《共识》的适用人群包括血管外科及头颈外科的医师、护士、康复医师等。此外,《共识》也为CBT患者自我报告结局(patient-reported outcome,PRO)和CBT患者围手术期护理提供参考依据。
1《共识》的形成
《共识》研究小组在系统回顾相关文献的基础上(表1)组织专家访谈并收集访谈资料,形成《共识》初稿。编制专家函询表并遴选专家,收集、整理专家的意见,并对专家提出的修改建议进行汇总分析,进一步完善《共识》。由中国微循环学会周围血管疾病专业委员会组织多学科专家经多次讨论、总结专家临床经验,并结合国内外文献报道,最终专家达成一致意见,形成《共识》终稿。
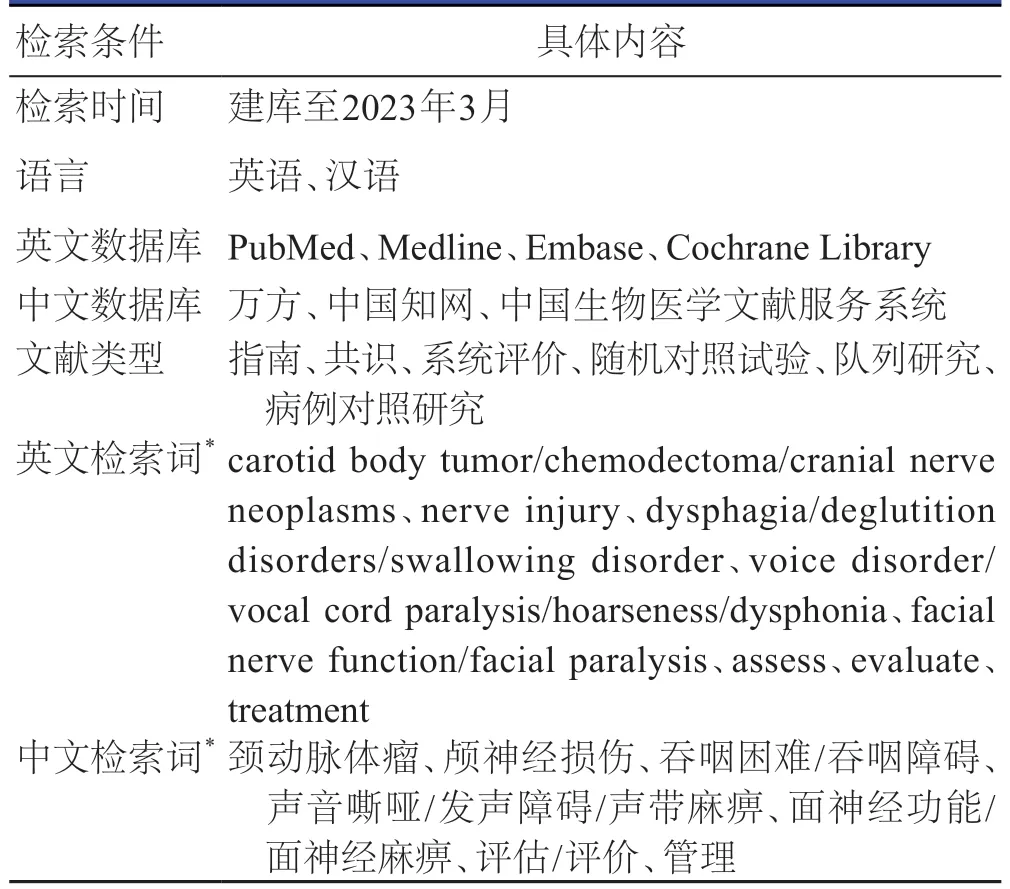
表1 文献检索策略
2 CNI 概述
尽管大部分CBT 常表现为无症状的颈部肿块,但当瘤体增大并累及神经时,会出现神经压迫的症状,例如,迷走神经受压迫而使患者出现声音嘶哑的症状。CBT 手术常因术中神经牵拉或淋巴结清扫等操作造成患者出现CNI的表现。术中操作可能累及的颅神经主要包括迷走神经、舌下神经、舌咽神经、喉上神经、面神经下颌支和交感干等,具体表现为伸舌偏斜、声音嘶哑、饮水呛咳、吞咽困难、嘴角歪斜、Honer综合征等[1-2]。患者的CNI症状可以是单一的,也可能是多种症状并存的。一项纳入4327例CBT 患者的Meta 分析结果显示,CBT 患者术后CNI 的总发生率为25.4%(1099/4327),95%CI:24.5%~31.3%,最常见的损伤是舌下神经(9.59%),其次是迷走神经(8.07%)[3]。颈动脉副神经节瘤国际合作登记处(Carotid Paraganglioma Cooperative International Registry,CAPACITY)的数据表明,CNI仍然是CBT切除术后最常见的并发症,短暂性CNI占17.1%,永久性CNI占2%[4]。
不同的CNI 造成的临床表现有交叠,而相同的损伤症状也可由多种神经损伤所致。例如,单侧迷走神经损伤可造成饮水呛咳、声音嘶哑的症状,双侧迷走神经损伤可造成吞咽困难、发声障碍的症状;声音嘶哑可由迷走神经损伤、喉返神经损伤造成,也可由气管插管所致的环杓关节脱位造成。面部表情肌受损甚至面瘫既可表现为面神经下颌缘支损伤造成的嘴角歪斜、鼻唇沟消失,也可表现为交感神经损伤造成的上睑下垂、外斜视。因此,考虑到在临床的普及性及实用性,本《共识》不以CNI 的类型作为划分依据,而从症状管理出发,以吞咽障碍、发声障碍、面部表情肌受损3个常见损伤症状为导向构建全文。
推荐意见1:CNI 既是CBT 患者围手术期常见症状,又是CBT 术后最常见的并发症之一。早期识别CNI 症状,无论是短暂性还是永久性CNI,都能为症状管理尽早提供依据。
3 CNI 影响因素
3.1 疾病相关因素
根据肿瘤与颈动脉的解剖关系,CBT 常被分为ShamblinⅠ型、ShamblinⅡ型、ShamblinⅢ型,其中,Shamblin分型越高,CBT切除难度越大。已有多项国内外研究表明,Shamblin分型是术后发生CNI的影响因素[5-7]。亦有研究表明,肿瘤至颅底的距离(tumor distance to base of skull,DTBOS)会影响CBT手术相关并发症的发生情况,特别是术后CNI的发生。一项来自不同国家纳入356例CBT 患者的多中心研究发现,DTBOS、肿瘤体积与Shamblin分型结合可以更好地预测术后出血和CNI的发生风险,其中,DTBOS 每减少1 cm,CNI的发生风险即增加1.5倍[8]。
随着手术及研究的深入开展,Shamblin分型对高位近颅病变的手术指导有限且对CNI的预测效果不佳[9-10],因此,有必要对CBT分型进行完善、革新,北京协和医院团队综合考虑肿瘤与颈动脉的包绕关系及生长高度,提出了CBT北京协和医院(Peking Union Medical College Hospital,PUMCH)分型[11-13],将CBT分为5型:(1)Ⅰ型,肿瘤上缘低于下颌角,手术通常不会发生永久性神经损伤。(2)Ⅱ型,肿瘤上缘位于下颌角与乳突下缘之间,且肿瘤不包绕颈动脉,手术通常无需行颈外动脉结扎或颈内动脉重建,不伴永久性神经损伤。(3)Ⅲ型,肿瘤上极位于下颌角与乳突下缘之间,且部分包绕颈动脉,多数肿瘤仍可成功剥离,一般不会发生永久性神经损伤。(4)Ⅳ型,肿瘤上缘位于下颌角与乳突下缘之间,且完全包绕颈动脉,神经损伤发生率高于Ⅰ~Ⅲ型。(5)Ⅴ型,肿瘤上缘高于乳突尖端水平,肿瘤位置高且体积巨大,手术出血量、颈动脉重建率和神经损伤发生率均极高。研究表明,PUMCH 分型与CBT 手术总体神经损伤、永久性神经损伤的发生率有显著关系[14]。因此,建议结合PUMCH 分型更好地对患者的神经损伤症状进行评估。
推荐意见2:Shamblin分型、DTBOS均是CBT术后出现CNI的主要疾病相关因素。
推荐意见3:临床诊断分型以传统Shamblin分型最常用,PUMCH 分型与CBT手术总体神经损伤、永久性神经损伤的发生率有显著关系,评估CNI症状时建议结合PUMCH 分型。
3.2 手术相关因素
由于CBT 与神经的解剖学关系,CBT 切除手术过程中发生神经损伤难以避免,手术相关因素也会影响CNI 的发生。对于患有双侧CBT 的患者,相较于一次性切除,分次切除双侧肿瘤所致的CNI 发生风险可显著降低[15]。蔡惠等[5]的回顾性研究发现,切断、结扎会造成永久性神经损伤,而钳夹、牵拉所致的神经损伤可在术后3~6个月恢复。研究发现,术中淋巴结清扫也是发生CNI 的独立危险因素[16]。在很长一段时间里,术前进行供养支动脉栓塞是CBT 切除术的重要辅助策略,但目前是否进行CBT 术前辅助栓塞在国际上引起学者争议。一项纳入4743例患者的Meta 分析表明,接受术前栓塞与否对CNI 的发生率没有显著影响,包括永久性CNI 和暂时性CNI[17]。
推荐意见4:一次性切除双侧CBT、术中淋巴结清扫、钳夹和牵拉均被认为是CBT术后发生CNI的手术相关因素。
4 CNI 的主要症状评估
4.1 吞咽障碍
4.1.1 概述
吞咽障碍是指因下颌、双唇、舌、咽喉等器官结构和/或功能受损,不能安全、有效地将食物输送至胃内的过程[18]。CBT 患者的吞咽障碍为生理解剖所致的狭义吞咽障碍,一般不包括认知及精神心理因素所致行为异常引起的摄食-吞咽障碍。PUMCH 分型中Ⅳ型、Ⅴ型患者的术前吞咽障碍可表现为声音喑哑和/或吞咽异物感,术后临床表现多样,例如,口腔分泌唾液但无法下咽、食物长时间停留在口腔内无法吞咽、饮水或进食出现呛咳、不能进食某些食物、咀嚼困难或伴有疼痛等。吞咽障碍除了会导致误吸、吸入性肺炎、营养失调等后果,严重的吞咽问题还可造成患者心理与社会交往障碍,因此,对CBT 患者开展吞咽能力的评估至关重要。
4.1.2 症状筛查
症状评估建议从筛查开始,目的是判断患者是否存在吞咽障碍及其风险程度,从而决定是否需要做进一步临床评估或仪器检查。临床医护人员应积极询问患者的吞咽感受,及早发现患者的吞咽问题。建议将术前筛查纳入吞咽障碍高风险人群的工作常规,筛查工作一般由主管医师或护士于床旁完成,若条件允许,言语治疗师等其他专业人员也可参与。CBT患者术后吞咽障碍高风险人群应包括但不限于术前触诊肿物较大的患者、PUMCH 分型为Ⅳ型及以上的患者、术前已出现咽部不适或声音嘶哑的患者、近期进行颈部手术的患者。在临床中,考虑到评估方法的可及性,推荐使用试验法和/或量表法开展吞咽障碍的筛查,具体如下。
(1)饮水试验(water swallow test,WST):在吞咽障碍筛查中应用广泛,但30 ml的饮水量会导致患者误吸的风险较高。为了保障WST的安全性,推荐使用国内改良版WST:饮水时间控制在5 s,首次饮水量1 ml,饮水呛咳时中止试验,若无呛咳的表现,则递增试水量,直至饮完30 ml 的水。
(2)反复吞咽唾液试验(repetitive saliva-swallowing test,RSST):观察患者30 s 内的吞咽次数,小于3次视为存在吞咽功能异常。此试验适用于老年患者,在进行WST之前使用此方法可降低患者误吸的风险。
(3)进食评估问卷调查工具-10(eating assessment tool-10,EAT-10):属于患者自评工具,共包含10个条目,每个条目的评分范围为0~4分,总分≥3分视为吞咽功能异常。建议结合WST进行评估,从而提高筛查的灵敏度和特异度。
(4)多伦多床旁吞咽筛查试验(Toronto bedside swallowing screening test,TOR-BSST):是以WST为主的吞咽障碍筛查他评工具。评估时要求患者在清醒状态下取端坐位,并能配合执行饮水、发声指令。TOR-BSST 判断3项内容,任何一项内容不通过则视为存在吞咽问题:①饮水前患者发声,观察嗓音和舌的运动状况;②给患者10茶勺水,最后用杯子饮水,每次饮水后即刻观察患者嗓音状况,并注意是否存在呛咳、流涎、湿音等改变;③观察饮水1 min后的嗓音状况。
推荐意见5:对疑似存在吞咽障碍的患者,主管医师和护士应积极开展针对吞咽障碍的筛查。筛查结果不作为吞咽障碍风险程度的量化,也不建议作为指导吞咽障碍管理的依据,不能取代临床功能评估或仪器检测。
推荐意见6:吞咽障碍的筛查旨在尽早发现患者的吞咽问题,不同方法的适用条件各异,建议评估者根据实际情况选择试验法、量表法单独使用或二者结合使用,从而提高筛查的灵敏度和特异度。针对一般患者,采用改良版WST结合EAT-10,将主观评价和客观评价相结合,提高评估的准确性。针对老年患者,推荐使用RSST作为筛查工具,降低误吸的风险。
4.1.3 临床评估
临床评估吞咽功能的目的是判断患者进食不同食物发生吞咽障碍的风险程度,应在获知吞咽障碍筛查异常结果后尽早进行临床评估。容积-黏度测试(volume-viscosity swallow test,V-VST)可安全、迅速、准确地评估吞咽功能,并能帮助患者选择摄取食物最合适的容积和黏稠度,因此,建议采用V-VST 进行临床吞咽功能评估。将观察患者吞咽功能时选择的容积分为少量(5 ml)、中量(10 ml)、多量(20 ml),稠度性状分为水样(低稠)、浓糊状(中稠)、布丁状(高稠),按照不同组合测试,共需进食9次。测试前应确保患者有足够的体力和耐力完成评估,且没有呼吸道问题。测试过程中重点观察进食的安全性和有效性,从而判断患者进食有无风险[19],具体如下。
(1)进食安全性指患者进食过程中是否存在误吸风险,可以通过下列指标判断有无必要继续进行增加稠度的测试:①咳嗽;②音质变化,吞咽后声音变得湿润或沙哑;③血氧饱和度下降。
(2)进食有效性指患者是否能够有效进食,是否能够满足所需的热量、营养和水分。有效的进食需满足以下指标:①唇部闭合,无食物漏出;②口腔无残留,舌运送能力未受损;③咽部无残留,咽部清除食物能力未受限;④可通过单次吞咽动作吞下食物,无需分次吞咽。
(3)测试时需注意的要点:①进食姿势。观察患者进食姿势的调整是否会对吞咽造成影响。②黏稠度和进食量。有研究建议,从黏稠度中等的糊状食物开始测试,若无法满足5、10、20 ml 的进食量顺序,也可调整为3、5、10 ml 的进食量顺序[9]。建议将V-VST 作为量化评估工具,不同于筛查工具,当无法满足原始评估工具要求的5、10、20 ml时,即可判定评估结果,不建议通过调整容积的方式进行评估。③食物清除能力。建议患者于进食前后发声,从而评估口腔内有无食物残留及残留量。④颈部听诊与血氧饱和度监测。可将听诊器置于患者颈部,通过听诊患者吞咽的声音辅助判断有无误吸情况发生;可使用血氧仪实时监测患者的血氧饱和度。⑤分泌物情况。观察患者的唾液分泌量是否正常、进食后痰液及唾液是否增多、咳出的痰液是否夹杂食物。
推荐意见7:若无禁忌证,吞咽障碍的临床评估建议采用V-VST。
推荐意见8:临床评估过程中需要关注安全性和有效性,临床医护人员应及时识别患者的进食风险。
4.1.4 辅助检查
吞咽造影检查(video fluoroscopic swallowing study,VFSS)是在X线的透视下,针对整个吞咽运动所进行的特殊造影检查,是诊断吞咽障碍的金标准[20],但不能经口进食、无法配合吞咽动作的患者不适合进行此项检查。VFSS不仅是定性和定量分析患者吞咽障碍的重要方法,还是指导患者调整进食姿势的干预依据。
软式喉内窥镜吞咽功能检查(flexible endoscopic examination of swallowing,FEES)通过软管喉镜检查患者吞咽时气道保护性吞咽反射功能和食团运输功能,虽然不能直观评价吞咽器官的协调性,但能更好地反映咽喉部解剖结构和分泌物积聚情况,适用于评估患者手术后的吞咽功能障碍情况。同时,FEES设备携带方便,检查时无X线辐射,因此,可多次进行检查,从而判断患者不同时期的吞咽能力,临床使用率高。
推荐意见9:尽管VFSS 和FEES是确定吞咽障碍的金标准,二者各有所长,但不同级别医疗中心的设备及技术条件不同,评估者应结合病例和技术条件选择应用,有条件的医疗中心推荐二者结合使用,以达到优势互补。
4.1.5 评估时机
对于双侧CBT 患者,在进行另一侧CBT手术前,无论患者是否有吞咽障碍的主诉,均建议常规评估吞咽功能。对于单侧CBT患者,术前一般不会硬性检查吞咽功能。由于术中插管所致喉部的激惹和水肿,大部分患者术后会出现吞咽不适,为了排除这个因素,需评估患者首次进食前的吞咽功能。此外,应积极询问患者的吞咽感受,并告知患者在进食不同食物时若出现任何程度的吞咽问题均应及时告知医务人员。术后患者吞咽功能的评估直至患者可正常进食为止。
4.2 发声障碍
4.2.1 概述
发声障碍可由声带麻痹引起,包括音调异常、响度异常和音质异常3种情况。声带麻痹是指支配喉内肌群的运动神经传导通路受损导致声带的运动障碍,可同时伴有喉部感觉神经障碍。除了发声障碍,呼吸困难、呛咳、误吸及吞咽障碍等也是声带麻痹的体现。CBT患者术后出现发声障碍主要与单侧声带麻痹有关,异常音质表现为嘶哑声、粗糙声、气息声。
术后出现发声障碍的原因除术前瘤体压迫、术中神经牵拉外,还包括术中气管插管所致的环杓关节脱位和半脱位、术后喉部的激惹和水肿,因此,术后应进行临床评估和仪器检查,有助于明确嗓音改变的原因,并为制定干预措施提供依据。
4.2.2 症状筛查
术前病史采集和患者的主诉是术后发声障碍筛查的基础,主要采集的病史因素应包括但不限于以下内容:有头部、颈部、胸部的近期外科手术史,近期进行了气管插管,颈部存在肿物,呼吸窘迫或出现喘鸣音,有吸烟史等[21]。同时还应关注患者是否为职业用嗓人群,如主持人、演员、歌唱家、配音员、教师、记者等[22]。
推荐意见10:初步筛查发声障碍时应确认患者是否有与发声有关的病史,分辨造成发声障碍的因素并关注患者是否为职业用嗓人群。
4.2.3 临床评估
发声障碍的标准化评估具有复杂性和专业性,特别是客观声学评估,受限于各地医疗中心的条件及评估者资质,通过听感知评估便可判断严重的发声障碍。因此,建议医务人员应该能够准确认定影响沟通或降低生活质量的发声障碍[23]。
(1)听感知评估:由评估者对声音进行多维度分级,评估嗓音的音质、音调、音量、音值。由于医务人员的听感知评估是一种主观评估,为了减少评估者之间的异质性,评估过程应使用标准的语言诵读样本,但目前国内尚无统一的标准。客观、系统、复杂而没有偏见的听感知评估是非常难做到的。目前,国际上最常用的主观听感知评估方法是日本言语语音学会提出的GRBAS 分级法[24],包含总嘶哑度、粗糙度、气息度、无力度、紧张度5个评估参数,重点分析总嘶哑度。
(2)客观声学评估:声音的客观评估是基于计算机辅助的声学分析,由临床医师诠释检查结果。受限于各级单位条件及评估者的资质,评估者应根据现实应用评估方法的条件和能力,以及患者的有效参与程度来选择患者的嗓音评估指标。客观声学指标主要包括声学分析指标和空气动力学指标。声学分析指标包括基频微扰、振幅微扰、噪谐比、倒频谱峰值突出;空气动力学指标包括最长发声时间、平均气流率[25]。
推荐意见11:临床医务人员应具备识别患者发声障碍的能力,并能明确影响患者生活质量的发声障碍。主观评估推荐使用GRBAS分级法。客观评估受限于各级医疗机构的条件,临床医务人员可基于评估者资质和客观条件来选择适合的评估指标。
4.2.4 辅助检查
喉镜检查是诊断发声障碍的必要检查,动态频闪喉镜检查可观察声带在不同发声时相的振动情况,目前被嗓音专业医师广泛采用,但频闪喉镜检查具有一定的局限性,纤维喉镜或电子喉镜检查方法仍然有其不可替代的价值,因此,建议合并吞咽障碍的发声障碍患者可先进行纤维喉镜或电子喉镜检查,再选择是否进行动态频闪喉镜检查[26]。喉肌电图检查可以诊断神经肌肉损伤程度,是诊断声带麻痹的金标准。考虑到喉肌电图检查在全国范围内并不普及,因此不做强制推荐。中国、美国、韩国制定的发声管理指南均认为患者出现发声障碍一般无需进行影像学检查[25,27-28]。对于以嗓音问题为主诉的患者,临床医务人员不应在喉镜检查之前进行计算机断层扫描(computed tomography,CT)或磁共振成像(magnetic resonance imaging,MRI)检查[21]。
推荐意见12:考虑到各级医疗中心的条件,诊断发声障碍建议先采取纤维喉镜或电子喉镜检查,再选择是否进行动态频闪喉镜检查,一般无需采取影像学检查。
4.2.5 患者自我评估
发声障碍通常在患者发声时被自己或他人发现,因此,患者的主观评估和医务人员的感知评估具有同等价值。对患者嗓音的评估通常以问卷调查的方式进行,推荐使用嗓音障碍指数(voice handicap index,VHI)量表进行调查,这是目前使用最多的患者自身评估方法。VHI 量表包括生理、功能和情绪3个维度,共计30个条目,每个条目包括5个评价等级。中文版VHI量表[29]已得到临床验证,可有效判断发声障碍对患者生活质量、生理功能、社会适应性、情感变化的影响,是当前评估发声障碍患者主观感受的最佳方法。
推荐意见13:患者的自我评估对异常嗓音的识别与医务人员的评估具有同等价值,推荐使用中文版VHI量表进行评估。
4.2.6 评估时机
CBT患者术后嗓音的改变受多种因素影响,目前尚无证据推荐最佳评估时机,很难给出统一的、标准化的评估时机,因此,基于临床实践,建议临床医务人员至少应在术前、术后发生症状时以及症状转归阶段对患者的嗓音情况进行评估,特别是针对术前PUMCH 分型可能会引起嗓音改变的患者进行评估,具体如下。
(1)初次评估。对于经术前影像学检查确定为PUMCH 高分型、术后可能造成嗓音改变的患者,在确定实施CBT 外科手术时,建议手术医师对患者的嗓音进行评估并记录,建立嗓音基线。对于术前已嗓音受损的患者应进行喉功能评估,检查声带的活动性。基线评估内容不仅包括判断患者的术前嗓音情况,对于术后易发生嗓音改变的高危患者,还应告知存在嗓音改变的手术风险,并询问患者对术后嗓音的预期值,特别是职业用嗓人群。对于双侧CBT 患者,在进行另一侧CBT 手术前,无论患者是否有发声障碍的临床表现,均建议常规使用喉镜检查声带功能[30]。
(2)术后评估。由于术后喉部激惹和水肿,患者术后通常会存在不同程度的发声受损表现,因此,术后水肿起始期、术后水肿恢复期是评估是否存在发声障碍的两个推荐时机。目前,尚无关于水肿期的准确定义,通常认为水肿期发生在术后3~10 d。患者应被提前告知,术后出现任何嗓音改变都应及时告知医务人员。
(3)症状转归评估。若发声障碍在发病后4周内未得到缓解或改善,或者怀疑有严重的潜在病因,医务人员应进行喉镜检查[23]。对于专业用嗓患者,需要增加客观声学评估或仪器评估。大部分患者的声带运动可在起病后6个月内自然恢复,也有患者的声带运动在发病后6~12个月恢复[28],因此,除非已明确无法恢复喉功能,在进行声带麻痹的永久性治疗前应至少观察6个月[25]。
推荐意见14:建议手术医师在术前评估患者的嗓音并建立嗓音基线,对于术后易发生嗓音改变的高危患者,应获取其对术后嗓音的预期值。双侧CBT患者行另一侧手术前应常规检查声带功能。
推荐意见15:术后患者的嗓音评估时机以喉部水肿期为准,术后水肿起始期、术后水肿恢复期为评估发声障碍的两个推荐时机。
推荐意见16:若发声障碍在发病后4周内未得到缓解或改善,或者怀疑有严重的潜在病因,医务人员应进行喉镜检查。大部分患者的声带运动在6个月内可自然恢复。
4.3 面部表情肌受损
4.3.1 概述
瘤体浸润生长压迫交感神经或术中损伤均会导致Horner综合征,临床表现为眼睑下垂、瞳孔缩小及同侧面部无汗。无论是哪一种分型,CBT 患者术后均有可能出现面神经下颌支损伤所致的面部表情肌受损症状。面神经损伤会导致面瘫,临床表现为额纹变浅或消失、抬眉困难、闭眼露白、眼裂增大、鼻唇沟变浅、鼓腮漏气、嘴角向健侧歪斜、流泪及流涎等,还可出现味觉减退或听觉过敏的症状[31]。相较于吞咽障碍、发声障碍的评估,关于面部表情肌损伤症状的评估发展较慢,现有的评价系统存在争议,尚缺乏一套适用于临床评估的金标准。
推荐意见17:无论是哪一种分型,术中操作均有可能造成CBT患者出现面部表情肌受损的症状。建议临床医务人员综合考虑评估方式及所在医疗机构的客观条件,选择适用的评估方法。
4.3.2 症状筛查
症状筛查的主要目的是早期识别患者面部表情肌的改变,以免错过最佳干预时机。临床医护人员应积极重视患者支配面部表情肌时的主观感受,并观察患者的面部是否对称。
推荐意见18:面部表情肌受损症状的筛查以患者支配面部表情肌的主观感受为主,以临床医务人员的肉眼观察评价面部对称性为辅。
4.3.3 临床评估
目前临床上对面神经功能损伤的病情程度、治疗效果及预后的评估均无统一的方法及标准。现有的评估系统根据是否依赖观察者的主观评价可以分为主观评价系统和客观评价系统。基于观察者视觉的主观评价系统具有易掌握、易推广、成本低的优势,但评价者的专科临床经验评估结果的稳定性不可控;基于视觉信息的客观评价系统在指标量化、可重复性、评价者间的一致性等方面具有明显的优势,但受限于现代化技术和成本因素而难以开展。考虑到客观评价系统在评估者培训及临床使用方面的不便,在此仅对主观评价系统进行介绍。
House-Brackmann(HB)面神经功能分级系统是目前应用最广泛的主观评价系统,美国耳鼻喉头颈外科学会(American Academy of Otolaryngology-Head and Neck Surgery,AAO-HNS)推荐HB面神经功能评估系统作为评估面神经功能的“金标准”。该系统的评价内容包括肉眼观察、静止和运动,适用于早期和恢复期的评估。HB面神经功能评估系统具有评估简单、评估结果直观明了的优点,但灵敏度较差,对于面神经功能正常或轻度面瘫,观察者间的评价稳定性较好;对于中重度面瘫,观察者间的评价稳定性较差。观察者的年资越高,评价的稳定性越好[32]。
Sunnybrook面神经功能评估系统的应用范围仅次于HB面神经功能评估系统,评估过程较为复杂,但评价者间的一致性高于HB面神经功能评估系统,且可靠性高。Sunnybrook 面神经功能评估系统结合面部肌肉静态运动、动态运动及联带运动来评定面神经功能,评分范围为0~100分,其中,0分视为面瘫程度最严重,100分视为正常。目前,已有中文版Sunnybrook面神经功能评估系统,信效度良好[33]。
适用于临床的面神经功能评价标准宜粗不宜细,过细的评价标准虽然具有较高的精确性和灵敏度,但会降低评估者间的稳定性。然而主观评价系统依赖于观察者的主观评价,很难做到稳定性和灵敏度的平衡,尽管客观评价系统对评价者的要求非常高,但其起到的作用亦不容忽视。
推荐意见19:主观评价系统是现阶段最易掌握和推广的面神经功能评估方式,建议根据患者的临床特点选择使用HB或Sunnybrook面神经功能评估系统。
4.3.4 辅助检查
神经电生理检查是面神经功能的定量评估方式,现有技术包括神经电图(electroneurography,ENoG)、肌电图(electromyography,EMG)、瞬目反射检测、面神经F 波、神经兴奋性试验(nerve excitability test,NET)、最大刺激试验(maximum stimulation test,MST)及经颅磁刺激技术等,临床应用较多的是ENoG和EMG。ENoG是经皮刺激面神经干,记录并分析健侧和患侧面肌收缩时诱发的复合肌肉动作电位,通过了解患侧面神经纤维变性的数量来判断神经功能损伤的程度,急性期多次复查ENoG可提高结果的可靠性,并有助于评估预后。EMG是一种记录肌肉安静状态下和随意收缩状态下神经-肌肉的电活动的检查方法,是检查周围神经系统功能状态的主要手段,根据测量方式可分为针极肌电图(needle electromyography,nEMG)和表面电极肌电图(surface electromyography,sEMG)。nEMG通过插入肌肉的针电极记录面肌的电活动,sEMG则通过置于皮肤表面的电极进行记录[31]。ENoG、EMG联合瞬目反射检测对面神经损伤的早期诊断、定位诊断及判断预后具有重要价值,建议广泛开展。
推荐意见20:当患者出现面部表情肌受损的症状时可行神经电生理检查。若医疗条件允许,推荐结合使用ENoG、EMG及瞬目反射检测。
4.3.5 患者自我评估
面部表情肌的改变不仅会影响患者的外观,也会对患者的社会行为、心理健康、工作、生活造成影响,因此,除了临床医师的评估,患者的自我评价也具有重要意义,目前应用最多的自我评价量表是临床面部评价(facial clinimetric evaluation,FaCE)量表,共15个条目,包含面部运动、面部感觉、口腔功能、眼睛感觉、泪液分泌、社会功能6个维度,该量表不仅关注患者生理、解剖导致的运动异常,也关注患者的生活质量,已被汉化译制[34],适合临床推广使用。
推荐意见21:患者的自我评估也是症状评估的重要部分,推荐使用FaCE 量表评估面部表情肌受损患者的生活质量。
4.3.6 评估时机
(1)术前评估。综合患者的术前检查结果和手术医师的临床经验,针对术后可能造成面部表情肌改变的患者,在确定实施CBT 外科手术时,建议手术医师对患者的面部表情肌进行评估并记录,并告知患者手术风险,充分询问患者对术后面部表情肌改变的预期值,特别是年轻女性患者。(2)术后评估。患者术后面部的主观评价对面部表情肌受损症状的评估具有重要意义,因此,应将这些情况提前告知患者,若术后发现嘴角歪斜、上睑抬起费力的症状,应及时告知医务人员。与吞咽困难、发声障碍的康复相比,面部表情肌受损症状的缓解需要更长的康复时间。
5 小结
本《共识》以症状管理为导向,基于国内外现有的文献证据及多年、多中心的临床经验,对CBT患者的CNI评估策略达成专家共识,为临床医务人员提供借鉴与参考。CNI的评估与管理涉及血管外科、口腔科、耳鼻咽喉科、头颈外科、神经内外科、康复医学科等多个学科,护理人员作为医疗护理的执行者,在患者术后评估与康复管理中发挥着重要作用。因此,护理人员应充分认识到症状评估对患者的重要意义,并结合临床实际,基于该领域的共识为制定评估策略及症状管理提供理论支持,最终使患者获益。
主要执笔专家(按姓氏汉语拼音排名)
梁和静(中国医学科学院北京协和医院)、王磊(中国医学科学院北京协和医院)、曾嵘(中国医学科学院北京协和医院)
参与本共识讨论、审校的专家(按姓氏汉语拼音排名)
蔡永华(中国医学科学院北京协和医院)、陈佳嫔(中国医学科学院北京协和医院)、成咏(上海交通大学医学院附属第九人民医院)、冯俊(西安交通大学第一附属医院)、顾光超(中国医学科学院北京协和医院)、郭明华(中国医学科学院北京协和医院)、黄文静(青岛大学附属医院)、金珊珊(首都医科大学附属北京友谊医院)、李海燕(海军军医大学第一附属医院)、李拥军(北京医院)、李震(郑州大学第一附属医院)、刘玲(首都医科大学附属北京安贞医院)、牛敬荣(首都医科大学附属北京朝阳医院)、秦晶(郑州大学第一附属医院)、邱菊(北京华信医院)、曲乐丰(海军军医大学第二附属医院)、沈谢冬(海军军医大学第二附属医院)、王豪夫(青岛大学附属医院)、王磊(中国医学科学院北京协和医院)、王伟娜(中国科学技术大学附属第一医院)、许慧平(内蒙古自治区人民医院)、许静(四川大学华西医院)、叶志东(中日友好医院)、虞奋(复旦大学附属中山医院)、曾嵘(中国医学科学院北京协和医院)、战颖(北京大学人民医院)、张丽(山东第一医科大学附属省立医院)、张丽金(首都医科大学附属北京朝阳医院)、张望德(首都医科大学附属北京朝阳医院)、赵纪春(四川大学华西医院)、赵珺(上海交通大学医学院附属第六人民医院)、赵肖奕(中国医学科学院北京协和医院)、赵志青(海军军医大学第一附属医院)、郑月宏(中国医学科学院北京协和医院)、周红艳(西安交通大学第一附属医院)、周瑾(中日友好医院)、祖金美(河北医科大学第一医院)
利益冲突所有作者均声明不存在利益冲突
