CuMgAl-LDH超分子材料的组装及其晶胞结构
2023-09-07吴健松许立淼李康艳陈乔华严大镔陈创浩黄保莹董江珊
吴健松,许立淼,李康艳,陈乔华,严大镔,陈创浩,黄保莹,董江珊
(1.广东茂名幼儿师范专科学校理学院, 广东 茂名 525000; 2.岭南师范学院化学化工学院, 广东 湛江 524048)
0 引言
全球快速发展都要求低碳、环保、清洁.因此,要求工农业都必须使用清洁能源,此乃全球共同呼吁。高效催化剂的研制是清洁能源研发极其重要的一个方面.CuMgAl-LDH正是一种具有高效催化性能的催化剂,因它具有高效且快速的优良性能而受高度关注[1-3],其中LDH(layered double hydroxides)是一种层状双金属氢氧化物,人工制备的LDH可设计组装为具有超分子结构的材料.超分子指的是由2种或2种以上的分子,凭借分子彼此之间的相互作用力结合在一起,组成较为复杂的、有一定空间结构的大分子聚集体,并能够保持一定的完整性,使聚集体具有明确的微观结构和宏观特性.这里的“明确的微观结构”是指晶体内部结构非常有序有规律,而不是杂乱无章.CuMgAl-LDH超分子材料就是铜取代原来LDH中部分的镁并且晶体内部结构十分规则,点阵排布井然有序等.铜取代镁,这种取代使得LDH具有更高的催化性能和更高的催化效率.LDH类催化剂结晶程度的大小、内部点阵的有序性和多孔结构对催化效率和速度都有重要影响[4-5].LDH超分子晶体内部结构越规律、比表面越大、微孔在所有孔总量中占的比率越高,可吸附的(催化)底物就越多,催化速度和效果将更优[6].不仅如此,超分子材料的孔可以更加有效地“绑住”(催化)底物,可更加有效地防止底物在转化过程中离开催化区域而致使催化作用半途而废,有效地抑制催化逆反应的发生.
CuMgAl-LDH是一类很有前景的含铜类催化剂[4,7].有关LDH类化合物的合成技术、特殊晶体结构与特殊化学功能、传统制备的方法与技术等的报道很多[8-11].这些方法有的是在有机介质体系下进行的,有的是在微波加热下制备的,也有借助“模板”合成的,都取得一定的成果.但是在传统制备方法技术上,LDH类材料普遍存在如下的问题:第一,在总量产物中CuO单相物质量百分比较大,也就是容易生成大量的氧化铜单相物且聚结严重.这是因为铜离子具有Jian-Tai效应,它不易进入LDH晶体中作为点阵的组成;第二,LDH产物经常有少部分无定形物与晶体共存,结晶度不高,例如有如Al(OH)3无定形物存在;第三,产物虽然具有孔状结构,但在孔的总量中却以中孔占有较大的比例,微孔在孔总量中占小比例,比表面积不够大等.这些问题都使作为催化材料的LDH化合物催化效率与性能不高.因此,本研究设法采用在缓冲介质下慢速生长晶体,希望在一定程度上解决上述这些问题,以制备具有超分子结构的CuMgAl-LDH.
1 实验部分
1.1 仪器与试剂Al (NO3)3·9H2O、Cu (NO3)2·3H2O、NaOH、Na2CO3、Mg(NO3)2·6H2O 、NaHCO3等试剂.纯度为分析纯,购于广州化学试剂厂.制备仪器有:CJF-1 L不锈钢高压反应釜(配磁力搅拌),上海科升.测试仪器有:D/Max-3C X射线衍射仪;HITACHI S-4800型扫描电镜(日本日立);ULTIMA型发射光谱仪(测定Cu、Al元素,法国JY公司) ; PE2400 SeriesⅡ CHNS /O分析仪(测定H、C元素,美国); ASAP 2010比表面积/空隙分析仪(美国 Micromeritics公司).
1.2 CuMgAl-LDH超分子的组装
1.2.1 多种溶液的配制 Na2CO3-NaHCO3混合液(即缓冲液)并使其pH=10.3,在这个混合液中,Na2CO3和NaHCO3浓度均为0.30 mol/L;0.60 mol/L Na2CO3溶液;0.5 mol/L Cu (NO3)2·3H2O溶液;0.2 mol/L Mg(NO3)2· 6H2O; 0.2 mol/L Al (NO3)3· 9H2O溶液;2.0 mol/L的NaOH溶液;0.1 mol/L的NaOH溶液.
1.2.2 溶液的混合 将上述浓度的Mg(NO3)2· 6H2O、Cu (NO3)2· 3H2O和0.2 mol/L Al (NO3)3· 9H2O作等体积混合后,在搅拌下用将混合体系pH值调至6.8(此时体系已有大量沉淀生成),调节过程为:先用2.0 mol/L的NaOH调至6.6左右,再用0.1 mol/L的NaOH小心调至6.8.继续搅拌2 h.将体系pH值调至6.8的目的是为了防止CO32-与Al3+发生双水解(下一步将加入CO32-).
1.2.3 加入缓冲液和沉淀剂 取一定量的缓冲液(Na2CO3-NaHCO3),加入到上述第2步得到的体系中,加入体积是第2步得到溶液的一半,再加0.6 mol/L Na2CO3溶液,加入Na2CO3的摩尔量是Al (NO3)3· 9H2O摩尔量的1.3倍,加入1.3倍Na2CO3的目的是提供足够的OH-.研究认为缓冲液中的CO32-不参与反应,或者说即使CO32-参与了反应,但随即又被后来加入的Na2CO3作了补充.关于缓冲溶液的作用,本研究将在介绍各样品的测试表征结果之后再另作讨论.
1.2.4 水热反应 取第3步得到的混合体系浆料于高压反应釜内,并使其装满度为70%,设置好一定的反应温度(T)和反应时间(t),水热反应结束后过滤,依次用蒸馏水、去离子水洗涤沉淀,然后将沉淀放于80 ℃烘箱内烘干(36 h)即得样品.
2 结果与讨论
2.1 最优组装条件试验为探索到最优的制备条件,作单因素试验.分别试验时间、温度、加入缓冲对体积比对产物的影响.
2.1.1 反应时间对CuMgAl-LDH超分子品质的影响 除了反应时间外,其他反应条件均不改变(如反应温度T=155 ℃不变,各物料浓度也不改变等,下同),仅改变反应时间t,以考察反应时间t对产物“品质”的影响.这里说产物的“品质”是指氧化铜含量的多少(通过目视法判断),氧化铜越多越是不好,越少越好.氧化铜越多,产物颜色就越黑,产物越黑即“品质”越不好,越不显得黑就越好.表中用“+++”表示产物非常黑,至少有30%以上的氧化铜混于其中;用“++”表示较黑,至少有10%以上的氧化铜混于其中;用“+”表示有黑色物质存在,但比例较少(可认为小于5%),用“-”表示肉眼已观察不到黑色物质存在(但不能肯定没有氧化铜混于其中,或认为氧化铜的含量小于1%).事实上,对于含铜类LDH,通常认为氧化铜含量小于1%就是“品质较好”的了,此时观察到样品是灰蓝色.表1列出了反应时间对CuMgAl-LDH产物品质的影响.从表1可见,反应时间105 h是最优的.
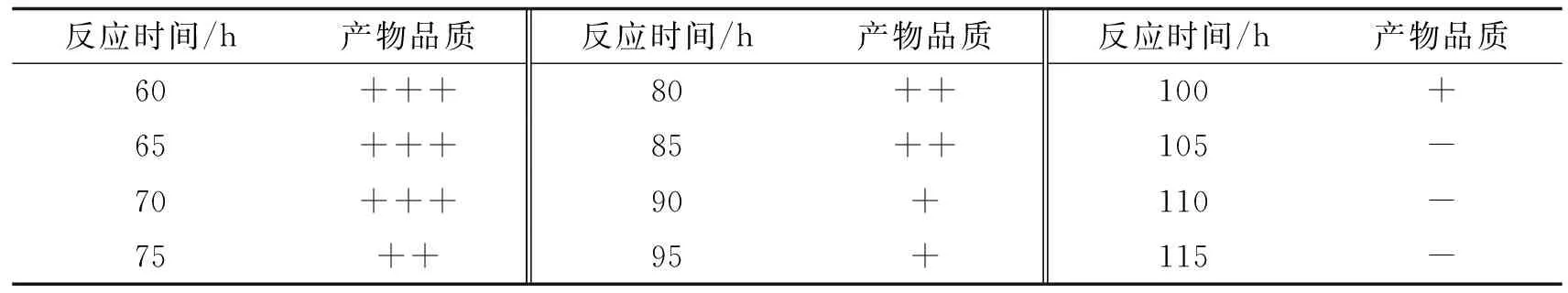
表1 反应时间对CuMgAl-LDH产物品质的影响
2.1.2 反应温度对CuMgAl-LDH超分子品质的影响 保持最优的反应时间(t=105)不变,仅改变反应温度,考察反应温度T对CuMgAl-LDH超分子品质的影响.表2列出了反应温度对CuMgAl-LDH产物品质的影响.从表2可见,反应时间155 ℃是最优的.

表2 反应温度对CuMgAl-LDH产物品质的影响
2.1.3 加入的缓冲溶液体积对CuMgAl-LDH超分子品质的影响 保持最优的反应时间(t=105 h)、反应温度(T=155 ℃)不变,仅改变缓冲溶液体积比(即加入的缓冲溶液的体积与反应体系体积之比),以考察缓冲溶液对CuMgAl-LDH超分子品质的影响,表3列出了缓冲溶液体积比对CuMgAl-LDH产物品质的影响.从表3可见,缓冲溶液体积比为0.5是最优的.
2.1.4 原料中 Cu (NO3)2·3H2O浓度对CuMgAl-LDH超分子品质的影响 保持上述最优条件不变(详见2.1.1~2.1.3),仅改变原料中Cu (NO3)2·3H2O浓度(这个浓度指的是一开始配制的浓度,并不是后来各种混合后的浓度),考察Cu (NO3)2·3H2O原始浓度对产物品质的影响,表4列出了Cu (NO3)2·3H2O原始浓度对产物品质的影响.从表4可见,Cu (NO3)2·3H2O原始浓度为0.5 mol/L是最优的.

表3 加入缓冲溶液的体积比对CuMgAl-LDH产物品质的影响

表4 Cu (NO3)2·3H2O原始浓度对产物品质的影响
2.1.5 原料中Mg(NO3)2·6H2O、Al (NO3)3·9H2O和Na2CO3浓度对产物品质的影响 研究发现,原料中Mg(NO3)2·6H2O、Al (NO3)3·9H2O和作为沉淀剂的Na2CO3浓度(原始浓度)对产物品质的影响不是很大,所以不在这里一一赘述.但须指出,这3种物质如果浓度太大(特别是Al (NO3)3·9H2O),也会因胶团凝聚严重而影响终产物的分散性,也不利于CuMgAl-LDH超分子的组装.

图1 样品A的XRD衍射图
2.2 最优样品的XRD衍射分析和化学式的确定取上述最优条件下得到的最优样品(为表述方便,将此样品记为“样品A”,下文的表征均是指样品A)作XRD分析.最优条件即上述单因素试验所得的最优参数:反应时间为105 h,反应温度为155 ℃,缓冲溶液体积比为0.5,Cu2+初始浓度为0.5 mol/L等.样品A的XRD衍射分析结果见图1,将图1的特征衍射峰与标准衍射比较,证明样品A为LDH类化合物.表5列出了样品A在(003)、(006)和(009)上的衍射数据.由布拉格公式2dsinθ=nλ, 可计算得d(003)、d(006)、d(009)一并列于表5中. 从表5可见,d(003)基本上是d(006)的2倍,是d(009)的3倍,证明CuMgAl-LDH晶体内部点阵排列非常有规则,层与层之间的排布井然有序.

表5 样品的XRD衍射数据
依文献示将衍射峰指标化并计算各晶胞参数 (其中a= 2d( 110),c=d( 003) + 2d( 006) + 3d( 009),h=层间距-层厚(约 0. 477 nm).计算结果如下:a=0.302 nm,c=2.411 nm,h=0.323 nm.计算结果表明CuMgAl-LDH与天然LDH的晶胞参数很接近[10].这表明用Cu2+部分代替Mg2+离子后,CuMgAl-LDH的晶胞参数基本不变,那是因为Cu2+和Mg2+离子半径很接近,Cu2+和Mg2+离子半径分别是0.077 nm和0.072 nm.LDH的a值是由Cu2+和Mg2+离子决定,c值由层间阴离子CO32-决定.CuMgAl-LDH有稳定有序的结构,部分Mg2+离子被Cu2+置换后层状有序的LDH晶胞结构基本没有改变.
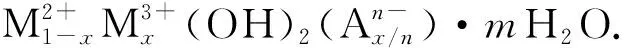
从表6的元素分析结果中发现铜、镁、铝与碳的摩尔比为0.8∶1.2∶1∶1,故认为CuMgAl-LDH分子中金属离子的组成为Cu0.8Mg1.2Al,又发现碳的摩尔比率与铝相同,因而推断CuMgAl-LDH只有1个CO32-.再根据氧和氢的比例,经热分析等辅证,推导结果正确.

表6 样品A元素分析结果

图2 样品A的SEM图
2.3 扫描电镜和透射电镜分析图2为样品A的SEM图,从图2可见,样品结晶良好,粒度分布均匀,分散性好.
图3为样品A的TEM图,(a)是低倍数图,(b)是(a)的高分辨图,(c)是(a)的电子衍射图((a)中红圈圈出处是衍射点).从图3(a)可见,样品具有棱角分明的晶体结构.从图3(b)可见,样品具有优良的晶格结构,证明LDH分子具有规则的晶格点阵和晶面结构,缺陷较少.因为如果有较多的缺陷,将会在图3(b)中应出现较大面积的暗区,但是,图中仅有较小暗区的面积分布.图3(c)的电子衍花样同样表明CuMgAl-LDH六方晶胞内部结构规则、结晶良好、离子或基团之间排列有序.

图3 样品的TEM图(a)是低倍数图,(b)是高分辨图,(c)是电子衍射图

图4 样品的吸附等温线
2.4 比表面分析及缓冲溶液的作用样品A的比表面分析结果列于图4,图4示样品A具有微孔和中孔结构.其吸附等温线在低压范围0.05
体系中有缓冲溶液的存在,可使铜、镁和铝离子的氢氧化物不会急剧地瞬时团聚致使大量无定形沉淀(无定形沉淀不会有显著孔状结构),而是有规则地进行基元联结,有规则的联结即可产生上述的微孔结构.经试验,发现如果没有缓冲溶液的“保驾护航”,是得不到具有超分子结构的CuMgAl-LDH的.
3 结论
在缓冲介质下组装了具有超分子结构的CuMgAl-LDH,其结晶度高,无显著氧化铜物质共存,粒子分布均匀,晶格排列有序规整,比表面积大.具有优良的微孔结构,孔径分布均匀.最优制备参数为:反应时间为105 h,反应温度为155 ℃,缓冲溶液体积比为0.5,Cu2+初始浓度为0.5 mol/L.
