沸石咪唑酯骨架材料载药策略的研究及药物递送应用
2022-08-08刘珊珊冯艺
刘珊珊,冯艺
(1.江苏经贸职业技术学院健康学院,江苏省食品安全工程技术研发中心,南京 211168;2.南京林业大学化学工程学院,南京 210037)
对大多数药物而言,存在水溶性差、化学稳定性差以及靶向性差等问题。因此,为提高药物的疗效,通常需用载体将药物包裹,进行保护和递送[1]。金属有机骨架(metal organic framework,MOFs)是一类由金属离子中心和有机配体通过配位作用形成的多孔材料[2-3],具有高比表面积和丰富的孔道结构,加之其结构和组成多样性以及其孔道和物理化学性能易于调控等特性,备受科研工作者的关注。沸石咪唑酯骨架材料(zeolitic imidazolate frameworks,ZIFs)是MOFs中的一类材料,主要是由钴离子和锌离子与咪唑配体结合而形成的一类多孔材料[4-7]。ZIFs不仅具有MOFs的优势,如丰富的孔道结构、高比表面积、结构多样性、易于改性调控等,还具有独有的优势。ZIFs具有良好的生物相容性和低毒性。以ZIF-8为例,主要由锌离子和2-甲基咪唑组成,锌离子对生物体的危害小,毒性低[8]。ZIFs的合成简单,可在室温下金属离子溶液与配体溶液搅拌混匀即可合成。因此,利用该特性,可在合成过程中的前驱体溶液中引入药物,实现一步法药物负载。ZIFs还具有较好的稳定性,可耐高温,因此ZIFs包裹药物后可保护药物不受到高温环境的破坏。此外,ZIFs具有 pH响应性,即在生理条件下稳定,但在酸性环境下解体。在大多数以ZIFs作为药物载体的研究中,就是利用ZIFs可在酸性环境中破坏而缓慢释放孔道内部药物的特性,作为抗肿瘤药物的靶向治疗。ZIFs解体后所释放的锌离子(Zn2+)本身具有抗菌杀菌的效果,具有某些特定形貌的ZIFs,如ZIF-L,其尖的棱角可物理破坏细菌的细胞壁,也可起到一定的杀菌作用[9]。FENG等[5]综述了ZIF-8颗粒的合成方法以及在药物传输中的应用,WANG等[6]总结了ZIF-8的合成、改性以及在肿瘤防治中的应用,以及胡强强等[7]综述ZIF-8颗粒尺寸的调控方法以及在医学中的应用。然而,这些综述主要侧重于ZIF-8的合成与应用,对其他ZIFs并未进行讨论。此外,对于材料合成而言,关键的一步在于ZIFs对药物包裹的合成策略。基于此,本综述主要讨论ZIFs作为药物载体的优势,针对ZIFs包裹药物的合成方法进行总结,并对各种合成手段的优缺点及在医药领域中的应用进行了总结归纳。
1 ZIF-8的合成与载药的策略
1.1ZIF-8的合成 目前,ZIF-8的合成主要有溶剂合成法、水热合成法、微波法、对流合成法、机械混合法等。溶剂合成法是将金属离子和咪唑配体溶解在水或有机溶剂中,在室温或加热条件下合成;水热合成法是将前驱液置于反应釜中加热,在一定压力、温度下合成;微波法是基于电磁波与富电荷材料的相互作用,为反应提供能量,从而促进ZIFs的形成;机械混合法通过研磨或球磨前驱体的方式得到最终产物;对流合成法是合成ZIFs膜常用的方法,是将金属离子溶液和咪唑配体分别置于多孔膜的两侧,通过对流形成晶核,进而得到ZIFs颗粒的方法。除上述方法外,ZIFs还可通过金属氧化物做模板剂和前驱体,与配体反应形成产物,例如以氧化锌做锌源和模板剂,与2-甲基咪唑配体结合可得到ZIF-8颗粒[10]。
1.2ZIF-8载药的策略 ZIFs载药策略可分为在线包裹/一步合成法、后处理负载法、相转化法以及表面活性剂协助负载法等,如图1所示。一步合成法是通过在ZIFs形成过程中对药物进行包裹;后处理负载法是先合成ZIFs材料通过浸渍的方式对药物进行包裹负载;相转化法是通过ZIFs之间的转化以及表面活性剂协助法是基于一步合成法,在负载过程中加入表面活性剂对载体的孔结构等进行调控,以促进药物负载过程。
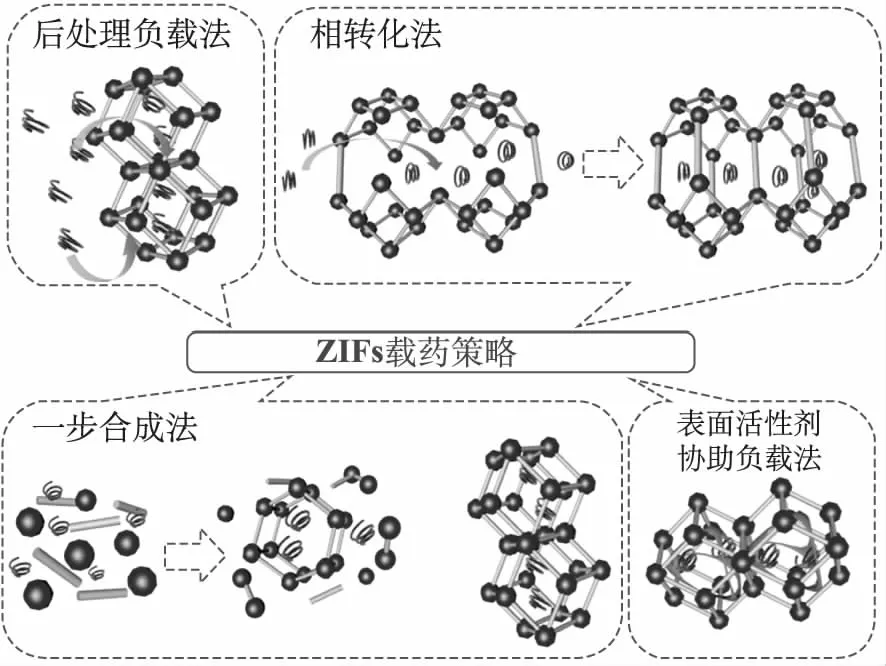
图1 常见的ZIF-8载药策略示意图 Fig.1 Schematic illustration of common strategies to encapsulate drugs into ZIFs-8
1.2.1一步合成法 由于ZIFs的形成是通过金属离子(主要是钴离子和锌离子)和咪唑配体配位形成,因此在配位过程中可引入药物,从而在ZIFs生长过程中形成对药物的包裹。在液相体系中,金属离子溶液与咪唑配体溶液混合,通过配位形成晶核后生长,最终得到ZIFs颗粒。在合成ZIFs过程中,药物可先分散或溶解在金属离子溶液或配体溶液中,从而在金属离子簇与配体结合形成骨架结构的过程中形成对药物的包裹。例如ALSAIARI等[11]将CRISPR/Cas9药物与二甲基咪唑溶液混合,随后加入锌源,成功将药物包裹在ZIF-8孔道内,其载药率可达17%。ZHENG等[12]将抗肿瘤药物多柔比星(DOX)与硝酸锌溶液混合,两者可通过配位作用力形成配位聚合物。随后,将二甲基咪唑加入到该溶液中,通过锌离子与二甲基咪唑的配位,达到ZIF-8包裹DOX(负载量达14%~20%)的目的。CHEN等[13]先将自噬抑制剂3-甲基腺嘌呤(3-MA)与锌离子溶液混合,随后加入咪唑配体溶液,得到ZIF-8@3-MA[图2(a)]。除上述加入顺序外,也可先将锌离子溶液与配体溶液混合,随后加入药物。如WANG等[14]通过这种加入顺序,将吲哚菁绿引入到ZIF-8的孔道内。体外药物试验表明,该方法得到的ZIF-8包裹药物具有较好的光热治疗疗效。在固相体系合成ZIFs过程中加入药物同样可达到ZIFs包裹药物的目的。例如在球磨ZIFs前驱体过程中加入药物,可在线合成ZIFs包裹药物的复合物[图2(b)]。该方法的海藻酸钠载药效率高达83.5%,负载量可达6.68%。84%的药物可在pH8的磷酸盐缓冲液中8 h内缓慢释放,展现出较好的药物缓释性能[15]。
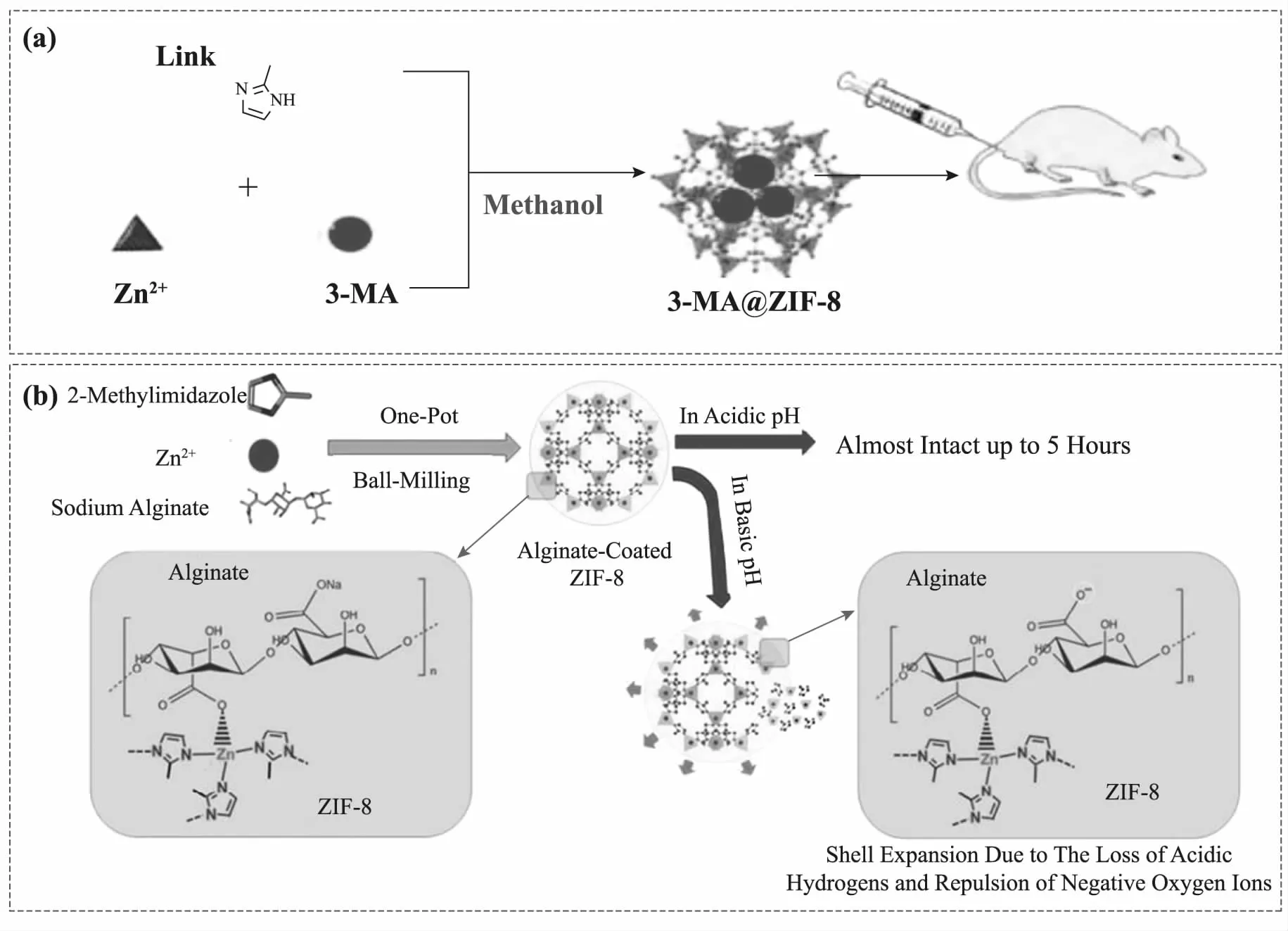
图2 (a)液相体系[13]和(b)固相体系[15]一步法ZIF包裹药物的合成示意图 Fig.2 One-pot synthesis of ZIF@drug in liquid solution (a)[13] and solid system (b)[15]
1.2.2后处理负载法 主要通过毛细作用力、静电相互作用、范德华力或配位作用力将药物与ZIFs进行结合。SHEARIER等[16]通过将合成好的ZIF-8颗粒经过球磨后分散到磷酸盐缓冲液中并加入羟基脲,从而通过范德华力与ZIFs结合实现ZIFs对羟基脲的包裹。SOLTANI等[17]将庆大霉素溶解在甲醇溶液中,随后加入预先合成的ZIF-8颗粒浸渍5 d,离心洗涤干燥即可得到ZIF-8包裹庆大霉素复合物(ZIF-8@GEN)。庆大霉素在ZIFs上的负载主要通过氢键和静电吸附作用力来结合。WANG等[18]将ZIF-67颗粒浸渍在DOX和氧化铁的前驱液中,得到ZIF-67包裹DOX和氧化铁颗粒的复合材料。GOMAR 等[19]通过吸附,在ZIF-6、ZIF-3以及ZIF-1上负载氟尿嘧啶和硫鸟嘌呤分子,并通过模拟计算发现这两类药物分子会优先吸附在ZIF-6和ZIF-1骨架上的Zn-咪唑配体的四元环上。与一步合成法相比,后处理负载法的优势在于可控制ZIFs的颗粒尺寸和形貌,即根据需要先合成具有一定颗粒尺寸和形貌的ZIFs进行药物负载。而一步合成法是在线生长ZIFs颗粒,其生长速度不易控制,从而导致颗粒大小不均一以及颗粒尺寸难调控等缺点。虽然后处理法具有上述优势,但也存在以下几个缺点,比如长时间浸泡会在一定程度上损坏ZIF的晶型,预先合成的ZIF由于其较小的孔道窗口,大分子无法进入孔道内部进行负载以及一般需较长的合成时间等。
1.2.3相转变法 具有叶片状的ZIF-L被认为是ZIF-8的中间态,是SOD结构的一部分[图3(a-c)]。ZIF-L的二维SOD层与层之间通过氢键连接。经研究发现,ZIF-L可在有机溶剂中加热转化成ZIF-8[20]。利用这种特性,GUAN等[21]首先将药物与ZIF-L混合,药物进入二维SOD层间空隙,在ZIF-L转化成ZIF-8的同时,咪唑配体连接相邻的二维SOD片层,从而将药物“关”在层间空隙中,形成包裹,如图3(d) 所示。该工作为ZIFs包裹药物提供了新的思路。
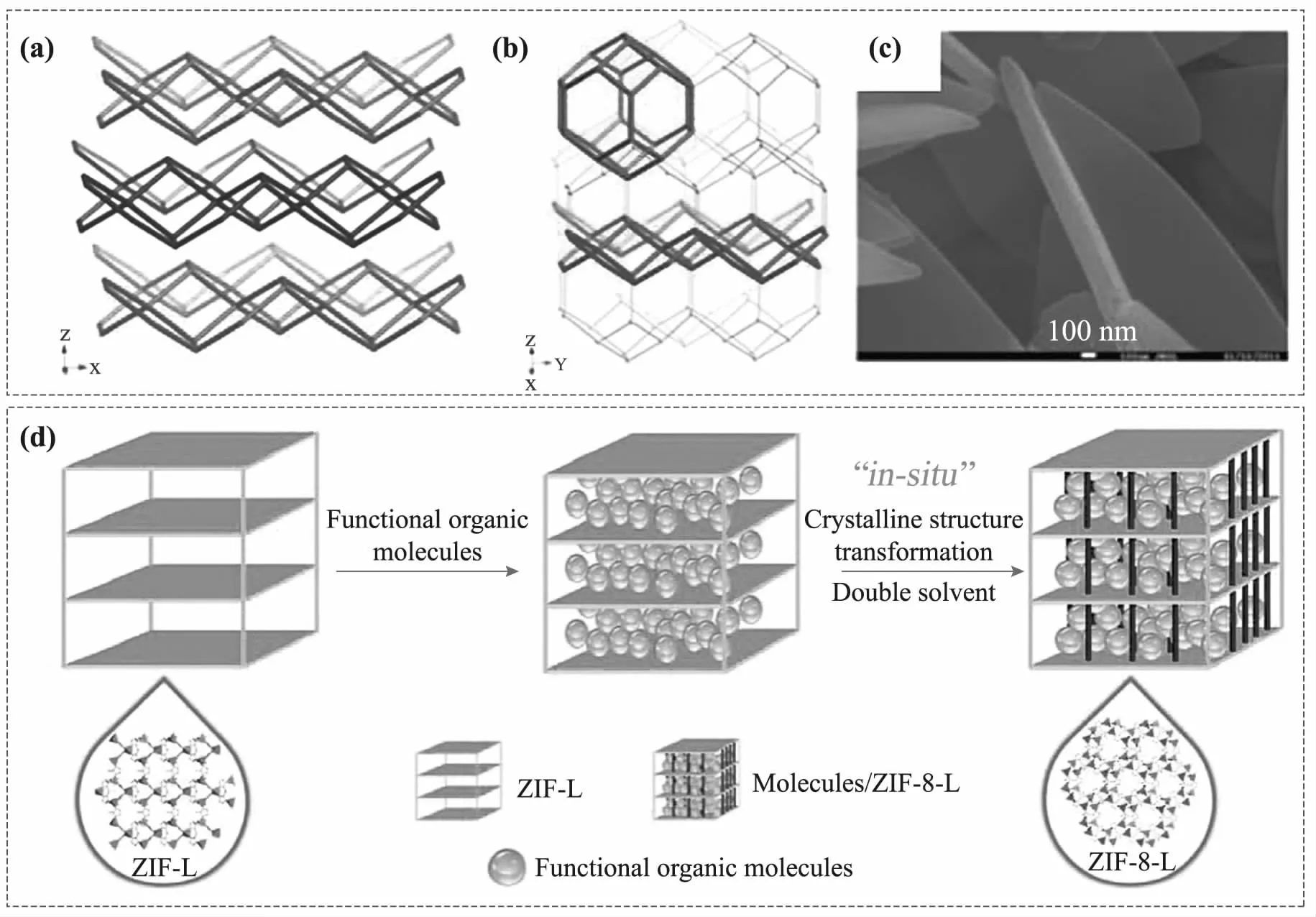
图3 (a)ZIF-L的拓扑结构示意图;(b)ZIF-8与ZIF-L的拓扑结构(绿色为ZIF-8拓扑结构,红色显示的为ZIF-L的层状拓扑结构);(c) ZIF-L的SEM形貌[22];(d)相转化法包裹分子示意图 Fig.3 (a) Topological structure of ZIF-L;(b) Topological structure of ZIF-8 and ZIF-L (green is ZIF-8 topology,red is ZIF-L layered topology);(c) SEM image of ZIF-L;(d) encapsulation of molecules into ZIFs via phase transformation method
除上述方法外,还可通过改性等方法对药物进行包裹,如在ZIFs上引入官能团促进ZIFs与药物之间的结合或通过模板剂协助包裹等。ABDELHAMID等[23]通过一步法合成ZIFs包裹药物的同时加入三甲胺,可对ZIF的孔道结构进行调控,如图4所示。三甲胺的加入不仅可促进ZIFs的形成,还可形成介孔,而所得到的ZIFs可有效保护包裹在内的染料分子(罗丹明B和亚甲基蓝)以及蛋白质分子(牛血清白蛋白),提高其分子稳定性和存活时间。综上,表1所示一步合成法,后处理负载法以及相转化负载法各有优缺点。
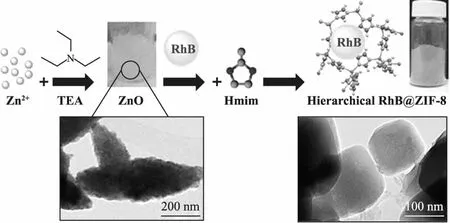
图4 三甲胺为表面活性剂得到的具有多级孔结构ZIF-8包裹罗丹明B复合物 Fig.4 ZIF-8 encapsulated rhodamine B complex with hierarchical pore structure obtained by trimethylamine as surfactant

表1 不同ZIF-8包裹药物的合成策略的比较 Tab.1 Comparison of different strategies to encapsulate drugs into ZIFs
2 ZIFs载药系统在医药领域中的应用
目前,抗肿瘤治疗的途径有化学药物治疗、光热治疗、光动力治疗等手段[24]。以ZIF为载体,负载相应的药物或其他功能性材料如具有光响应、磁响应的材料,达到相应的治疗的目的。最常见的手段是结合ZIFs的pH响应特性,即在酸性环境中ZIFs可解体,这一特性是其他MOFs如UiOs和MILs等不具有的。其主要原因是因为在酸性环境中,ZIFs的有机配体会被质子化,从而导致金属离子簇与咪唑配体之间的配位键解离,导致骨架的破坏[25]。一般情况下,肿瘤细胞处在弱酸环境中,ZIFs到达靶向部位后在弱酸环境中解体,缓慢地释放药物。例如在ZHUANG等[26]的研究中,当pH值在7.4时,ZIF-8在24 h后药物释放小于10%,而在pH值为6的环境下1 h后药物释放可达50%,12 h后接近100% 。此外,ZIF解体所产生的金属离子,尤其是Zn2+,本身具有一定的杀菌抗菌作用,也会对治疗起到一定的贡献。
ZIFs还可通过特定的化学试剂使其解体达到释放药物的目的。例如通过ZIF-90可在三磷酸腺苷(ATP)中解体的特性,可得到ATP响应的ZIF-90包裹蛋白质分子的复合物,并通过ATP使ZIF骨架发生分解,从而达到在目标区域释放蛋白质分子的目的[27]。在该研究中,ZIF-90包裹蛋白质分子的复合物主要通过一步合成法得到,即将蛋白质分子分散在ZIF-90的前驱液中,通过金属离子和咪唑配位形成骨架结构的同时,包裹蛋白质分子。上述两种方法主要是通过ZIF的特性在特定环境中(pH变化或化学试剂刺激)响应,发生解体而使药物释放。除此之外,在合成过程中包裹具有功能化特性的材料,可使得ZIFs在其他刺激下如光、热、磁性等发生响应,达到药物释放的效果:WU等[28]将Fe2O3颗粒包裹在ZIF-8中,使ZIF-8载体具有磁响应;SILVA等[29]报道了一种以金颗粒做内核以及ZIF-8做外壳的核壳结构,并通过引入Eu3+和Tb3+离子,使该材料具有热响应,用于运输和释放氟尿嘧啶和咖啡因等药物; SHARSHEEVA等[30]将光催化剂TiO2与ZIF-8结合,利用TiO2的光催化特性,使载体具有光响应特性。对光、热、磁响应释放药物的途径,通常不需要破坏ZIF的结构,而且由于其功能化材料的特性,会附带其他功能,例如光照下光催化剂会产生光生电子和空穴,具有一定的氧化还原特性,而具有磁响应的载体可通过磁力为ZIFs传输产生动力。值得注意的是,上述提到的药物释放响应机制可组合使用(如pH-光响应等),利用多种响应激发或促进ZIFs在靶向部位的药物释放。
除肿瘤治疗外,ZIFs作为载体还在生物成像和生物大分子保护等展现出良好的应用价值。例如通过ZIFs包裹磁性的Fe3O4、荧光碳量子点等功能性材料使其具有一定的检测能力,可实现诊断治疗一体化:以ZIF-8为载体,同时包裹具有荧光效应的量子点和氟尿嘧啶,其中荧光量子点可在肿瘤部位显影成像,而抗肿瘤药物氟尿嘧啶在肿瘤部位的可控释放又可达到治疗的目的,如图5所示[31]。氟尿嘧啶的释放,通过pH响应,充分利用ZIF-8在酸性中结构缓慢破坏的特点,达到药物在靶向目标中的可控释放。在该研究中,荧光碳量子的负载通过一步合成法,即在ZIF-8的合成前驱液中,分散碳量子点,得到包裹碳量子点的ZIF-8材料。随后,通过后处理负载的方式,将氟尿嘧啶负载在已成型的ZIF-8颗粒之上,从而达到ZIF-8负载包裹碳量子点和氟尿嘧啶的目的。FENG等[32]通过ZIF-8包裹抗体分子、免疫球蛋白等蛋白质分子,对其进行保护。实验结果表明,ZIF-8包裹的蛋白质分子在3周后仍具有很高的活性,从而突显ZIF-8的保护作用 。

图5 (a,f)ZIF-8,(b,g)ZIF-8包裹量子点,(c,h)ZIF-8与量子点混合,(d,i)甲醇洗涤后的ZIF-8包裹量子点以及(e,j)甲醇洗涤后的ZIF-8与量子点混合分别在(a-e)自然光和(f-j)365 nm紫外光下的表观图像和(k)ZIF-8包裹荧光量子点和药物分子的示意图 [31] Fig.5 Powder photographs of ZIF-8 (a,f),ZIF-8@carbon dots(b,g),ZIF-8 mixed with carbon dots(c,h),ZIF-8@carbon dots after methanol washing (d,i) and ZIF-8 mixed with carbon dots after methanol washing (e,j);schematic diagram of ZIF-8 encapsulating fluorescent carbon dots and drug molecules (k) [31]
3 结语与展望
ZIF-8具有高比表面积、丰富的孔道结构以及pH响应等特性,使其成为药物负载的良好载体,目前,ZIF-8作为药物载体,可负载化疗药物等用于肿瘤治疗、光热治疗等领域,且在生物成像、生物大分子存储与保护中也展现出良好的应用价值。虽然目前ZIFs载药系统已有很多研究并取得一定的成绩,但在以后的相关研究应注意以下几个方面:①ZIF-8以微孔为主,孔道窗口较小,对一些生物大分子的包裹依然存在挑战,因此需要合成具有多级孔结构或刻蚀ZIF-8对大分子药物分子进行有效包裹。此外,ZIF-8多以颗粒为主,具有其他形貌如二维片层或一维结构的ZIF-8包裹药物的研究尚未报道;②对药物的负载要区分孔道内负载与表面负载,对某些药物,可通过吸附作用吸附在ZIF表面,并未进入孔道内部。此外,药物负载后应充分的洗涤,将表面游离态的药物脱除;③药物负载或改性处理后的ZIF-8,其抗酸稳定性会发生变化,因此,负载药物的ZIFs在酸性环境中解体释放需与纯ZIFs的数据进行比较;④IF-8在解体后分解为锌离子和咪唑配体。虽有研究表明,Zn2+具有低毒性,但对咪唑配体的毒性研究较少,因此,ZIF-8在分解后的安全性还需进一步的研究;⑤相关文章不仅需要对合成后样品的性能进行测试,还需对合成机理研究进行探讨以及合成条件优化。综上,ZIFs是一种具有前景的药物载体,未来期待有更多的研究推动ZIFs在药物递送系统中的广泛应用。
