缺血性心肌病与非缺血性心肌病的临床特征及预后对比分析
2022-07-21孟凡琦王希星朱伟亮
孟凡琦 王希星 黄 珊 朱伟亮 伍 源*
(1 厦门大学附属心血管病医院心血管内科,福建 厦门 361000;2 厦门大学附属心血管病医院心脏大血管外科,福建 厦门 361000)
近年来,心力衰竭仍然是威胁公共健康的重大课题。流行病学资料显示,美国心力衰竭患病率约为2.7%[1],亚洲的心力衰竭患病率为1.2%~6.7%[2]。在中国,35岁以上人群的心力衰竭患病率为1.3%,累计约有1 370万心力衰竭患者[3]。尽管心力衰竭的治疗已不断取得进展,心力衰竭患者的病死率仍然很高,心力衰竭5年生存率约为50%[4],美国因心力衰竭死亡人数达310 000/年[5]。泵衰竭和心脏性猝死(sudden cardiac death,SCD)是心力衰竭患者死亡的两大主要原因[6],其中,由致命性室性心律失常导致的SCD在心力衰竭患者死亡中的比例高达50%[7-8]。近年来涌现众多心力衰竭预后评估模型,包括SHFM[9]、MAGGIC[10]、3C-HF[11]等,但这些模型的构建大多基于不同病因和类型的心力衰竭人群。然而,有研究表明,不同心力衰竭病因患者的临床特征及预后存在差异[12]。本研究对缺血性心肌病(ischemic cardiomyopathy,ICM)和非缺血性心肌病(nonischemic cardiomyopathy,NICM)这两个特定类别心力衰竭人群的临床特征和预后进行对比分析,探讨其临床特征的差异,分析其预后的影响因素。
1 资料与方法
1.1 研究对象 本研究回顾性纳入2016年1月至2017年12月在厦门大学附属心血管病医院住院的心力衰竭患者,并对这些患者进行持续前瞻性随访(注册号:ChiCTR-POC-17011842,伦理号:2017-SR-060)。本研究入选标准如下(需同时满足):①符合2016年欧洲心脏病协会(European Society of Cardiology,ESC)心力衰竭指南中心力衰竭诊断标准的心力衰竭患者[13]。②优化药物治疗至少3个月后左室射血分数(left ventricular ejection fraction, LVEF)小于50%,优化药物治疗包括血管紧张素转化酶抑制剂(angiotensin converting enzyme inhibitors,ACEI)或血管紧张素受体拮抗剂(angiotensin receptor blocker,ARB)、β受体阻滞剂和醛固酮受体拮抗剂。排除符合任一以下标准的心力衰竭患者:肥厚型心肌病;风湿性心脏瓣膜病;先天性心脏病;肺源性心脏病;各种类型的心包疾病、心肌炎;近3个月内发生的急性心肌梗死,包括ST段抬高型心肌梗死和非ST段抬高型心肌梗死;主动脉夹层;白血病、淋巴瘤、再生障碍性贫血等严重的血液病;自身免疫性疾病;恶性肿瘤;激素替代治疗;同时参加其他干预性临床试验;已接受心脏再同步化治疗(cardiac resynchronization therapy,CRT)、植入性心脏复律除颤器(implantable cardioverter-defibrillator,ICD)、微创左室重建术(Revivent(TM)/Parachute(TM))、二尖瓣反流的介入治疗(MitraClip(TM),Amend(TM)等)、外科心室重建术、心脏移植等其他用于改善心功能的非药物治疗措施。知情同意并签署知情同意书,本研究已获得我院伦理委员会的批准。
1.2 研究分组 将入选的心力衰竭患者根据心力衰竭病因分为ICM组和NICM组。ICM的诊断标准[14](满足以下至少1项):①既往有心肌梗死病史。②冠状动脉造影证实左主干或LAD近端狭窄≥75%。③冠状动脉造影证实两支或两支以上主要的冠状动脉狭窄≥75%。④因以上3种原因行再血管化治疗的病史。NICM的诊断标准(满足以下至少1项):①不符合ICM的诊断标准。②CT冠状动脉血管成像或心肌核素检查排除冠心病。
1.3 资料采集 采集患者的基线信息包括年龄、性别、抽烟状况、饮酒状况、血压、心率、纽约心功能(New York Heart Association,NYHA)分级、心力衰竭病因、心力衰竭住院史以及病史资料,包括冠心病、心律失常、晕厥、心脏骤停/心肺复苏、高血压、糖尿病、慢性阻塞性肺疾病等。采集超声心动图的参数,包括左室舒张末内径、左室收缩末内径、LVEF、左房内径、肺动脉收缩压(pulmonary artery systolic pressure,PASP)、室壁瘤、瓣膜反流情况。心电图指标包括QRS波时限、QT间期、QTc间期、Tp-e间期、Tp-e离散度以及各类心律失常及束支阻滞情况。采集实验室检验结果,包括血清尿素氮、血清肌酐、血清钠、血清尿酸、血红蛋白、甲状腺功能、NT-proBNP等。并记录患者药物使用情况,包括ACEI/ARB、β受体阻滞剂、醛固酮受体拮抗剂、利尿剂、洋地黄类药物、抗血小板药物、抗凝药物、他汀类药物、钙离子拮抗剂、抗心律失常药物等。
1.4 随访和研究终点 患者入组后每隔3个月进行随访,随访方式包括门诊访视和电话访视。通过随访,追踪患者的状况,判断有无终点事件发生,包括有无室速、室颤等恶性心律失常或心肺复苏、心力衰竭再住院、死亡。研究的一级终点包括全因死亡、心脏性死亡及SCD;二级终点包括恶性心律失常、心脏骤停、心肺复苏及因心力衰竭再住院等事件。心脏性死亡是指与心脏的电学或机械功能障碍直接相关的死亡。SCD的定义为急性症状发作后24 h内突然发生的以意识骤然丧失为特征的、由心脏原因引起的自然死亡[15]。
1.5 统计分析方法 运用SPSS 22.0软件进行分析,正态分布的计量资料以均数±标准差(±s)表示,多组计量资料比较采用单因素方差分析,组间两两比较采用Student'st检验。计数资料之间比较采用卡方检验。采用Kaplan-Meier法进行生存分析,绘制生存函数曲线,并采用Kaplan-Meier生存曲线比较不同组别病死率和事件发生率。采用COX比例风险回归方法分别对ICM和NICM组患者进行预后分析。P<0.05表示差异有统计学意义。
2 结 果
本研究纳入2016年1月至2017年12月厦门大学附属心血管病医院住院的531例心力衰竭患者。9例患者在入选后3个月内即接受非药物干预措施,3例患者完全失访,将这12例患者剔除,剩余519例用于数据分析,其中ICM组215例,NICM组211例,其余93例患者心力衰竭病因不明。所有患者在入组后均接受前瞻性随访,平均随访(55.16±6.78)个月。
2.1 ICM与NICM的基线特征对比分析 与ICM组相比较,NICM组患者的男性比例、年龄、既往心力衰竭住院的比例、NYHA Ⅲ~Ⅳ的比例、合并心房颤动的比例、合并非持续性室速的比例、合并高血压病的比例、合并糖尿病的比例、合并慢性阻塞性肺疾病的比例、收缩压、LVEF≤35%的患者比例、PASP、中重度二及三尖瓣反流的比例、左束支阻滞比例、肾小球滤过率、血清钠和血红蛋白水平更高,心力衰竭病程更长,舒张压、右束支阻滞的比例、全因死亡比例更低,左房内径和左室舒张末内径更大,差异显著(P<0.05);而其他指标两组比较无显著性差异(P>0.05)。见表1。
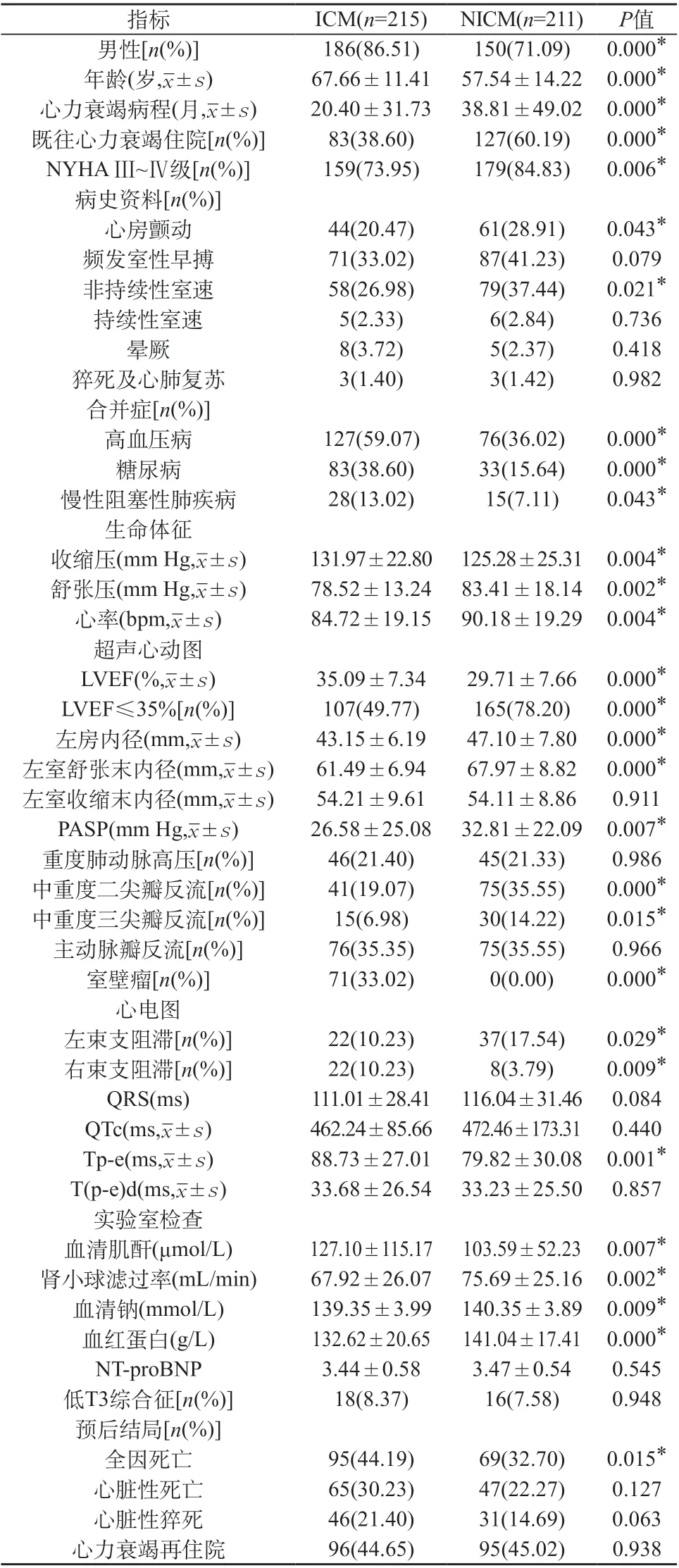
表1 ICM与NICM的临床特征对比
2.2 ICM与NICM的生存情况分析 截至2021年8月的末次访视,纳入的519例心力衰竭患者中201例(38.73%)患者死亡,其中心脏性死亡139例(69.15%),非心脏性死亡14例(6.97%),不明原因死亡48例(23.88%),93例(46.27%)患者死于SCD,41例患者(20.40%)死于泵衰竭。1年、2年、3年、4年和5年的病死率分别为13.73%、24.40%、31.31%、39.67%和47.06%。随访期间224例(43.16%)患者因心力衰竭再次住院,其中59例(11.37%)患者因心力衰竭再住院的次数超过3次。随访期间,ICM组215例患者中共95例(44.19%)患者死亡,其中心脏性死亡65例(68.42%),SCD 46例(48.42%);NICM组211例患者中共69例(32.70%)患者死亡,其中心脏性死亡47例(68.12%),SCD 31例(44.93%)。使用Kaplan-Meier法进行生存分析,绘制全因死亡和心力衰竭再住院的生存曲线(图1),ICM组的全因病死率高于NICM组,存在统计学差异(P<0.05)但两组的心力衰竭再住院无明显差异(P>0.05)。ICM组和NICM组1年、2年、3年、4年及5年的病死率分别为17.67%vs.10.05%,26.19%vs.21.67%,34.13%vs.26.77%,44.63%vs.34.1.%,48.91%vs.45.07%,ICM组高于NICM组,其中1年和4年的病死率存在统计学差异(P<0.05),其余无统计学差异。
2.3 ICM与NICM 预后影响因素的对比分析
2.3.1 全因死亡的危险因素分析 COX回归分析显示,ICM全因死亡的影响因素包括:年龄、NYHAⅢ~Ⅳ级、既往心力衰竭住院、心力衰竭病程、频发室性早搏、重度二尖瓣反流、主动脉瓣反流、肾小球滤过率、血清尿素氮、血清钠、血红蛋白、低T3综合征和lg NT-proBNP(P<0.05)。见表2。基于单因素回归分析,建立ICM全因死亡的多因素COX比例风险预测模型,模型最终纳入4个风险变量,结果显示,既往心力衰竭住院、重度二尖瓣反流、低T3综合征和lg NTproBNP是影响ICM全因死亡的危险因素(P<0.05)。见表3。
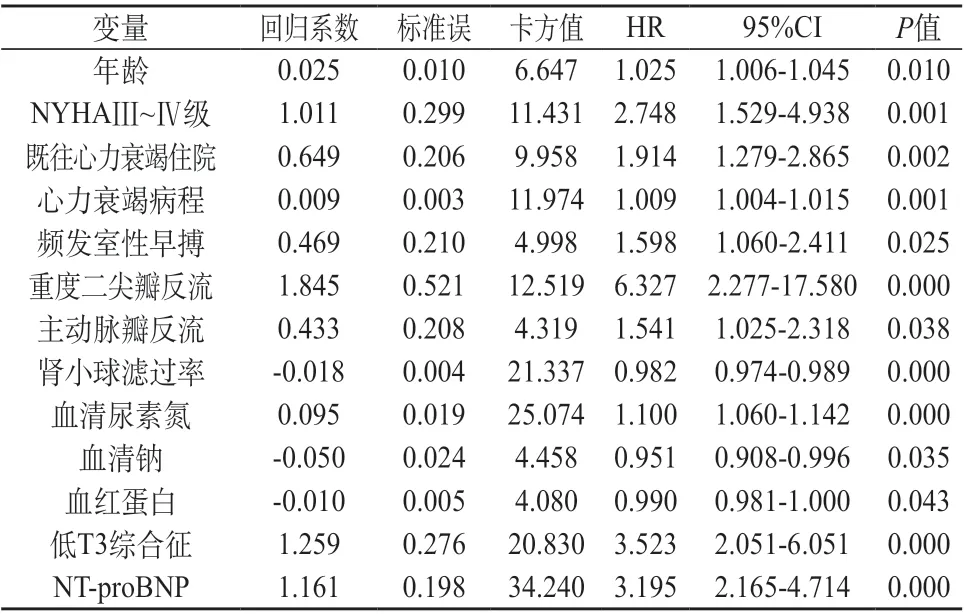
表2 ICM组全因死亡的单因素COX回归分析
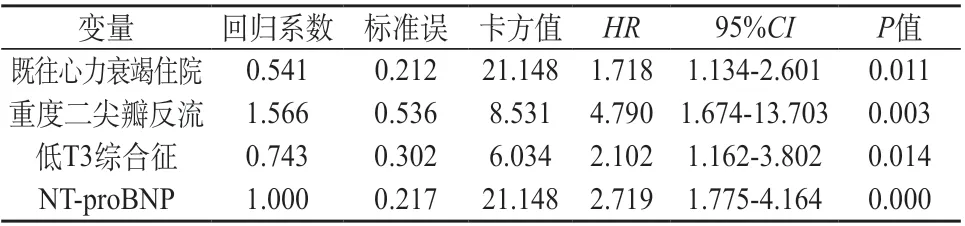
表3 ICM组全因死亡的多因素COX回归分析
COX回归分析显示,NICM全因死亡的影响因素包括:收缩压、舒张压、心率、NYHAⅢ~Ⅳ级、既往心力衰竭住院、心力衰竭病程、心房颤动、频发室性早搏、非持续室性心动过速、SCD/心肺复苏史、高血压、慢性阻塞性肺疾病、LVEF、左房内径、左室舒张末内径、PASP≥50 mm Hg、重度二尖瓣反流、肾小球滤过率、血清尿素氮、血清钠、低T3综合征和lg NT-proBNP(P<0.05)。见表4。基于单因素回归分析,建立NICM全因死亡的多因素COX比例风险预测模型,模型最终纳入6个风险变量,结果显示,既往心力衰竭住院、频发室性早搏、LVEF、重度二尖瓣反流、低T3综合征和lg NT-proBNP是影响NICM全因死亡的危险因素(P<0.05)。见表5。
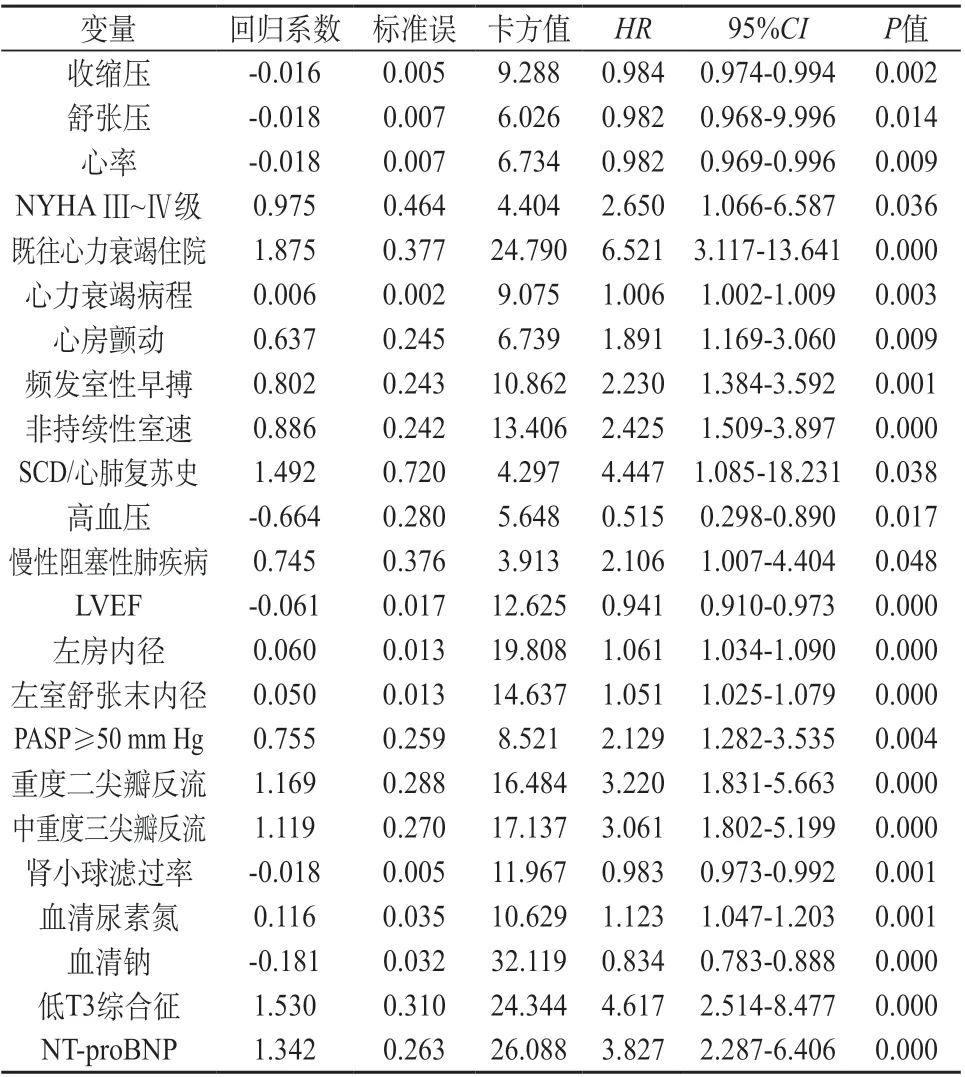
表4 NICM组全因死亡的单因素COX回归分析
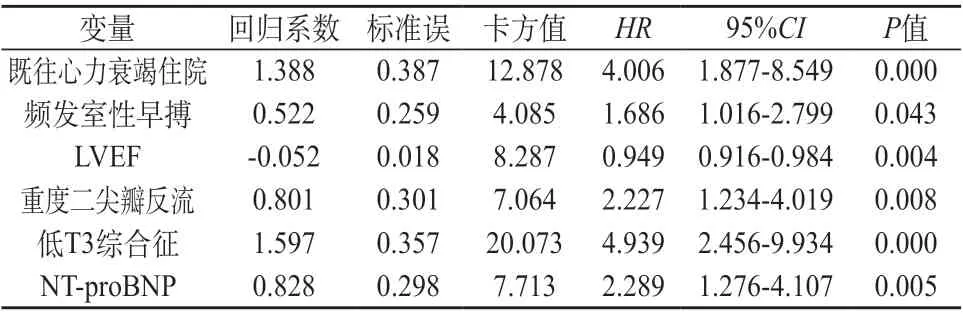
表5 NICM组全因死亡的多因素COX回归分析
2.3.2 心力衰竭再住院的危险因素分析 单因素COX回归分析显示,ICM心力衰竭再住院的影响因素包括:舒张压、NYHA Ⅲ~Ⅳ级、既往心力衰竭住院、心力衰竭病程、心房颤动、频发室性早搏、糖尿病、左房内径、PASP≥50 mm Hg、重度二尖瓣反流、肾小球滤过率、血清尿素氮、低T3综合征、lg NTproBNP(P<0.05)。见表6。基于单因素回归分析,建立ICM心力衰竭再住院多因素COX比例风险预测模型,模型最终纳入5个风险变量,结果显示,既往心力衰竭住院、频发室性早搏、左房内径、低T3综合征和lg NT-proBNP是影响ICM心力衰竭再住院的危险因素(P<0.05)。见表7。
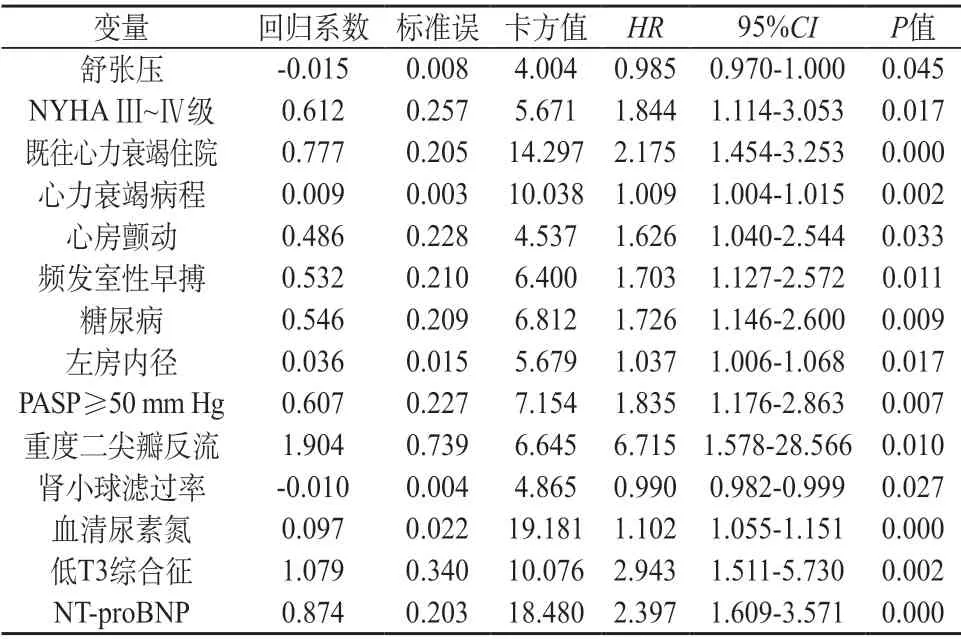
表6 ICM组心力衰竭再住院的单因素COX回归分析
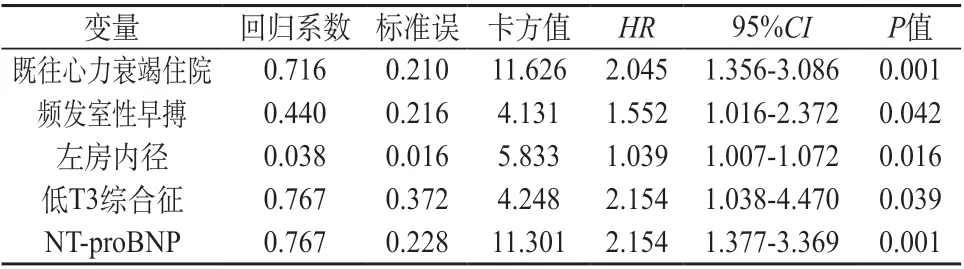
表7 ICM组心力衰竭再住院的多因素COX回归分析
单因素COX回归分析显示,NICM心力衰竭再住院的影响因素包括:收缩压、舒张压、既往心力衰竭住院、心力衰竭病程、频发室性早搏、非持续性室性心动过速、LVEF、左房内径、左室舒张末内径、PASP≥50 mm Hg、重度二尖瓣反流、中重度三尖瓣反流、左束支阻滞、血清钠、低T3综合征、NT-proBNP(P<0.05)。见表8。基于单因素回归分析,建立NICM心力衰竭再住院多因素COX比例风险预测模型,模型最终纳入6个风险变量,包括心力衰竭病程、非持续室速、左房内径、二尖瓣重度反流、左束支阻滞和NT-proBNP是影响NICM心力衰竭再住院的危险因素(P<0.05)。见表9。
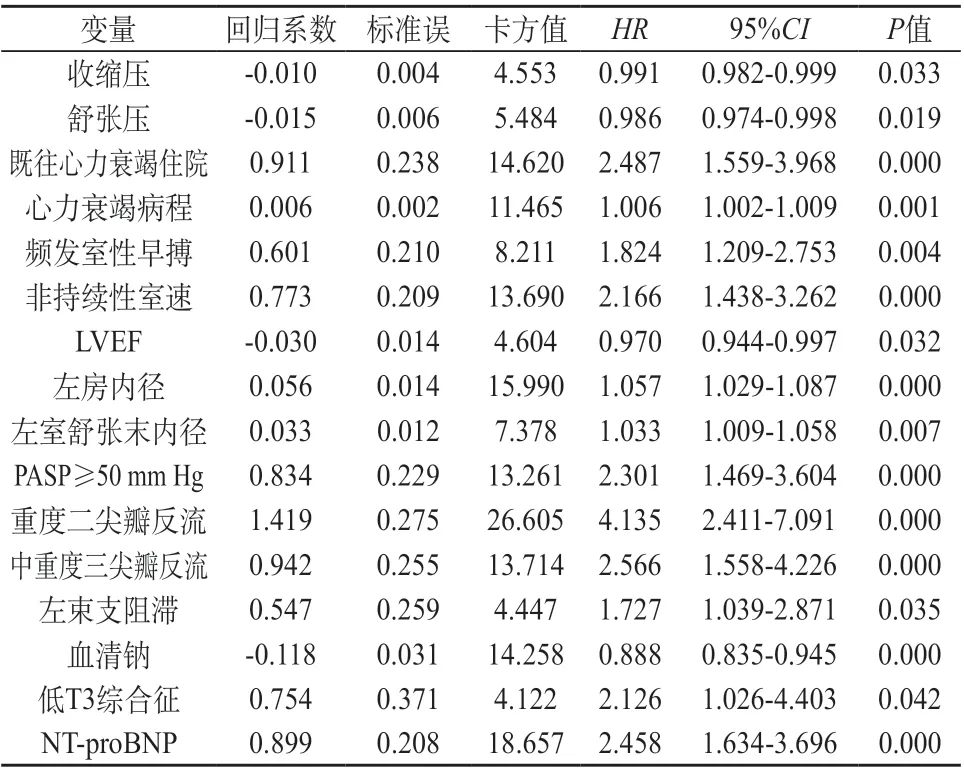
表8 NICM组心力衰竭再住院的单因素COX回归分析

表9 NICM组心力衰竭再住院的多因素COX回归分析
3 讨 论
本研究对象是LVEF小于50%的心力衰竭患者,我们排除了肥厚型心肌病、风湿性心脏瓣膜病、先天性心脏病等结构性心脏病,同时还排除了接受心力衰竭非药物干预的患者,以观察心力衰竭药物治疗背景下心力衰竭患者的自然病程。根据心力衰竭病因不同,将入选的患者分为ICM组和NICM组,并剔除了因缺乏诊断依据无法确认病因的患者,从而对ICM和NICM患者的临床特征及预后进行对比分析。
本研究显示ICM与NICM患者的临床特征存在较大差异。ICM组患者各类心血管危险因素的比例均显著高于NICM,包括年龄、男性性别、高血压病、糖尿病、COPD,这与基于心力衰竭病因的分组特点有关。与ICM相比,NICM患者心力衰竭病程更长、既往心力衰竭住院比例更高、NYHA Ⅲ~Ⅳ级的比例更高,合并心房颤动及非持续性室速的比例也更高。NICM组患者的平均射血分数比ICM组患者更低,同时左房、左室更大,这似乎可以解释NICM组重度二尖瓣反流的比例显著高于ICM组的原因。
众多研究报道了心力衰竭的病死率。CIBIS Ⅱ研究[16]共纳入1327例心力衰竭患者,平均随访15个月,总病死率12%,其中心脏性死亡占比54%(泵衰竭死亡23%,SCD31%);Watnabe[17]研究共纳入3319例心力衰竭患者,平均随访16个月,总病死率14.4%,其中泵衰竭死亡占比22%,SCD占比34%;Haghfelt[18]研究共纳入816例心力衰竭患者,平均随访23个月,总病死率11.9%,其中泵衰竭死亡占比16%,SCD占比62%。本研究纳入519例心力衰竭患者,平均随访(55.16±6.78)个月,总病死率为38.73%,其中心脏性死亡占比69.15%,SCD占比46.27%,泵衰竭死亡占比20.40%。本研究中,心力衰竭患者整体的1年、2年、3年、4年和5年的病死率分别为13.73%、24.40%、31.31%、39.67%和47.06%。在本研究中,将ICM和NICM组患者的预后进行对比分析,发现ICM组和NICM组心脏性死亡和SCD的比例无明显差异,且NICM组患者的生存情况优于ICM组患者,但两组患者的心力衰竭再住院无统计学差异。
本研究利用单因素COX比例风险回归分析,以全因死亡和心力衰竭再住院为研究终点,分别在ICM和NICM组患者中进行分析,筛选P<0.05的变量。年龄是影响心力衰竭预后的独立危险因素[19],本研究中,随着年龄的增长,ICM全因死亡风险增加,但对NICM患者未见无明显影响。基础血压与NICM患者的死亡风险相关,本研究发现患者血压越高,死亡和心力衰竭再住院的风险越高,但ICM患者的死亡风险未受血压影响。本研究中,与NYHA心功能Ⅰ~Ⅱ级相比,NYHA心功能Ⅲ~Ⅳ级是全因死亡的危险因素,这提示心功能状态与死亡风险相关,心功能状况越差,死亡风险越高。心力衰竭病史与ICM和NICM的死亡均相关,既往心力衰竭住院会增加死亡风险,该指标对NICM的患者影响更大,同时,心力衰竭病程越长,患者死亡风险越高,这与既往研究结果一致[20]。本研究中频发室性早搏会同时增加ICM和NICM组的死亡和心力衰竭再住院风险,但非持续性室速仅与NICM患者死亡和心力衰竭再住院相关,而并未增加ICM患者的风险。国内外研究中关于LVEF对预后影响的结论并不一致,在多数的既往其他心力衰竭预后研究中,LVEF仍然是心力衰竭死亡及再住院的独立预测因子[21]。本研究中LVEF仅与NICM组的死亡及心力衰竭再住院风险相关,而对ICM预后无影响。本研究中,左房内径、左室舒张末内径同样与ICM患者的全因死亡和心力衰竭再住院无关,但在NICM组,随着左房内径和左室舒张末内径增加,患者的死亡及心力衰竭再住院风险都是明显增加的;肺动脉高压(PASP≥50 mm Hg)与ICM患者死亡预后无关,但会显著增加NICM患者的死亡风险;重度二尖瓣反流可同时显著增加ICM和NICM患者的死亡和心力衰竭再住院风险,中重度三尖瓣反流仅会增加NICM患者的死亡和心力衰竭再住院风险,主动脉瓣反流也仅会增加ICM患者的死亡风险。本研究发现,肾功能不全是ICM和NICM患者死亡的独立危险因素,随着肾小球滤过率的下降、血清尿素氮水平升高,两组患者死亡风险均显著增加。低钠血症在两组中均为患者死亡的危险因素,随着血清钠水平的下降,死亡风险显著增加。低T3综合征在本研究中同时是ICM和NCIM患者死亡的独立预测因子,可显著增加患者的死亡和心力衰竭再住院风险。而NT-proBNP作为临床评估心力衰竭严重程度的重要指标,在本研究中也是ICM和NCIM患者死亡和心力衰竭再住院的危险因素,其升高将显著增加患者的死亡风险。然而也有一些因素在其他研究中被证实在预测心力衰竭的预后方面有重要意义,但在本研究中未能得到有意义的结果。如男性在Collier等[19]、O'connor等[22]多个研究中证实是心力衰竭的危险因素,但在本研究人群的单因素回归中并未被证实与心力衰竭预后有关,因此性别是否可以作为ICM和NICM预后的危险因素尚无定论,这可能与研究人群所纳入的患者群体、性别比例、人种等有关。糖尿病作为传统的心力衰竭预后危险因素,在本研究也并未增加ICM和NICM组患者的死亡和心力衰竭再住院风险,这有待于更大样本量、多中心研究进一步证实其作为心力衰竭预后危险因素的价值。
本研究在单因素COX回归的基础上,分别以全因死亡和心力衰竭再住院为终点,对ICM和NICM组进行多因素回归分析,建立简单的预测模型,但由于单中心研究的样本量有限,在本研究中未能进行模型的验证,模型是否具有良好的预测效能有待于进一步研究证实。
综上所述,ICM和NICM具有不同的临床特征;与NICM组相比,ICM组患者死亡风险更高;ICM和NICM具有不同的心力衰竭预后危险因素。
