左乳癌根治术后两种调强放疗计划的甲状腺辐射剂量研究
2022-01-11袁美芳孙梦真文晓博
袁美芳,杨 毅,孙梦真,文晓博,赵 彪
(昆明医科大学第三附属医院/云南省肿瘤医院 放射治疗科,云南 昆明,650118)
研究[1-3]显示,70%~80%的乳腺癌根治术后患者需行放疗以提高局部控制率,调强放疗的剂量分布明显优于常规电子线照射和三维适形放疗,在提高靶区适形性和剂量均匀性的同时,减少了危及器官(OAR)的受照剂量。锁骨上区放疗会对患者甲状腺造成一定程度的辐射损伤,早期无明显症状,晚期容易出现甲状腺体积缩小、功能减退甚至诱发肿瘤,而放射性甲状腺损伤在临床中常被忽视,未从辐射剂量学方面进行严格控制[4-5]。本研究分析左乳癌根治术后静态调强放疗(sIMRT)与容积旋转调强放疗(VMAT)的甲状腺受照剂量特点,旨在为保护甲状腺提供一定的剂量学参考。
1 资料与方法
1.1 一般资料
回顾性选取2018年1月—2019年10月本科收治的68例左乳癌改良根治术后放疗患者作为研究对象。患者均为女性,年龄32~66岁,平均(45.63±1.31)岁;病理分期为pT2N1M020例、pT3N2M013例、ypT1N2M018例、ypT2N2M017例,均为浸润性导管癌;外象限23例,内象限45例。
1.2 体位固定和CT扫描
患者取舒适体位仰卧于乳腺托架板,双上臂放于托架上,头右偏,弯膝,左右调整体位使体中线与托架板中线保持一致;调整激光灯至靶区中心附近,然后在3个激光标记点上贴上铅点并用皮肤墨水做十字标记;行大孔径CT平扫定位(层厚、层间距均为0.5 cm),扫描范围为上颈部至上腹部,将CT影像传至Pinnacle310.0放射治疗计划系统(TPS)[6]。
1.3 靶区和OAR的勾画
参照肿瘤放射治疗协作组(RTOG)乳腺癌根治术后靶区标准勾画靶区:① 锁胸联合靶区(锁骨上区+胸壁区),锁骨上区上至环状软骨水平,内至胸锁乳突肌内缘,外至肩关节内侧;胸壁区内至胸骨旁,外至背阔肌前缘,下至手术引流口;② OAR,包括左、右侧甲状腺、全甲状腺、对侧乳腺、左肺、心脏。
1.4 计划设计
计划靶区(PTV)的处方剂量为50 Gy/25F;应用Pinnacle310.0 TPS分别回顾性设计sIMRT计划和VMAT计划,sIMRT采用7个主野(2个切线野+ 0度野+4个斜角野),其中0度野做铅门固定设置,射野范围限于锁骨上下淋巴结区;VMAT采用以切线为基础的双弧模式;两种计划目标函数一致,按照ICRU83号报告标准对靶区和OAR进行评估[7]。
1.5 计划评价指标
左肺接受5 Gy辐射剂量体积(V5)和接受20 Gy辐射剂量体积(V20),心脏接受30 Gy辐射剂量体积(V30)和平均辐射剂量(Dmean),左甲状腺V5、接受10 Gy辐射剂量体积(V10)、V20、V30、接受40 Gy辐射剂量体积(V40)、接受50 Gy辐射剂量体积(V50)和Dmean,右甲状腺V5、V10、V20、V30和Dmean,全甲状腺V30、V40和Dmean。
1.6 统计学分析
采用SPSS 24.0软件对sIMRT计划、VMAT计划的剂量学参数进行配对t检验分析,P<0.05为差异有统计学意义。
2 结 果
2.1 左肺和心脏受照剂量比较
sIMRT计划、VMAT计划的肿瘤靶区均归一到相同条件,即处方剂量均包绕95%的靶区体积、均匀性和适形度基本一致的前提下,VMAT左肺的V5、V20和心脏的V30、Dmean均低于sIMRT,差异有统计学意义(P<0.05)。见表1。
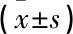
表1 不同放疗计划的左肺和心脏剂量学参数比较
2.2 甲状腺受照剂量比较
VMAT的左侧甲状腺V20略低于sIMRT,但差异无统计学意义(P>0.05);VMAT的左侧甲状腺V30、V40、V50和Dmean均低于sIMRT,差异有统计学意义(P<0.05)。VMAT的右侧甲状腺V20、Dmean均低于sIMRT,差异有统计学意义(P<0.05)。VMAT的全甲状腺V30、Dmean均低于sIMRT,差异有统计学意义(P<0.05)。见表2。
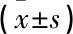
表2 不同放疗计划的甲状腺受照剂量比较
3 讨 论
近年来,放疗所致甲状腺功能减退(HT)已逐渐引起关注,放疗射线可造成甲状腺血管内皮细胞和腺细胞损伤以及自身免疫反应而导致HT,可引起全身各系统脏器低代谢综合征,严重者还可发生甲减危象而危及生命[8-11]。DARVISH L等[12]将甲状腺作为乳腺癌放疗风险器官进行Meta分析,发现放疗后促甲状腺激素水平升高,提示放疗时应重视甲状腺保护。KANYILMAZ G等[13]回顾性分析243例乳腺癌患者放疗后的HT发生率及预测因素,发现Dmean是预测HT的唯一预后因素,且Dmean>21 Gy是HT演变的阈值。TUNIO M A等[14]研究乳癌放疗甲状腺受照剂量与HT的关系,结果显示,甲状腺平均体积为19.6 cm3,锁胸组、单纯胸组的甲状腺Dmean分别为25.8、5.6 Gy,52个月时锁胸组HT发生率为15.0%(3/20),单纯胸组为5.0%(1/20),锁胸组V30>50%和甲状腺体积较小是有意义的预后因素,提示锁胸联合野放疗发生HT的危险性取决于甲状腺体积和V30。
精确放疗时代,临床常用双靶(锁骨上区、胸壁区)或单靶(锁骨上区+胸壁区)技术进行放疗。王天昶等[15]比较乳腺癌根治术后三维适形放疗(3DCRT)的单靶计划和双靶计划,发现靶区剂量分布差异无统计学意义(P>0.05),而单靶计划的甲状腺剂量V30、V40和肺平均剂量(MLD)分别高于双靶计划,差异有统计学意义(P<0.05);双靶计划基本达到甲状腺剂量阈值要求,单靶计划甲状腺V30显著高于剂量阈值,提示单靶计划患者发生HT的概率更高。洪潮等[16]比较左乳癌根治术后单靶调强放疗(IMRT)(6野调强与7野调强)的剂量学差异,发现靶区与大部分正常组织的受照剂量差异不大,但健侧甲状腺Dmean、最大剂量(Dmax)更高,提示单靶技术对健侧甲状腺的影响不容忽视,尤其6野调强技术的健侧甲状腺剂量明显升高。张明等[17]研究发现,乳腺癌术后IMRT计划靶区剂量分布优于3DCRT计划,但IMRT计划的甲状腺V20、V30和V40分别高于3DCRT计划,差异有统计学意义(P<0.05),提示3DCRT对甲状腺的保护作用显著优于IMRT。上述报道中,甲状腺剂量均未得到很好的控制。VMAT是一种具有旋转照射特点的动态IMRT,已被广泛应用于乳腺癌术后放疗中,杨健等[18]分析了左乳癌根治术后不同放疗计划(6野sIMRT与VMAT单靶技术)的剂量学差异,发现VMAT计划靶区剂量分布更均匀,可显著减少肺的高剂量受照体积和降低心脏的平均剂量。陈舒婷等[19]研究指出,乳腺癌根治术后单靶VMAT放疗对靶区的适形度和均匀性指数显著优于IMRT,两者对危及器官的保护各有优点,但未报道甲状腺受照剂量。
本研究分析了左乳癌根治术后单靶sIMRT和VMAT技术的剂量学特点,并重点探讨甲状腺不同梯度的受照剂量。结果显示,VMAT对甲状腺的保护作用总体优于sIMRT,但sIMRT、VMAT计划的左侧甲状腺V5、V10和V20均达100%或近100%,V30在90%以上,Dmean也超过40 Gy,而右侧甲状腺V20、V30迅速下降(V30为0),Dmean仅为19、17 Gy左右;sIMRT、VMAT计划的全甲状腺Dmean均超过26 Gy的阈值,但剂量波动范围较大,与相关研究[11-13]结论类似。进一步分析发现,首先,甲状腺紧邻锁骨上靶区,散射线和漏射线会对其形成低剂量照射;其次,左锁骨上靶区上界达环甲膜水平,左侧甲状腺下部和PTV部分重叠,为了保证靶区良好覆盖率,牺牲了对重叠部分甲状腺的保护;最后,向健侧方向照射的X射线对右侧甲状腺形成一定剂量照射,导致左右侧甲状腺低剂量体积明显增大,但左侧甲状腺剂量明显偏高。
单靶放疗技术的主要优点是摆位投照简单和省时,缺点是锁骨上区和胸壁区轮廓形状差异较大,对危及器官的保护比较困难。sIMRT和VMAT单靶技术的靶区分布、心脏和左肺等危及器官剂量限制均能满足临床要求,但在甲状腺保护方面均存在一定缺陷,部分患者会超过阈值。因此,放疗医师和物理师应高度重视,放疗时首先必须对两侧甲状腺进行严格的剂量限制,其次对于患侧甲状腺下极与PTV重叠部分应与医生充分沟通,对非重点区域的剂量进行评估和合理取舍,最后在投照时先打开加速器铅门,射野上界外用铅皮遮挡以防散射线和漏射线的照射,从而更好地保护患者甲状腺功能。虽然甲状腺辐射损伤的受照体积和剂量与放射性HT的阈值尚未统一,但甲状腺体积大小、Dmean和V30与放射性HT的发生密切相关,且Dmean>21~26 Gy和V30>50%可能是HT演变的阈值[9-10]。因此,任何放疗技术都必须严格控制甲状腺受照剂量和受照体积,放疗前和随访时有必要对患者的甲状腺功能进行监测,HT患者还应适时补充甲状腺激素。
