外泌体介导的lncRNA在结直肠癌发生发展过程中的作用及研究进展
2021-12-01智洁李亚星综述贾漪涛审校
智洁 李亚星 综述 贾漪涛 审校
结直肠癌是最常见的恶性肿瘤之一,在全球范围内,其发病率和死亡率均居第3 位[1]。在中国,随着经济和社会的发展以及人们生活方式的改变,其发病率已上升至恶性肿瘤的第3 位,且呈逐年攀升的势态[2]。外泌体是一类直径约40~100 nm 的脂质双分子层微小囊泡,广泛分布于人体中,富含多种生物活性分子如蛋白质、脂质、DNA、mRNA、microRNA 及长链非编码RNA(long non-coding RNA,lncRNA)等,在细胞间信息传递过程中发挥着重要作用。lncRNA 为长度大于200 nt 的非编码RNA,可在表观遗传、转录及转录后水平调控基因表达,与肿瘤的发生发展密切相关。研究发现,外泌体可通过lncRNA 参与恶性肿瘤的发生、侵袭和转移[3]。近几年来,越来越多的学者开始致力于研究外泌体lncRNA 在结直肠癌中的作用,并取得了一些重要突破。
1 外泌体lncRNA 的生物学特性
lncRNA 通常不具备蛋白质编码能力,在外泌体和微泡的保护下,可稳定地存在于组织体液中,且不受内源性RNA 酶影响[4,5]。外泌体lncRNA 在细胞间生物信息的远距离传递过程中发挥重要作用[6]。目前,研究者们通常认为,lncRNA 主要通过以下机制参与调控基因的表达:1)表观遗传水平:lncRNA 可通过DNA 甲基化或去甲基化、组蛋白修饰及染色体重塑等方式在表观遗传学水平调控基因表达,导致目标基因的表观遗传沉默或激活,例如lncRNA SNHG1 可以直接与起始复合体2(polycomb repressive complex 2,PRC2)相互作用,促进Krueppel 样因子2(Krueppellike factor 2,KLF2)和周期素依赖性激酶抑制因子2B(cyclin dependent kinase inhibitor 2B,CDKN2B)启动子的组蛋白甲基化,介导结直肠癌细胞增殖、侵袭和转移[7];2)转录水平:lncRNA 可与转录因子、增强子或启动子相互作用,调控RNA 转录、定位和稳定性,例如lncRNA TCF7 通过招募BAF170 可激活TCF7(transcription factor 7,TCF7)启动子并促进TCF7 表达,过表达的TCF7 则能加速结直肠癌细胞的迁移和侵袭[8];3)转录后水平:lncRNA 可通过碱基互补配对与靶mRNA 形成RNA 二聚体,阻碍其与转录因子结合,或直接募集某些翻译抑制蛋白,或直接与miRNA相互作用,调控mRNA 的剪切、翻译和降解,例如lncRNA GAS5 高表达通过作用于miR-221 可抑制结直肠癌细胞的增殖、侵袭和转移[9-10]。lncRNA 还可以通过海绵吸附miRNA 发挥拮抗作用,阻断miRNA对其下游靶mRNA 的抑制作用,导致内源性的靶点过表达,即竞争性内源RNA(competitive endogenous RNA,ceRNA)机制。例如:lncRNA CRNDE 在结直肠癌组织中呈高表达状态,可通过抑制miR-181a-5p导致下游的靶基因 β-catenin 和转录因子4(transcription factor 4,TCF4)表达升高,活化Wnt/β-catenin 信号通路,促进肿瘤细胞增殖,导致耐药[11]。不仅如此,在结直肠癌中,lncRNA 还可直接与靶蛋白结合间接调控靶基因的表达。Ling 等[12]发现,lncRNACCAT2 可直接与转录因子7 类似物2(transcription factor 7-like 2,TCF7L2)结合,激活Wnt/ β-catenin,上调MYC 表达,加速肿瘤进展。探索lncRNA 在结直肠癌中的相关调控机制有助于研究者了解结直肠癌发生发展的确切机制,为结直肠癌治疗提供新的视角。
2 外泌体lncRNA 在结直肠癌发生发展中的作用
在特定信号的“指示”下,结直肠癌细胞能够“选择”特异性的lncRNA 及其他活性物质进入外泌体中,外泌体则携带这些活性成分到达靶细胞发挥其特定的生物学功能。Cha 等[13]发现,KRAS 突变可影响结直肠癌细胞特异性的外泌体miRNA 输出,但对外泌体lncRNA 的输出过程并未显现出同样的作用。有研究者进一步采用了基于CRISPR/Cas9 的RNA 追踪系统进行监测,旨在通过引导RNA(gRNA)动态观察lncRNA靶向至特定基因组位点的过程,结果发现,携带lncRNA输出信号的gRNA 能够从供体细胞移至新的靶细胞,与特定的基因位点结合,而这一过程的发生与KRAS突变并无相关性,表明结直肠癌细胞可能通过一种尚未阐明的机制选择性地输出不同类型的lncRNA[14]。
肿瘤细胞分泌的lncRNA 被外泌体输送到达靶细胞,一方面可以在远处产生适合肿瘤细胞转移的微环境(即转移前生态位,pre-metastatic niche,PMN);另一方面还可直接作用于其他肿瘤细胞,改变肿瘤细胞本身的特性,甚至改变肿瘤的代谢编程,最终加速肿瘤的侵袭、转移及耐药的产生[15-17]。有研究发现,结直肠癌中的外泌体源性lncRNARPPH1 表达明显上调,它既可通过与TUBB3 结合防止其泛素化,诱导上皮-间质转化;又可与肿瘤相关巨噬细胞(tumor associated macrophages,TAMs)相互作用,促进TAM 向M2 型极化,从而加速肿瘤进展[18]。另有研究显示,无论是在肿瘤相关成纤维细胞还是结直肠癌细胞来源外泌体中,lncRNAH19 均呈高表达,该lncRNA 可竞争性结合miR-141,激活β-catenin 信号通路,参与并维持结直肠癌干细胞的干性状态,导致结直肠癌对化疗药物的抵抗[19]。Gao 等[20]研究发现,肿瘤细胞来源外泌体中的lncRNA 91H 能够促使异质性胞核核糖核蛋白K(heterogeneous nuclear ribonucleoprotein K,HNRNPK)表达升高,显著增加结直肠癌细胞的迁移和侵袭能力(图1)。
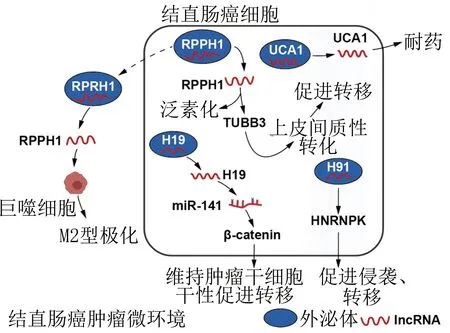
图1 lncRNA 在结直肠癌发生发展中的相关机制
结直肠癌中还有一种独特的现象,即lncRNA UCA1在癌组织和外泌体中的表达呈现出分离的趋势:lncRNA UCA1 在结直肠癌细胞中表达升高,但在外泌体中表达却明显下降。研究者推测这可能是肿瘤细胞“限制”了lncRNA UCA1 进入到外泌体中,而“为己所用”,以促进自身的发生发展。进一步研究证实,lncRNA UCA1 可与miR-135a、miR-143、miR-214和miR-1 271 结合,促进ANLN、BIRC5、IPO7、KIF2A、KIF23 等mRNA 表达,而功能富集的结果提示这些蛋白表达升高又与结直肠癌的转移密切相关(图1)[21]。这一现象的确切机制、临床意义值得深入研究。
lncRNA 亦可参与调节肿瘤细胞的代谢重编程而影响肿瘤的进展。Chen 等[22]在乳腺癌中发现,有氧糖酵解显著的肿瘤细胞周围通常伴随着大量巨噬细胞浸润,而糖酵解的存在与肿瘤细胞的凋亡水平呈负相关。巨噬细胞来源的外泌体可携带lncRNA HISLA到达肿瘤细胞,通过抑制缺氧诱导因子1α(hypoxiainducible factor-1α,HIF-1α)与其羟化酶2(prolyl hydroxylase 2,PHD2)的结合而减少HIF-1α 的降解,从而促进肿瘤细胞持续增殖。目前结直肠癌中尚缺乏外泌体lncRNA 与代谢调控的相关研究,需进一步的实验探究。
3 外泌体lncRNA 在结直肠癌诊断和预后评估中的价值
外泌体lncRNA 在组织体液中稳定性良好,且其含量变化可反映出个体的生理病理状态,近年来研究人员就其诊断价值进行了广泛的研究。现已证实,lncRNA CCAT2 在结肠癌、胃癌、乳腺癌和肝癌等多种肿瘤中发挥促癌作用。结直肠癌患者肿瘤组织及血清外泌体源性的lncRNA CCAT2 均显著升高,而术后血清水平明显下降,提示其有望成为结直肠癌诊断的潜在预测因子[23]。一项基于基因芯片的生物信息学分析显示,外泌体来源的LNCV6_116109、LNCV6_98390、LNCV6_38772、LNCV_108266 、LNCV6_84003 和LNCV6_98602 在早期结直肠癌患者的血浆中呈现高表达状态,研究者进一步通过ROC 曲线对其准确性进行了验证,表明其可作为早期诊断结直肠癌的有效血清学标志物[24]。另有研究表明,lncRNA CRNDE-h在区分结直肠癌患者与良性结肠疾病、健康人群方面甚至优于CEA(敏感性为70.3%vs.37.16%,特异性为94.4%vs.88.75%)。当两种标记物联合使用时,可更加准确地预测结直肠癌患者的总生存,联合检测外泌体lncRNA CRNDE-h 和CEA 水平,可能会得到更高的肿瘤检出率[25]。由此可见,外泌体lncRNA 作为肿瘤标志物,具有更高的灵敏度和稳定性,临床应用的潜力很大。
另外,外泌体lncRNA 在结直肠癌患者的预后评估中也有一定的价值。Liu 等[25]发现,结直肠癌细胞外泌体源性的lncRNA CRNDE-h 不仅具有一定的临床诊断价值,更是与结直肠癌的预后密切相关。与结直肠良性疾病或健康人群相比,结直肠癌患者血清中外泌体源性的lncRNA CRNDE-h 表达明显升高,其高表达与淋巴结转移及其它部位远处转移呈正相关,还与结直肠癌患者的预后呈负相关。相反,lncRNA GAS5 作为抑癌基因,在结直肠癌患者肿瘤组织、血清及外泌体中表达均是下调的。外泌体源性的lncRNA GAS5 高表达可通过作用于miR-221 而抑制肿瘤细胞的增殖、侵袭和转移,其表达水平升高与肿瘤患者的淋巴结转移、局部复发及远处转移呈负相关(局部复发率为55.06%vs.58.99%,P<0.05;远处转移率为29.75%vs.33.09%,P<0.05),与3年总生存期呈正相关(67.72%vs.64.75%,P<0.05)[26]。Baassiri 等[27]研究发现,lncRNA APC1 在结直肠癌组织中的表达明显降低,这类结直肠癌更易发生淋巴结及远处转移,临床分期更晚,预后更差(41.4 个月vs.64.3 个月,P<0.05)。相关机制研究证实,lncRNA APC1 低表达时可激活MAPK 信号通路诱导肿瘤血管形成,加速肿瘤的进展;APC 基因能够通过抑制PPARα 在lncRNA APC1 启动子上的富集而增加lncRNA APC1 的表达,当lncRNA APC1 表达上调时可直接与Rab5b mRNA 结合,降低其稳定性,同时减少外泌体的产生,最终抑制结直肠癌细胞的增殖和转移[28]。上述研究结果为外泌体lncRNA 作为结直肠癌患者的潜在预后预测标志物提供了有力依据。
4 外泌体lncRNA 在结直肠癌治疗中的价值
近年来,结直肠癌内科治疗特别是药物治疗虽已取得可观的成效,但仍面临着耐药和肿瘤复发等问题,寻找新的治疗策略十分必要。现已证实,肿瘤细胞可通过分泌外泌体,携带多种lncRNA 进入肿瘤细胞,介导耐药的发生[29]。例如,结直肠癌中的成纤维细胞可通过其所分泌的外泌体将lncRNA CCAL 传递给肿瘤细胞,lncRNA CCAL 进一步与HuR 蛋白相互作用,激活β-catenin 信号通路,介导癌细胞对奥沙利铂和5-Fu 的耐药,而下调lncRNA CCAL 的表达可延缓甚至逆转这一过程的发生[30]。Yang 等[31]还发现,lncRNA UCA1 在对西妥昔单抗耐药的结直肠癌细胞及其外泌体中表达明显增高,且在进展期肠癌患者外周血外泌体中的表达水平亦明显升高。如前所述,lncRNA UCA1 本身在癌细胞和外泌体中的表达呈现出分离的趋势(即在细胞中高表达,在外泌体中低表达),提示外泌体能够通过lncRNA UCA1 介导西妥昔单抗耐药,抑制外泌体源性lncRNA UCA1 的表达有望逆转或延缓获得性耐药的发生。探索外泌体lncRNA 对结直肠癌药物耐药的影响将有助于进一步阐明结直肠癌耐药的分子机制,为克服或逆转耐药提供新思路(表1)。
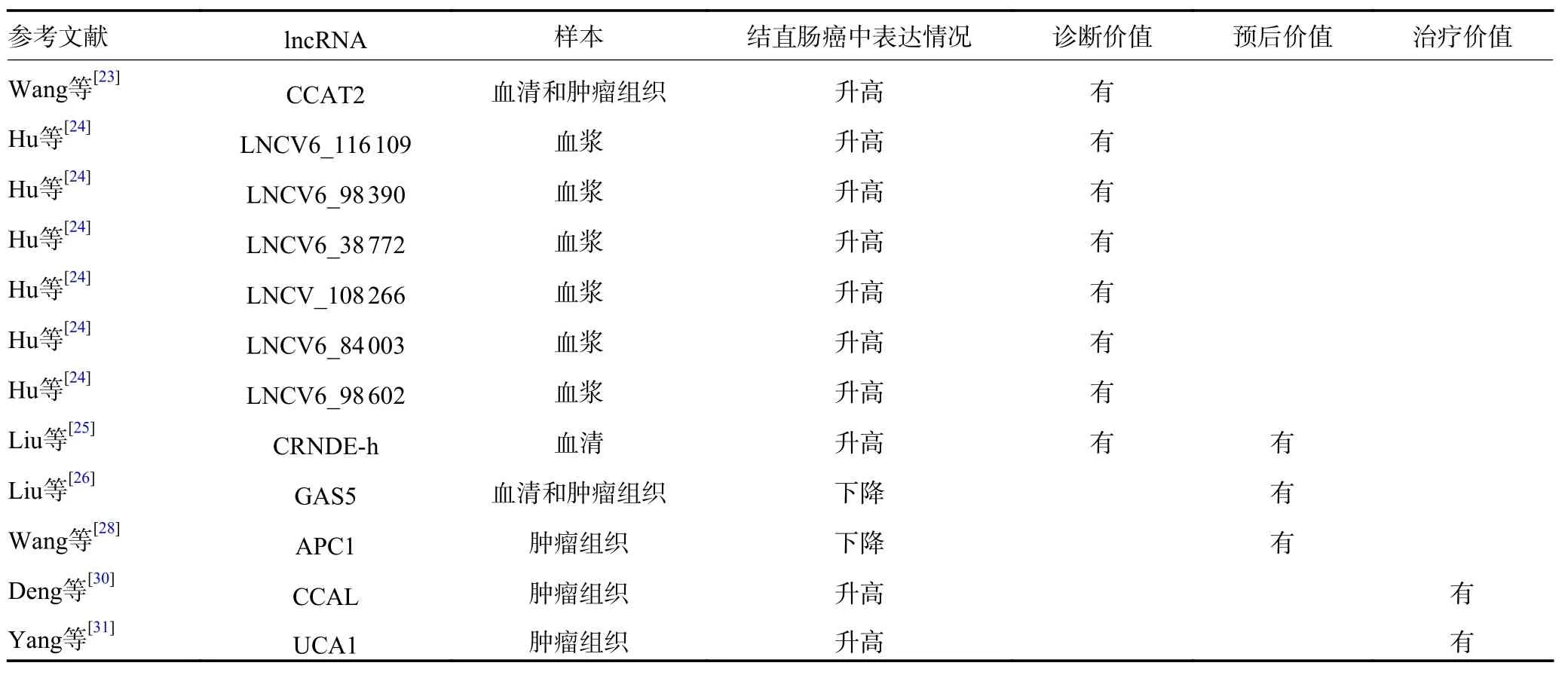
表1 结直肠癌中lncRNA 表达与诊断、预后和治疗之间的研究进展
当前研究仍局限于外泌体lncRNA 与结直肠癌耐药之间的相互影响,具体机制尚不明确。而现有证据表明,肿瘤微环境、肿瘤代谢的改变同样与结直肠癌治疗密切相关[32]。外泌体lncRNA 到达相应的靶细胞后亦可能通过影响局部免疫微环境,调节靶细胞的糖代谢、脂质代谢,对结直肠癌治疗疗效产生影响。然而目前相关的研究依旧匮乏,需进一步探索其中的机制。
此外,外泌体lncRNA 作为细胞间的通讯工具,具效率高、靶向性强等优势,可作为药物载体用于靶向治疗,在临床治疗中有着较强的应用前景。靶向作用于外泌体lncRNA,调控外泌体lncRNA 细胞间通讯为结直肠癌精准治疗提供了新的领域和方向。
5 结语
LncRNA 与结直肠癌的发生发展密切相关,这些异常表达的lncRNA 能够通过影响癌症相关的关键信号通路,促进或抑制结直肠癌的进展。由于外泌体在体液中浓度较高,易于富集,其所包含的lncRNA 能长期稳定存在,所以能够及时、准确地反映疾病进展、治疗反应及转归。一方面,液态活检标本中外泌体lncRNA表达的特异性改变可能有助于结直肠癌的早期诊断和预后评估;另一方面,lncRNA 作为潜在的药物靶点,将来可用于研发新的抗癌药物。如今,免疫治疗为众多肿瘤患者带来了生存获益,但结直肠癌患者往往对免疫治疗不敏感[33]。外泌体lncRNA 可与结直肠癌免疫微环境相互作用,或许能成为提示结直肠癌患者免疫治疗效果的一个重要指标。
当然,目前针对外泌体lncRNA 的研究依旧存在许多问题,如:1)外泌体源性lncRNA 之间的交互作用尚不明确;2)寻找对结直肠癌的进展、耐药、免疫耐受影响最大的lncRNA 仍面临挑战;3)结直肠癌中外泌体lncRNA 水平及作用与其他肿瘤的差异及背后的机制值得深入研究;4)不同的lncRNA 在结直肠癌发生发展过程中可能存在时空动态性,其中的意义有待阐明。
随着蛋白质组学、高通量测序、转录组学及生物信息学分析等技术的快速发展,研究者对外泌体lncRNA在结直肠癌发生发展过程中的机制及其临床应用价值的认识将不断深入。外泌体lncRNA 在不久的将来很有可能会成为结直肠癌早期筛查、治疗、疗效预测与预后评估中的研究热点。
