高剂量甲氨蝶呤治疗骨肉瘤致白细胞降低的风险因素分析
2021-12-01夏文彬吴海啸胡阳张瑾张超
夏文彬 吴海啸 胡阳 张瑾 张超
骨肉瘤是青少年最常见的原发恶性肿瘤,全球年发病率约为3~4 例/百万人。骨肉瘤患者的生存情况随着治疗模式的革新,得以显著改善[1-2]。目前,高剂量甲氨蝶呤(methotrexate,MTX)作为多药联合选择药物之一,已成为国内外骨肉瘤化疗指南的推荐药物[3-4]。高剂量MTX 治疗骨肉瘤的推荐应用剂量是8~12 g/m2,当MTX血药浓度(concentration of methotrexate,CMTX)≥700 μmol/L 并持续6 h 以上可引起药物延迟代谢,严重者可致死[5]。MTX 治疗后Ⅰ~Ⅱ度骨髓抑制发生率高达45%,Ⅳ度达12%[6]。白细胞降低(leukopenia,LP)是MTX 治疗后最常见的并发症之一。既往研究表明,16.8%的骨肉瘤患者在经过MTX 治疗后出现了4 度LP[7]。研究指出,3~4 度LP 可显著增加患者的继发感染风险,引起肺炎、心内膜炎和泌尿系统感染等,甚至造成患者死亡。因此,临床亟需深入探讨骨肉瘤患者在接受高剂量MTX 围化疗期间发生LP 的风险。本研究回顾性分析单中心骨肉瘤队列,建立MTX 应用后第0、24、48、72 h 的CMTX曲线,分析MTX 的整体CMTX变化趋势,各血药浓度监测点与LP 发生的相关性,探索能早期预测发生LP 的监测点;同时,联合患者的临床和病理特征,分析LP 发生的风险因素,为MTX 用药后LP 的早期预防和治疗奠定基础。
1 材料与方法
1.1 临床资料
选取2017年1月至2019年12月天津医科大学肿瘤医院85 例骨肉瘤患者资料,根据纳入排除标准,43 例骨肉瘤患者纳入研究,其中男性28 例,女性15 例,平均年龄(20.8±11.2)岁。43 例骨肉瘤患者中,骨肉瘤位于股骨远端21 例,胫骨近端12 例,肱骨近端2 例,髂骨、锁骨、腓骨8 例。病理类型:成骨型30 例,成软骨型9 例,成纤维型2 例,骨巨细胞瘤恶变型1 例,小细胞型1 例;根据美国癌症联合委员会(AJCC)分级,ⅡA 级11 例,ⅡB 级29 例,Ⅲ级3 例。首诊时伴发病理性骨折3 例。本组患者临床病理特征见表1,2。
纳入标准:经病理诊断明确为原发性骨肉瘤患者、完整接受术前2 个周期完整的MAP 方案(甲氨蝶呤、顺铂和多柔比星)或IMD 方案(异环磷酰胺、甲氨蝶呤和多柔比星)序贯新辅助化疗以及术后含至少2 个周期的MAP 化疗者,每个周期化疗前血常规结果提示骨髓功能无显著异常者,病例资料详尽者。排除标准:病理诊断难以明确和(或)多重恶性肿瘤者、未进行新辅助化疗的骨肉瘤患者、骨旁骨肉瘤及继发性骨肉瘤患者、化疗前血常规结果提示骨髓功能异常者,病例资料缺失者。
1.2 方法
1.2.1 高剂量MTX 治疗方案及CMTX监测 患者在给予高剂量MTX 治疗前12 h 进行水化和碱化:500 mL 0.9% NaCl+500 mL 0.9% NaCl+250 mL 5%NaHCO3。MTX 滴注期间连续给予:1)500 mL 5%NaCL+500 mL 0.9% NaCl+10 mL 15% KCl ;2)500 mL 5% NaHCO3;3)2 mg 长春新碱+50 mL 0.9%NaCl;4)1 000 mL 0.9% NaCl+8~12 g/m2MTX 连续滴注5 h;5)100 mL 0.9% NaCl+5 mg 托烷司琼,250 mL 0.9% NaCl+200 mg 维生素B6,100 mL 0.9%NaCl+1 mg 地塞米松,100 mL 0.9% NaCl+呋塞米;总液体量根据患者的体质量指数达到3 200~4 000 mL。记录24 h 内尿量,维持尿pH 值为7~9。MTX 滴注完毕后继续给予2 天的水化和碱化治疗。患者在整个MTX 化疗期间,口服NaHCO31.0 g,tid 和别嘌呤醇200 mg,tid。
MTX 滴注完毕后即刻(0 h)、第24、48、72 h 分别取外周静脉血监测CMTX。第6 h 开始亚叶酸钙和利尿剂解毒治疗,亚叶酸钙解毒方案为12~15 mg/m2,q6h,d1~3,肌注。随后依据CMTX进行个性化亚叶酸钙的解毒治疗,直至MTX 外周血浓度低于0.05 μmol/L,停止解毒治疗。
1.2.2 白细胞降低的治疗 1 度LP,白细胞水平范围:正常值下限至3.0×109/L。治疗:继续观察,加强营养,口服升白药对症治疗。
2 度LP,白细胞水平范围:(2.0~3.0)×109/L。治疗:继续观察,加强营养,口服升白药对症治疗。如呈进行性下降,给予重组人粒细胞集落刺激因子(rhGCSF)75 μg,ih,qd,连用3 天后复查血常规。
3 度LP,白细胞水平范围:(1.0~2.0)×109/L。治疗: rhG-CSF 150μg,ih,qd,每天复查血常规,如呈进行性下降,提高用药剂量至225 μg,必要时给予聚乙二醇化重组人粒细胞集落刺激因子(PEG-rhG-CSF)3.0 mg,ih,st。并监测体温。
4 度LP,白细胞水平范围:<1.0×109/L。治疗:rhG-CSF 150 μg,ih,bid,每天复查血常规,并监测体温。给予预防性抗生素。给予PEG-rhG-CSF 6 mg,ih,st。
1.2.3 不良反应分析 患者在MTX 治疗前进行血常规、肝肾功能和心电图检查,序贯化疗治疗后1 周内监测血常规和肝肾功能。根据美国国立癌症研究院通用毒性标准(NCI-CTCAE 4.0),化疗后LP 定义为化疗后第1 天至化疗后1 周内白细胞计数<3.0×109/L[8-10]。
1.3 统计学方法
采用SPSS 23.0 软件进行统计学分析。所有连续性变量记为平均值及标准差,包括年龄及血清学指标;分类变量为数量及比例,包括新辅助化疗类型、病理类型等。组间患者各变量差异进行t检验或χ2检验。采用Logistic 回归分析确定发生LP 的危险因素,计算相关指标的OR 值及95% 置信区间(confidence interval,CI)。以P<0.05 为差异具有统计学意义。
2 结果
2.1 患者临床病理特征
每例患者平均进行了4 个周期的MTX 治疗,经筛选后,共177 个周期的化疗被纳入本研究。其中87 个周期的化疗发生了LP(LP 组),90 个周期的化疗未发生LP(正常组),见表1,2。
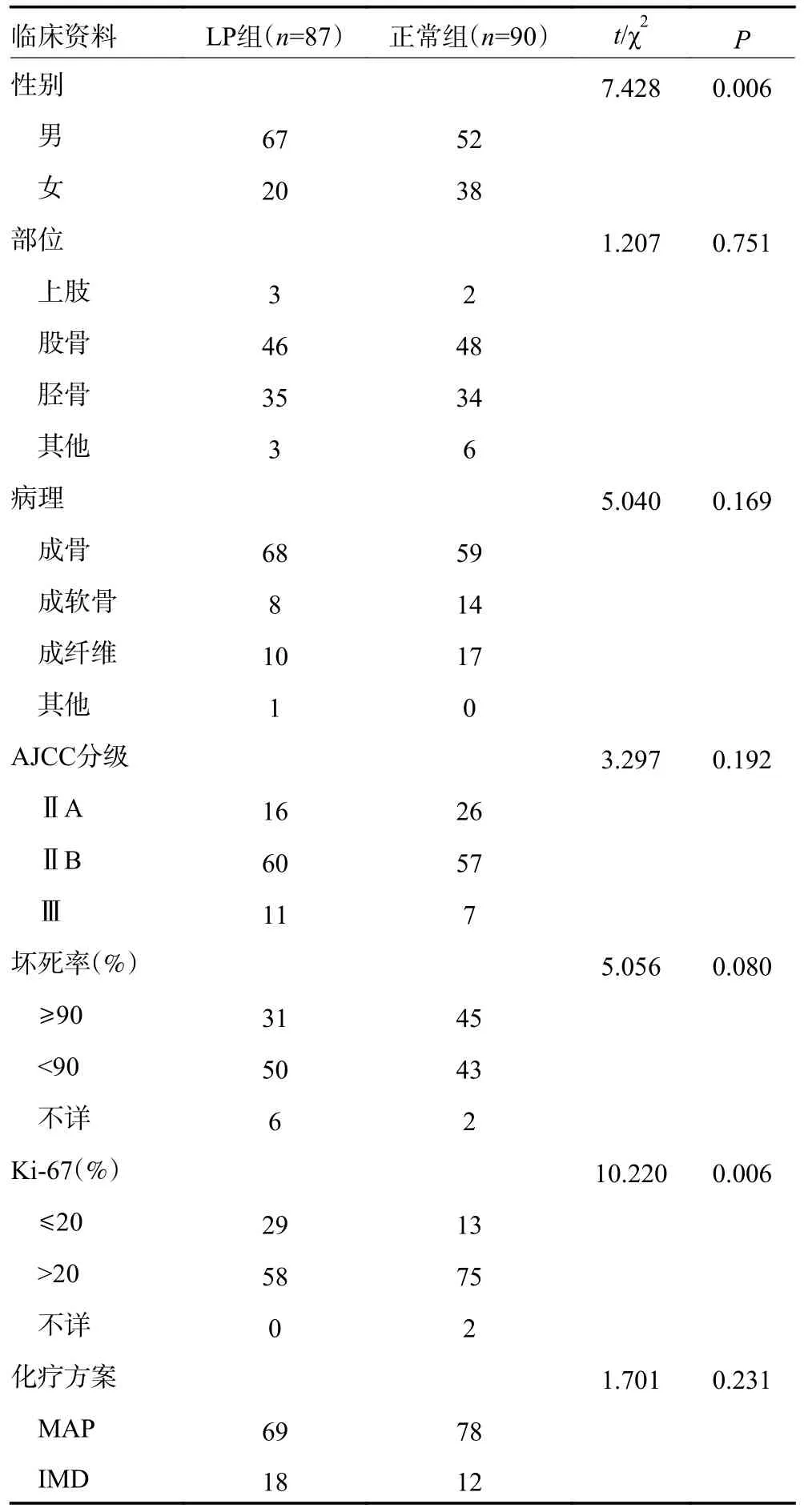
表1 LP 组与正常组患者的临床病理特征 (周期数)
2.2 MTX 血药浓度分布情况
LP 组和正常组患者MTX 总剂量分别为(13.99±1.68)g 及(14.83±1.89)g。MTX 治疗后0、24、48、72 h 平均CMTX分别为(922.84±345.26 )μmol/L、(0.964±0.694)μmol/L、(0.136±0.192)μmol/L 和(0.033±0.044)μmol/L。化疗后LP 组的患者,MTX 给药后0、24、48、72 h 的CMTX分别为(890.20±359.57)μmol/L、(0.610±0.378)μmol/L、(0.117±0.215)μmol/L 及(0.027±0.030)μmol/L。化疗后正常组的患者,MTX 给药后0、24、48、72 h 的CMTX分别为(954.38±329.78)μmol/L、(1.305±0.757)μmol/L、(0.155±0.164)μmol/L 和(0.039±0.054)μmol/L。不同时间点CMTX变化趋势见图1。
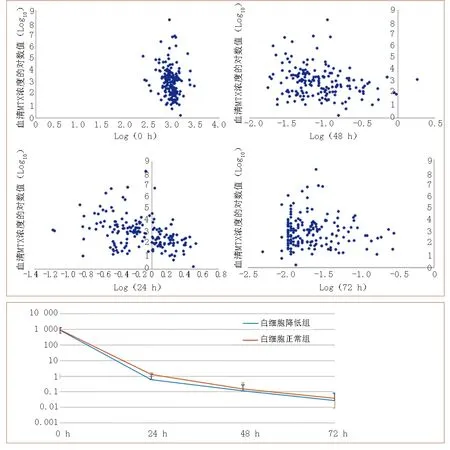
图1 MTX 血药浓度分布和变化趋势(对数值Log10)
MTX 给药后第24 h CMTX均<10 μmol/L,两组间第24 h CMTX存在显著性差异。75 次MTX 治疗后CMTX为1.0 ~3.34 μmol/L,共发生60 次LP;其余102 次MTX 治疗后CMTX<1.0 μmol/L,发生30 次LP。本研究共计有10 次MTX 化疗后第72 h 出现CMTX>0.1 μmol/L,提示MTX 发生了延迟排泄,其中9 次发生白细胞降低。CMTX以1.0 μmol/L 为临界值,预测MTX 给药后白细胞低于3×109/L 敏感性与特异性分别为66.7%和82.8%。不同时间点CMTX与术后白细胞水平的关系见图2。
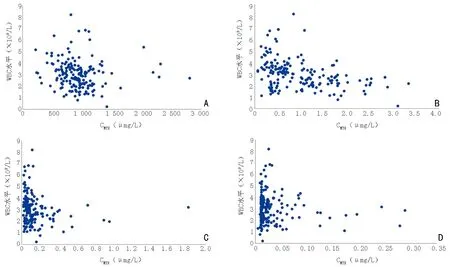
图2 不同时间点CMTX 水平与LP 的关系
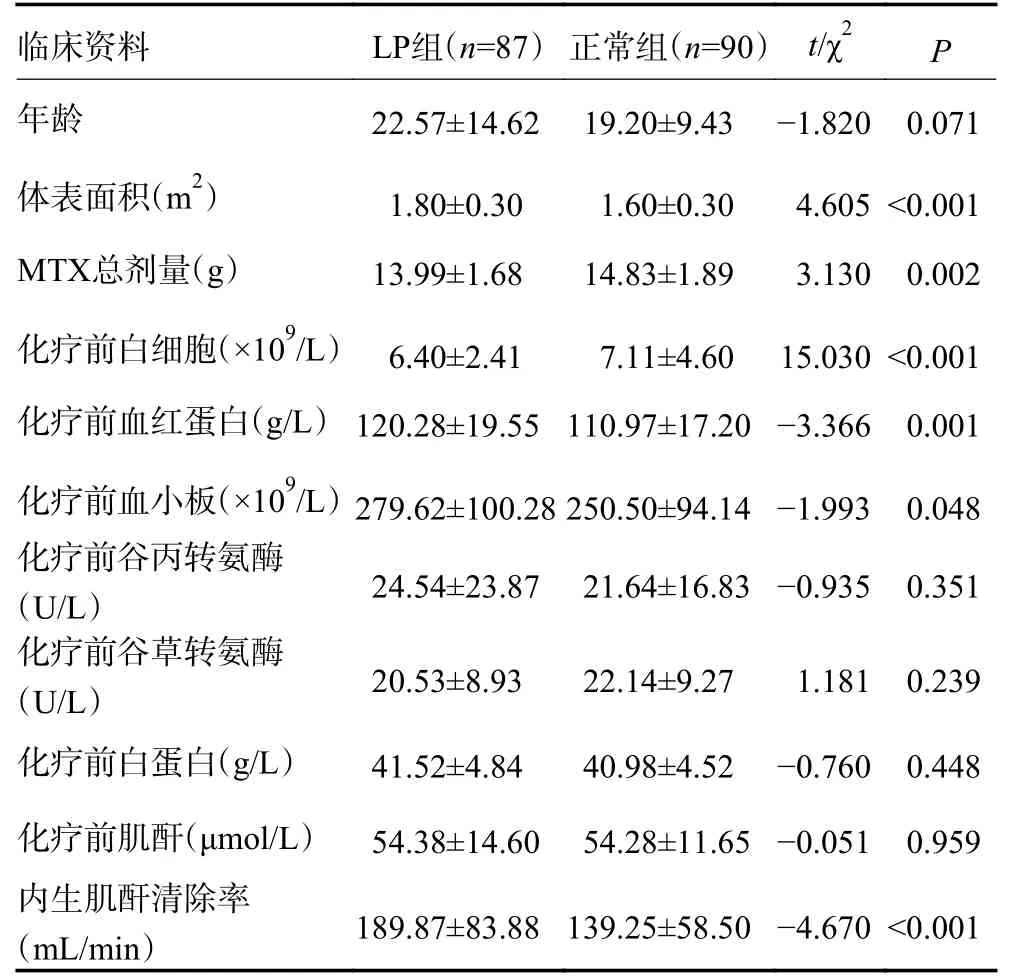
表2 LP 组与正常组患者的临床病理特征 (周期数)
2.3 MTX 后发生LP 的危险因素
术前两组患者的谷丙转氨酶、谷草转氨酶、白蛋白及内生肌酐清除率水平比较均无显著性差异(均P>0.05)。根据Logistic 单因素分析,化疗前病理检测Ki-67>20%(OR=2.962,95%CI:1.416~5.092;P=0.004)、24 h CMTX>1.0 μmol/L(OR=9.600,95%CI:4.728~19.491;P<0.001)及轻度贫血(OR=2.157,95%CI:1.125~4.134;P=0.021)是化疗后出现LP 的危险因素(表3,4)。
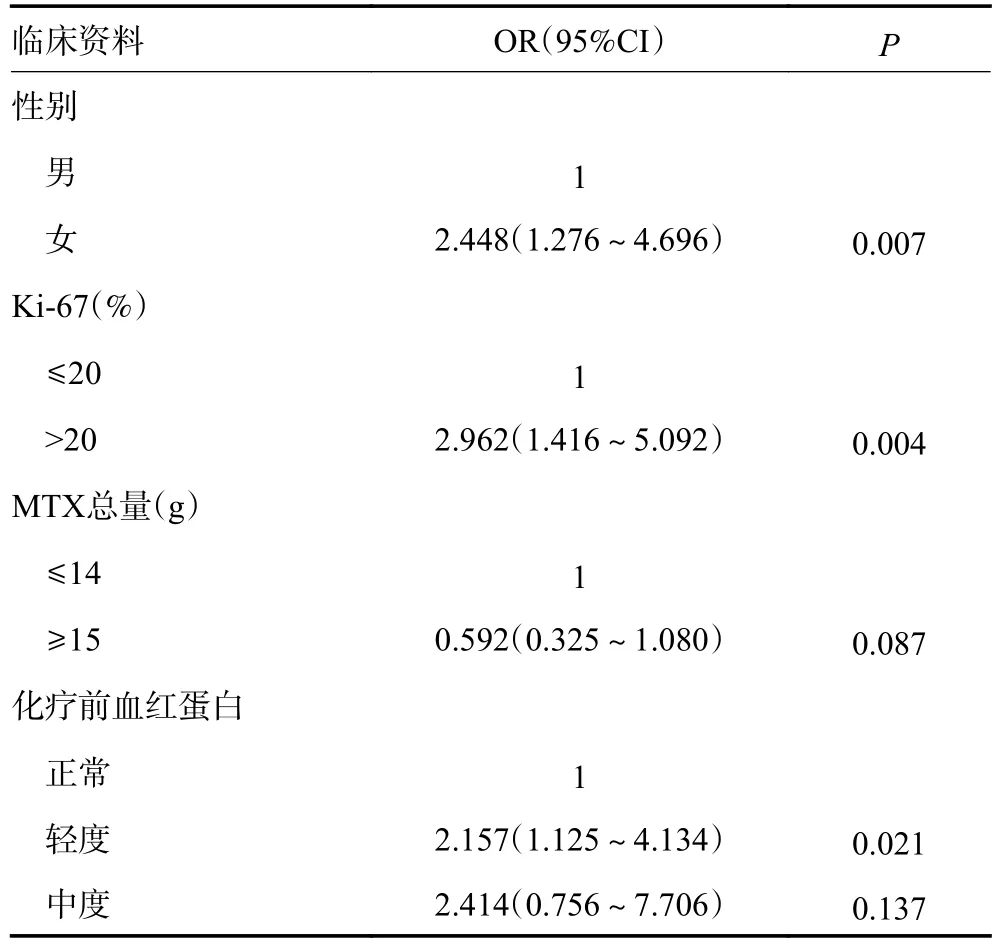
表3 白细胞降低的临床病理学风险因素分析
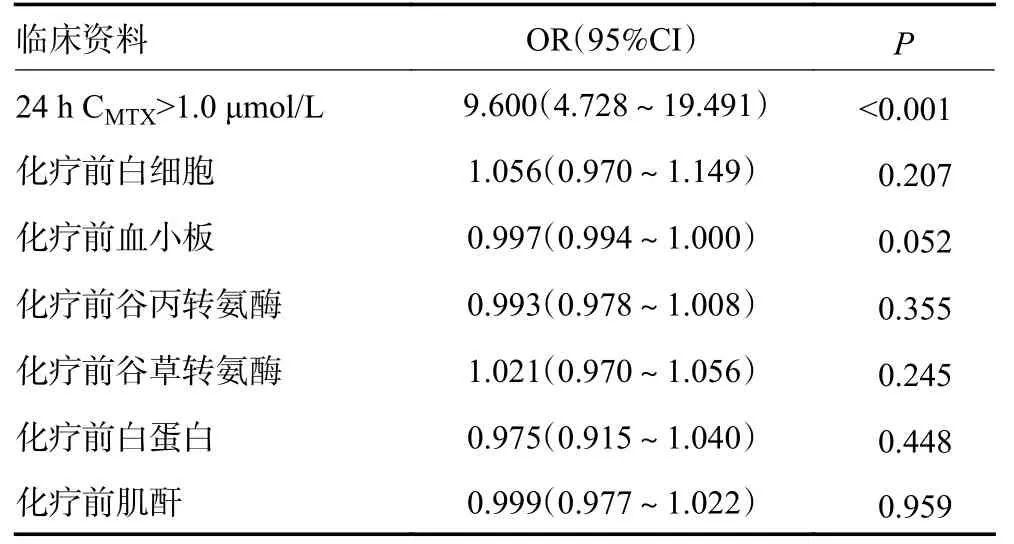
表4 白细胞降低的检验学风险因素分析
3 讨论
骨肉瘤是一种来源于中胚层间叶源性的高度恶性肿瘤,自Rosen 等[11]提出以MTX 为主的化疗模式出现以后,治疗效果取得了巨大进步。然而,MTX 的严重不良反应限制其广泛应用,其代谢存在10 倍以上的个体差异,即使在美国国立综合癌症网络(NCCN)推荐的标准辅助治疗模式下仍有24%的患者在治疗过程中发生LP,严重者甚至导致死亡,MTX 的毒性反应已成为序贯化疗方案制约骨肉瘤治疗效果的重大瓶颈之一[5]。
MTX 各时间点CMTX存在较大的个体差异。大剂量MTX 治疗骨肉瘤后第0 h 的最佳CMTX应为700~1 000 μmol/L,第24、48、72 h 的平均CMTX应分别低于10、1、0.1 μmol/L,否则存在MTX 发生排泄延迟的可能,进而预示严重肝、肾等毒性反应发生的可能[12]。既往研究表明,MTX 的剂量与不同时间点的CMTX相关,不同剂量MTX 对第0 h 和24 h 的CMTX有显著影响,而对第48 h 和72 h 的CMTX比较差异无统计学意义[13]。在众多因素中,性别、年龄与CMTX无明显相关性,而肝功能损伤级别与0 h 的CMTX显著相关[10]。本研究观察到0 h 平均CMTX为(922.84±345.26)μmol/L,该趋势与前期报道一致,而第24、48、72 h CMTX显著低于其他报道,考虑可能与充分的碱化、水化和标准亚叶酸钙解毒有关。
早期发现并及时治疗LP 可显著降低继发性感染的发生率,进而保障骨肉瘤患者的治疗。目前临床中常采用48 h 的CMTX作为发生肝、肾毒性的预测依据,然而CMTX是否可预测LP 发生鲜见深入研究[12]。本研究发现,第24 h CMTX>1 μmol/L 时,LP 的发生率显著增加,此时间点的CMTX可为LP 早期预警,及早发现并给予必要的预防干预治疗,可有效预防LP 和继发性感染的发生[14]。
前期研究发现,女性患者是MTX 治疗骨肉瘤后发生LP 的独立危险因素[15]。目前,性别对MTX 代谢的影响研究较少,且存在一定的争议。有研究表明,女性骨肉瘤患者发生MTX 重度延迟排泄的发生率明显高于男性[15]。相较男性患者,女性患者肝脏代谢功能较弱,这可能是引起继发性LP 降低的重要因素之一[16]。因此,对于肝脏代谢功能较差的女性骨肉瘤患者在进行MTX 治疗时,有必要进一步增加水化和碱化程度,并建立更加严格的临床监测系统。然而,本研究结果未提示性别可影响LP 发生,原因可能由于本组人群构成偏向青少年(平均年龄20.8±11.2 岁),肝功能差异不明显,MTX 的代谢较快。
本研究发现LP 的发生与Ki-67 指数密切相关,Ki-67>20%的患者更易发生LP。其潜在机制可能为G1 期细胞主要表达Ki-67[17],而MTX 多作用于细胞周期的S 期,对G1 期细胞杀伤能力较弱。因此,骨肉瘤Ki-67 指数越高,MTX 对肿瘤细胞的杀伤能力就越差,从而导致血清中MTX 含量增加,进而发生LP。由此可见,Ki-67 指数增高是发生LP 的不良独立风险因素,该指数或可用于骨肉瘤患者的分层管理,指导筛查潜在可能发生LP 的骨肉瘤患者。同时,本研究发现MTX 治疗前有轻度贫血的患者更易发生LP,需要对合并贫血的患者进行必要干预和纠正,预防化疗后LP 的发生。
本研究存在一定的局限性:1)为单中心数据回顾性研究,患者数量较少,需要进一步扩大数据样本量;2)未深入探索各监测点CMTX与化疗后发生LP 级别的相关性,该相关性可早期预警MTX 治疗后发生骨髓抑制的程度,进而在MTX 治疗前提早使用升白细胞药物预防LP 发生。未来将开展进一步探索。
综上所述,第24 h CMTX、Ki-67 和MTX 治疗前血红蛋白水平是接受高剂量MTX 治疗的骨肉瘤患者发生LP 的风险因素。临床医护人员可在围化疗期间密切监测上述指标,以预判LP 的发生可能,进而保障骨肉瘤患者更安全的接受高剂量MTX 治疗,以期改善其远期生存和生存质量。
