盐酸羟考酮缓释片12 小时滴定方案用于中重度癌痛患者的有效性和安全性—前瞻性 随机 开放 多中心 平行对照研究
2021-12-01石志永何钎铖郭银红王燕邵银仙薛宏怡林晓骥陈传军诸静文郭俊华应申鹏肖建军赵春花邢旻琰陈韵蔡国英寿佳威宋斌斌余国林史敏王永辉王剑邵婷婷黄芳芳张沂平
石志永 何钎铖 郭银红 王燕 邵银仙 薛宏怡 林晓骥 陈传军 诸静文 郭俊华 应申鹏 肖建军 赵春花 邢旻琰 陈韵 蔡国英 寿佳威 宋斌斌 余国林 史敏 王永辉 王剑 邵婷婷 黄芳芳 张沂平
癌痛是肿瘤患者最常见的症状,未缓解的疼痛显著影响患者各方面生存质量。有研究结果显示,88%的癌痛患者报告为中重度疼痛,平均持续时间为6 个月[1]。美国国立综合癌症网络(National Comprehensive Cancer Network ,NCCN)成人癌痛指南(2009年版)明确指出,疼痛控制是肿瘤综合治疗的重要内容之一[2]。
阿片类药物是中、重度癌痛治疗的首选药物[3]。特别是阿片受体完全激动剂,具有镇痛强度随药物剂量增加而逐渐增强的特性,无剂量封顶效应。该类药物不存在“标准剂量”,最佳镇痛剂量是指在整个用药期间既可以缓解患者疼痛又无不可耐受副作用的剂量。因此,对于每一例疼痛患者,均需要逐渐调整剂量,以获得最佳用药剂量,这个过程称为滴定[4]。
国内外权威癌痛管理指南均对强阿片类药物的滴定方法给出了明确指导。NCCN 成人癌痛指南的滴定方案,包括口服吗啡即释片的滴定流程以及静脉吗啡滴定流程[2]。中国癌症疼痛诊疗规范(2018年版)中也对口服吗啡即释片的滴定方案进行了比较详细的阐述。口服即释药物或静脉给药的滴定方案,具有滴定迅速的特点,但同时也存在滴定流程复杂不易掌握、调整过程需要严密监测从而增加医务人员工作负担、不适合门诊患者等问题。
2012年EAPC 阿片类药物癌痛治疗指南明确指出[5]:即释或缓释剂型的口服吗啡、羟考酮均可用于阿片类药物的滴定,无论采用这两种剂型中的哪一种进行阿片类药物的滴定,都应按需给予即释阿片做为补充药物治疗爆发痛。中国癌症疼痛诊疗规范(2018年版)也明确指出:在初始滴定过程中,对疼痛病情相对稳定的患者,可考虑使用阿片类药物缓释剂作为背景给药,在此基础上备用短效阿片类药物,用于治疗爆发性疼痛。以上指南信息,为盐酸羟考酮缓释片用于中重度癌痛的阿片类药物滴定提供了理论依据。盐酸羟考酮缓释片作为强阿片类药物,兼有速释和缓释双相释放特点,缓释部分药物浓度呈平台状态,持续释放12 h[6],在此基础上联合即释吗啡滴定,能够加速滴定的完成。
本研究中的12 h 滴定方案,是根据临床医生的实际癌痛治疗经验整理开发出来,具有一定的临床癌痛治疗的实践基础,与传统调整方案比较,主要差异在于:为了快速的将阿片药物调整到合适剂量,采用了12 h调整一次剂量,这种调整方式一方面与羟考酮缓释片持续作用时间12 h 相吻合,另一方面避免了重度疼痛患者需要忍受24 h 调整剂量的痛苦,加快了滴定的频率,使患者更快获得疼痛缓解。另外,该治疗模式已经通过部分的回顾性和观察性研究获得初步证实[7]。
本研究旨在证实12 h 滴定方案的可行性和安全性,从而为癌痛患者提供一种安全、有效、方便的滴定方案选择。
1 材料与方法
1.1 临床资料
选取2018年2月至2019年12月浙江省24 家医院肿瘤科住院治疗的中重度癌痛患者作为研究对象(表1)。纳入标准:1)年龄≥18 岁;2)根据临床诊断和/或病理学诊断确认的肿瘤患者 ;3)过去24 h 平均疼痛强度(NRS)≥4 分;4)阿片药物未耐受患者(根据NCCN 指南,阿片药物未耐受患者包括没有长期将阿片类药物作为每天基础用药的患者。 FDA 将每日至少接受 60 mg 吗啡、每日至少口服 30 mg 羟考酮或者其他等量阿片类药物达到一周或更长时间视为耐受,否则即为阿片未耐受患者);5)能够口服药物,且经医生判断适合应用羟考酮缓释片剂量调整方案;6)镇痛药物剂量调整期间,能够排除抗肿瘤治疗(放疗、化疗、靶向治疗等) 对镇痛作用的影响;7)使用奥施康定12 h内使用即释吗啡补救镇痛至少1 次;8)神志清楚,能够理解医生的用药方案指导;9)患者必须了解研究过程和评估,同意参加本试验,并签署知情同意书。排除标准:1)妊娠或哺乳期患者;2)已知对羟考酮或研究药物中任何其它成分过敏者;3)患有非肿瘤相关性疼痛或原因不明的疼痛,如骨关节炎疼痛、下腰痛等;4)癌痛急诊;5)复杂性癌痛或难治性癌痛;6)顽固性便秘患者;7)最近2 周内服用过单氨氧化酶抑制剂(MAOIs)或该类型药物;8)有潜在胃肠功能疾病和/或外科手术治疗危险,可能导致胃肠道狭窄、盲袢或胃肠道梗阻;9)存在不稳定的合并疾病;或存在重要脏器功能障碍的患者;10)正在患有感染、脓肿或发烧症状的患者;11)肝、肾功能异常者,如肌酐值≥2 倍正常值上限或ALT 或AST≥2.5 倍正常值上限(肝转移患者可放宽到≥5 倍正常值上限);12)正在服用抗癫痫或心律不齐药物的患者;13)属于产品说明书或研究者手册中羟考酮或吗啡的禁忌证、药物不良反应(ADRs)和药物相互作用中的患者;14)有药物或酒精滥用史的患者;15)研究前1 个月内参加其他药物临床试验研究的患者;16)在研究期内可能会改变其合并用药(治疗阿片类药物不良反应的除外)的患者;17)根据研究者的判断,属于除入选标准和排除标准以外的因其它任何原因而不适合参加本研究的患者。根据纳入和排除标准共114 例患者入组,所有患者均签署麻醉药品使用知情同意书。
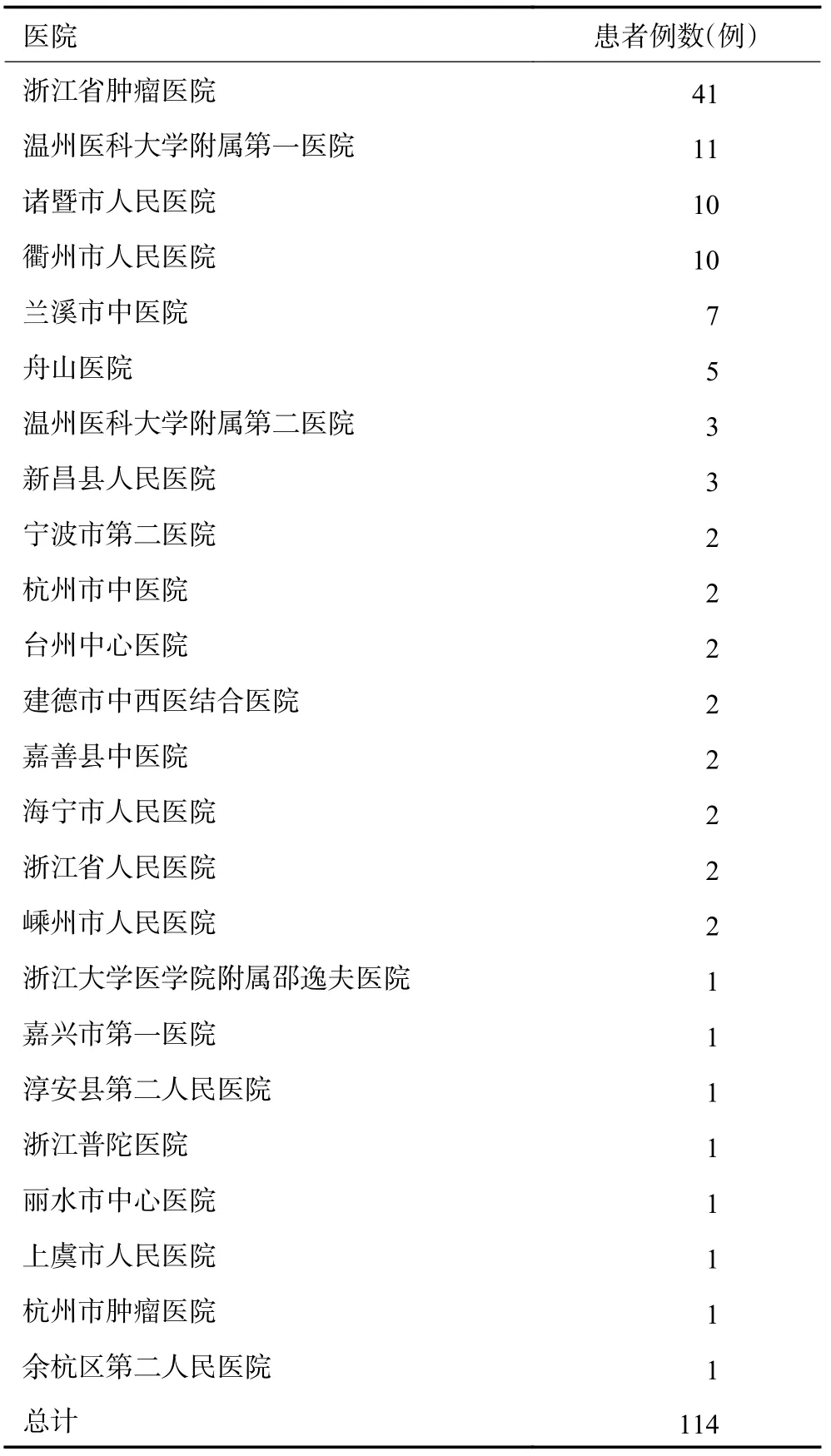
表1 拟定纳入114 例患者来源医院名称和病例数
1.2 方法
1.2.1 研究使用药物 盐酸羟考酮缓释片(商品名:奥施康定,规格10 mg/片),已经上市,BARD Pharmaceut 由萌蒂(中国)制药有限公司进口并分装。
盐酸吗啡片(商品名:盐酸吗啡片,规格10 mg/片),东北制药集团沈阳第一制药有限公司。
1.2.2 治疗流程 筛选中重度癌痛的阿片未耐受患者,给予起始剂量盐酸羟考酮缓释片10 mg q12h,同时按需给予口服吗啡即释片10 mg/次行补救镇痛;给药后12 h 进行评估,补救镇痛次数≥1 次的进入随机分组。
随机分组及滴定,研究对象经过筛选期后,采用随机数字表法进行随机分组。纳入的符合研究方案的患者按盐酸羟考酮缓释片剂量调整的时间不同随机分为试验组(12 h 滴定组,n=45)和对照组(24 h 滴定组,n=42),见图1。初始剂量:两组中重度癌痛患者(NRS≥4 分)初始剂量盐酸羟考酮缓释片10 mg;滴定:试验组,盐酸羟考酮缓释片背景给药,同时采用即释吗啡处理爆发痛,首次给药后12 h 时调整盐酸羟考酮缓释片剂量(前12 h 盐酸羟考酮固定量+前12 h 即释吗啡解救量),后续调整方案同前。对照组,盐酸羟考酮缓释片背景给药,即释吗啡处理爆发痛,首次给药后24 h 时调整盐酸羟考酮缓释片剂量, 即计算出前24 h 镇痛药物总量(前24 h 盐酸羟考酮缓释片固定量+前24 h 即释吗啡量),并将该剂量分成2 份,q12h 给药,后续调整方案同前。本研究已经得到浙江省肿瘤医院医学伦理委员会的审查和批准。所有受试者均自愿加入本临床试验并签署了书面知情同意书。
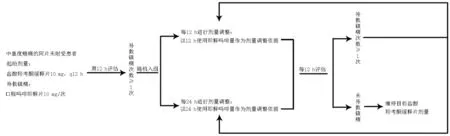
图1 滴定治疗流程
1.2.3 观察指标 主要研究终点:盐酸羟考酮缓释片给药后24 h 疼痛缓解率,包括完全缓解(complete response,CR)率和部分缓解(partial response,PR)率。
次要研究终点:盐酸羟考酮缓释片给药后48、72 h疼痛缓解率(CR+PR);在两组方案中24、48、72 h 补救镇痛用药情况(吗啡即释片使用次数和剂量);治疗满意度评估;患者生活质量评分。研究完成或终止时,要求患者及其研究者使用以下分级,对患者镇痛治疗的满意程度进行评估。
1.2.4 疗效评定标准 疼痛评估方法:采用数字分级法(NRS)对疼痛程度进行评估。0 分:无痛;1~3 分:轻度疼痛,有疼痛但可以忍受,生活正常,睡眠无干扰;4~6 分:中度疼痛,疼痛明显,不能忍受,要求服用镇痛药物,睡眠受干扰;7~10 分:重度疼痛,不能忍受,需用镇痛药物,睡眠受严重干扰,可伴有自主神经紊乱或被动体位。
主要研究终点为应用盐酸羟考酮缓释片后24 h疼痛(CR+PR)的患者比例。
关于疼痛缓解程度的判定:1)CR:服药12h 后,患者过去12 h 平均NRS 评分≤3 分;2)PR:服药12 h 后,患者过去12 h 平均NRS 评分从基线的重度疼痛(7~10 分)下降至中度疼痛(4~6 分);3)未缓解(NR):服药12 h 后,患者过去12 h时平均NRS 评分和基线相比仍在同等疼痛程度(例如:基线为中度疼痛,12 h后NRS 仍然为中度疼痛)。满意度评价:1=非常不满意, 2=不满意, 3=一般, 4=满意, 5=非常满意。生活质量评价:采用EORTC QLQ-C15-PAL 量表(中文版)对患者生存质量进行评价。
1.3 统计学分析
采用SPSS 24.0 软件包和R 3.6.0 软件对数据进行统计学分析。采用频数和构成比描述定性资料分布情况;采用Clopper-Pearson确切法计算缓解率的95%可信区间;采用χ2检验比较组间差异;采用平均数±标准差描述服从正态分布定量资料分布情况;采用独立样本t检验比较组间差异;采用中位数和四分位数描述非正态分布定量资料;采用Wilxcon符号秩和检验比较镇痛前后差异。所有检验均为双侧检验,以P<0.05 为差异具有统计学意义。
2 结果
2.1 研究结果概述
纳入研究的114 例患者中,经过筛选进入随机分组的患者87 例,其中,试验组45 例,对照组42 例;男性64 例,女性23 例,最小年龄31 岁,最大年龄91 岁,平均年龄(62.21±9.95)岁;前24h 最小NRS 为4,前24h 最大NRS 为7,前24h 平均NRS 为4.59±0.77,两组患者间的年龄、性别等一般资料比较差异无统计学意义(P>0.05,表2)。
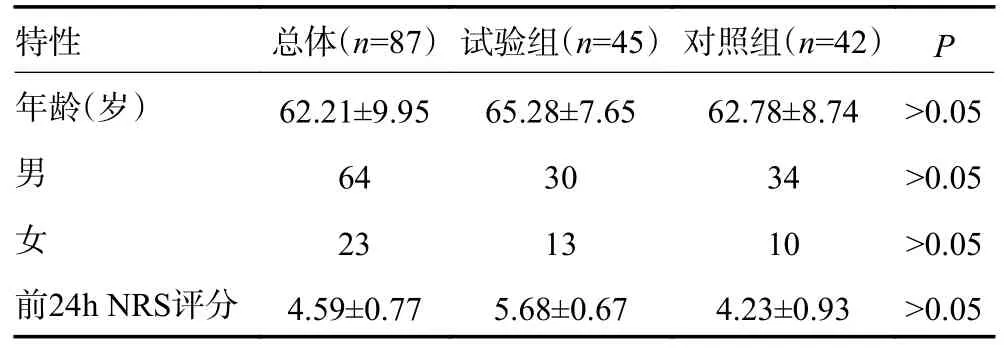
表2 114 例患者一般临床资料比较
2.2 疗效指标
2.2.1 疼痛缓解情况 表3 显示两组患者用药后24 、48 、72 h 的疼痛缓解比较。24 h 后两治疗组均显示较高的疼痛缓解率。在给药后24h,试验组疼痛缓解率在数值上优于对照组(95.45%vs. 83.37% ),但组间比较差异无统计学意义(P=0.851);给药后48 h、72 h两组间疼痛缓解率相当(100%vs. 100%;100%vs.94.87%);另外,试验组在36 h 后所有患者均达到疼痛完全缓解(缓解率 100%)并维持。
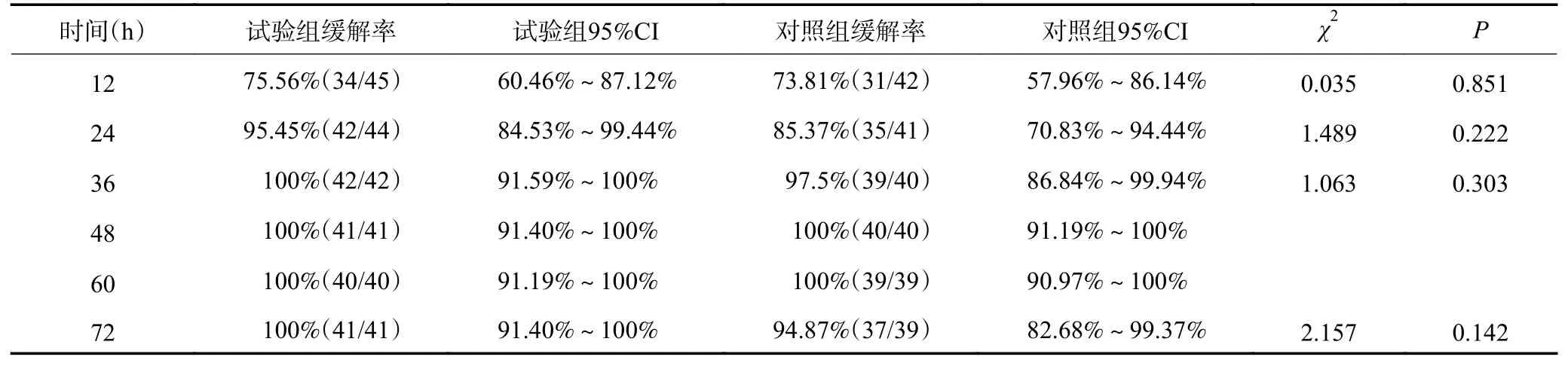
表3 两组间72 h 内疼痛缓解比较
2.2.2 补救镇痛次数和剂量 研究显示相对于对照组,试验组在24 、48 h 及72 h 补救镇痛次数均显著减少(P<0.05);同样,试验组补救镇痛剂量(即释吗啡用量)相对对照组显著减少,且差异具有统计学意义(P<0.05,表4,5)。
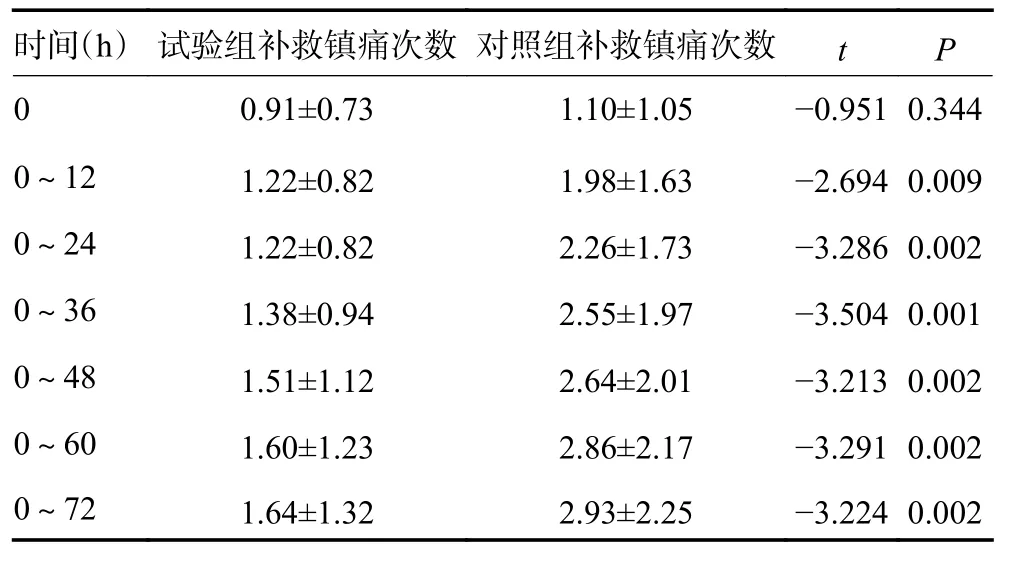
表4 两组间72 h 内补救镇痛次数比较
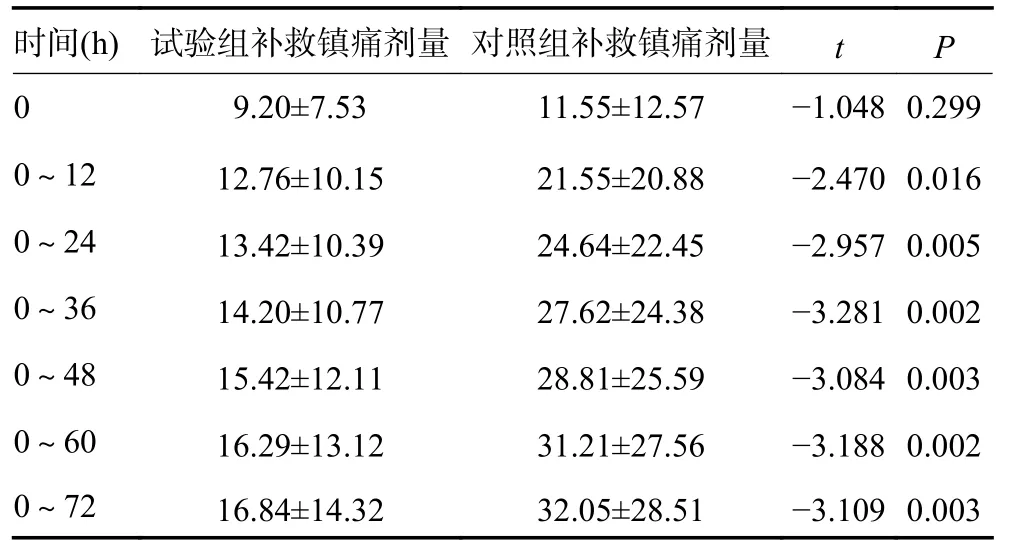
表5 两组间72 h 内补救镇痛剂量比较
2.3 安全性指标
纳入可评价的患者87 例,两组患者主要不良反应类型为便秘、恶心、呕吐、头晕等;不良反应大多数为轻中度(试验组 95.45%;对照组 98.31%),组间比较差异无统计学意义(P=0.354,表6);不良反应对于镇痛用药的后续使用影响小,试验组无患者因不良反应而出现用药中断,对照组3 例患者因不良反应而中断用药,试验组有2 例因发生不良反应后经评估进行减剂量调整,虽未中断治疗但不适用于本研究后续的剂量滴定调整方案分析,组间比较差异无统计学意义(P=0.087)(表7)。
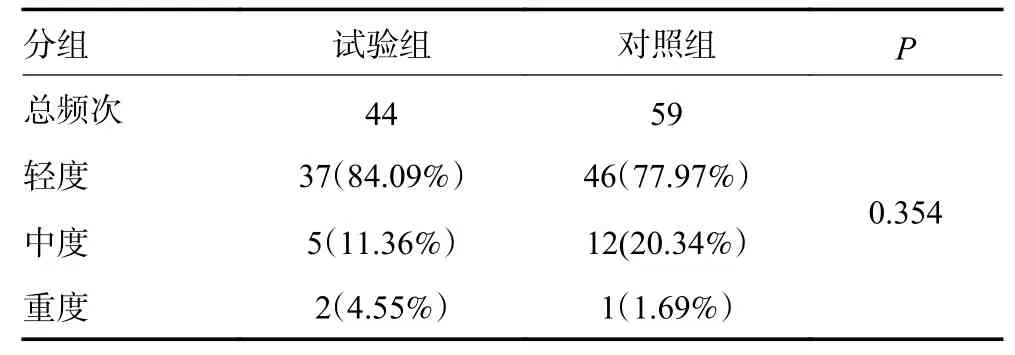
表6 两组间不良反应严重程度
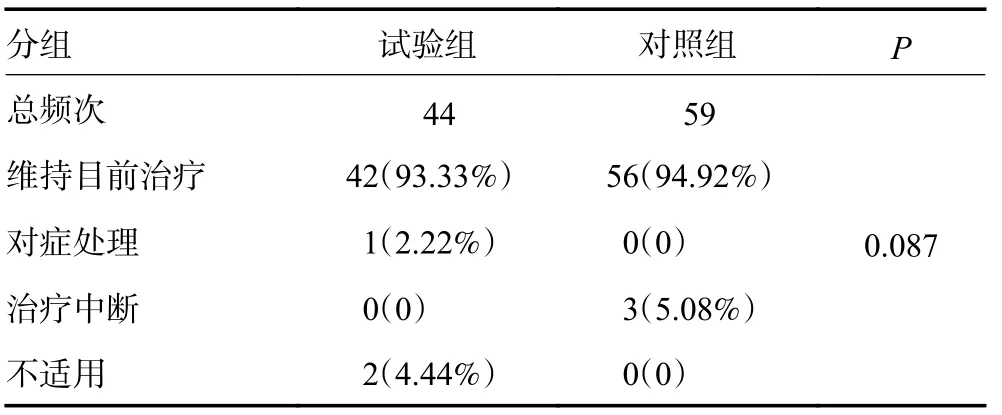
表7 对药物的措施(两组间不良反应对镇痛用药的影响)
2.4 满意度调查
受试者评价中,纳入可评估的患者81 例。试验组满意及非常满意比例为90.48%,对照组为84.61%,两组间满意度比较差异无统计学意义(P=0.134,表8);研究者评价中,可纳入可评估的患者78 例。试验组满意及非常满意比例为90.24%,对照组为86.48%,两组间满意度比较差异无统计学意义(P=0.298,表9)。
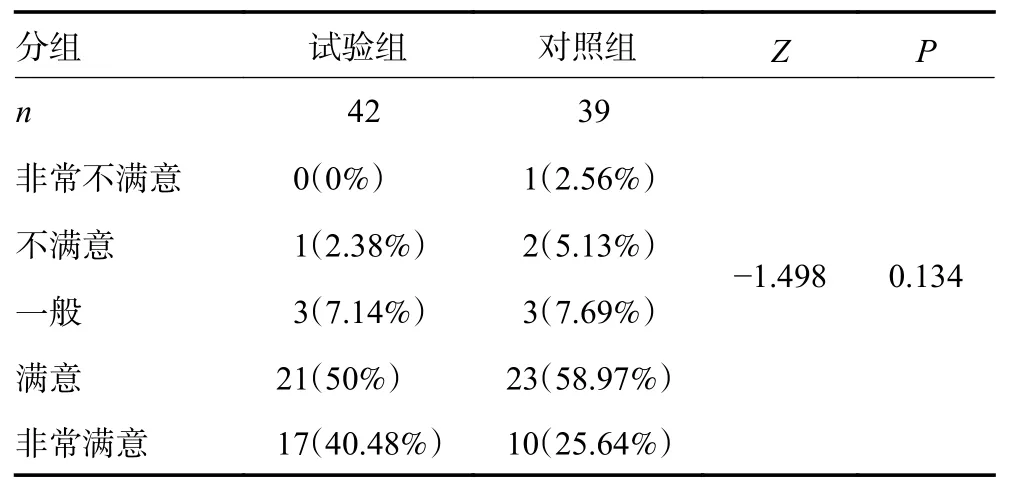
表8 两组间满意度比较-受试者评价
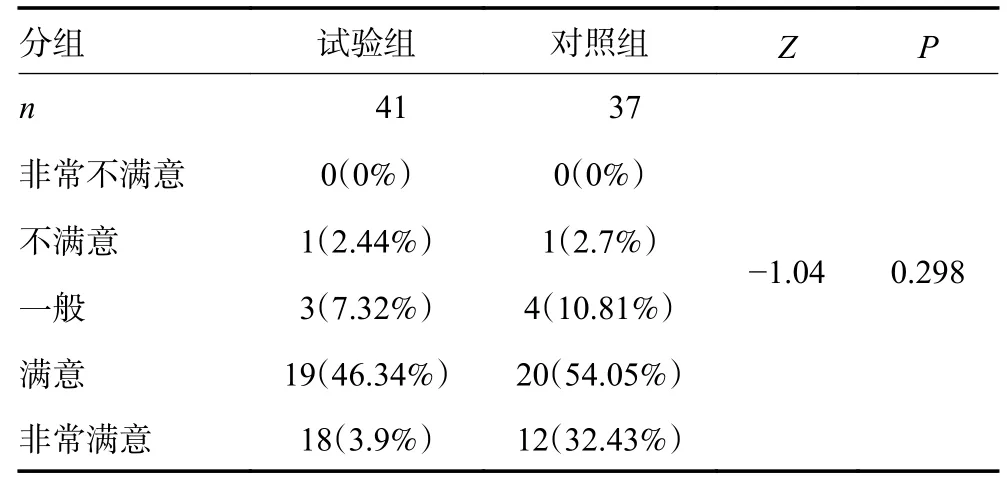
表9 两组间满意度比较-研究者评价
2.5 生存质量
结果显示,在基线,试验组与对照组在各维度及整体生活质量比较差异均无统计学意义(P>0.05);8天后的组间比较也得到类似的结果(P>0.05)(表10)。
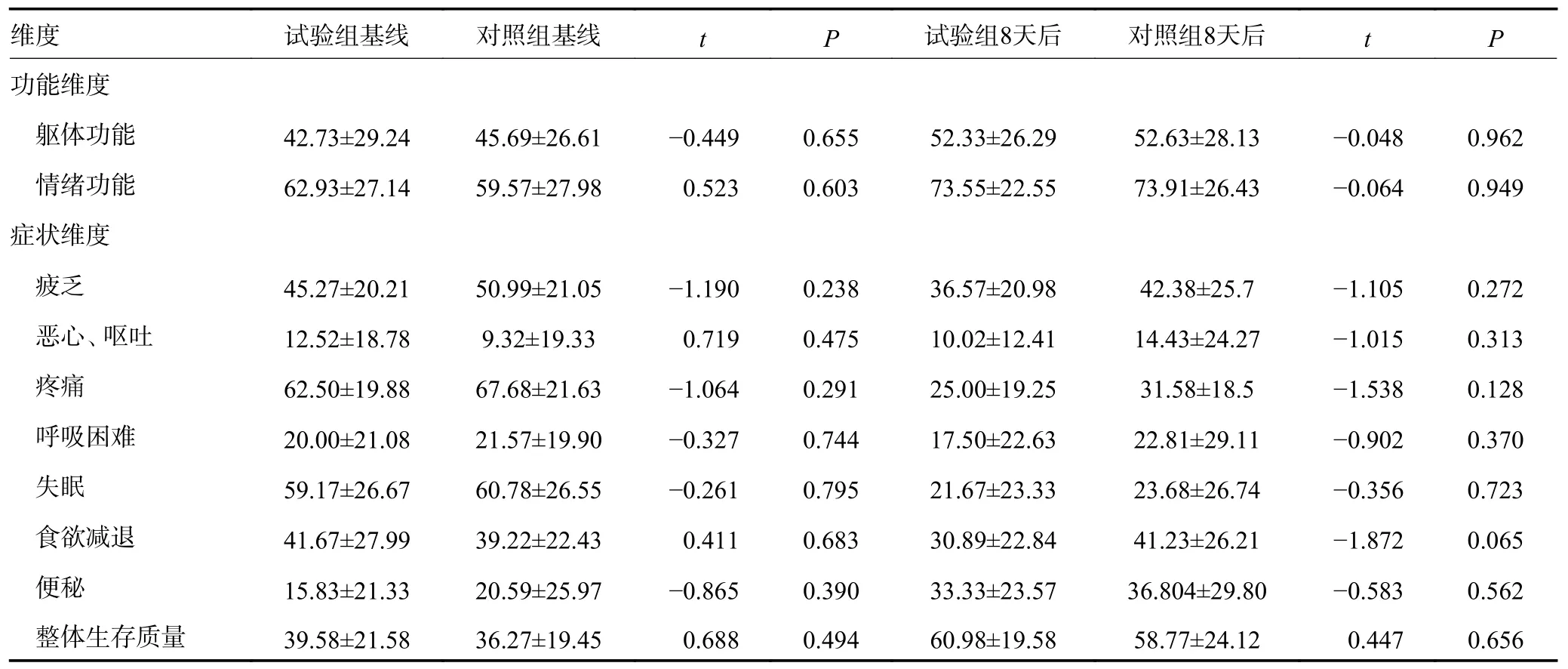
表10 两组间生活质量比较
3 讨论
癌痛应采取规范化、个体化治疗的原则。根据患者的病情和身体状况,采用各种治疗方法,及早、充分、持续、有效地消除疼痛,预防和控制药物不良反应,减轻患者可能产生的心理负担和障碍,达到优化患者生存质量的目的[8]。
早期镇痛可以增加患者的疼痛阈值,从而减少患者的疼痛感知,获得更好的疼痛缓解[9-10]。在及早镇痛的合理实施中,癌痛治疗第1 天尤为关键。疗效迅速稳定的滴定可以减轻患者的疼痛症状、增加患者对后续治疗的信心、增加患者对医务人员的信任度、增加患者对抗肿瘤治疗的依从性、缩短住院时间[11-12]。
盐酸羟考酮缓释片给药1 h 内快速镇痛,持续镇痛长达12 h,血药浓度稳定,与传统即释吗啡相比效果相近、安全可靠,但是在持续平稳镇痛等多方面具有优势,可作为首选镇痛药物。对于盐酸羟考酮缓释片为背景的12 h 滴定的可行性,既往有国内的学者已进行了初步的探索。易基群等[13]的研究中,纳入48例中重度癌痛患者,根据疼痛控制情况,在12 h、24 h进行盐酸羟考酮缓释片剂量调整。结果显示,经过中间12 h 的评估和剂量调整,95.8%患者在24h 完成滴定,疼痛评分降到3 分以下。1 、12 、24 h 疼痛明显缓解率分别为66.7%、77.1% 和95.8%。曾娟紫等[14]的研究中,纳入42 例重度癌痛患者,根据患者疼痛控制情况和爆发痛情况于12 h 和24 h 调整盐酸羟考酮缓释片的剂量,24 h 疼痛缓解率达到73.8%,不良反应以消化道症状为主。以上两项研究结果显示盐酸羟考酮缓释片在中重度癌痛患者中的滴定具有快速、有效的优势。另外有研究[7]回顾性分析了盐酸羟考酮缓释片12 h 调整剂量治疗中重度癌痛的疗效及安全性。结果显示,相对于24 h 调整剂量治疗组,12 h 调整剂量组可明显提高24h 和48 h 疼痛缓解率,并且明显改善患者生存质量,且安全性良好。Liang 等[15]的一项研究评估了12 h 阿片剂量调整方案的安全性和有效性,并进一步比较了方案中缓释羟考酮和即释吗啡的安全性和疗效。其研究发现12 h 剂量调整快速镇痛滴定具有良好的早期镇痛效果,伴有轻度不良反应,而且基于羟考酮缓释片的快速滴定方法可以更好地降低NRS 评分,减少爆发痛发作,增强患者对后续治疗的信心,提高生活质量。
本研究为多中心、随机、对照试验,在既往研究结果的基础上,首次前瞻性探索盐酸羟考酮缓释片为背景12 h 调整方案的有效性及安全性。结果显示,在中重度癌痛患者应用盐酸羟考酮缓释片为背景的滴定方案中,补救镇痛方面,相对于24 h 滴定方案,12 h 滴定方案的补救镇痛次数显著减少(P<0.001),并延续至72 h;同时,补救镇痛剂量的组间比较也呈现类似的结果(P<0.01),且维持较高的镇痛缓解率和镇痛满意度,安全性良好。在回顾性研究中,12 h 滴定组相对于24 h滴定组在第1 天处理爆发痛的即释吗啡总剂量显著性减少(P=0.046)相符。该优势可体现为医护人员及患者满意度的提高。较少的补救镇痛对于医患均有更好的治疗体验,可减少医护人员的工作负担,保障规范化的癌痛评估、随访、干预过程。
既往研究报道羟考酮缓释片背景用药辅以吗啡即释片背景滴定,疼痛控制率为73.8%~95.8%[13-14]。本研究中,两组患者在治疗24 h 后,均保持较高的疼痛缓解率并维持。相对于24 h 滴定,12 h 调整在24 h的疼痛缓解率体现了数值上的优势,但差异无统计学意义,这与既往类似研究存在一定的差异。原因可能包括以下两个方面。首先,本研究纳入的患者样本量偏小,未能体现出具有统计学差异的优势;其次对中度和重度疼痛的患者均10 mg 盐酸羟考酮缓释片起始给药,未能进行区分给药。平均NRS 评分4.59±0.77 说明大部分患者为中度疼痛,10 mg 盐酸羟考酮缓释片起始给药可以有效缓解疼痛。
阿片类药物的不良反应很常见,主要包括便秘、恶心、呕吐、嗜睡、瘙痒、头晕、尿潴留、谵妄、认知障碍、呼吸抑制等[8]。因此,需要重视阿片类药物的不良反应,更需要积极预防和处理阿片类药物的不良反应,使疗效与不良反应平衡,患者获益最大化。本研究中,两组患者主要不良反应类型为便秘、恶心、呕吐、头晕,大多数为轻中度,且对于镇痛药物应用影响小,试验组无患者因不良反应中断用药,对照组有3 例患者因不良反应中断用药。不良反应的总频次方面,对照组多于试验组。可能的原因是由于对照组治疗过程中更多的补救镇痛剂量,造成即释吗啡在体内血药浓度增加,从而出现更多的阿片类药物不良反应。
本研究局限性:1)样本量较小 在这种情况下,有效的干预可能产生阴性结果。期待更大样本量的多中心随机对照研究。 2)较短的随访时间,72 h。3)随机入组前的筛选:补救镇痛1 次以上者进入随机分组。此种筛选模式可能会漏掉那些出现爆发痛而未报告或者本身存在持续性中重度以上疼痛而未报告的患者。
