ERCP联合EST治疗的胆管梗阻患者术后发生急性胰腺炎危险因素分析
2021-08-25宛星宇毛屏赵晟南柳青峰
宛星宇,毛屏,赵晟南,柳青峰
中国医科大学人民医院肝胆外科,沈阳110000
近年来,经内镜逆行胰胆管造影术(ERCP)联合乳头括约肌切开术(EST)已经成为治疗胆总管结石及胆道相关疾病的重要手段,相比较于传统开放手术,此种术式对患者的创伤更小,恢复及住院时间更短。研究[1]显示,EST 作为当前最常应用的取石手段之一,对于数量较少、体积较小的肝外胆管结石患者可以缩短手术时间、提高一次取石成功率。但EST 造成的热灼伤极易引起Oddi 括约肌功能障碍,一旦损伤胰管括约肌,导致胰液排出障碍、胰液反流甚至胰液外渗,将大大增加术后胰腺炎的患病风险。研究[2]显示,ERCP+EST 术后并发症发生率高达10%~12%,包括十二指肠乳头出血、十二指肠穿孔、急性胰腺炎及反流性胆管炎等,其中术后急性胰腺炎(PEP)是最常见的并发症,其发生率在1.6%~15.0%[3]。本研究分析了接受ERCP+EST治疗的胆管梗阻患者术后发生PEP的危险因素,现报告如下。
1 资料与方法
1.1 临床资料 选取2019年1月1日—2021年1月1日于中国医科大学人民医院接受ERCP + EST治疗的胆管梗阻患者392 例,男202 例、女190 例,年龄23~93(66.9±16.8)岁。纳入标准:①患有胆总管结石、急性胆管炎且具备取石手术指征;②存在原因不明的梗阻性黄疸;③疑似患有胆道及壶腹周围占位性病变;④经医院伦理委员会审核批准,并获得患者及家属知情同意。排除标准:①妊娠期女性;②患有严重心肺疾病、血液疾病及过敏史;③术前诊断为急性胰腺炎;④存在ERCP禁忌症。
1.2 ERCP+EST 手术方法 患者入院后完善血常规、肝功能、血清淀粉酶、脂肪酶及磁共振胰胆管造影(MRCP)等术前检查,术前禁食12 h、禁饮4 h,术前应用质子泵抑制剂抑制胃酸、联合抗生素抗感染及营养支持治疗。术前充分进行麻醉评估,患者均采取全身麻醉。手术时患者侧卧位,经口将十二指肠镜插入至十二指肠降部,观察十二指肠乳头解剖位置;选用乳头切开刀带斑马导丝插管后,X 线透视下可见导丝已成功进入胆管后,回抽出胆汁,注入造影剂并观察胆管显影情况;于十二指肠乳头11点方向行括约肌小切开,根据结石体积、数量及术中情况采取乳头球囊扩张术(EPBD),用取石网篮取出结石,再用取石球囊多次拉取清理胆道,常规留置胆道塑料支架,根据术中情况留置胰管支架。
1.3 PEP 诊断方法及分组 根据ERCP+EST 术后是否发生PEP,将392 例胆管梗阻患者分为胰腺炎组和对照组。术后PEP 诊断标准:①术后持续性上腹部疼痛;②术后24 h 血清淀粉酶或脂肪酶大于正常值上限3 倍以上;③影像学具备PEP 特征性表现。具备以上2 项即可诊断为PEP。胰腺炎组患者32例,术后血清淀粉酶、脂肪酶分别为695.00(492.00,1 436.50)、2 747.50(1 781.25,3 950.75)U/L,对照组患者360 例,术后血清淀粉酶、脂肪酶分别为60.00(38.00,103.50)、156.00(68.00,367.00)U/L,两组相比,P均<0.05。
1.4 两组一般资料、实验室检查指标、ERCP+EST手术相关指标资料收集 收集两组患者的性别、年龄、BMI、高血压病史、糖尿病史、胆囊炎病史、胆管及壶腹肿瘤病史等一般资料,术前及术后白细胞计数(WBC)、丙氨酸转氨酶(ALT)、γ-谷氨酰转肽酶(γ-GT)、总胆红素(TBil)等实验室检查指标,胆道结石性状、是否同时行胆囊切除、联合EPBD 及球囊扩张时间、胰管支架置入、术后静脉使用帕瑞昔布钠、导丝进入胰管≥3 次等ERCP + EST 手术相关指标。
1.5 统计学方法 采用SPSS22.0 统计软件。计量资料呈非正态分布时以中位数[M(P25,P75)]表示,比较用Mann-WhitneyU检验;计数资料比较采用χ2检验。采用Logistic 回归分析法分析接受ERCP+EST治疗的胆管梗阻患者术后发生PEP 的危险因素。P<0.05表示差异具有统计学意义。
2 结果
2.1 两组一般资料、实验室检查指标、ERCP+EST手术相关指标资料比较 胰腺炎组32 例患者中,男8 例、女24 例,年龄≥60 岁者20 例、<60 岁者12 例,BMI≥24者16例、BMI<24者16例,有高血压病史者8例、糖尿病史者9 例、胆囊炎病史者14 例、胆管及壶腹肿瘤病史者4 例;术前WBC 6.58(4.38,8.17)×109/L,术前ALT 28.75(18.88,102.13)U/L,术前γ-GT 102.50(38.75,400.25)U/L,术前TBil 13.90(10.25,20.00)µmol/L,术 后WBC 11.65(7.32,15.14)×109/L,术后ALT 45.95(28.25,88.50)U/L,术后γ-GT 170.50(50.75,371.00)U/L,术后TBil 16.55(9.63,26.75)µmol/L;胆道泥沙样结石者12例、颗粒样结石者20例,同时行胆囊切除者10例,未联合EPBD 者18例、联合EPBD 球囊扩张时间<2 min者7 例、联合EPBD 球囊扩张时间≥2 min 者7 例,胰管支架植入者4 例,术后静脉使用帕瑞昔布钠者8例,导丝进入胰管≥3次者12例。
对照组360 例患者中,男194 例、女166 例,年龄≥60 岁者276 例、<60 岁者84 例,BMI≥24 者174 例、BMI<24者186例,有高血压病史者134例、糖尿病史者74例、胆囊炎病史者184例、胆管及壶腹肿瘤病史者26 例;术前WBC 6.97(5.30,8.94)×109/L,术前ALT 37.00(22.10,133.75)U/L,术前γ-GT 127.00(31.25,394.00)U/L,术 前TBil 20.90(13.08,47.38)µmol/L,术后WBC 8.58(6.20,11.27)×109/L,术后ALT 47.50(28.00,103.68)U/L,术后γ-GT 150.50(40.50,366.25)U/L,术 后 TBil 19.65(12.13,33.60)µmol/L;胆道泥沙样结石者162 例、颗粒样结石者198 例,同时行胆囊切除者132 例,未联合EPBD 者213 例、联合EPBD 球囊扩张时间<2 min 者116 例、联合EPBD 球囊扩张时间≥2 min 者31 例,胰管支架植入者46 例,术后静脉使用帕瑞昔布钠者96例,导丝进入胰管≥3次者39例。
其中,胰腺炎组女性比例、术后WBC、术前TBil、联合EPBD 球囊扩张时间≥2 min、导丝进入胰管≥3次等资料与对照组相比,P均<0.05。
2.2 接受ERCP+EST 治疗的胆管梗阻患者术后发生PEP 的危险因素 建立Logistic 回归模型,因变量为ERCP + EST 术后是否发生PEP,自变量为性别(赋值:男=0,女=1)、术后WBC(连续性变量)、术前TBil(连续性变量)、联合EPBD 及球囊扩张时间(赋值:无=0,<2 min=1,≥2 min=2)、导丝进入胰管≥3 次(赋值:否=0,是=1),Logistic 回归分析结果显示,女性、术后WBC 升高、导丝进入胰管≥3 次是接受ER⁃CP+EST治疗的胆管梗阻患者术后发生PEP的危险因素,见表1。
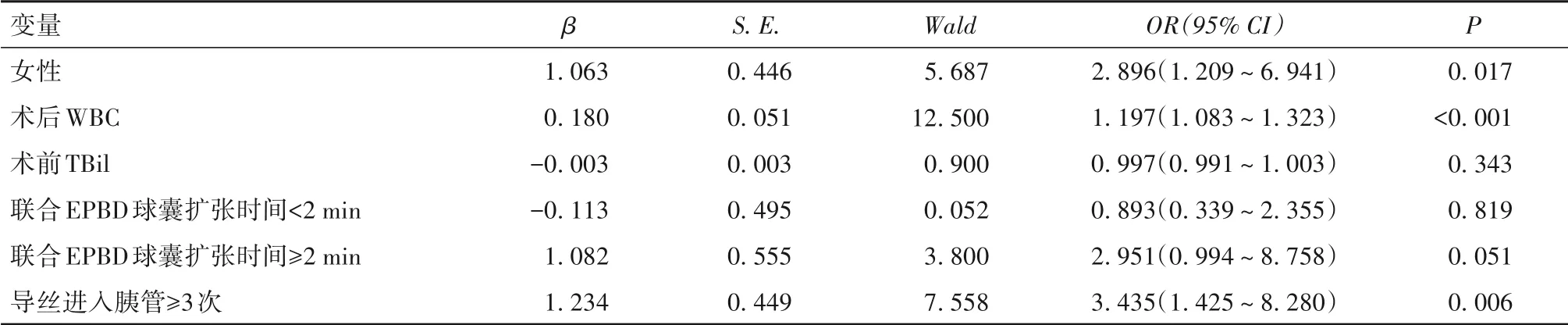
表1 接受ERCP+EST治疗的胆管梗阻患者术后发生PEP的危险因素
3 讨论
研究[4]显示,ERCP+EST 术后发生PEP 的危险因素包括患者因素和手术因素,患者因素包括Oddi括约肌功能不全、女性、年轻、PEP病史等,手术因素包括插管困难、乳头括约肌切开、导丝进入胰管及造影剂注射进入胰管等。本研究结果显示,女性、术前低TBil 水平和术后WBC 升高、联合EPBD 球囊扩张时间≥2 min、导丝进入胰管≥3 次与PEP 密切相关(P均<0.05),而女性、术后WBC升高、导丝进入胰管≥3次是PEP的独立危险因素(P均<0.05)。
多数研究[5]证实,女性是ERCP+EST 术后发生PEP 的确切危险因素,其具体发病机制尚不完全清楚。但有研究[6]指出,女性是其他危险因素的前提条件,例如女性患者更可能存在Oddi 括约肌功能不全,这使得女性患者术后更容易出现胰胆管流出道梗阻、胰液引流不畅及胰液反流,在这种情况下,行EST 会进一步增加胰管括约肌损伤的机率;同时,Oddi 括约肌功能不全也增加了插管难度和导丝进入胰管的可能[7],这也提高了女性患者术后发生PEP的风险。
EST 作为当前较为常见的取石术式,对直径<10 mm 且数量较少的胆总管结石效果较好,但对于多发或直径>10 mm的结石治疗效果欠佳,且一旦术中手术医师操作不当,极易引起乳头括约肌永久性功能损伤。对于复杂、多发结石或插管困难的患者,EST 联合EPBD 可以显著提升胆总管结石的一次清除率,降低机械碎石使用率。此外,联合EPBD 可缩小十二指肠乳头的切口范围,减少胰管括约肌损伤的可能性,并尽可能保留了乳头括约肌的功能。本研究结果显示,EST联合EPBD的患者PEP的发病率与单行EST 相比无统计学差异。然而,当球囊扩张时间过长时会显著增加PEP 的患病风险,其主要原因是长时间的球囊扩张,持续压迫胰管括约肌并增加了胆汁反流进胰管的可能。
研究[8]发现,ERCP 手术过程中导丝进入胰管是一种直接的机械损伤。当反复插管或导丝多次进入胰管后,胰管黏膜上皮组织破损、水肿,引起胰管梗阻、胰管内压力增高、胰液反流等,严重者甚至会出现胰酶对胰腺的自身消化[9]。
目前,非甾体抗炎药物已被证实对预防PEP 有效。然而,本研究结果发现,术后经静脉使用帕瑞昔布钠的患者PEP的发生率并没有明显降低。与此同时,LEVENICK 等[10-11]的实验结果表明,经直肠给予小剂量的双氯芬酸或吲哚美辛不能有效预防PEP。然而,非甾体类抗炎药对于PEP 的预防作用还取决于用药剂量、用药时期和不同风险人群[12-13]。术后即刻经直肠给予中等剂量的非甾体类抗炎药可以有效降低高危人群发生PEP 的概率,而对于低风险人群却无明显保护作用[14-15]。本研究虽然是对乳头括约肌切开患者进行分析,但患者皆为术后静脉途径给药,而关于给药途径对PEP的预防目前研究较少,且经静脉应用非甾体类抗炎药能否使药物在术后即刻达到最佳效果仍需进一步实验验证[16-17]。
值得注意的是,本研究结果发现,发生PEP患者的术后WBC 水平显著高于未发生PEP 的患者。Lo⁃gistic 回归分析结果也表明,术后WBC 水平升高是PEP 的独立危险因素。当胰腺受损时,损伤的胰腺组织和周围炎症细胞会释放细胞因子,细胞因子和趋化因子的大量释放会进一步增加血液中的炎症细胞和炎症因子,从而再次加重胰腺损伤,严重者可发展为全身炎症反应综合征及多器官功能损害,甚至危及生命[18]。炎症细胞浸润和炎症因子的释放决定了PEP 的严重程度。IL-6是急性胰腺炎中最具代表的炎症因子,尤其在急性出血坏死性胰腺炎中,IL-6的血清水平要明显升高,且显著高于水肿型胰腺炎[19]。赖坤等[20]的实验发现,通过调控Gli1 信号来降低IL-6的表达可以有效减少急性胰腺炎过程中的组织损伤。因此,减少术后炎症细胞的浸润和炎症因子的释放对PEP 的预防、治疗和预后具有至关重要的作用。
综上所述,接受ERCP+EST 治疗的胆管梗阻患者术后可能发生PEP,女性、术后WBC 升高、导丝进入胰管≥3 次是其危险因素。在临床治疗过程中,对于女性患者,应充分做好术前准备及预防措施,缩短手术时间,减少插管次数。术中尽量避免导丝进入胰管,对于不可避免需放置胰管支架的患者,导丝不得进入胰管超过3 次。乳头括约肌切开时,应选择指定区域进行切开,范围局限于乳头凸起上缘内以减少出血及感染的风险,联合EPBD 时球囊扩张时间应控制在2 min 以内。术后应合理控制炎症细胞浸润并减少炎症因子的释放,尤其当患者术后WBC升高时,应更加警惕PEP的发生。
