婴儿纤维性错构瘤超声组织成像特征:与病理相对照
2021-02-24陈喜萍杨春江
陈喜萍,杨春江*,唐 毅,朱 进,范 晓,肖 欢
[1.重庆医科大学附属儿童医院超声科,儿童发育疾病研究教育部重点实验室,国家儿童健康与疾病临床研究中心(重庆),儿童发育重大疾病国家国际科技合作基地,儿科学重庆市重点实验室,重庆 400014;2.重庆医科大学附属儿童医院病理科,3.放射科,重庆 400014]
婴儿纤维性错构瘤(fibrous hamartoma of infancy, FHI)是好发于2岁以内婴幼儿的良性纤维组织增生性疾病,常发生于真皮或皮下软组织,占儿童软组织肿瘤的0.5%~0.6%[1];其组织结构复杂多样,影像学所见常缺乏特异性[2],易误诊。本研究回顾性分析FHI病灶,借助超声定量分析仪测量来源于相同仪器声像图中瘤体低回声成分与瘤旁正常脂肪组织的回声强度(echo intensity, EI),并比较其差异,探讨瘤体内低回声与组织病理间的联系。
1 资料与方法
1.1 一般资料 回顾性分析2013年11月—2019年11月重庆医科大学附属儿童医院经术后病理证实的28例FHI患儿,男16例,女12例,年龄1~65个月,中位年龄13.5个月;均以局部无痛性包块就诊,27例单发、1例多发;病灶位于胸壁5例,上肢和腰背部各6例,腋下和会阴部各3例,面部、骶尾部、项部、下腹壁、小腿各1例;肿块直径1~10 cm,中位直径3 cm。
1.2 仪器与方法 采用GE Logiq E9、Vivid E9超声仪,ML6~15线阵探头;Logiq S6,Hitach Aloka、Samsung RS80A以及Philips EPIQ5、iU22等彩色多普勒超声诊断仪,高频线阵探头,探头频率6~15 MHz,预设条件smallparts,频率15 MHz,扫描深度4.0 cm,扫描增益分别为12和32 dB,时间补偿增益(TGC)均设置为直线,保持前场后场一致。由1名工作15年以上的医师进行观察并记录病灶大小、形态、边界、内部回声、与周围组织的关系及病灶内血流信号等,存储瘤体及瘤周二维声像图及CDFI图像。组织声学定量分析:由同一观察者采用“DFY-Ⅱ型”超声图像定量分析仪[3]于人眼辨识的瘤体低回声区及瘤周正常脂肪组织手动取样,分别设置10个ROI,测量各ROI的EI(图1)。部分病例接受CT、MR扫描。

图1 患儿男,2个月,FHI 以DFY-Ⅱ型超声图像定量分析仪测量病灶内低回声区EI,椭圆形虚线为ROI取样框
1.3 组织病理学检查 对所有手术切除标本进行固定、包埋及HE染色。采用EnVison两步法及DAB显色行免疫组织化学检查。
1.4 统计学分析 采用SPSS 25.0统计分析软件。正态分布的计量资料以±s表示,采用区组设计,将扫查病例最多的2台仪器所采集声像图分为2组,定量分析瘤体低回声区及瘤周正常脂肪组织的EI;采用t检验进行组间(2台仪器间正常脂肪组织)比较,以配对t检验比较同一仪器瘤体与瘤周正常脂肪组织EI。P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 本组28例FHI患儿中,25例发病年龄≤1岁(25/28,89.29%);共30个FHI病灶,27例单发肿块触诊表面光滑,1例触诊有结节感者手术证实存在3个相邻病灶;2例局部皮肤发青,3例表面有少许毛发覆盖。
2.2 超声表现 3例确诊为错构瘤,10例误诊为纤维脂肪瘤,余15例超声仅提示实质性病变。30个病灶中,27个形态不规则、边界不清者(27/30,90.00%),以不均质高回声为主,间杂条状或小片状低回声,少数混杂小片状无回声,其中20个病灶血供稀少(20/30,66.67%);7例病变局部见较粗的纡曲血管近乎垂直指向皮肤层,13个病灶呈“栅栏状”(低回声与高回声相间并垂直于皮肤分布),6个病灶呈“蛇形”,见图2~5。7例病变累及皮肤及皮下软组织,未见明确累及肌层者。
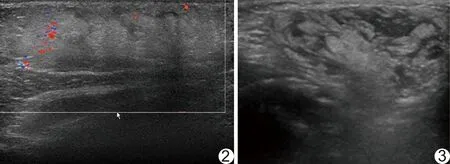
图2 女性患儿,7月龄,左胸壁FHI 超声示高、低回声相间并垂直于皮肤形成“栅栏状” 图3 患儿男,7月龄,右腋下FHI 超声示低回声纡曲嵌入高回声,呈“蛇形”

图4 患儿男,1岁,右小腿FHI A.CDFI示病灶内粗大血管; B.测得低速动脉频谱; C.病理图(HE,×40)示纤维组织(黑短箭)、原始间叶细胞(白长箭)、大量脂肪组织增生(白短箭)及扩张小血管(黑长箭)
Logic E9图像中瘤周正常脂肪EI显著高于Vivid E9图像(t=3.82,P<0.05);2台仪器图像中瘤体低回声与瘤周脂肪组织EI差异均无统计学意义(P均>0.05),见表1。
表1 源自两台仪器超声图像的病灶EI比较(±s)

表1 源自两台仪器超声图像的病灶EI比较(±s)
仪器病灶数目(个)部位EI(dB)t值P值GELogicE99瘤体低回声区64.88±20.790.340.74瘤周脂肪回声区63.85±22.34GEVividE99瘤体低回声区38.54±11.751.420.19瘤周脂肪回声区35.18±11.82
2.3 其他影像学表现 11例接受CT和/或MR检查,包括CT平扫及增强扫描5例、MR平扫及增强扫描5例以及1例同时先后接受CT、MR平扫及增强扫描,提示纤维脂肪瘤2例,纤维瘤2例,脉管畸形3例,脂肪瘤1例,3例性质待定。
2.4 组织病理学 所有病例均经术后病理确诊为FHI。光镜下见致密纤维成分交错排列,成熟脂肪组织及原始间叶细胞呈“巢状”或“器官样”排列。7例接受免疫组织化学检查,CD34(+)、Vim(+),S-100(+),SMA(+),CD99(+),Ki-67(阳性细胞<2),Bcl-2(+)等。
3 讨论
WHO定义FHI为发生于儿童的界限欠清的良性表浅软组织肿瘤,组织学上由3种成分混合构成特征性的器官样结构,即交叉梁状排列的致密纤维胶原组织、含不成熟小圆形原始间叶细胞的疏松组织和成熟脂肪组织[4]。FHI虽为良性病变,但术后部分可复发,临床多主张及早完整手术切除病灶,故早期诊断极为关键。FHI影像学表现缺乏特异性,定性诊断价值尚未被认可。超声常仅描述为边界不清、不均匀高回声团块,多混杂低回声,多数血供稀少,部分肿块内可见扩张的血管等[5-6]。此种高回声嵌入纡曲走行的低回声被称为“蛇形”图像,为FHI的特征性表现之一[5]。目前确诊FHI主要依赖组织病理学检查。本组FHI病灶超声表现为不均质高回声混杂低回声,其中6例可见“蛇形”图像,但其与病理组织结构的对应关系尚不明确。ARIONI等[7]认为FHI病灶中的高回声是其内部结构交叉排列形成较多界面所致;LEE等[5]则推测高回声可能源自肿块内的脂肪成分,低回声源自相间其中的纤维成分。正确识别瘤体内组织成分是超声诊断的关键,识别脂肪组织有助于缩小鉴别诊断范围[8]。
本研究采用DFY定量仪比较瘤体低回声区及瘤周正常脂肪组织的EI,发现采用不同仪器采集图像的EI差异显著;对比分析来自两台仪器的图像,瘤体低回声区与瘤周脂肪组织EI值差异均无统计学意义。结合病理及声学理论,考虑瘤体低回声可能为脂肪组织,高回声区为致密的纤维组织(胶原纤维为主);瘤内低回声EI均略高于瘤周脂肪组织,不除外低回声中混杂原始间叶细胞,其回声强度与脂肪接近,与之混杂而不易识辨,有待进一步探讨。
本研究发现超声识别脂肪优于CT,5例经CT检查,仅1例似可见点状脂肪影,而超声显示该例病灶内低回声脂肪成分占比较高,术后病理证实病灶内含大量脂肪;另外2例出现极低回声,推测可能为间充质细胞包埋于黏液样基质中,形成近似无回声的极低回声区,与MR间充质成分中混杂液体后断层图像重建信号强度增高相对应[1]。本组43.33%(13/30)病灶显示为高回声间以低回声呈条状或“栅栏状”并列走行,6例MRI中3例出现栅栏状表现(图5),与CT宽窗显示“淡云征”、其间见栅栏状结构及轻微强化类似。文献[5]报道FHI呈背肤性向皮下生长,甚至可伸入毗邻骨骼肌间隙,且大多数FHI病灶少血供。本组中66.67%(20/30)病灶中仅见星点状血流信号,7例超声显示粗大血管穿行于病灶中,指向或垂直于皮肤。既往研究[9-10]发现FHI病灶局部皮下组织可见1支或多支增粗、纡曲的血管,可能因纤维、原始间叶组织及血管背肤性生长,形成扩张的血管及高、低回声垂直于皮肤分布与走行这种特异的组织结构形态,或与皮肤韧带相关。NASH等[11]认为浅表脂肪中均有连接真皮与肌肉深筋膜的皮肤韧带(纤维隔膜)分布。FHI非呈恶性生长,病变局限于纤维隔膜内,与皮肤表面垂直生长,可能是形成栅栏状结构的病理基础。这些低回声除包含原始间叶组织及脂肪组织外,可能还包括扩张血管。因此,多条垂直于皮肤的高、低回声相间的形态可作为超声诊断FHI的要点之一;垂直于皮肤走行的粗大血管则可作为更有力的依据。

图5 女性患儿,6月龄,左胸壁FHI A.超声示高、低回声条形相间,形似“栅栏状”,CDFI显示血供稀少; B.MR T1WI示高信号条状脂肪与等低信号软组织间杂存在,呈栅栏状或小梁状
FHI组织成分混杂,结构多样,需与以下疾病鉴别:①脂肪纤维瘤病,极易与FHI混淆,本组因超声发现脂肪和纤维回声而将33.33%(10/30)病灶诊断为脂肪纤维瘤;不同于FHI,脂肪纤维瘤内通常不存在扩张的血管[12];②血管瘤,本组超声误诊1例FHI为血管瘤,2例超声提示病灶血供丰富,术后病理均提示病灶含较多小血管成分,而CT/MRI将其中2例误诊为血管瘤或脉管瘤,可能与FHI的3种成分呈现无序纤维化形成假血管瘤形态相关,亦与部分瘤体内粗大血管相关。约50%FHI病灶病理可见假性血管瘤结构,与许多软组织肿瘤类似,如血管瘤、脉管瘤、神经纤维瘤及神经鞘瘤等[13];密集的透明胶原纤维与纺锤形细胞混合,胶原纤维间的裂口可模拟血管形态而导致影像学误诊。
本研究的局限性:为回顾性分析,所用超声设备及参数均未统一,无法归于一组进行定量分析;病理未对各种成分进行定量分析。
