盐酸罗哌卡因中添加羟考酮在硬膜外分娩镇痛中的作用
2020-09-21谢海燕李仁虎郑立东
谢海燕 程 峰 李仁虎 郑立东
羟考酮的结构和药理特性与吗啡相似,但起效更快且镇痛时间长。静脉注射羟考酮已广泛应用于术后镇痛和缓解急性疼痛。据报道,羟考酮在治疗内脏痛方面优于其他阿片类药物[1]。在第一产程中,产妇的疼痛主要是由子宫收缩引起的,羟考酮非常适合分娩镇痛。羟考酮用于硬膜外镇痛的报道很少,特别是在产科[2~3]。本研究探讨盐酸罗哌卡因中添加羟考酮对硬膜外分娩镇痛的作用。
1 资料与方法
1.1 一般资料 本研究通过本医院伦理委员会批准,获得所有产妇或其家属的书面分娩镇痛的知情同意书。2018年1月-11月共招募了60例22~38岁的参与者,美国麻醉医师协会(ASA)Ⅰ~Ⅱ级。入选标准包括孕期≥37周、单胎妊娠、初产妇,并经产科医生评估受试者能够进行阴道分娩。使用计算机随机数字代码将受试者随机分为羟考酮组(A组)和对照组(B组)。排除标准如下:合并有重度心肺疾病,宫颈扩张>3 cm,有语言沟通障碍的产妇;有椎管内麻醉禁忌症的产妇;产前服用镇痛、镇静药史;高危妊娠等。
1.2 镇痛方法 产妇进入产房后监测生命体征并建立外周静脉通道,同时使用视觉模拟评分法(VAS)对镇痛前的疼痛强度进行评估(0表示无痛,1~3分为轻度疼痛,4~7分为中度疼痛,10分为严重疼痛)。于宫颈扩张约3 cm时,进行硬膜外分娩镇痛。产妇左侧卧位行L2~3行硬膜外穿刺,硬膜外导管置入硬膜外腔内留约4 cm,经导管注入1.5%利多卡因2 mL实验量,观察五分钟排除误入血管或者蛛网膜下腔后,接同款镇痛泵。A组镇痛药为0.2 mg/mL的羟考酮+0.1%盐酸罗哌卡因+0.9%生理盐水混合液150 mL。B组镇痛药为0.1%盐酸罗哌卡因+0.9%生理盐水150 mL。两组镇痛泵设定参数相同,首剂量10 mL,背景剂量6 mL/h,补救剂量为6 mL/次,锁定20 min,镇痛泵药物持续输注直至产妇出产房。注入首剂量后30 min内,使用酒精棉球,每30 s进行一次躯干中部感觉评估。镇痛起效的标志为T10皮肤处没有冷感及VAS值<3。当产程进展较慢时,缓慢静脉点滴0.5%缩宫素以增加收缩。
1.3 观察指标 记录镇痛起效和持续时间、产程时长、产妇血压、心率和分娩结果、新生儿脐动脉血气分析和出生1 min及5 min时Apgar评分。同时记录低血压、瘙痒和呼吸抑制、下肢运动阻滞、寒战、心动过缓、过度镇静等不良反应。低血压的定义为收缩压低于基线值的80%;心动过缓的定义为心率<60次/分;呼吸抑制的定义为SpO2<91%,呼吸频率<10次/分;镇痛起效时间为从硬膜外给药到VAS值<3且T10皮肤处没有冷感的时间;镇痛持续时间为从硬膜外给药到VAS>3且不使用泵进行额外推注的时间。使用Bromage评分评估运动阻滞(0=无运动丧失,1=无法移动臀部,2=无法移动臀部和膝盖,3=无法移动臀部、膝盖和脚踝)。
1.4 统计学方法 本文采用SPSS 21.0统计学软件进行数据分析,正态分布的计量资料采用均数加减标准差表示,两组数据组间比较采用两独立样本t检验;组内比较采用配对t检验。非正态分布的计量资料采用中位数和25四分位数、75四分位数表示,两组数据组间比较采用Mann-Whitney Test;计数资料采用例数(%)表示,组间比较采用Fisher确切概率法。P<0.05表示差异有统计学意义。
2 结 果
2.1 两组产妇一般情况、分娩过程及结局比较 所有产妇均成功实施了硬膜外分娩镇痛并自然分娩,两组产妇的年龄、身高、体质量、孕周差异无统计学意义,具有可比性。两组分娩方式、催产素的使用,产后出血量和产程时长、新生儿Apgar评分、新生儿脐动脉血pH值差异无统计学意义(P>0.05)。A组镇痛开始时间明显早于B组(P<0.01),而A组的镇痛持续时间又明显长于B组,差异有统计学意义(P<0.01)。见表1。
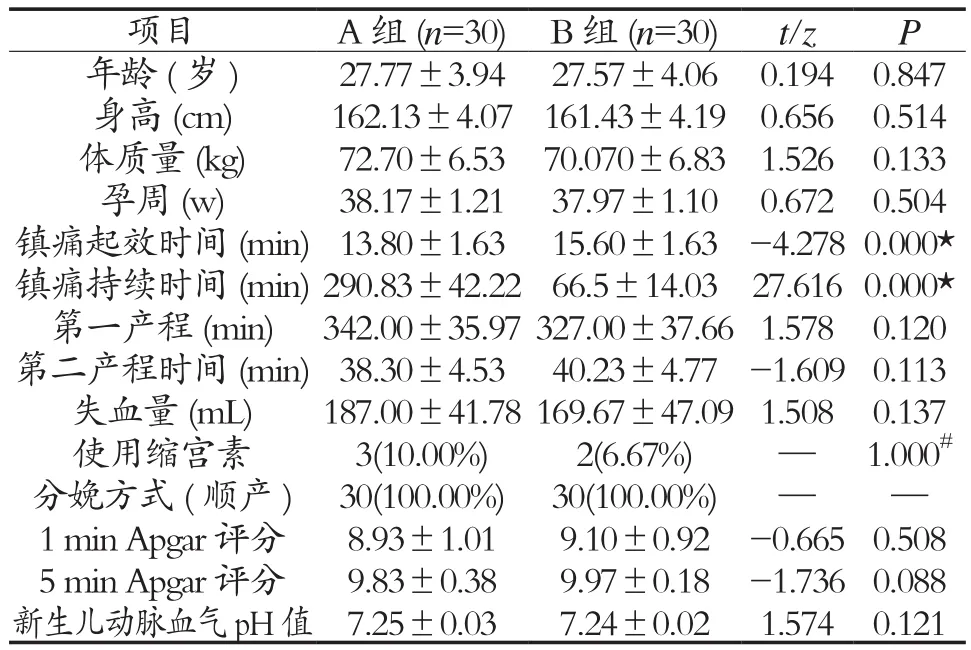
表1 两组一般情况比较
2.2 两组产妇不同时间点生命体征及VAS评分比较 两组T0、T1VAS值无显著差异,但两组T2~T4之间VAS值差异存在统计学意义(P<0.01),见表2。两组产妇在T0~T2时间点时监测的心率、收缩压、舒张压差异无统计学意义(P>0.05),见表3~5。
表2 两组产妇不同时点、麻醉前后VAS评分比较(±s,分)

表2 两组产妇不同时点、麻醉前后VAS评分比较(±s,分)
注:⋆⋆P<0.01,#表示与麻醉前比较P<0.05
组别 n T0 T1 T2 T3 T4
表3 两组产妇不同时点、麻醉前后心率比较(±s)

表3 两组产妇不同时点、麻醉前后心率比较(±s)
注:⋆⋆P<0.01,#表示与麻醉前比较P<0.05
组别n T0 T1 T2 T3 T4 A组 30 84.53±8.78 84.43±8.86 81.93±9.74 76.60±7.52#86.67±6.45 B组 3080.43±16.7983.87±8.62 81.40±9.97 75.53±8.11 88.40±5.76#t 1.185 0.251 0.210 -1.426 -1.099 P 0.241 0.803 0.835 0.221 0.276
表4 两组产妇不同时点、麻醉前后收缩压比较(±s)
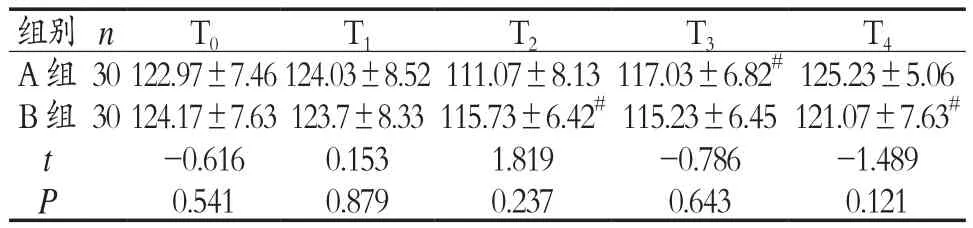
表4 两组产妇不同时点、麻醉前后收缩压比较(±s)
注:⋆⋆P<0.01,#表示与麻醉前比较P<0.05
组别n T0 T1 T2 T3 T4 A组 30122.97±7.46 124.03±8.52111.07±8.13 117.03±6.82#125.23±5.06 B 组 30124.17±7.63 123.7±8.33115.73±6.42#115.23±6.45 121.07±7.63#t -0.616 0.153 1.819 -0.786 -1.489 P 0.541 0.879 0.237 0.643 0.121
表5 两组产妇不同时点、麻醉前后舒张压比较(±s)

表5 两组产妇不同时点、麻醉前后舒张压比较(±s)
注:⋆⋆P<0.01,#表示与麻醉前比较P<0.05
组别 n T0 T1 T2 T3 T4 A组 30 74.53±7.62 78.07±9.67 75.43±8.52 71.23±6.21 74.17±6.36 B组 30 73.13±7.68 75.63±7.54 76.03±8.63 74.77±7.58 75.13±5.81#t 0.709 1.087 -0.271 -1.974 -1.157 P 0.481 0.281 0.787 0.053 0.068
2.3 两组产妇分娩镇痛不良反应比较 两组产妇分娩过程中均未观察到低血压和心动过缓、运动障碍的发生(Bromage评分>0)、寒战、过度镇静、呼吸抑制,两组恶心、呕吐、瘙痒发生率差异均无统计学意义(P>0.05)。
3 讨 论
硬膜外镇痛由于其出色的镇痛作用以及对母体的不良影响少而较早被用于缓解产程的痛苦。在局部麻醉药中添加阿片类药物可增强其镇痛作用,并减少分娩时的副作用。在本研究中,我们发现硬膜外镇痛药中添加羟考酮可加速镇痛起效作用,并明显延长镇痛时间。分娩时不增加新生儿的不良事件。羟考酮的作用类似于吗啡,是蒂巴因的半合成阿片类物质衍生物。作为一种 u和k受体激动剂,可口服羟考酮来缓解中度至重度的急性或慢性疼痛,例如癌症、神经系统疾病或严重的非癌症相关的慢性疼痛[4~6]。羟考酮主要通过激活u和 k受体而产生镇静和镇痛作用。当羟考酮激活u受体时,它会产生止痛作用,但这种作用会伴有恶心、呕吐和呼吸抑制等副作用。k受体广泛存在分布在脊髓中。羟考酮的镇静和镇痛作用与k受体激活有关。
本项研究中所有新生儿Apgar评分均超过7分,并且没有脐动脉pH<7.2。因此,当添加羟考酮用于硬膜外分娩镇痛时,并且不会对新生儿产生不良影响比如呼吸抑制。Dostbil A等[7]报道称在小剂量布比卡因中进行硬膜外分娩镇痛时增加吗啡可显著减少局麻药剂量并增加镇痛作用,而不会对母亲和胎儿产生不良影响。Wang X等[8]通过比较在罗哌卡因中添加舒芬太尼对硬膜外分娩镇痛的效果,他们发现分娩的第一产程疼痛评分明显降低。我们的研究得出结论,罗哌卡因中添加羟考酮进行硬膜外分娩镇痛对于母亲和胎儿都是安全的。当用于硬膜外分娩镇痛时,小剂量盐酸罗哌卡因对血流动力学没有可检测的影响。羟考酮与罗哌卡因的组合可减少交感神经冲动传递并减轻产妇疼痛。此外,出色的镇痛作用可以放松骨盆底和阴道肌肉,这有利于降低胎儿头部的位置并加快分娩过程。在我们的研究中,两组在分娩期间的持续时间上没有统计学差异,这表明使用硬膜外罗哌卡因和羟考酮进行分娩镇痛不会影响分娩期的持续时间。硬膜外分娩镇痛的羟考酮与局麻药配伍的最佳浓度仍需要进一步的研究来评估。
总之,本项研究表明硬膜外羟考酮可以加速镇痛的起效时间,并显著延长分娩过程的镇痛时间,且不会对新生儿产生不良影响。
