大脑皮层弥漫性星形细胞瘤MRI分析
2018-07-21王朝晖高培毅
王朝晖,高培毅
(首都医科大学附属北京天坛医院神经影像中心,北京 100050)
弥漫性星形细胞瘤(DA)在WHO中枢神经系统肿瘤恶性程度分级中定为Ⅱ级,由于其具有侵袭性和向更高级别胶质瘤转化的趋势,近年来主张积极的手术治疗方式[1],术前尽早明确诊断显得尤为重要。成人DA好发于大脑白质,也可发生于大脑皮层或侵及皮层,肿瘤易沿脑白质纤维束扩散,在MR图像上表现为边界不清的云雾状影;大脑皮层是神经元胞体所在的位置,血运较丰富,其内神经纤维较少且走行不同于白质内纤维,故其内DA生长方式和影像特征可能有特殊性。研究表明[2],大脑皮层DA常表现出较强的生长惰性,进展相对缓慢,预后相对较好;有关DA的影像研究已经有大量报道[3],其MRI可表现为多种类型[4],每种影像类型除了与肿瘤自身特点有关外,还可能和肿瘤所在部位的解剖结构有关;主体位于大脑皮层的DA的影像表现报道较少,而大脑皮层也是多种疾病的好发部位;为提高诊断水平,笔者将对大脑皮层DA的MRI表现进行回顾性分析。
1 材料与方法
1.1 一般资料
收集2013年12月—2015年4月在首都医科大学附属北京天坛医院诊治,经手术病理证实为脑内DA的21例脑肿瘤患者的术前MR图像;男12例,女9例;年龄21~51岁,平均39岁;症状主要是癫痫、头痛、头晕。21例均行常规MR平扫和增强检查。经MR冠、矢、轴多平面精准定位,确保脑肿瘤全部或主体位于大脑皮层。
1.2 扫描技术与方法
使用GE Signa 1.5T和Siemens Trio3.0T MR扫描仪,采用8通道头线圈、SE序列和FSE序列,平扫行轴面T1WI、T2WI扫描,增强行T1WI冠、矢、轴面扫描; 参数为:GE Signa 1.5T:SE-T1WI(TR 450ms、TE 12ms),FSE-T2WI(TR 4500ms、TE 96ms);Siemens Trio3.0T:FLAIR-T1WI:(TR 1980ms、TE 9ms),FSE-T2WI(TR 4 500ms、TE 96ms),层厚 5mm,层间距0.5mm,矩阵512×512像素。增强扫描采用对比剂钆喷酸葡胺注射液(Gd-DTPA),剂量0.2mL/kg体质量,流率 2.0mL/s。
1.3 图像分析
由两名高年资神经放射医师对病灶位置、MR信号分别进行阅片和分析,如有异议,则经协商统一意见。观察内容包括:肿瘤在脑叶的分布、肿瘤形态、病变范围、肿瘤边界、瘤体信号、强化特点、瘤周水肿、生长方式。在T2WI上把瘤体中稍长T2信号定为实性,把肿瘤中接近脑脊液的信号定为囊性;在横切面上测量囊性部分直径及肿瘤的最大直径,二者比值即为肿瘤囊性成分百分比。根据肿瘤囊性成分百分比,将病灶分为囊性、囊实性及实性三种。囊性成分百分比>80%为囊性病灶,<20%为实性病灶,其余病灶为囊实性病灶。在T2WI上肿瘤周围的近似脑脊液信号定为水肿带,根据肿瘤周围水肿宽度,将水肿程度分为轻度水肿(<5mm),中度水肿(5~10mm)及明显水肿(>10mm)。增强后强化灶明显低于同层脂肪信号者,定为轻度强化,强化信号与同层脂肪信号近似的,定为中重度强化。
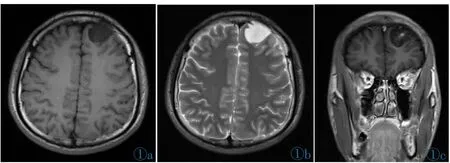

图1 左额叶DA。图1a:轴面T1WI平扫见低信号囊实性肿块,信号稍不均,局部颅板受压,信号减低;图1b:轴面T2WI平扫见肿块呈长T2信号,无明显瘤周水肿;图1c:冠面T1WI增强:皮层肿块内见斑片状轻度强化。 图2左颞、顶叶 GemA。图2a:轴面 T1WI平扫见长T1信号囊实性肿块,信号不均;图2b:轴面T2WI见肿块呈长T2信号,信号不均,可见中度瘤周水肿;图2c:冠面T1WI增强:皮层肿块见斑片状中度强化,左海马钩回疝形成。Figure 1.Left frontal DA.Figure 1a:Axial plain T1WI image shows a low and mild heterogeneous hypointense solid cystic mass,with slight compression of local cranial plate of decreased signal intensity;Figure 1b:Axial T2WI image shows T2 hyperintensity of the lesion,with no peritumoral edema.Figure 1c:Coronal enhanced T1-weighted image demonstrates that the cortical mass has patchy slight enhancement.Figure 2.Left temporal and parietal GemA.Figure 2a:Axial precontrast T1-weighted image shows a solid cystic mass with slight heterogeneous signal intensity.Figure 2b:Axial T2-weighted image shows a mass of heterogeneous hyperintensity with moderate peritumoral edema.Figure 2c:Coronal postcontrast T1-weighted image demonstrates moderate patchy enhancement in the cortical mass with left hippocampal gyrus herniation.
2 结果
共 21 例,23 个病灶;额叶最多见(16/23);多发病灶1例;病灶主体T1WI呈低信号,T2WI呈高信号,平扫瘤体内未见T1WI高信号,除了肥胖细胞型星形细胞瘤(GemA)外,信号多较均匀。囊性肿块最多见(15/23),囊实性肿块(5/23)和脑回肿胀(3/23)相对少见;本组DA的形态与所在的脑叶位置有关,位于大脑半球凸面上部的病灶形态多呈类圆形囊性或囊实性肿块,其中2个额叶肿块压迫颅板,表现为T1WI颅板局部变薄并信号减低;位于脑底部的DA多表现脑回肿胀并皮层下斑片状长T1长T2信号,脑回形病灶长径可达6 cm;1例GemA范围较大,直径约6 cm:其余病灶直径2.5~3.5 cm;未见跨中线浸润生长;瘤周水肿:多为无至轻度,1例GemA表现为中度水肿。增强扫描:20个DA灶表现为不强化,2个DA表现为皮层或皮层下斑片状轻度强化,1例GemA表现为大片中度强化。
3 讨论
2016年WHO中枢神经系统肿瘤的最新分类将分子信息结合到诊断当中。Ⅱ级的DA包括IDH突变型、IDH野生型及NOS型;如果IDH基因无法检测或完成不好,则诊断为NOS。GemA,IDH突变型为DA的亚型[5];新版分类法取消了2007年版中纤维型星形细胞瘤和原浆型星形细胞瘤两个亚型。根据新的分类标准,本组DA病例属于NOS型。DA多见于成年人,发病高峰年龄段为30~40岁,男性略多于女性[5]。颅内多发胶质瘤发病率较低,多个病灶间病理类型常相同[6],本组大脑皮层DA患者年龄、性别与文献资料相仿。
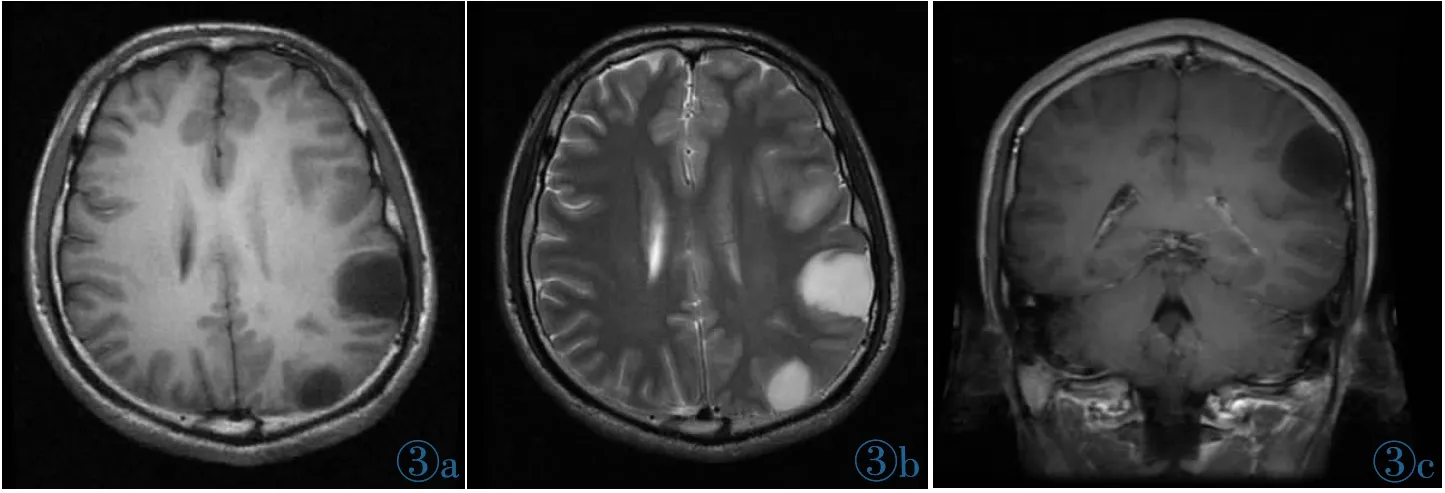
图3 左大脑额、顶、枕叶多发DA。图3a:轴面T1WI平扫见低信号囊性肿块及囊实性脑回肿胀;图3b:轴面T2WI平扫见病灶呈高信号,无明显瘤周水肿;图3c:冠面T1WI增强:肿块未见强化。Figure 3.Multiple DA of left frontal,parietal and occipital lobes.Figure 3a:Axial T1-weighted image reveals hypointense cystic masses with cystic and solid gyrus swelling.Figure 3b:Axial T2-weighted image shows hyperintense masses with no obvious peritumoral edema.Figure 3c:Coronal enhanced T1-weighted image shows that the mass is unenhanced.
有文献报道[4],DA的MRI主要表现为3种类型,即囊性肿块、囊实性肿块和弥漫型。但大脑皮层以哪种类型为主少见报道。DA可发生于中枢神经系统的任何部位,但主要位于大脑半球白质,以额叶最为常见。本组大脑皮层DA位于额叶的最多,与相关文献一致。本组大脑皮层DA大部分表现为囊性肿块,少部分表现囊实性肿块或囊实性脑回肿胀,脑回肿胀常伴有皮层下斑片状长T1长T2信号。从大小上看,本组皮层病灶除1例GemA外,其余DA肿块直径均小于4 cm;典型的DA多不强化,瘤周水肿轻微,占位效应相对轻,若有强化则表示该区域生长活跃[7];GemA由于生长较为缓慢,体积可较大[8],常见轻中度强化,瘤周水肿可较重;本组大脑皮层DA信号均符合上述典型特征。
大脑皮层DA的影像学特征可能与肿瘤的生物学行为和预后相关。脑肿瘤囊变由肿瘤内血管源性水肿所致;大脑皮层DA易囊变,可能与肿瘤沿皮层内纤维生长、破坏血脑屏障导致血管源性水肿[9]以及额、顶叶上部皮层血供较丰富有关。研究表明[10],DA平均年生长速度约为每年4mm,但各个病灶间的差距较大(0~11mm/年),生长速度与预后有关,尚未见各个影像类型病灶生长速度的报道。陈绪珠等[11]经MR动态观察后发现,原发于大脑皮层的DA常先在皮层内形成囊性肿块,生长较缓慢,呈膨胀式生长;若皮层被破坏,则肿瘤易沿白质内纤维束浸润生长,占位效应相对较轻,生长速度加快,给肿瘤全切造成困难并对预后产生不良影响。由于GemA多含有tp53突变基因,更易于向更高级别的星形细胞瘤转化,所以表现出了高级别胶质瘤的部分典型MR特征(中度强化、瘤周水肿中度、出现占位效应),其预后不良。
大脑皮层囊性肿块常需要与以下病灶鉴别:①胚胎发育不良性神经上皮肿瘤(WHOⅠ级):多发生于青少年,影像上可见“三角征”和“小泡征”等囊性病灶;增强后不强化或轻微结节样、小环样强化,无占位效应。②节细胞胶质瘤(WHOⅠ级):好发于儿童及30岁以下成人,可位于脑表面,可表现为囊性为主型[12],增强后壁结节呈明显均匀强化;脑回肿胀合并皮层下斑片状异常信号需要与以下病灶鉴别:①少突胶质细胞瘤(WHOⅡ级):好累及大脑皮层,脑回肿胀较明显,囊变相对较轻,由于常伴有索状钙化而信号不均,增强后多为轻度强化[13];②病毒性脑炎:脑炎可表现为双侧大脑多发病变,且脑炎的临床病程较短,病情变化快,多数有其他部位的感染病史;③线粒体脑病:常发生于大脑后部,单侧或双侧,病变范围与大血管供血区不一致,且可呈游走性,肌肉活检可明确诊断。
总之,大脑皮层DA多表现为长T1长T2信号囊性肿块,周围无水肿,增强后多不强化,具有较明显的MR特征;GemA瘤体可较大,信号不均,占位效应及瘤周水肿明显,增强扫描明显不均匀强化;熟悉以上MR特征将有利于诊断、鉴别诊断及对肿瘤预后的判断。
