非等温氧化工艺下含Si低碳钢氧化行为的实验研究
2017-07-07梁伟成
梁伟成,徐 光,袁 清,何 贝
(1. 武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北 武汉,430081;2.武汉科技大学国际钢铁研究院,湖北 武汉,430081)
非等温氧化工艺下含Si低碳钢氧化行为的实验研究
梁伟成,徐 光,袁 清,何 贝
(1. 武汉科技大学钢铁冶金及资源利用省部共建教育部重点实验室,湖北 武汉,430081;2.武汉科技大学国际钢铁研究院,湖北 武汉,430081)
模拟工业生产现场板坯在加热炉中的分段式加热制度和氧化气氛,在同步热分析仪(TGA)中进行氧化实验,研究氧化温度对硅的质量分数分别为1.21%和0.25%的两种低碳钢试样(HS1.21和LS0.25)氧化行为的影响。同时,用场发射扫描电镜(SEM)观察氧化后试样氧化铁皮及Fe2SiO4的微观形貌,用Image-pro Plus 6.0测量不同硅含量钢种在不同氧化温度下氧化后试样的Fe2SiO4渗透深度,用能谱仪(EDS)分析其氧化铁皮的结构组成。结果表明,温度达到剧烈氧化温度后,两种试样中硅含量低的低碳钢氧化增重随时间呈抛物线变化,而硅含量较高的低碳钢氧化增重随时间呈直线性变化;氧化一定时间后,硅含量不同的两种试样的氧化增重曲线相交,出现临界时间点,在该临界时间点之前,LS0.25低碳钢的氧化增重较多,而临界时间点之后,HS1.21低碳钢氧化增重较多,且临界时间点随着氧化温度的升高逐渐推迟。
低碳钢;硅含量;非等温氧化;氧化铁皮;硅酸亚铁;氧化行为
固溶强化可以提高碳钢的综合性能,硅元素作为常用的固溶强化元素之一,被广泛使用于低碳钢中[1-3]。当钢中硅的质量分数超过0.5%时,热轧带钢表面通常会出现红色氧化铁皮缺陷,对带钢表面质量造成不利影响[4-5]。另外,在高温环境下,含硅钢中Si易与O发生反应,在氧化铁皮与金属基体之间产生一层硅酸亚铁(Fe2SiO4),当温度低于Fe2SiO4的凝固温度1170 ℃时,高黏度Fe2SiO4的存在使得氧化铁皮与基体黏附在一起,采用高压水除鳞方法很难完全除尽,氧化铁皮中残留的FeO在后续轧制和冷却过程中转变成Fe2O3,形成红色氧化铁皮缺陷,严重阻碍了产品档次的提升[6-7]。
Mouayd等[8]在研究含硅钢高温等温氧化过程中铁皮形貌及形成时指出,当温度高于1177 ℃时,液态Fe2SiO4会促进离子扩散,导致氧化铁皮厚度增加。此外,Cao等[9]对低碳钢在500~900 ℃下保温时氧化动力学的研究表明,低碳钢单位面积氧化增重随时间呈抛物线变化,氧化速率随保温时间的延长而降低。Abuluwefa等[10]研究了在1000~1250 ℃等温条件下低碳钢的氧化行为,结果表明初始氧化增重与时间呈线性关系,氧化速率随氧浓度的增加而增大,氧化一定时间后氧化增重则与时间呈抛物线关系。Chen等[11]研究了在700~1100 ℃等温条件下低碳钢的氧化行为,结果表明其氧化动力学曲线近似为抛物线。
以上对于低碳钢氧化行为的研究都是在等温阶段通入氧气,但实际生产中,钢坯在加热、保温阶段始终处于氧化气氛中。为此,本文立足工业生产现场的实际加热制度,运用热重分析仪研究了低碳钢在不同温度下的氧化行为,重点分析温度及硅含量对低碳钢氧化行为的影响,定义了低碳钢氧化过程中的临界时间点概念,并分析了临界时间点随温度的变化规律,以期对低碳钢氧化铁皮的控制提供参考。
1 实验材料及实验方法
1.1 实验材料
实验材料来自国内某大型钢铁企业热轧带钢厂实际生产的两种不同Si含量的含Nb低碳钢,具体成分如表1所示,其中w(Si)=1.21%的试样标记为HS1.21,w(Si)=0.25%的试样标记为LS0.25。试样尺寸为15 mm×10 mm×3 mm,为便于实验,沿试样长度中心方向靠近边部打上直径为4 mm的小孔。

表1 试样的化学成分(wB/%)
1.2 氧化实验
在Setaram Setsys Evo型同步热分析仪(TGA)上进行氧化模拟实验。实验之前,先将试样进行打磨抛光,以去除表面的氧化铁皮及其他杂质。先将试样以20 ℃/min的速率加热到850 ℃,再以6.6 ℃/min的速率加热到1180 ℃,然后以0.9 ℃/min的速率分别加热到1210 ℃、1260 ℃和1300 ℃,在这3个温度下分别保温95、40、0 min,以保证各试样氧化时间相同。加热和保温阶段的氧化气氛均为体积分数为4.0%的O2和体积分数为96.0%的N2的混合气体。氧化后的试样以50 ℃/min的速率冷却到室温,在冷却过程中控制炉腔内氧气的体积分数为21.0%,以模拟工业加热炉钢坯加热出炉后的空冷环境。在整个氧化实验过程中,通过仪器自带的电子天平测量试样的氧化增重情况。实验中加热温度精度控制在±0.5 ℃,因此可以忽略同步热分析仪中的温度偏差对氧化增重的影响。由于氧化后试样表面的氧化铁皮脆性较高,容易剥落,为了充分保护试样氧化铁皮的完整性,采用冷镶嵌法进行制样,冷镶嵌料采用由冷埋树脂粉、冷埋树脂水双组份按3∶2比例组合的室温快速固化胶,冷镶嵌后30 min左右即可固化,打磨、抛光后备用。
1.3 氧化铁皮检测分析方法
采用Nova 400 Nano 场发射扫描电子显微镜(SEM)观察不同温度下氧化试样的氧化铁皮微观组织,加速电压为20 kV。采用能谱仪(EDS)分析氧化铁皮结构组成。采用图像分析软件Image-pro Plus 6.0 测量不同硅含量试样的Fe2SiO4渗透深度,首先测出铁皮最内层Fe2SiO4所占的总面积,将其除以测量区域的宽度即可得到单位宽度上Fe2SiO4的面积,该值即可代表Fe2SiO4层的平均渗透深度[12]。
2 实验结果与分析
2.1 Fe2SiO4的形貌及渗透深度
图1所示为氧化过程氧化温度为1260 ℃时HS1.21试样氧化铁皮形貌及其EDS取样点,取样点元素的原子百分数如表2所示。由表2所示3层氧化铁皮层中铁、氧、硅元素的原子比可以知道,氧化铁皮主要由最外层Fe2O3、中间层Fe3O4+FeO以及最内层FeO+Fe2SiO4组成[13,14]。其他温度下试样的氧化铁皮能谱分析结果与此

图1 氧化温度为1260 ℃时HS1.21试样氧化铁皮组织形貌
Fig.1 Structure of oxide scale of HS1.21 steel oxidized at 1260 ℃
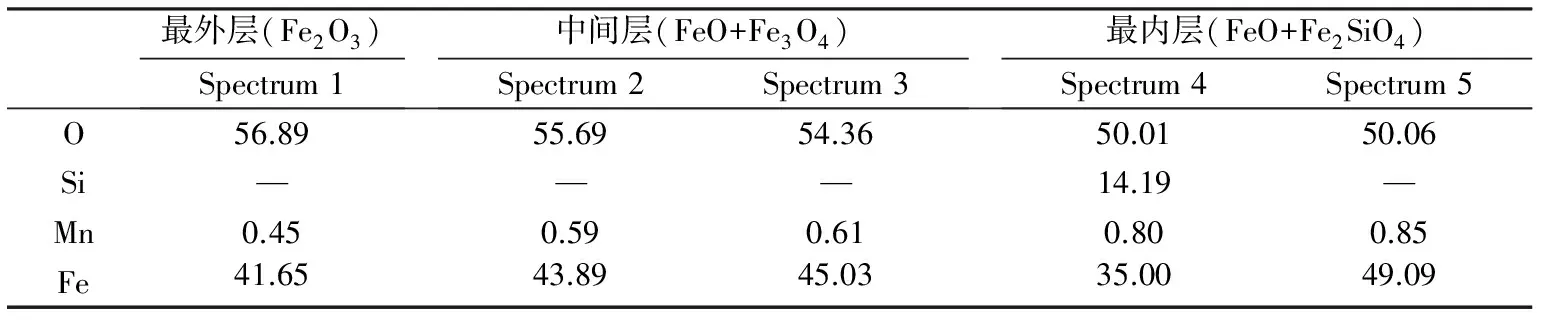
表2 氧化温度为1260 ℃时HS1.21试样各层氧化铁皮的原子百分比(xB/%)
结果基本相同。
图2所示为试样HS1.21和LS0.25在不同温度下氧化后Fe2SiO4的渗透形貌。图2中红色区域是通过Image-pro Plus 6.0 的色差自动识别功能得到,红色所覆盖区域即为Fe2SiO4分布的区域,目的是更加清晰地观察液态Fe2SiO4的渗透形貌。由图2中可以看出,Fe2SiO4主要集中于铁基体与最内层氧化铁皮的交界处。随着氧化温度的升高,Fe2SiO4含量增多且树枝状形貌愈发明显,其原因是当温度升高时,形成氧化铁皮所

(a) HS1.21-1210 ℃ (b) HS1.21-1260 ℃ (c) HS1.21-1300 ℃
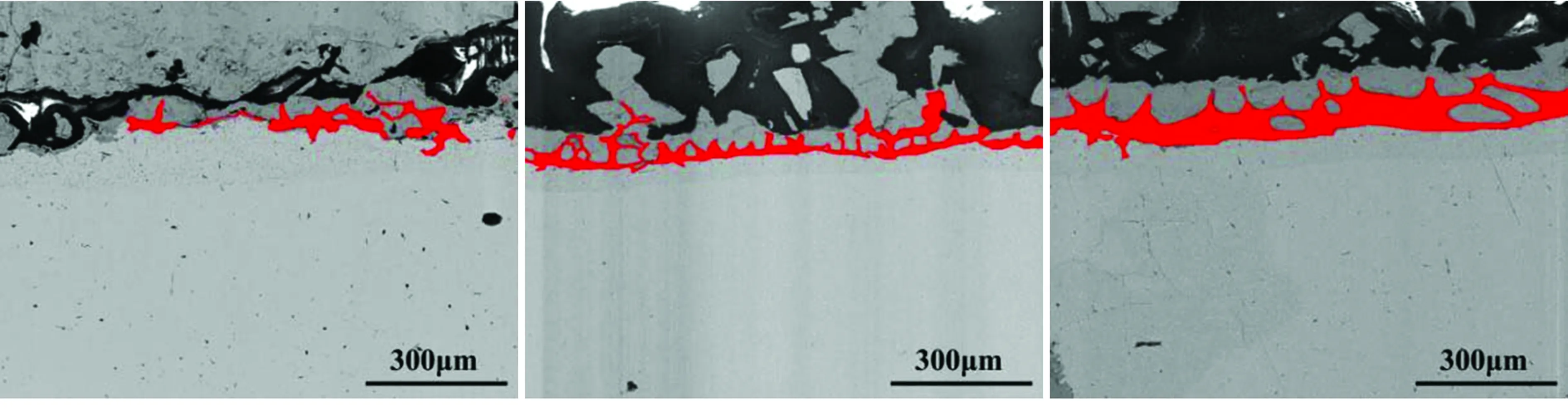
(d) LS0.25-1210 ℃ (e) LS0.25-1260 ℃ (f)LS0.25-1300 ℃
图2 HS1.21钢和LS0.25钢在不同温度下氧化后的Fe2SiO4渗透形貌
Fig.2 Penetration morphology of Fe2SiO4in HS1.21 and LS0.25 steels oxidized at different temperatures
需离子及原子的扩散及结合速率提高,氧化程度的加剧使得Fe2SiO4的生成量增多。此外,硅含量较高的HS1.21试样较硅含量偏低的LS0.25试样中Fe2SiO4的树枝状形貌更明显,这是因为Fe2SiO4的渗透过程必须满足一定的浓度条件才能顺利进行,当硅含量增多时,Fe2SiO4生成量也会增多,从而促进了Fe2SiO4沿晶界处的蔓延扩散,最终呈现明显的树枝状。
图3所示为两种试样在不同温度下氧化后的Fe2SiO4渗透深度。由图3中可以看出,随着氧化温度的升高,两种试样中的Fe2SiO4渗透深度都逐渐增加,相同温度下硅含量高的试样Fe2SiO4渗透得更深,与上述Fe2SiO4的渗透形貌规律一致。对于同一试样,当温度由1210 ℃上升至1260 ℃时,Fe2SiO4的渗透深度增加量较少,而当温度继续上升至1300 ℃时,Fe2SiO4的渗透深度增加明显。这是因为形成氧化铁皮及Fe2SiO4的铁离子、氧原子及硅原子的扩散与结合程度与温度呈指数关系,当温度升高时,原子及离子扩散速率呈指数形式增加,使试样的氧化反应更加剧烈,氧化铁皮增长较快,同时液态的Fe2SiO4明显增多,在氧化铁皮内部压应力的作用下Fe2SiO4不断沿着晶界向外侧的氧化铁皮中渗透,使得其渗透深度增加明显。

图3 HS1.21试样和LS0.25试样在不同温度下氧化后Fe2SiO4渗透深度
Fig.3 Penetration depth of Fe2SiO4in HS1.21 and LS0.25 steels oxidized at different temperatures
2.2 氧化增重曲线及临界时间点
图4所示为HS1.21和LS0.25两种试样在不同温度下氧化后的单位面积氧化增重随时间的变化曲线。单位面积的氧化增重间接反映了试样氧化铁皮的厚度,试样的氧化增重可以代表脆性较高、完整性较差且难以统计的氧化铁皮厚度。氧化增重曲线可分为3个阶段:开始氧化阶段、剧烈氧化阶段及停止氧化阶段[12];图4(a)中A、B、C3个临界温度点分别定义为开始氧化温度点、剧烈氧化温度点和停止氧化温度点。在开始氧化温度点A点之前,几乎没有氧化反应,原因是此时温度较低,离子的扩散及结合程度十分微弱,表面形成钝化膜。在开始氧化温度点A点和剧烈氧化温度点B点之间,氧化反应缓慢进行,钝化膜随着温度的上升而逐渐破裂,氧化反应开始进行。当温度上升至剧烈氧化温度时,HS1.21试样的氧化增重呈线性增加,而LS0.25试样的氧化增重近似呈抛物线性增加。氧化一段时间后,呈抛物线型的LS0.25试样的氧化增重曲线与HS1.21试样的直线型氧化增重曲线相交,将其交点定义为临界时间点,如图4(a)中D1、D2、D3。当温度到达停止氧化温度点C后,开始出现氧化增重平台,氧化增重不再增加,氧化反应过程基本停止。在临界时间点之前,LS0.25试样的氧化增重多于HS1.21试样;在临界时间点之后,HS1.21试样的氧化增重多于LS0.25试样, 这与文献[9,11]中所得的规律不同,这是由于加热制度不同引起的。以往的研究都是在某个温度下等温氧化,氧化气氛在等温过程中才通入,而本文模拟的是现场分段式加热制度,氧化气氛从加热一开始就通入,因此,本文所得到的低碳高强钢的氧化增重规律更加贴近实际。
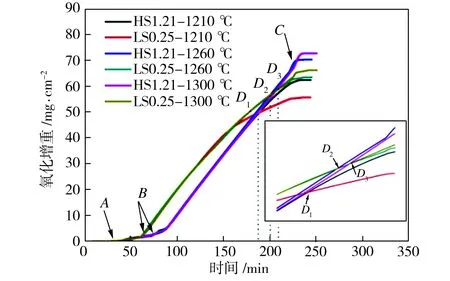
(a)
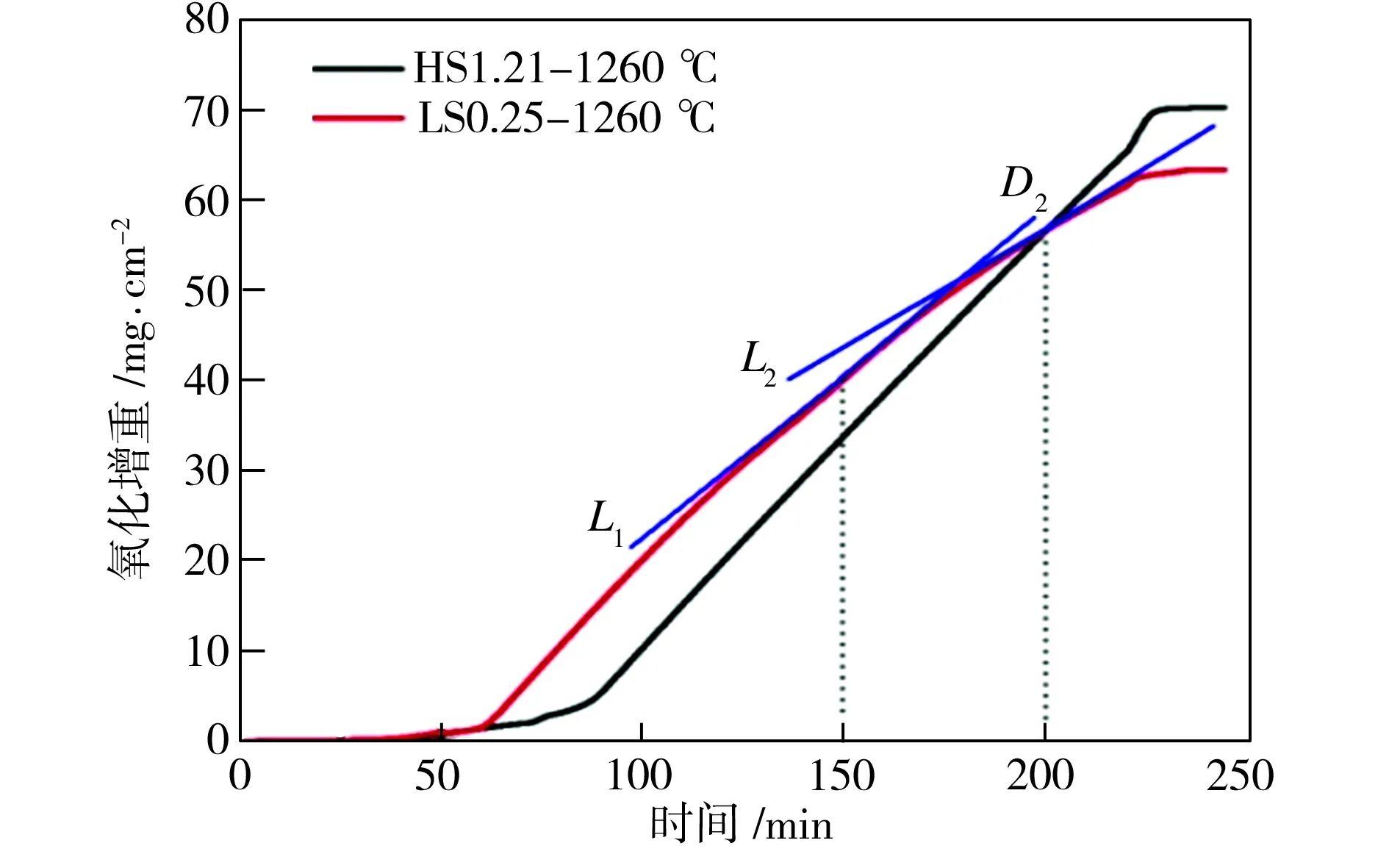
(b)
Fig.4 Oxidation mass gains versus time in different samples
低碳钢的氧化反应主要取决于两个因素,即液态Fe2SiO4对离子及原子扩散与结合的促进作用和氧化铁皮对离子及原子扩散与结合的阻碍作用[12]。当温度达到剧烈氧化温度点后,HS1.21试样的氧化增重与时间呈直线关系,这是因为随着氧化时间的增加,氧化铁皮逐渐增厚,其对氧化反应进程的阻碍作用增加,但是在HS1.21试样中,硅含量较充足,能够形成较多的液态Fe2SiO4,对离子扩散的促进作用增强,此时液态Fe2SiO4对氧化反应的促进作用和氧化铁皮本身对氧化反应的阻碍作用达到动态平衡,因此氧化速率保持不变。当温度达到剧烈氧化温度点后,LS0.25试样的氧化增重与时间呈抛物线关系,这是因为LS0.25试样中含硅量较低,形成的液态硅酸亚铁含量较少,虽然对离子的促进作用增加,但氧化铁皮厚度增加对离子扩散的阻碍作用增加得更加明显,导致氧化速率随时间的延长逐渐降低,表现为氧化增重曲线呈斜率不断下降的抛物线型。
Kofstad等[15]提出了遵循线性、抛物线和立方规律的低碳钢氧化动力学方程:
(1)
式中:ΔW为氧化反应t时刻单位面积的氧化增重,mg·cm-2;n是一个常数,当n取1、2、3时分别对应线性、抛物线和立方规律;K为氧化速率常数(KL表示线性规律的氧化速率常数,mg·cm-2·min-1;KP表示抛物线规律的氧化速率常数,mg2·cm-4·min-1);t为氧化时间。
图4(b)给出了氧化温度为1260 ℃时两种试样的氧化增重曲线,由氧化动力学方程可以计算得到,LS0.25试样较早进入剧烈氧化阶段,氧化速率常数KP为4.35 mg2·cm-4·min-1,但氧化速率逐渐降低(如切线L1→L2所示);HS1.21试样的氧化速率常数KL为0.45 mg·cm-2·min-1。在临界时间点D2之前,LS0.25试样的氧化增重高于HS1.21试样;在临界时间点D2之后,LS0.25试样的氧化增重少于HS1.21试样。由图4(a)中可见,HS1.21试样与LS0.25试样在1210 ℃、1260 ℃和1300 ℃下对应的临界时间点分别为D1、D2和D3,临界时间点随着氧化温度的升高而推迟。这是因为当温度较低时,低硅钢形成的液态Fe2SiO4含量较少,难以提供较多的离子扩散通道,在氧化铁皮不断增厚阻碍作用愈发增强的同时,液态Fe2SiO4对离子及原子扩散与结合的促进作用逐渐小于氧化铁皮厚度对离子及原子扩散与结合的阻碍作用,使得LS0.25试样的抛物线更早地与HS1.21试样的直线相交。当温度升高时,低硅钢中硅等原子及铁离子的扩散与结合加剧,形成的液态Fe2SiO4含量增加,虽然氧化铁皮本身厚度对离子及原子扩散的阻碍作用也在增加,但液态Fe2SiO4含量增加对氧化反应的促进作用使得临界时间点推迟出现。在文献[1,3,9,11]中,不同硅含量的低碳钢的氧化增重曲线没有出现相交的现象,原因是加热通氧制度不同,以及氧化时间的区别,以上文献中部分采用等温通氧,而且氧化时间较短。不同温度下两个试样的单位面积氧化总增重与液态Fe2SiO4的渗透深度如图5所示。由图5中可以看出,随着氧化温度上升,氧化增重和液态Fe2SiO4渗透深度均增加。
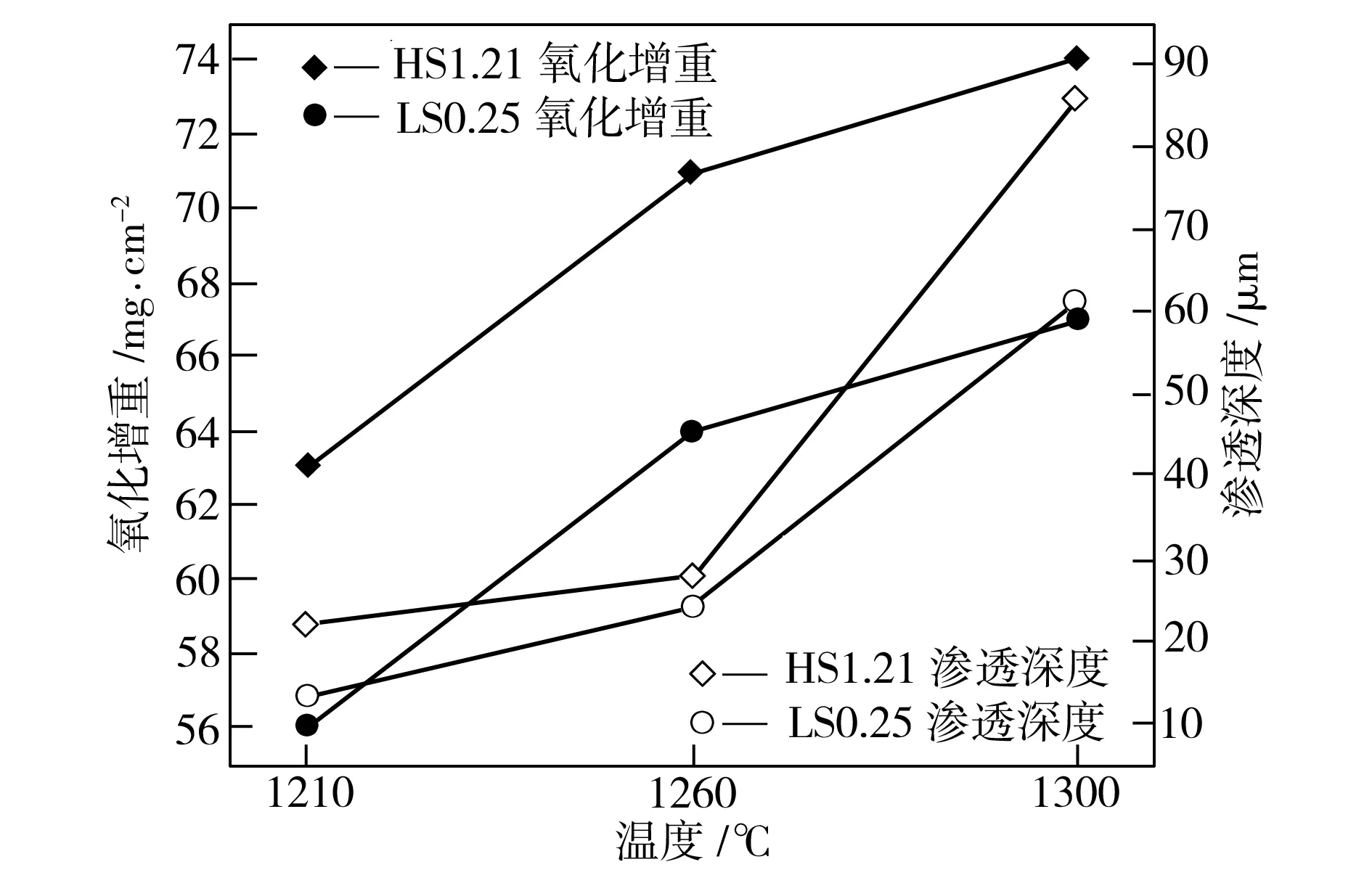
图5 不同试样氧化增重和Fe2SiO4渗透深度的关系
Fig.5 Relationship between oxidation mass gain and penetration depth of Fe2SiO4
3 结论
(1)与等温氧化相比,非等温氧化工艺下含Si低碳钢的氧化行为呈现明显差异。
(2)温度达到剧烈氧化温度后,硅含量低的低碳钢氧化增重随时间呈抛物线变化,而硅含量较高的低碳钢氧化增重随时间呈直线变化。
(3)氧化一定时间,硅含量不同的两种低碳钢氧化增重曲线相交,出现临界时间点,在该临界时间点之前,硅含量低的低碳钢氧化增重较多,而临界时间点之后,硅含量较高的低碳钢氧化增重较多,且临界时间点随着氧化温度的升高而逐渐推迟。
[1] 李舒笳,柳洋波,张玮,等. 2%残氧气氛下硅对弹簧钢氧化速率的影响[J]. 钢铁研究学报,2015,27(5): 55-60.
[2] Hu H J, Xu G, Wang L, et al. The effects of Nb and Mo addition on transformation and properties in low carbon bainitic steels[J]. Materials and Design, 2015, 84(4): 95-99.
[3] 刘小江,曹光明,何永全,等. 单道次热轧对Fe-1.5Si硅钢氧化层形貌的影响[J]. 东北大学学报:自然科学版,2013,34(12): 1730-1733.
[4] 曹光明,孙彬,刘小江,等. 热轧高强钢氧化动力学和氧化铁皮结构控制[J]. 东北大学学报:自然科学版,2013,34 (1):71-74,84.
[5] He B, Xu G, Zhou M X, et al. Effect of oxidation temperature on the oxidation process of silicon-containing steel[J].Metals,2016,6(6):137.
[6] 孙彬,曹光明,刘振宇. 热轧带钢粉状氧化铁皮的形成机制及柔性化控制[J]. 钢铁研究学报,2013, 25(10): 53-57.
[7] Okada H, Fukagawa T, Ishihara H, et al. Prevention of red scale formation during hot rolling of steels[J]. ISIJ International, 1995, 35(7): 886-891.
[8] Mouayd A A, Koltsov A, Sutter E, et al. Effect of silicon content in steel and oxidation temperature on scale growth and morphology[J]. Materials Chemistry and Physics, 2014, 143: 996-1004.
[9] Cao G M, Liu X J, Sun B, et al. Morphology of oxide scale and oxidation kinetics of low darbon steel[J]. Journal of Iron and Steel Research: International, 2014, 21(3): 335-341.
[10]Abuluwefa H, Guthrie R I L, Ajersch F. The effect of oxygen concentration on the oxidation of low-carbon steel in the temperature range 1000 to 1250 ℃[J]. Oxidation of Metals, 1996, 46(5): 423-440.
[11]Chen R Y, Yeun W Y D. Review of the high-temperature oxidation of iron and carbon steels in air or oxygen[J]. Oxidation of Metals, 2003, 59(5/6): 433-468.
[12]Yuan Q, Xu G, Zhou M X, et al. New insights into the effects of silicon content on the oxidation process in silicon-containing steels[J]. International Journal of Minerals, Metallurgy and Materials, 2016, 23(9): 1048-1055.
[13]Yuan Q, Xu G, Zhou M, et al. The effect of the Si content on the morphology and amount of Fe2SiO4in low carbon steels[J]. Metals—Open Access Metallurgy Journal, 2016, 6(4): 94-102.
[14]Cao G M, Teng-Zhi W U, Rong X U, et al. Effects of coiling temperature and cooling condition on transformation behavior of tertiary oxide scale[J]. Journal of Iron and Steel Research: International, 2015, 22(10): 892-896.
[15]Kofstad P, Hauffe K, Kjöllesdal H, et al. Investigation on oxidation mechanism of titanium[J]. Acta Chemica Scandinavica, 1958, 12(2): 239-266.
[责任编辑 郑淑芳]
An experimental study on oxidation behavior in low carbon steel containing Si under non-isothermal oxidizing process
LiangWeicheng,XuGuang,YuanQing,HeBei
(1. Key Laboratory for Ferrous Metallurgy and Resources Utilization of Ministry of Education,Wuhan University of Science and Technology, Wuhan 430081, China; 2. International Research Institute for Steel Technology, Wuhan University of Science and Technology, Wuhan 430081, China)
The influence of oxidation temperature on oxidation mass gain of low carbon steel was investigated by stimulating segmented heating route and oxidation atmosphere similar to that used in an industrial reheating furnace, using thermal gravimetric analyzer (TGA). Meanwhile, the morphology of Fe2SiO4was observed by scanning electron microscope (SEM). The penetration depth of the Fe2SiO4layer under different oxidation temperatures was determined by the Image-Pro Plus 6.0 software and the structure of oxide scale was analyzed by energy disperse spectroscopy. The results show that the mass gain versus time follows an almost linear relationship in HS1.21 steel, whereas it is a near parabolic relationship in LS0.25 steel after the intense oxidation temperature. After a certain holding time, the curves of mass gain in LS0.25 steel and HS1.21 steel will intersect, and the critical time point appears corresponding to the intersection point. The mass gain of low-silicon steel is larger before and smaller after the critical time point than that of high-silicon steel. The critical point gradually postpones with the increase of oxidation temperature.
low carbon steel; Si content; non-isothermal oxidation; oxide scale; Fe2SiO4; oxidation behavior
2017-05-05
国家自然科学基金面上项目(51274154);湖北省科技创新专项重大项目(2017000011).
梁伟成(1993-),男,武汉科技大学硕士生.E-mail:m15671625348@163.com
徐 光(1961-),男,武汉科技大学教授,博士生导师.E-mail:xuguang@wust.edu.cn
10.3969/j.issn.1674-3644.2017.04.002
TG176
A
1674-3644(2017)04-0245-06
