有序介孔硅微球吸附钌联吡啶修饰碳糊电极电致化学发光测定阿替洛尔
2016-09-03秦彩霞夏新泉周兴旺
秦彩霞,刘 瑶,夏新泉,陈 灵,周兴旺
(湖北师范大学 化学化工学院,湖北 黄石 435002)
有序介孔硅微球吸附钌联吡啶修饰碳糊电极电致化学发光测定阿替洛尔
秦彩霞,刘瑶,夏新泉,陈灵,周兴旺
(湖北师范大学 化学化工学院,湖北 黄石435002)
合成了一种有机-无机介孔硅微球材料,以此材料吸附钌联吡啶制备了修饰碳糊电极,并以此电极为工作电极,以Ag/AgCl电极为参比电极,铂丝电极为辅助电极,考察了以三丙胺作为Ru(bpy)32+共反应剂的电致化学发光性能。基于阿替洛尔对钌联吡啶电致化学发光增强作用,建立了药片及尿样中阿替洛尔含量测定的新方法。该方法对阿替洛尔检出限为0.5μg/mL,线性范围是5~40μg/mL.
钌联吡啶;碳糊电极;电致化学发光;阿替洛尔
阿替洛尔(Atenolol,ATN)为心脏选择性β-受体阻断剂[1],主要用于治疗高血压[2]和心血管疾病[3]等,目前其常用分析测定方法有色谱法[4]、荧光法[5]、毛细管电泳法[6]、化学发光法[7]和电化学方法[8]等。
电致化学发光(Electrochemiluminescence,ECL)[9],集化学发光和电分析化学与一体,具有两者的综合优势,不仅可控性强、灵敏度高,而且选择性好、检出限低,备受很多研究者关注。
介孔材料是孔径介于2~50nm 之间的一种多孔材料[10]。由于其具有孔径大小可调,比表面大,吸附能力强,可应用于钌联吡啶等发光试剂在电极表面的固定化,用于制作生物传感器,既能节省试剂,又能提高ECL检测灵敏度,使操作更加简便和环保。
本文利用合成的介孔硅微球吸附钌联吡啶修饰碳糊电极作为工作电极,构建了钌联吡啶-三丙胺电致化学发光体系测定阿替洛尔新方法。
1 实验部分
1.1仪器与试剂
MPI-B型多参数化学发光分析测试系统(西安瑞迈电子科技有限公司),pH/ION510型酸度计(新加坡EUTECH公司),Hitachi(日立)S-3400N扫描电子显微镜(日本日立公司); ASAP 2020 PLUS快速比表面与孔隙度分析仪(美国麦克仪器公司);AL204型电子天平(梅特勒-托利多仪器有限公司)。
钌联吡啶、三嵌段共聚物P123(聚乙二醇-聚丙二醇-聚乙二醇)购于sigma-aldrich(上海)贸易有限公司;1,2-二(三甲基硅基)乙烷(BTME)、苯基三甲氧基硅烷(PTMS)购于百灵威科技有限公司;阿替洛尔标准品购于中国食品药品鉴定研究院;十二水合磷酸氢二钠、十二水合磷酸二氢钠、氢氧化钠、铁氰化钾、十六烷基三甲基溴化铵(CTAB)、无水乙醇、盐酸、硝酸、液体石蜡均购于中国国药集团化学试剂有限公司,纯度为分析纯;石墨粉购于青岛华泰润滑密封科技有限责任公司;实验用水均为二次蒸馏水,其他实验试剂均为分析纯。
1.2介孔硅微球的合成
按照文献[11]合成有机无机杂化介孔硅微球,以1,2-二(三甲基硅基)乙烷(BTME)、苯基三甲氧基硅烷(PTMS)为硅源,三嵌段共聚物P123为模板剂,表面活性剂CTAB为共模板剂,乙醇为共溶剂,在酸性条件下制备有机-无机杂化介孔微球材料。
1.3电极的制作
取一定量钌联吡啶储备液与已合成的介孔硅微球材料混合混匀,浸泡一天后过滤干燥后备用。按一定比例取有序介孔硅微球吸附钌联吡啶的样品、光谱纯石墨粉和石蜡油混合均匀填入直径为2mm的PVC塑料管中,PVC塑料管的另一端插入铜棒作导线,制成有序介孔硅微球吸附钌联吡啶修饰的碳糊电极;并按同样方法制作不含钌联吡啶的介孔微球硅碳糊电极、普通碳糊电极作为对照。
1.4实验方法
实验用MPI-B型多参数化学发光分析测试系统进行测试同时记录循环伏安及电致化学发光信号,以自制的有序介孔硅微球吸附钌联吡啶修饰碳糊电极为工作电极,以Ag/AgCl电极为参比电极,以铂丝电极为辅助电极;实验均在10.0 mL的磷酸缓冲溶液中进行;设置电位为0.6~1.4V,光电倍增管高压为600V;采用循环伏安法进行扫描,记录发光信号。
1.5样品制备
取5片(标示含量为25mg/片)阿替洛尔药片研磨成粉状,用乙醇溶解,超声波清洗器超声后用蒸馏水稀释并定容至250mL待用。实验尿样是选自半个月内未使用任何药物的健康人尿液,尿样离心后取上清液5mL稀释至50mL,在稀释后的溶液中分别加入0.5mL、1.0mL、2.0mL的0.1mg/mL的阿替洛尔标准溶液,再加入30μg TPA稀释至10mL待测。
2 结果与讨论
2. 1有序介孔硅微球的表征
分别采用SEM、BET、IR等对合成的有序介孔硅微球进行了表征。图1是有序介孔硅微球的扫描电镜图,制备的有序介孔微球的颗粒大小相对比较均匀和饱满,但颗粒之间还存在一定程度的粘联。

图1 有序介孔硅微球的扫描电镜图
图2给出了有序介孔硅微球材料的N2吸附-脱附等温线(a)和相应的孔径分布曲线(b),其结构参数为SBET(m2/g-1):738.33,Pore volume(cm3/g-1):0.5397,Pore diameter (nm):2.9240.由图2(a)可知制备的有序介孔硅微球的吸附等温线为典型的 IV 型,表明制备的材料中存在介孔。

图2 制备的有序介孔硅材料的N2吸附-脱附等温线(a)和相应的孔径分布曲线(b)
图3是介孔硅微球与介孔硅微球-钌联吡啶-石墨粉红外光谱对照图。由图可以看出介孔硅微球有介孔二氧化硅的特征峰,1035cm-1左右的吸收带是Si-O-Si反对称伸缩振动,800 cm-1、470 cm-1左右处的峰为Si-O对称收缩振动和弯曲振动。3443 cm-1处的宽峰是结构水-OH的反对称伸缩振动峰,1629 cm-1附近的峰是水的H-O-H弯曲振动峰[12]。受掺杂比例的影响,掺杂钌联吡啶-石墨粉之后介孔硅微球峰吸收强度变小,峰位置与个数无明显变化。

图3 介孔硅微球与介孔硅微球-钌联吡啶-石墨粉红外光谱对照图
2.2不同工作电极的电化学性能比较
在[13]基础上,分别采用自制的碳糊电极、含介孔硅微球的碳糊电极、有序介孔硅微球吸附钌联吡啶修饰的碳糊电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为辅助电极;设定实验条件,采循环伏安法及电致化学发光比较了不同工作电极的电化学检测性能。设定实验条件为:10.0 mL磷酸盐缓冲溶液(0.1 mol/L,pH=8.0);设置电位为0.6~1.4V,光电倍增管高压为600V,扫描速率为100mV/s.
将介孔硅微球-Ru(bpy)32+-CPE、介孔硅微球-CPE、CPE电极分别在0.1mol/L pH=8.0 PBS溶液中进行循环扫描。介孔硅微球-CPE相比CPE电极有较大的背景电流。介孔硅微球-Ru(bpy)32+-CPE在+1.042V和+1.108V处出现了一对氧化还原峰,表明Ru(bpy)32+被固定在电极表面。
由图4可知,将上面修饰过且已经打磨好的介孔硅微球-Ru(bpy)32+-CPE电极在磷酸盐缓冲溶液中进行循环伏安扫描,随着扫描速率由25mV /s增加到200 mV /s,氧化峰电流和还原峰电流也随之线性地增加,相应地它们的峰电压分别向正极和负极移动。峰电位的差值在100mV以内,并且不随扫描速率变化;ipa≈ipc,且ipa和ipc与相应V1/2呈线性关系,由此可知该电极反应过程为可逆过程。
2.3不同工作电极的电致化学发光性能比较
设定实验条件为:10.0 mL磷酸盐缓冲溶液(0.1mol/L,pH=8.0);设置电位为0.6~1.4V,光电倍增管高压为600V,扫描速率为100mV/s.介孔硅-CPE电极50 m mol/L TPA溶液中与介孔硅-钌联吡啶-CPE电极在50 m mol/L TPA溶液中,由图5电致化学发光动力学曲线对比可知,介孔硅-钌联吡啶-CPE电极在50 m mol/L TPA溶液中可以产生电致化学发光强度,而介孔硅-CPE电极在50 m mol/L TPA溶液中几乎不产生电致化学发光强度,由此可知钌联吡啶被固定在电极表面,并且在三丙胺作为共反应剂的条件下,连续扫描10个循环可以产生稳定的ECL信号。

图4 不同扫描速率(25,50, 100 ,150, 200 mV /s)下介孔硅微球-Ru(bpy)32+-CPE
电极在磷酸盐缓冲溶液中的循环伏安图

图5 电致化学发光动力学曲线
(a):介孔硅微球-CPE电极在TPA溶液中; (b):介孔硅微球-钌联吡啶-CPE电极在TPA溶液中及曲线;(c):介孔硅微球-Ru(bpy)32+-CPE电极在含有TPA溶液中连续扫描10个循环的电致化学发光图,TPA浓度为50 m mol/L.
2.4阿替洛尔对钌联吡啶体系电致化学发光信号的增敏作用
由图6电致化学发光动力学曲线对比可知,介孔硅微球-钌联吡啶-CPE电极在50 m mol/L TPA溶液中含阿替洛尔的溶液中比在不含阿替洛尔的溶液中,其电致化学发光强度有较大程度的增强,可知阿替洛尔对钌联吡啶-三丙胺体系有增敏作用。
由于阿替洛尔存在仲胺结构,类似于三丙胺对钌联吡啶发光体系的增强作用,我们推测阿替洛尔引起电致化学发光信号增强的原因可能机理如下:
Ru(bpy)32+→ Ru(bpy)33++ e-
(1)
Ru(bpy)33++ ATN →Ru(bpy)32++ ATN+*
(2a)
ATN → ATN+*+ e-
(2b)
ATN+*→ ATN*+H+
(3)
Ru(bpy)33++ ATN*→[Ru(bpy)32+]*
(4)
[Ru(bpy)32+]*→Ru(bpy)32++ hν
(5)
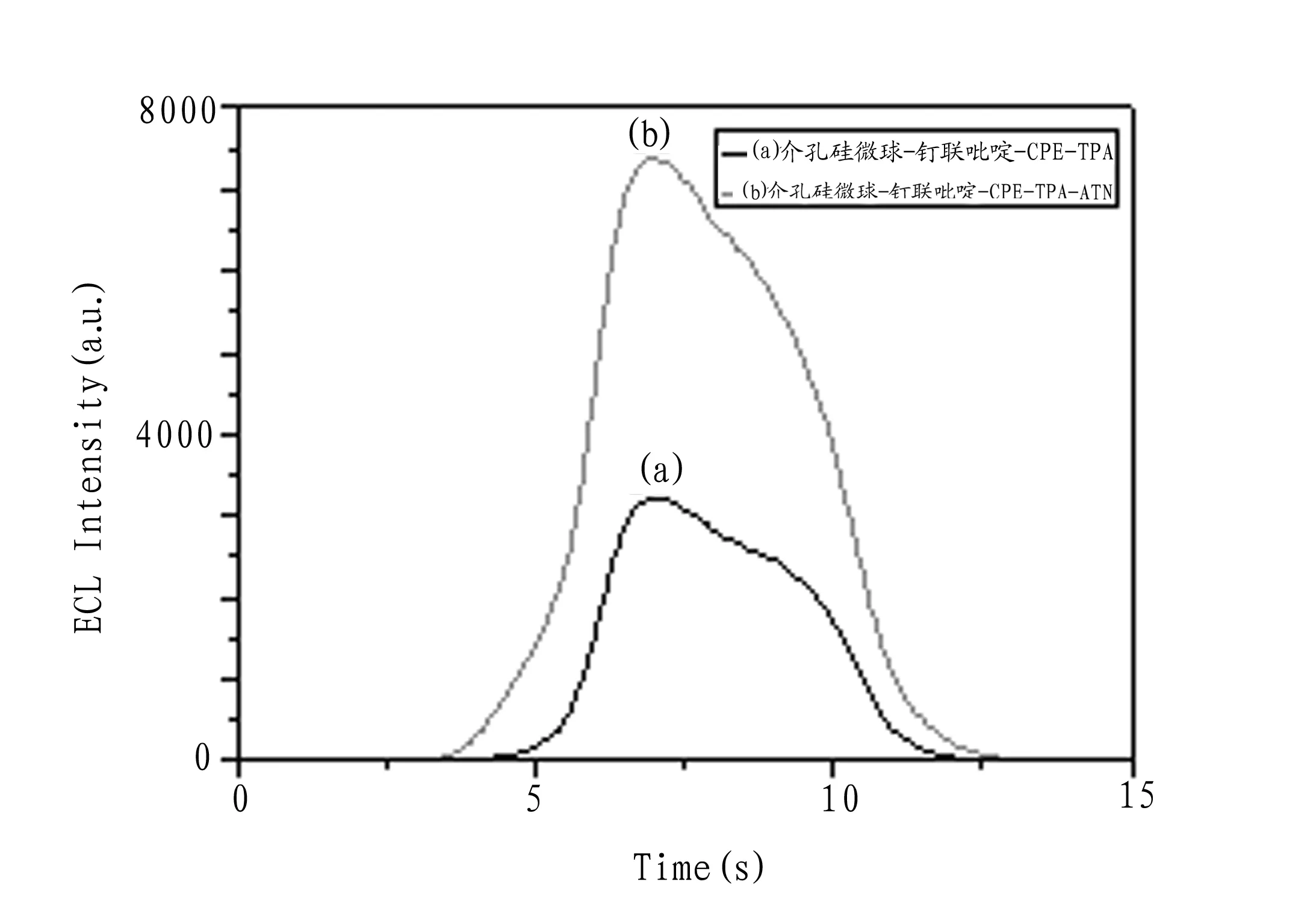
图6 电致化学发光动力学曲线
(a):介孔硅微球-钌联吡啶-CPE电极在TPA溶液中, (b):介孔硅微球-钌联吡啶-CPE电极在TPA含阿替洛尔的溶液中,TPA浓度为50 m mol/L,阿替洛尔浓度为40μg/mL.
2.5电致化学发光条件优化
实验分别考察了缓冲溶液pH值、三丙胺用量、扫描速率对钌联吡啶体系的电致化学发光的影响。
在实验中设定扫描速率为100mV/s、三丙胺用量为60μL,考察不同pH值磷酸盐缓冲溶液对钌联吡啶-三丙胺体系的电致化学发光的影响。当磷酸盐缓冲溶液pH值从6.0增加到8.0时,随着pH值的增加,电致化学发光强度增强,当pH值为8.0时电致化学发光达到最大值,随后随着pH值的增加,电致化学发光强度减弱,这可能是因为三丙胺在酸性条件下不稳定。因此,我们选择磷酸盐缓冲溶液pH值为8.0作为实验的最佳缓冲溶液pH值。
三丙胺作为钌联吡啶-三丙胺体系的电致化学发光的共反应剂,其浓度对整个体系电致化学发光有很大的影响;设定最佳扫描速率为100mV/s,控制缓冲溶液pH值为8.0,考察三丙胺用量浓度在10~90μL对钌联吡啶-三丙胺体系的电致化学发光的影响。如图7所示,结果表明三丙胺用量在60μL时电致化学发光强度达到最大,这可能是无辐射去激发过程造成的,主要归因于高浓度三丙胺对发射光的吸收。

图7 三丙胺用量对ECL的影响
在实验中,我们控制缓冲溶液pH值为8.0、三丙胺的用量定为60μL,考察了不同扫描速率对钌联吡啶-三丙胺体系的电致化学发光的影响。当扫描速率由25mV/s增加到150mV/s时,随着扫描速率的增加,电致化学发光强度增强,当扫描速率为150mV/s时,电致化学发光达到最大值,随后随着扫描速率的增加,电致化学发光强度减弱,这是因为电极反应由扩散控制。当扫描速率增加时会导致基线不稳定,为避免对阿替洛尔测定的影响及为了获得较大的电致化学发光强度,扫描速率选定为150mV/s.
2.6对阿替洛尔的分析性能评价
2.6.1在优化的检测条件下,本方法对阿替洛尔的线性范围是5~40μg/mL(y=3944+144x,R2=0.9939),检出限(S/N=3)为0.5μg/mL.
2.6.2药片中阿替洛尔含量测定药片样品制备后配制成5份平行溶液测定,测定后计算结果为平均值24.73 mg/片,药片中阿替洛尔含量标示值为25 mg/片。
2.6.3尿样中阿替洛尔含量测定取阿替洛尔标液和经处理过的尿液采用标准加入法测定尿样中阿替洛尔的含量,测定结果如表1所示。
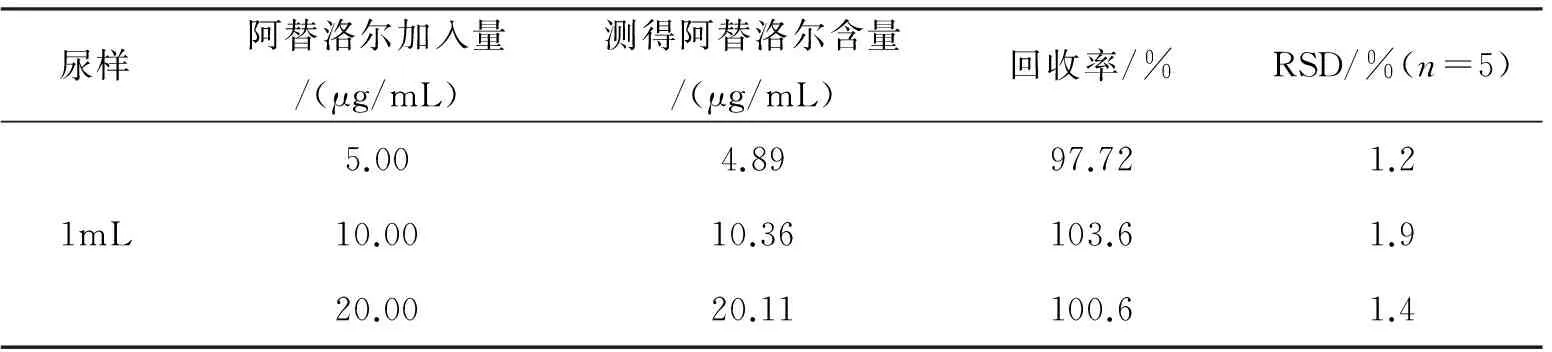
表1 尿样中阿替洛尔含量的测定
3 结论
本文合成了一种介孔硅微球材料,以此材料吸附钌联吡啶制备了修饰碳糊电极,基于阿替洛尔对钌联吡啶电致化学发光体系有很好的增强作用,建立了药片及尿样中阿替洛尔含量测定的新方法。该方法具有灵敏度高、准确性好、操作简单等优点,能够应用用于实际样品中阿替洛尔含量的检测。
参考文献:
[1]Alder A C, Schaffner C, Majewsky M, et al. Fate of β-blocker human pharmaceuticals in surfacewater: Comparison of measured and simulated concentrationsin the Glatt Valley Watershed,Switzerland [J]. Water Research, 2010, 44(3): 936~948.
[2]Hapeshi E, Achilleos A, Vasquez M I, et al. Drugs degrading photocatalytically: Kinetics and mechanisms of of loxacin and atenolol removal on titania suspensions [J]. Water Research, 2010,44(6): 1737~1746.
[3]Alireza K, Roya L, Aliyeh Hasanzadeh, et al. Flow injection chemiluminescence analysis for sensitive determination of atenolol using cadmium sufide quantum dots [J]. Molecular and Biomolecular Spectroscopy, 2016, 157: 88~95.
[4]Elgawish M S, Mostafa S M, Elshanawane A A. Simple and rapid HPLC method for simultaneous determination of atenolol and chlorthalidone in spiked human plasma [J]. Pharm J, 2011, 19: 43~49.
[5]赛那, 金蓉, 顾艳丽,等.紫外分光光度法测定阿替洛尔缓释微囊含量 [J]. 北方药学, 2015, 12(1): 19~20.
[6]Zhao K, Chen H T,Yuan Y. Platinum nanoparticle-doped multiwalled carbon nanotube modified glassy carbon electrode as a sensor for simultaneous determination of atenolol and propranolol in neutral solution [J]. Ionics 2015, 21: 1129~1140.
[7]Miao W J. Electrogenerated chemiluminescence and its biorelated applications [J]. Chem Rev,2008, 108: 2506~2553.
[8]Sir'es I, Oturan N, Oturan M A. Electrochemical degradation of β-blockers studies on single and multicomponent synthetic aqueous solutions [J]. Water Research, 2010, 44(10): 3109~3120.
[9]Liu Z Y, Qi W J, Xu G B. Recent advances in electrochemiluminescence [J]. Chem Soc Rev, 2015, 44: 3117~3142.
[10]Zhao D J. Li S Q. Morphological control of highly ordered mesoporous silica SBA-15 [J]. Chem Mater, 2000, 12: 275~279.
[11]Feng S H , Li W, Wang J X. Hydrothermal synthesis of ordered mesoporous carbons from a biomass-derived precursor for electrochemical capacitors [J]. Nanoscale, 2014, 6: 146~157.
[12] 陈和生, 孙振亚, 邵景昌. 八种不同来源二氧化硅的红外光谱特征研究 [J]. 硅酸盐通报, 2011, 30(4): 934~937.
[13]Zhuang Y F, Zhang D M, Ju H X. Sensitive determination of heroin based on electrogenerated chemiluminescence of tris(2,2'-bipyridyl)ruthenium(II) immobilized in zeolite Y modified carbon paste electrode [J]. Analyst, 2005, 130: 534~540.
Sensitive determination of atenolol based on electrogenerated chemiluminescence of tris(2,2'-bipyridyl)ruthenium(II) immobilized inmesoporous silica modified carbon paste electrode
QIN Cai-xia,LIU Yao,XIA Xin-quan,CHEN Ling,ZHOU Xing-wang
(College of Chemistry and Chemical Engineering,Hubei Normal University,Huangshi435002,China)
The mesoporous organic-inorganic hybrid microspheres was sythesized and employed to immobilize the tris(2,2'-bipyridyl)ruthenium(II) to modify carbon paste electrode. The modified carbon paste electrode as the working electrode, Ag / AgCl electrode as the reference electrode, platinum electrode as auxiliary electrode, the electrochemical and ECL behaviors of Ru(bpy)32+immobilized in ordered mesoporous silica modified carbon paste electrode was investigated. The modified electrode showed an electrocatalytic response to the oxidation of atenolol, producing a sensitive ECL signal. Under the optimum conditions, the ECL sensor showed a linear response to atenolol in the range of 5~40μg/mL with a detection limit of 0.5μg/mL. The method was successfully applied for the determination of atenolol in pharmaceutical samples and urine samples.
tris(2,2'-bipyridyl)ruthenium(II); carbon paste electrode;electrochemiluminescence; atenolol
2016—02—26
秦彩霞(1990—),女,河南驻马店人,硕士研究生,主要从事电致化学发光方面的研究.
O653.7
A
1009-2714(2016)02- 0108- 07
10.3969/j.issn.1009-2714.2016.02.024
