CuS/RGO纳米复合物的制备及对葡萄糖的无酶电化学传感
2016-01-15焦守峰
CuS/RGO纳米复合物的制备及对葡萄糖的无酶电化学传感
焦守峰
(淮北职业技术学院 医学系, 安徽 淮北235000)
摘要:以L-半胱氨酸作为硫的供应体、还原剂、联接剂采用一锅法合成了硫化铜修饰的还原石墨烯纳米复合材料,发现此纳米复合物修饰电极对葡萄糖有良好的电催化效果,并且表现出很高的抗干扰能力、优良的选择性,适用于人体中血清的检测有很好的准确性,有望应用于葡萄糖的无酶传感。
关键词:纳米复合物; 修饰电极; 电催化氧化; 无酶传感器
收稿日期:2015-07-05
基金项目:本文系国家自然科学基金项目“单一纳米电极的制备与应用”(编号:21375002)的研究成果。
作者简介:焦守峰( 1974-),男,安徽濉溪人,淮北职业技术学院医学系讲师,分析化学博士,研究方向为生物化学、药理学。
中图分类号:O657.1
文献标识码:A
文章编号:1671-8275(2015)04-0137-03
Abstract:One-pot synthesis of CuS nanoparticle-decorated reduced graphene oxide (CuS/RGO) nanocomposites was prepared with the use of L-cysteine, an amino acid, as a reducing agent, sulfur source, and linker to anchor CuS nanoparticles onto the surface of RGO sheets. It was found that the CuS nanoparticles decorated reduced graphene exhibit a remarkable catalytic performance for glucose oxidation. The proposed sensor also showed high anti-interference ability, excellent selectivity and was successfully used for glucose detecting in human serum with good accuracy and satisfactory recovery. It is believed that CuS/RGO composites show good promise for further application on non-enzymatic glucose biosensors.
0引言
糖尿病是影响人类健康的一种常见病,葡萄糖的检测对糖尿病诊断和治疗有重要的实际意义。葡萄糖酶传感器具有高度的选择性和灵敏度,但由于酶自身的特点,使其在使用中最普遍和突出的问题是缺乏持久性和稳定性,且易受温度、酸碱度和有毒化学物质的影响。
本文采用了环境友好的合成方法,以L-半胱氨酸作为硫的供体,同时又作为还原剂用一步水热法合成了石墨烯-硫化铜纳米复合物。对所制备的材料经过扫描电镜、EDS表征,发现硫化铜纳米颗粒均匀地分布在石墨烯表面,然后把制得的纳米复合物制备成修饰电极,研究其对葡萄糖的无酶传感。结果表明,运用该方法制备的传感器与以前报道的无酶传感器相比,显示出更高的敏感性,并且能避免多巴胺、尿酸、抗坏血酸的干扰。在实际样品的测定中效果良好,有望运用于人体血浆中葡萄糖的测定。
1实验部分
1.1药品与仪器
药品:氧化石墨烯,氯化铜,L-半胱氨酸,过氧化氢(30 wt %),葡萄糖,萘酚(5 wt%水溶液),其它所有药品均为分析纯,实验前不需要进一步提纯。每次电化学实验前通氮除氧20分钟,并保持在氮气环境中进行。实验中使用水全部为二次水。
仪器:日立S-4800扫描电化学显微镜(操作电压为10千伏);电化学实验在CHI 660C电化学分析仪(上海辰华仪器公司)上进行。玻碳电极(3mm内径)或其修饰电极作为工作电极,饱和甘汞电极和铂丝电极分别作为参比电极和对电极。
1.2CuS/RGO纳米复合物的制备
合成过程:首先,将氧化石墨烯溶解到水里超声1小时制成0.2 mg/mL的溶液。然后把23mg L-半胱氨酸加入到6 mL上述制备好的石墨烯水溶液里继续超声5分钟,接下来20 μL 1 M的氯化铜溶液滴加到石墨烯-L-半胱氨酸混合液中,搅拌15分钟,溶液的颜色明显由棕黄色变成深蓝棕色。最后,将上述溶液转移到反应釜中160°C加热12小时。所得产品为棕黑色,过滤,去离子水洗涤,然后再分散到水里供进一步表征、使用。
1.3CuS/RGO纳米复合物修饰电极的制备
在进行电极修饰前,玻碳电极先在麂皮上分别用0.3和0.05μm的铝粉先后对裸玻碳电极进行打磨抛光处理,然后用乙醇和二次水对其进行超声清洗,最后再用N2进行干燥处理。为了制备石墨烯-硫化铜纳米复合物修饰电极,将0.5%的萘酚溶液与4.0 mg mL-1石墨烯-硫化铜纳米复合物溶液混合,之后超声5min。通过微量注射器,将5μL的石墨烯-硫化铜纳米复合物的萘酚溶液滴加到处理干净的玻碳电极表面,然后置于室温空气中晾干备用。
2结果与讨论
2.1CuS/RGO纳米复合物的表征
为了证明石墨烯-硫化铜纳米复合物的形貌特征,它们的扫描电镜如图1所示。可以明显地看到反应生成的硫化铜颗粒比较均匀,粒径大约在80纳米左右,并且在石墨烯表面上的分散程度很好,这说明采用的方法完全可以制取理想的石墨烯-硫化铜纳米复合物。

图1 CuS/RGO扫描电镜图
2.2CuS/RGO纳米复合物修饰电极对葡萄糖的电催化
图2所示的是在4.0 mM葡萄糖存在情况下裸电极、氧化石墨烯/萘酚修饰电极和石墨烯-硫化铜纳米复合物/萘酚修饰电极的循环伏安曲线。当葡萄糖不存在时,裸玻碳电极上没有任何氧化还原峰。而在石墨烯-硫化铜纳米复合物/萘酚修饰电极上有Cu (II)/Cu(III)转换的特征峰。如图中看到,一个很宽的还原峰出现因为Cu(III)转变成了Cu (II),但是Cu (II)转化成Cu(III)的氧化峰没有明显看到,这可能是因为水的分解氧化峰把它掩盖住了。随着4.0 mM葡萄糖的加入,因为葡萄糖的不可逆电化学氧化,一个明显的不可逆的氧化峰出现在石墨烯-硫化铜纳米复合物/萘酚修饰电极上,而裸电极和氧化石墨烯/萘酚则无氧化峰出现。这些现象说明在葡萄糖的氧化过程中,硫化铜起着关键作用。其催化过程可能如下:
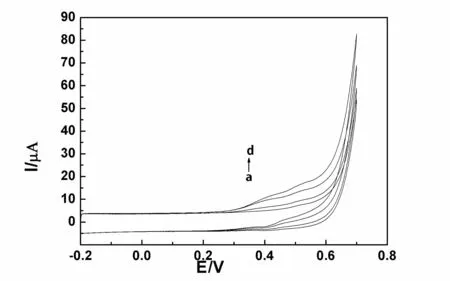
图2 对葡萄糖的电化学响应 (a)GCE;(b) GO-PDDA/GCE; (c) CuS/RGO-PDDA/GCE (d,10 mM Glucose)
(1)

(2)
2.3CuS/RGO纳米复合物修饰电极对葡萄糖的计时电流测量
图3是石墨烯-硫化铜纳米复合物修饰电极在0.15M NaOH溶液中随着葡萄糖的连续加入等到的计时电流曲线,所用电压为+0.4V,间隔时间为20秒。可以看出随着葡萄糖的不断加入,电流强度逐渐增强。电流强度的大小与加入葡萄糖的浓度成线性关系(如图4所示),在0.2 μM到12 mM范围内,线性方程为:Ipa(μA) = -18.85 + 3118.5c (mM) (R2= 0.998)。在信噪比为3 的情况下,检测限为0.05μM。
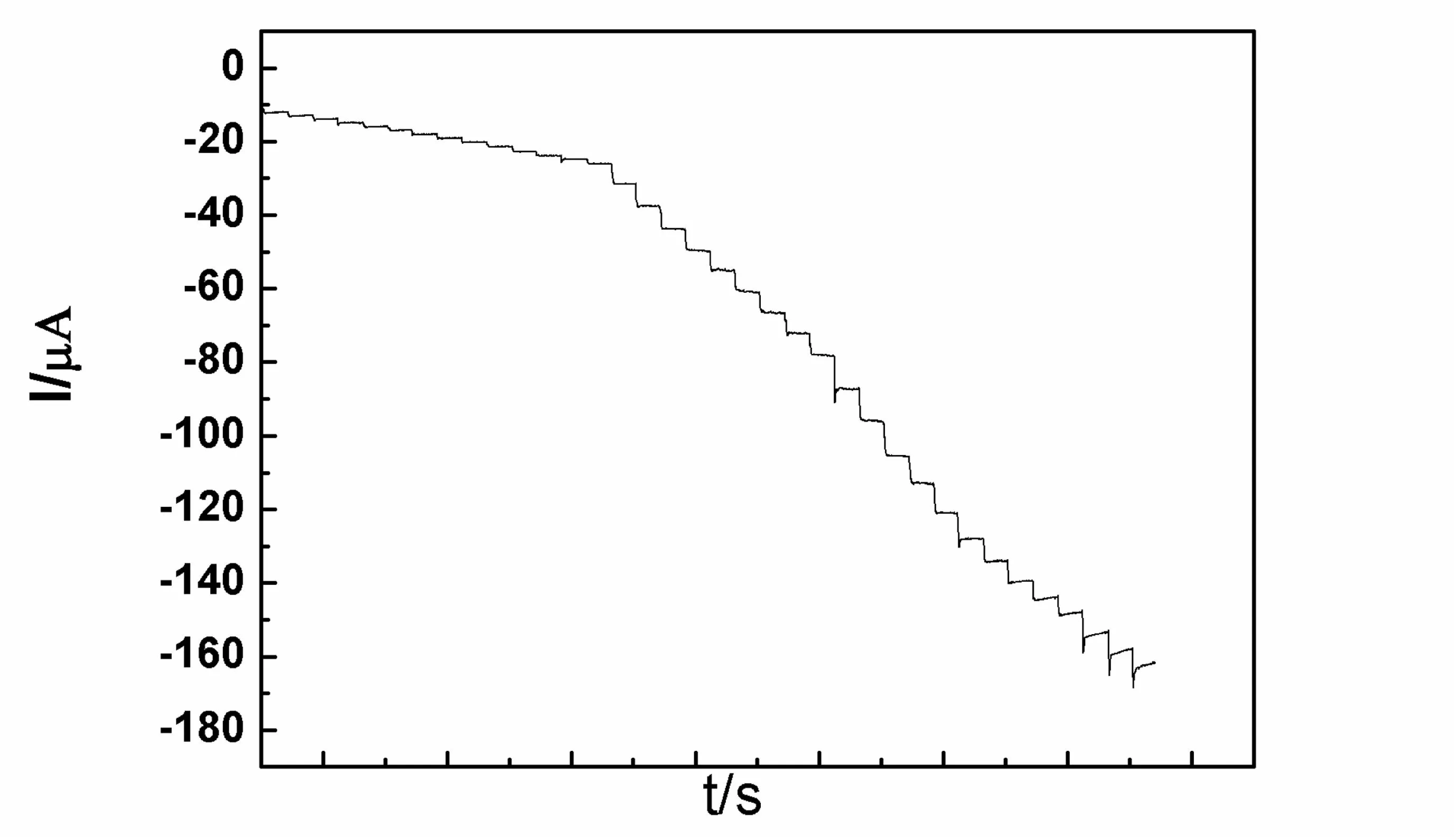
图3 CuS/RGO-PDDA/GCE 对葡萄糖的 计时电流测定
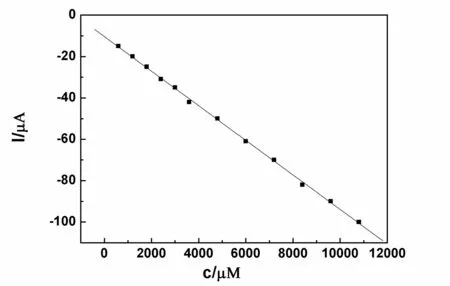
图4 电流强度与葡萄糖浓度的线性关系
2.4CuS/RGO纳米复合物修饰电极的的再现性和稳定性和抗干扰性测定
在本文中,通过对1 mM的葡萄糖的电流响应考察了所制传感器的的表现。10次连续平行测定当中,修饰电极显示出极好的稳定性能,相对标准偏差为2.4% 。8根不同的修饰电极分别适用同一种溶液,相对标准偏差为3.6%,此结果表明所制备传感器有优良的再现性。室温下每3天间隔时间测量1 mM的葡萄糖溶液,连续3周电流响应能保持在93%,这足以说明该传感器稳定性良好。另外,抗干扰能力是衡量电化学生物传感器的另外一个重要因素。各种易被氧化的干扰物如尿酸、多巴胺、抗坏血酸和碳水化合物都共存于人体的血浆中,该修饰电极也经过了类似的干扰物研究,实验通过连续加入0.10 mM混合干扰物(蔗糖、多巴胺、尿酸、抗坏血酸)到正在测定的葡萄糖溶液里,结果发现对葡萄糖的响应几乎没有任何影响。总的来看,利用该方法制备的修饰电极具有很好的稳定性和抗干扰能力。
2.5实际样品分析
为进一步证实该修饰电极的可靠性,其被用于测定实际人体血浆样品中的葡萄糖浓度。将预先处理好的20.0μL血浆样品加入到10.0 ml 0.15M的氢氧化钠底液中,通氮除氧后,持续加上0.4V的电压,葡萄糖的回收率通过标准添加纯葡萄糖溶液来考察,所得结果如表1所示。可以看到回收率达到99%以上,结果再一次证明石墨烯-硫化铜纳米复合物修饰电极可用于生物样品中葡萄糖的测定。
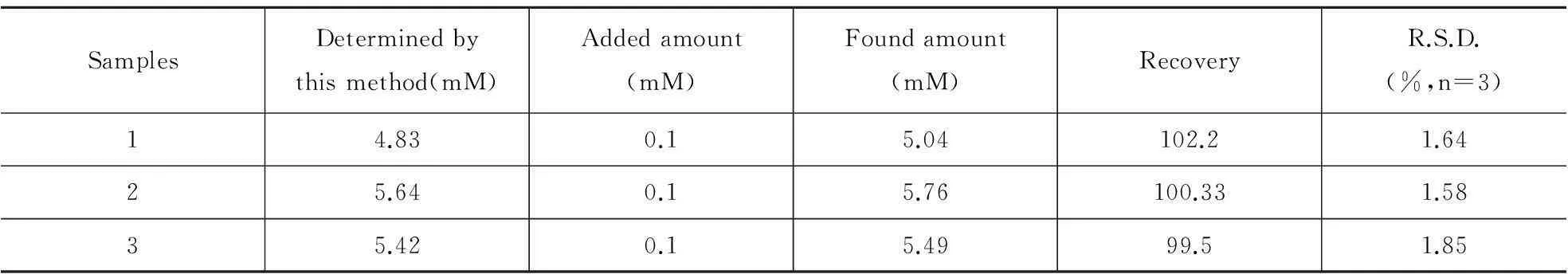
表1 对人血清中葡萄糖的测定
3小结
我们采用一锅法合成了CuS/RGO纳米复合物,在这个反应体系中,L-半胱氨酸起三种作用:还原剂、硫供体、联接剂。在加热的过程中,L-半胱氨酸能够释放出硫化氢气体,既提供硫又有还原性,促进金属硫化物纳米颗粒的形成并使氧化石墨烯还原成还原石墨烯,然后把合成的纳米复合物通过萘酚固定修饰到玻碳电极上,发现该修饰电极对葡萄糖有很好的电催化作用。此传感器检测葡萄糖的灵敏度高,检测限低,抗干扰能力强,能够用于实际样品中葡萄糖的测定。
参考文献:
[1]S.Wild,G.Roglic,A.Green,R.Sicree,H.King.Global prevalence of diabetes estimates for the year 2000 and projections for 2030[J].Diabetes Care,2004(27):1047-1053.
[2] J.C.Pickup,F.Hussain,N.D.Evans,N.Sachedina.In vivo glucose monitoring: the clinical reality and the promise[J].Biosen Bioelectron.2005(20):1897-1902.
[3] L.C.J.Clark,C.Lyons.Electrode systems for continuous monitoring in cardiovascular surgery[J].Annals of the New York Academy of Sciences,1962(102):29-45.
[4] J.W.Huang,Z.P.Dong,Y.D.Li,J.Li,J.Wang,H.D.Yang,S.W.Li,S.J.Guo,J.Jin,R.Li.High performance non-enzymatic glucose biosensor based on copper nanowires-carbon nanotubes hybrid for intracellular glucose study[J].Sens Actuators,B:Chem,2013(182):618-624.
[5] X.H.Niu,M.B.Lan,H.L.Zhao,C.Chen.Highly sensitive and selectivenonenzymatic detection of glucose using three-dimensional porous nickelnanostructures[J].Anal.Chem,2013(85):3561-3569.
[6] K.Chang,W.X.Chen.l-Cysteine-assisted synthesis of layered MoS2/graphene composites with excellent electrochemical performances for Lithium ion Batteries[J].ACS Nano 2011(5):4720-4728.
责任编辑:之者
The Fobrication of Cus/RGO Nanocomposite and
Its Electrochemical Non-enzyme Sensing of Glucose
JIAO Shou-feng
Key words:nanocomposites; modified electrode; electrocatalytic oxidation; non-enzymatic biosensors
