肝动脉栓塞术联合射频消融术治疗肝细胞癌的临床应用评价
2014-11-10邱忠华焦桂花乔元岗张伟伟樊树鹏
邱忠华 焦桂花 乔元岗 张伟伟 刘 松 胡 蒙 樊树鹏
肝细胞癌(hepatocellular carcinoma,HCC)是目前最常见的恶性肿瘤之一,我国是乙肝病毒性肝炎的高发区,肝细胞肝癌的患者往往合并乙肝后肝硬化,因此肝细胞癌的手术切除率并不十分高,另外术后复发率高(手术切除后复发率可达60%)也是困扰外科医师的另一难题[1]。近年来射频消融(radiofrequency ablation,RFA)治疗小肝细胞癌(最大径≤3cm),5年生存率与手术切除相似,且因微创性、并发症少,在临床上逐步被采用[2],但对于直径>3cm的HCC,肿瘤完全毁损率并不令人满意[3]。近年来,我科尝试应用TACE及射频消融联合治疗的肿瘤直径大于3.0cm的肝细胞癌患者。现搜集自2007年1月至2011年1月期间,98例TACE+RFA(肿瘤直径或多个瘤体直径总和在3.0~10.0cm)住院患者,与110例单纯TACE治疗进行临床对比,分析评价联合治疗的临床疗效。
1.材料与方法
1.1 材料 参照《原发性肝癌诊疗规范(2011年版)》中HCC的临床诊断原则,根据患者有无乙肝病史、AFP数值、影像学检查或肝穿刺活检临床诊断为肝细胞性肝癌,搜集208例HCC患者,肝功能Child分级为A~B级,其中男性患者130例,女性患者78例,年龄26~78岁,平均年龄50岁。癌灶数目1~4个,肝癌直径3~10cm之间,其中大于5cm的患者156例。TACE+RFA治疗组98例,对照组单独行 TACE110例。
1.2 所用设备 PHILIPS公司FD20型血管造影机,Emotiom-16德国CT机,北京WE7568-II多极肿瘤射频消融仪等。
1.3 方法
1.3.1 射频消融联合TACE方案设计:根据强化CT或者MRI显示肿瘤的大小、边界、血供情况决定是先行TACE还是先行RFA。对于血供丰富(影像学强化明显)、边界不清、瘤体大于5.0cm的病灶,先行TACE,复查肝功能恢复、凝血无异常,CT显示瘤体内存在无碘油沉积区域者,2周内行射频消融治疗。对于CT扫描边界清晰、强化不明显、血供较差、瘤体直径小于5.0cm的患者,先行RFA治疗,复查肝功能恢复后,再行TACE治疗,术中先行替加氟1.0g、奥沙利铂甘露醇注射液300ml动脉灌注,后给予碘化油+盐酸吡柔比星乳化剂栓塞。对于CT平扫呈等密度,强化不明显、血供较差的病灶,因行RFA治疗CT下定位困难者,可先行TACE,术中推注3~5ml碘化油,术后1周内行CT引导下RFA,利用正常肝组织的碘油弥漫沉积效应,衬托出乏血供瘤体的边界与范围,便于RFA的穿刺与消融。对于病灶较大者,可先行1~2次TACE术,术后2周复查CT观察碘油沉积情况,对术后残余病灶再行RFA治疗。
1.3.2 RFA技术方法:术前常规查体,行血常规,凝血常规,肝、肾功能,电解质,三抗体及丙肝抗原,AFP,心电图,胸片等辅助检查,排除RFA治疗禁忌;术前6小时禁食水,术前半小时给予鲁米那镇静药物,常规预防性应用抗生素。根据瘤体位置,患者平卧、侧卧或俯卧CT诊疗床。体表定位后,局麻下经皮穿刺至肿瘤中心,根据瘤体大小选择不同的消融程序和功率,逐步展开电极针进行消融。对小病灶可一次完成消融;对较大病灶,可改变针道进行多次消融。术中注意温度均衡上升,以尽量彻底消融瘤灶。消融范围大于病灶范围0.5~1.0cm左右,但是邻近肝包膜、门脉主干分支或肝门部的病灶,要慎重消融,严防损伤上述重要管腔和神经。治疗结束后应进行针道消融。术后常规应用止血药物,对术中疼痛明显者可给予杜冷丁、盐酸吗啡注射液等镇痛药物,术后预防应用抗生素3天。14~30天复查血常规、肝肾功能、AFP及影像学检查。
1.3.3 对照组单纯TACE:术前常规查体同RFA,排除介入治疗禁忌症。患者仰卧导管床,术前核对患者身份、手术部位及方式无误,双侧腹股沟区常规消毒铺巾,2%利多卡因局部麻醉,Seldinger穿刺法穿刺右侧股动脉,置入5F动脉导管鞘,透视下5FRH导管腹腔干造影,明确肿瘤位置及供血血管,随后超选肿瘤供血动脉(必要时使用微导管超选)。导管到位后,经导管行化疗药物灌注(替加氟注射液1.0g、奥沙利铂甘露醇注射液300ml),然后缓慢注入乳化碘油(吡柔比星+超液化碘油)栓塞肿瘤血管,对于无门脉主干(或左右支主干)癌栓的患者,肿瘤血管丰富者,必要时可给予明胶海绵胶栓塞,以阻断肿瘤血供。栓塞过程中注意患者心率、血压、血氧饱和度等生命体征变化,出现异常时减慢推注速度甚至停止,并给予相应的对症处理。有些术中患者可出现腹部胀痛不适,可予以镇痛处理。术后常规给予硫普罗宁等药物积极保肝,并给予抑酸、利尿、补液、止吐、抗炎等对症处理。对于出现栓塞后综合征的患者,及时给予镇痛、退热处理。住院时间一般10天左右,术后1个月复查血常规、肝肾功能、AFP及影像学检查。根据复查结果确定下一次TACE时间,一般情况下3次为1个疗程,间隔时间30天左右。对于碘油沉积较好,瘤体强化不明显,复查AFP数值正常的患者,可给予定期随访,随访间期为1个月、3个月、6个月~3年。
1.3.4 检测与随访:每30天、60天、90天行CT或MRI(平扫+增强)和(或)DSA随访1次,并常规行血常规、肝肾功能、凝血功能、AFP等检查。如瘤灶稳定,可每3~6个月行CT或DSA检查。
1.3.5 疗效评价:根据CT、MRI或DSA检查结果评价疗效,CT或MRI显示病变区无强化,结合DSA造影无异常肿瘤染色,为肿瘤组织完全坏死;若瘤灶部位有强化,根据CT或MRI征象须排除异常灌注和周围炎性反应,根据肿瘤组织强化的范围,对于坏死范围80%~99%为不完全坏死,坏死范围在50%~80%为部分坏死;治疗1个疗程后,于3~6个月内原发病灶增大或发现新病灶者,则判为肿瘤复发。
1.4 统计学方法 数据应用SPSS17.0统计学软件处理,采用χ2检验进行差异显著性检验,P<0.05认为差异有统计学意义。
2 结果
2.1 肿瘤毁损及复发情况 两组均在1个疗程结束后1~1.5个月行CT和DSA随访,根据病变的强化程度判断肿瘤坏死程度,单纯TACE组的完全坏死率为29.09%(32/110),而联合治疗组的完全坏死率为71.43%(70/98),两组间差异有统计学意义(P<0.05)。
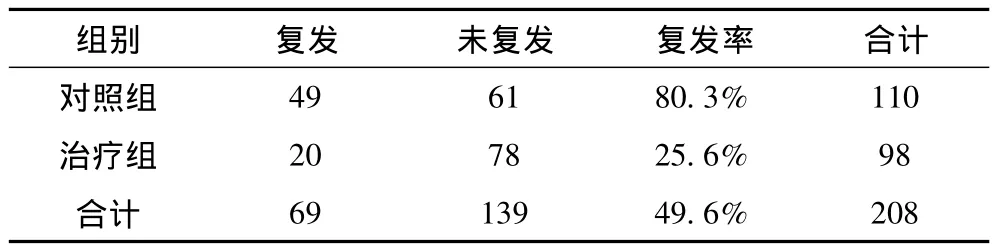
表1 两组复发情况
2.2 治疗前后血清APF情况 (见表2)。
表2 两组治疗前后AFP变化(μg/L,±s)

表2 两组治疗前后AFP变化(μg/L,±s)
注:与治疗前比较,P<0.05;组间比较P<0.05。
组别 治疗前 治疗后对照组 503.6±3.1 156±1.5治疗组525.3±2.6 120±1.6
2.3 两组治疗后生存率及中位生存期的比较 (见表3)。本实验两组1、2、3年生存率有显著差异(P<0.05)。
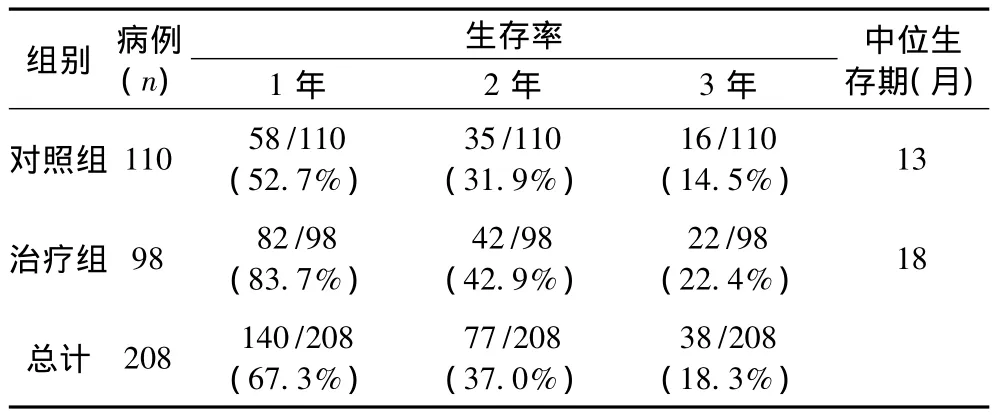
表3 两组患者生存率及中位生存期
3.讨论
肝细胞性肝癌的发病率在全球呈上升趋势[4],患者早期多数症状不明显,往往确诊时多已属于中晚期,仅有10%~30%的患者能接受外科切除手术,中晚期肝细胞性肝癌的患者平均自然生存期仅为3~6个月[5]。介入治疗为此类失去手术机会的患者提供了重要的治疗手段。
中晚期肝癌治疗的主要目标是延长患者生存期和提高患者生存质量,微创介入治疗因其微创性、可重复性具有较明显的优势。目前其治疗方式主要分两类,即以TACE为代表的肝动脉栓塞化疗和以RFA为代表的血管外局部物理消融治疗。TACE是将药物直接动脉灌注至肿瘤血管,引起肿瘤坏死,另外碘化油、明胶海绵等栓塞材料的应用,还可有效阻断肿瘤组织的血流灌注。但单纯TACE治疗体积较大肿瘤病灶时治疗常不彻底术后肿瘤残余及复发率仍较高[6]。据文献报道,治疗后仅有30%左右的病例肿瘤组织呈完全性坏死[7],而大部分病例肿瘤组织坏死不完全,这可能是导致其生存期缩短的重要原因。肿瘤组织坏死不完全可能与肝脏有双重供血、滞留碘油的瘤细胞代谢清除、TACE后癌灶周围侧支循环的形成、供血动脉再通以及多支动脉供血等种种因素有关。另外反复多次的TACE治疗加重了患者的肝功能损害,对患者的生存率产生了直接的影响。
经皮射频消融术因其侵袭性小、操作简单、疗效肯定,是肝癌治疗的一种新的途径[8,9]。肝肿瘤的RFA治疗已由10多年的历史,其临床疗效逐步得到认可。Huang等[10]在2005年公布的一组随机临床研究数据证实了手术治疗和RFA治疗在总生存率和无病生存率上无显著差异。射频消融治疗肝癌的效果与其所产生的组织坏死灶大小直接相关,RFA对于直径小于3cm的小肝癌治疗效果较好,特别是对伴有严重肝硬化、位于肝门区毗邻大血管的肝癌,可明显减少血管损伤的发生,治疗效果明确。多数研究证实了RFA可对小肝癌(直径<3cm病变)有根治的效果,RFA以其较短的住院时间及较高的生存率而被临床广泛应用[11]。研究表明,90%以上的小肝癌可以被射频消融完全破坏,对于短期内肿瘤的原位复发的小病灶也有很好的抑制作用[12]。近几年来,多电极射频针的出现,提高了肿瘤毁损体积,可产生直径5cm的凝固毁损灶,与其他局部治疗方法相比,肿瘤完全坏死率较高、肝内复发率较低,而治疗次数减少、患者生存时间延长[13]。但是,RFA也有其治疗缺陷,治疗不彻底可导致癌灶残留是RFA治疗过程中的重要问题。中晚期肝癌大多数瘤体较大,对于直径>5cm的病灶,生长不规则,难免出现三维空间上的无消融区,导致治疗不彻底,影响了治疗效果和预后。另外,对于靠近大血管的肿瘤,由于血流带走热量,降低治疗温度导致肿瘤不能完全灭活。
近来少数研究表明,TACE术后未栓塞的肿瘤组织可出现代偿性增生,增殖活性亦相对得到增强,说明TACE治疗后残存的肿瘤细胞仍会存在复发和转移。而综合治疗可弥补TACE的不足,达到互相增强作用的效果,改善肝癌治疗的总体预后。RFA及TACE在肝癌的治疗上各有优缺点,且优势互补,这就为两者的联合使用创造了契机。TACE治疗可减少肿瘤的血供,增强了肿瘤消融治疗的坏死程度及治疗面积[14];而RFA可增加肿瘤组织对化疗药物的摄取敏感度,提高肿瘤细胞对药物的吸收,从而有效地预防肿瘤复发可能。有研究表明,区域动脉灌注化疗使肿瘤局部具有高浓度的化疗药物,而热消融可使癌细胞通透性增加,化疗药物更易进入肿瘤细胞,因此RFA与TACE联合治疗肝癌可以明显提高疗效。
本研究结果表明比较单纯TACE与射频消融联合TACE治疗后两组的肿瘤灭活情况、术后复发率及患者生存期等方面,有明显的差别,这与报道一致[15]。随着当代医学医疗科技的发展与进步,肝脏恶性肿瘤的综合介入治疗前景广阔,但仍缺乏大宗临床试验数据评估其疗效,同时治疗过程中应遵循个体化治疗的原则,选择最佳的个体化治疗方案。
1 吴盂超,沈峰,吴东.原发性肝癌的外科治疗[J].中华肝胆外科杂志,2005,11:75-77.
2 Park MH,Rhim H,Kim YS,etal Spectrum ofCT findings after radiofrequency ablation of hepatic tumors[J].RadioGraphics,2008,28:379-390.
3 Xu HX,Lu MD,Xie XY,etal.Prognostic factorsfor long—termoutcome after percutaneoua thermal ablation for hepatocellular carcinoma:a survival analysis of 137 consecutive patients[J].ClinRadiol,2005.60:1018-1025.
4 Lam CM,Ng KK,Poon,etal.Impact of radiofrequency ablation on the Management of patients with hepatocellular carcinoma in a specialized centre[J].British Joumal of Surgery,2004,91:334-338.
5 刘允怡,赖俊雄.肝癌治疗新进展[J].临床放射学杂志,2008,2:2-5.
6 Llovet JM Bruix J.Novel advancements in the management of hepatocellular carcinoma in 2008 J[J].J Hepatol,2008,48(1):S20-S37.
7 Takayasu K,Arii S,Lkai I,etal.Prospective cohort study of transarterial chemoembolization for unresectable hepatocellular carcinoma in 8510 patients[J].Gastroenterology,2006,131(2):461-466.
8 Teratani T Yoshida H Shiina Setal.Radiofrequency ablation for hepatocellular carcinoma in so-called high-risk locations J[J].Hepatology,2006,43:1101-1108.
9 Yang B Zou JXia Jetal.Risk factors for recurrence of smallhepatocellular carcinoma after long-term follow-up of percutaneous radiofrequency ablation J[J].Eur JRadiol,2011,79:196-200.
10 Huang GT,Lee PH,Tsang YM,etal.Percutaneous ethanol injection versus surgical reseetion for the treatment of small hepatocellular carcinoma:a prospective study[J].Ann Surg,2005,242:36-42.
11 Netto GJ,Altrabulsi B,Katabi N,etal.Radio-frequency ablation of hepatocellular carcinoma before liver transplan-tation:a histologic and‘TUNEL’study[J].Liver Int,2006,26(6):746-751.
12 Kuvshinoff BW,Ota DM.Radiofrequency ablation of liver tumors:influence of technique and tumor size[J].Sur-gery,2002,132(4):605-612.
13 shiina S,Teratani T,Obi S,etal.Prospective randomized controlled trial comparing percutaneous radio-frequency ablation and percutaneousethanol injection therapy for small hepatocellular carcinoma[J].Gastroenterology,2000,118:959.
14 Goldberg SN,G azelle GS,M ueller PR.Therm al ab lation th erary for focalm al ignan cy:a un ited approach to underlying princip le,techniques,and d iagnostic imaging gu idance[J].AJR,2000,174:323.
15 Koda M,Murawak Y,Mitsuda A,etal.Combination therapy with transcatheter arterial chemo-embolization and percutaneous ethanol injection along for patients with small hepatocellular carcinoma:a randomized control study[J].Cancer,2001,92(6):1516-1524.
