离体猪胰腺钬激光消融的实验研究
2014-08-04邢铃王东王凯旋张晓兰张华高金震东
邢铃 王东 王凯旋 张晓兰 张华高 金震东
钬激光是以钇铝石榴石(YAG)为激活媒质,掺入敏化离子铬(Cr)、传能离子铥(Tm)、激活离子钬(Ho)的激光晶体(Cr∶Tm∶Ho∶YAG)制成的脉冲固体激光装置产生的新型激光。钬激光的优点:(1)波长为2 140 nm,恰位于水的吸收范围,易于被水吸收;(2)脉冲时间0.25 ms,远远小于组织热传导时间(1 ms),故对周围组织损伤极小,组织穿透深度小于0.4 mm,术后反应轻,伤口愈合快[1];(3)脉冲式激光的热效应仅于组织表层,脉冲之间的冷作用限制了组织的损害;(4)使用光纤传输,可与各种内镜或穿刺针联合使用;(5)手术中通过气化进行治疗,修整组织边缘光滑有坡度,止血效果好;(6)对术中的监护仪器无干扰;(7)钬激光可借助内镜用于对人体组织进行消融、气化、切除、凝固及碎石治疗。鉴于以上优点,钬激光已被应用于泌尿外科[2-3]、皮肤科[4]、神经外科[5-8]及耳鼻喉科[9]等诸多疾病的治疗。本研究观察不同参数设置的钬激光对离体猪胰腺的消融范围,为内镜超声引导下钬激光对胰腺肿瘤的临床应用提供实验基础。
材料和方法
一、实验材料及设备
新鲜离体猪胰腺,体质量为0.75~1 kg。钬激光治疗机,钬激光光纤(端发射)及配套的电极踏板均由美国科医人医疗激光公司提供。
二、实验方法
根据钬激光的能量、时间、频率3个作用参数,在预实验基础上确定的可取值范围内各分别取5个数值进行不同组合,建立一个包含125种不同组合的随机化参数表。光纤消融之前,先剥离光纤末端的外包层约2 mm,露出光纤芯,使其头端透光(红色指引光)。然后将光纤插入离体猪胰腺头部或体部,设置参数表中的参数,踩下电极踏板开始消融,共行125次消融。消融后超声内镜探头测量消融范围,然后沿光纤剖开胰腺,用游标卡尺(精确度0.05 mm)测量消融灶的长径(a)、短径(b)及斜径(c)。长径指消融灶在光纤所在直线上的最大距离的一半;短径指消融灶在垂直于光纤的直线上的最大距离的一半;若组织均匀,光纤在组织中均匀分布,则斜径等于短径。由于钬激光的光纤为头端发射光纤,所以消融灶的形状类似椭圆球体,消融灶体积V=4/3πabc。完整切下消融部位,10%甲醛固定,HE染色,光镜下观察组织学改变。
三、统计学处理
结 果
一、消融灶的内镜超声征象
消融部位呈云雾状高回声区,随着时间的延长,云雾状区域呈椭圆形逐渐扩大(图1)。
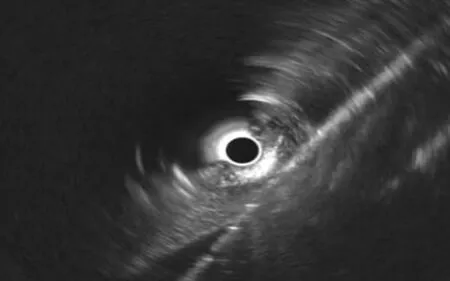
图1 消融灶的内镜超声征象
二、消融灶的胰腺组织学改变
切开消融部位,肉眼见消融灶截面近似椭圆形,中心为碳化坏死组织,有许多细微的小颗粒,边缘为灰白色损伤区,与周边正常胰腺组织分界较清晰。钬激光的能量越大,消融范围越大(图2)。显微镜下见消融灶中间为“水池样”空腔,周围为胰腺组织凝固性坏死区,胰胞结构不清,核固缩,染色质浓染,坏死胰腺组织的四周可见炎症细胞浸润,边缘为正常的胰腺组织(图3)。
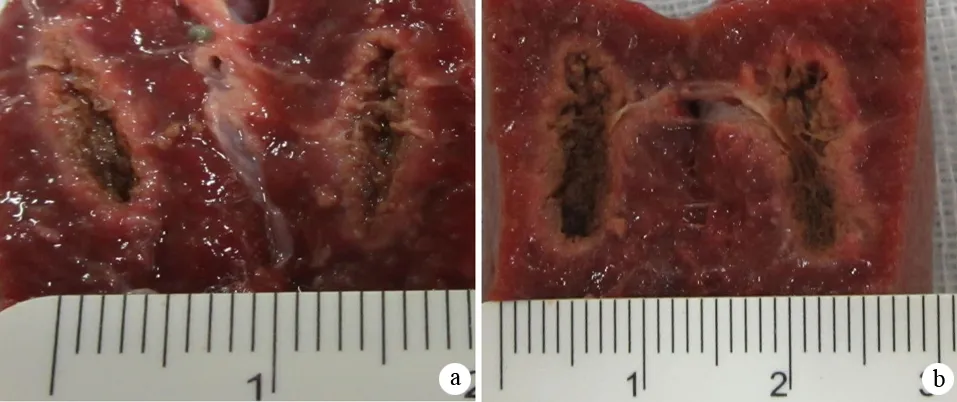
图2 参数为25 s、5 Hz、1.0 J(a)及25 s、5 Hz、1.8 J(b)的钬激光消融灶
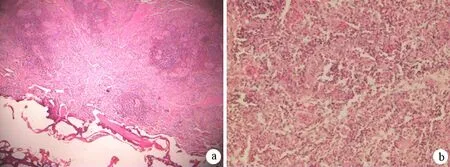
图3 参数为25 s、5 Hz、1.0J(a)及25 s、5 Hz、1.8 J(b)钬激光消融灶的组织学改变(a ×10,b ×20)
三、不同参数钬激光对消融灶体积的影响
钬激光的作用时间、频率、能量均呈正方向影响消融灶的体积,当作用时间延长、频率增强或能量增加时,消融灶的体积也会随之增大,其中频率的影响程度最强,其次是时间,再次是能量(P值均<0.01,图4)。分析总共125次的实验样本,没有发现参数对消融灶体积的拐点,即在现有的5个数值水平上,数值越大,消融灶体积也就越大,最优的参数组合是25 s,25 Hz,1.8 J。此外,时间与频率,频率与能量之间存在交互作用。在不同时间作用下频率的变化对消融灶体积的影响存在差异;同样,在不同频率作用下时间的变化对消融灶体积的影响亦存在差异。在不同频率的作用下能量的变化对消融灶体积的影响存在差异;同样,在不同能量的作用下频率的变化对消融灶体积的影响亦存在差异,且差异均具有统计学意义(表1)。

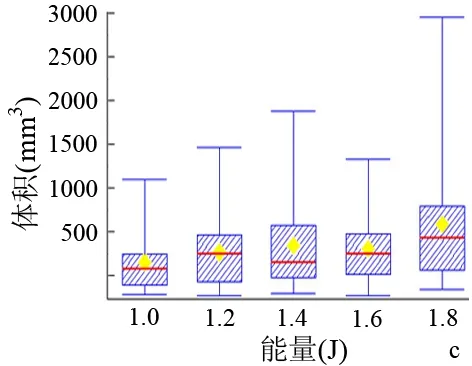
图4 钬激光作用不同时间(a)、频率(b)、能量(c)后消融灶体积的变化
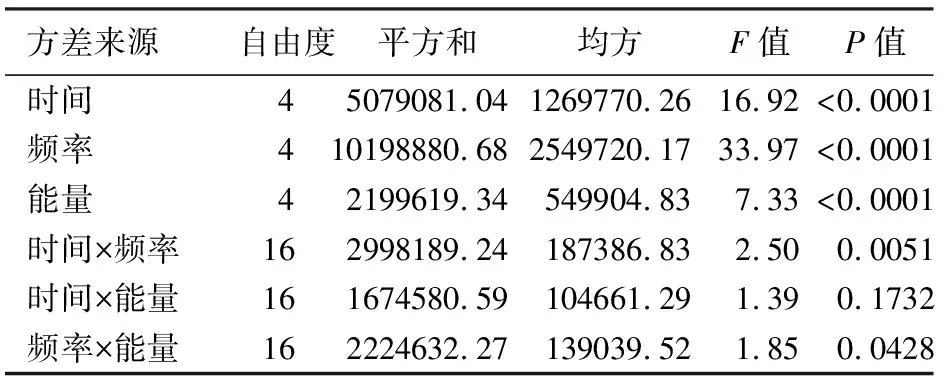
表1 钬激光作用时间、频率、能量效应的检验表
以时间、频率、能量为变量和取对数后的体积为因变量的线性回归模型的方程式为ln(消融体积)=β0+β1×时间+β2×频率+β3×能量(β为回归系数),模型的决定系数R2=0.68。分析结果表明该模型能够较好地解释不同参数组合下体积的变化(表2,图5)。
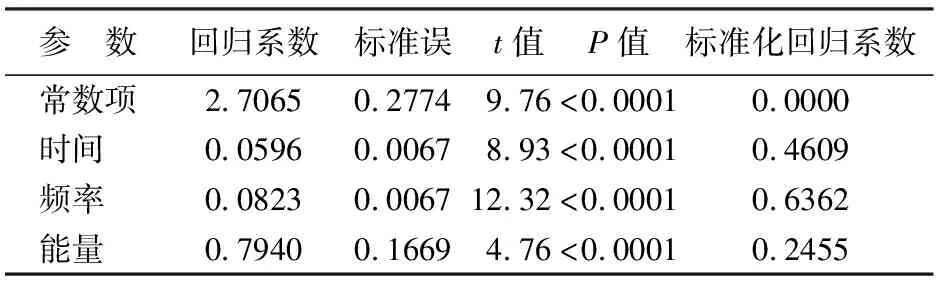
表2 消融灶体积线性回归分析模型的系数及检验值
讨 论
胰腺癌是恶性程度较高的肿瘤之一,其发病快,病死率高,手术缓解率较低,且创伤大,预后不良,平均生存期不足半年,故胰腺癌的治疗已经成为医疗工作者致力于研究的重点。内镜超声引导下治疗胰腺肿瘤已经成为重要的治疗手段,主要有内镜超声引导下的无水乙醇注射治疗[10-11]、放射性粒子植入治疗[12-15]、射频消融治疗及钕-钇-铝激光治疗[16-17]、双频激光消融治疗等等。内镜超声引导下的光动力消融治疗目前只有活体猪正常胰腺的实验报道[18-19],尚未应用于临床。
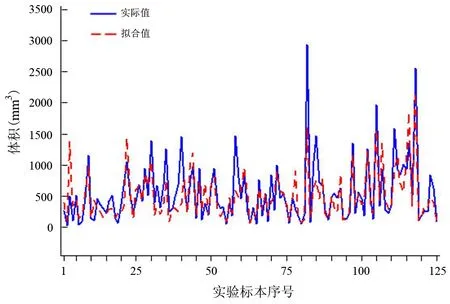
图5 消融灶体积线性回归分析模型的拟合值与实际值的分布图
本研究应用钬激光对猪正常胰腺进行消融治疗。虽然钬激光的能量、时间、频率有较多的可设定值,但由于钬激光作用强度较剧烈,几秒钟就可使组织达到明显坏死,故本研究在大量预实验的基础上,设定既可以使组织坏死,又考虑到以后体内实验安全性的可取值的范围。在此范围内,3个参数各取5个数值,其中时间及频率都是成倍递增的,而能量的每个数值之间相差0.2 J,人为地减少了能量对作用范围的影响。
为了模拟人体环境温度,在实验前首先将离体胰腺在37℃温箱内预热,这样所得到的消融范围更接近于人体。同时为了模拟胰腺肿瘤周围血管及组织液的环境,本研究组进行了有水及无水两种环境下钬激光消融的实验,即将离体猪胰腺浸入缓冲液中和未浸入缓冲液中两种状态。预实验证明,这两种状态下所获得的消融范围相似,本实验是将猪胰腺放入缓冲液中。
本研究结果显示,钬激光的作用时间、频率、能量均呈正方向影响消融灶的体积,且时间与频率、频率与能量之间存在交互作用,并建立以时间、频率、能量为变量和取对数后的体积为因变量的线性回归模型的方程式,为下一步内镜超声引导下钬激光消融治疗胰腺肿瘤的体内实验提供实验依据。
参 考 文 献
[1] Erhard MJ,Bagley DH.Urologic applications of the holmium laser:preliminary experience[J].J Endourol,1995,9(5):383-386.
[2] Parsons RL, Campbell JL, Thomley MW, et al. The effect of the laser of dog bladders: a preminary report[J]. J Urol,1966,95(5):716-717.
[3] Johson DE,Gromeens DM,Price RE. Use of the holmium: YAG laser in urology[J]. Lasers Surg Med,1992,12(4): 353-363.
[4] 朱菁,张慧国,聂凡,等. HO: YAG激光治疗巨大型及腔内型尖锐湿疣13年总结[J]. 应用激光,2007,27(4): 351-354.
[5] Stellar S,Polanyi TG. Lasers in neurosurgery: a historical overview[J]. J Clin Laser Med Surg,1992,10(6): 399-411.
[6] Sakai T,Fujishima I,Sugiyama K,et al. Interstitial laserthermia inneurosurgery[J]. J Clin Laser Med Surg,1992, 10(1): 37-40.
[7] 丁新民,保庭毅. 钬激光生物学效应的研究进展[J]. 医学研究生学报,2005,18(5): 465-466.
[8] 吴江平,严文兵,郭宇明. 钬激光经尿道输尿管碎石术的临床应用(附56例报告)[J].广州医药,2004,35(5): 56-57.
[9] 万涛,田兴华,李国伟.微波治疗耳鼻喉科疾病的并发症及预防[J].临床耳鼻喉科杂志,2001,15(8):378-379.
[10] Jürgensen C, Schuppan D, Neser F, et al. EUS-guided alcohol ablation of an insulinoma[J]. Gastrointest Endosc,2006,63(7):1059-1063.
[11] Artifon EL, Lucon AM, Sakai P, et al. EUS-guided alcohol ablation of left adrenal metastasis from non-small-cell lung carcinoma[J]. Gastrointest Endosc,2007,66(6):1201-1205.
[12] 金震东,李兆申.消化超声内镜学[M].第2版. 北京:科学出版社,2011:870.
[13] Chang KJ. EUS-Guided Fine Needle Injection and anti-tumor therapy[J]. Endoscopy, 2006, 38 Suppl 1:S88-S93.
[14] Sun S, Qingjie L, Qiyong G, et al. EUS-guided interstitial brachytherapy of the pancreas:a feasibility study[J]. Gastrointes Endosc,2005,62(5):775-779.
[15] Lah JJ, Kuo JV, Chang KJ, et al. EUS-guided brachytherapy[J]. Gastrointest Endosc,2005,62(5):805-809.
[16] Petrone MC, Arcidiacono PG, Carrara S, et al. US-guided application of a new hybrid probe in human pancreatic adenocarcinoma:an ex vivo study[J]. Gastrointest Endosc,2010,71(7):1294-1298.
[17] Matteo F, Grasso R, Pacella OM, et al. EUS-guided Nd:YAG laser ablation of a hepatocellular carcinoma in the caudate lobe[J]. Gastrointest Endosc,2011,73(5):632-636.
[18] Chan HH, Nishioka NS, Mino M, et al. EUS-guided photodynamic therapy of the pancreas: a pilot study[J]. Gastrointest Endosc,2004,59(1):95-100.
[19] Yusuf TE, Matthes K, Brugge WR. EUS-guided photodynamic therapy with verteporfin for ablation of normal pancreatic tissue: a pilot study in a porcine[J]. Gastrointest Endosc,2008,67(6):957-961.
