超临界CO2酶法合成低热量三酰甘油工艺条件的优化
2014-03-13于殿宇张春艳李万振解桂东江连洲
于殿宇 张春艳 宋 鹏 李万振 解桂东 江连洲
(东北农业大学食品学院,哈尔滨 150030)
油脂是食品的重要组成成分,能赋予食品独特的口感、风味和质地,但大量摄入会引发高血脂、心脏病和动脉硬化等慢性病,严重损害人类的健康[1-3]。以往的油脂代用品和模拟品会不同程度地影响人类的基础代谢,有些产品的风味和口感也不易保存[4-5]。因此,开发特性、口感和风味效果与天然油脂相同的功能性油脂已成为各国食品行业的热门研究方向[6-8]。即将短链脂肪酸和油脂进行酯化,形成的至少包含一个低热量短链脂肪酸和一个不被吸收长链脂肪酸(被称为构造脂质)的长短链三酰甘油[9-10]。因长短链脂肪酸具有发热量低,可刺激肠道电解质和水的吸收等特点,故长短链三酰甘油具有降低血糖水平和胆固醇水平的功能[11-12]。低热量油脂代用品在综合评分中优于以往的油脂代用品和模拟品[13-14]。
近年来,生产低热量油脂的方法大都是在常规的方式下进行,不仅生产周期长,且酯化率低,而在化学随机酯交换反应研究背景下研究的超临界CO2酶法酯交换反应,是近年来生物工程新开拓的领域[15-16]。在这种状态下,反应物在超临界CO2流体中的溶解度大,且超临界CO2流体的传质速率高,进而使反应物能与催化剂充分接触,提高酯化反应的速度,大大缩短反应时间。这些特点使其在食品工业上的应用具有广阔的发展前景。
本试验以短链脂肪酸与葵花油的甘油酯混合进行酯化反应,利用具有更高活性的脂肪酶Lipozyme RM IM,对超临界CO2状态下酶法合成长短链甘油酯进行了初步研究,并确定了酯化条件。
1 材料与方法
1.1 试剂
葵花油:金龙鱼嘉里粮油(营口)有限公司;脂肪酶Lipozyme RM IM:丹麦诺维信公司;二氧化碳(纯度>99.9%):哈尔滨黎明气体有限公司;乙酸甲酯标准品:美国sigma公司;正己烷(色谱纯)、甲醇(色谱纯)、乙酸(分析纯)、乙酸酐:天津市科密欧化学试剂有限公司;氢氧化钾(分析纯):天津光复精细化工研究所;浓硫酸:固安县清运化工厂。
1.2 设备
高压反应釜:江苏太仓市医器械厂;恒温水浴锅:上海申生科技有限公司;DF-101S集热式恒温加热磁力搅拌器:巩义市英峪高科仪器厂;低速离心机:北京医用离心机厂;7890A型气相色谱仪:安捷伦公司。CP-Sil 88毛细管柱(100 m×0.25 mm i.d×0.2μm):美国Varian公司。
1.3 试验方法
1.3.1 酶促酯化方法
向反应釜中加入一定比例的乙酸、乙酸酐、葵花油、甘油及一定量的脂肪酶和纯净水,放入转子,进行充分搅拌,确保反应物混合均匀。将反应釜密封后充入少量CO2以置换出反应釜中的空气,同时试漏,确定反应釜密封情况良好不漏气后,在加压泵的作用下充入CO2使反应釜内达到一定压力,然后将反应釜置于水浴锅中,调节转速至200 r/min,在一定温度下反应一定时间。
1.3.2 酯化率的测定分析
取1.3.1中的液体产物3~5滴,称重,采用无水硫酸钠过滤除去水分,以1%H2SO4-甲醇甲酯化后溶于正己烷,供气相色谱分析[17]。乙酸的质量含量通过利用乙酸甲酯标准品绘制的标准曲线算出。
检测器:FID;进样口温度:250℃;检测器温度:250℃;空气压力:50 kPa;氢气压力:60 kPa;氮气压力:220 kPa;程序升温:70℃时保持 4 min,然后以13℃/min的升温速率将温度升至175℃,保持此温度27 min,最后以4℃/min的升温速率将温度升至215℃,保持31 min。
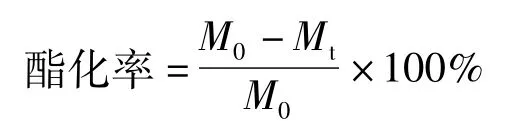
式中:M0为反应初始体系中酸的单位含量;Mt为反应完毕后体系的游离酸的单位含量。
2 结果与分析
2.1 单因素试验
2.1.1 反应压力对酯化率的影响
固定反应温度55℃,反应时间15 h,水分添加量为2%,酶用量为4%,乙酸与葵花油底物比为3∶1,反应压力分别取8、9、10、11、12 MPa进行酯化反应,测定样品的酯化率。
压力是超临界酯化反应的主要影响因素,压力不同必然影响底物浓度从而影响反应速率及酯化率。如图1所示,随着反应压力的增加,酯化率先增加,后有所下降。随着压力的不断增大,反应物与酶接触面积不断增大,反应速率加快,从而相应提高转化率,并缩短了反应时间。但当压力达到11 MPa以上时,酯化率略有下降,因此反应压力为11 MPa较为适宜。
2.1.2 反应温度对酯化率的影响
固定反应压力11 MPa,反应时间15 h,水分添加量为2%,酶用量为4%,乙酸与葵花油底物比为3∶1,反应温度分别取45、50、55、60、65℃进行酯化反应,测定样品的酯化率。
如图2所示,随着温度的升高,酯化率逐渐增大,当达到一定温度时,再升高温度,酯化率反而呈下降趋势。这是由于随着温度的增加,一方面,反应物在超临界流体中的溶解度会有很大提高,另一方面,酶的催化效率升高,当温度到达55℃时,酶的结构逐渐被破坏使其活性逐渐下降,从而影响了反应效果。由此可见,此催化酯化反应中脂肪酶Lipozyme RM IM的最适温度在55℃。本试验选择反应温度为55℃。
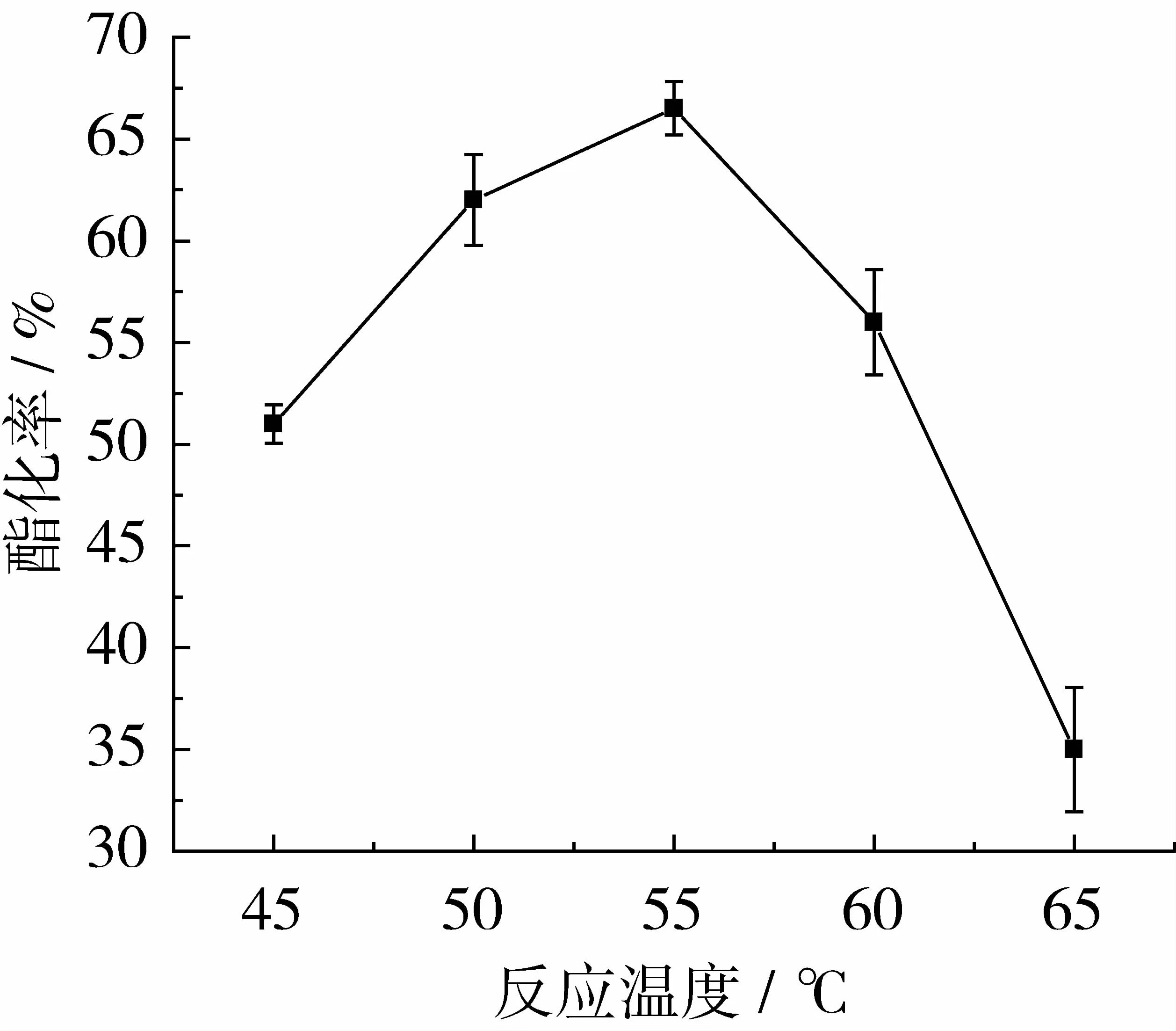
图2 反应温度对酯化率的影响
2.1.3 反应时间对酯化率的影响
固定反应压力11 MPa,反应温度55℃,水分添加量为2%,酶用量为4%,乙酸与葵花油底物比为3∶1,反应时间分别取 5、10、15、20、25 h进行酯化反应,测定样品的酯化率。
如图3所示,随着反应时间的延长,酯化率不断提高,当反应时间达到15 h后,酯化率先下降后趋于平缓,这是因为随着反应时间的延长,底物浓度和酶活力开始降低,反应速度逐渐减小,酯化率最后趋于平缓,是因为酯化反应达到平衡后略向逆反应方向进行的缘故。综合考虑反应时间以15 h为宜。

图3 反应时间对酯化率的影响
2.1.4 体系水份添加量对酯化率的影响
固定反应压力11 MPa,反应温度55℃,反应时间15 h,酶用量为4%,乙酸与葵花油底物比为3∶1,水分添加量分别取1%、2%、3%、4%、5%进行酯化反应,测定样品的酯化率。
如图4所示,随着水分的增加,酯化率先升高后降低,结合到葵花油中的乙酸含量随着水分的增加而提高,这是由于少量水的存在,起着增加酶活性的作用,促进酸解反应,而且少量水分有利于保持酶活性部位构象,使酶充分发挥活力。当水分添加量不足2%时酯化率低,是因为含水量不足以使酶发挥其最大活性;当反应体系中水分添加量超过2%时酯化率下降,是由于水量过多时会在酶的活性位点上形成一层水的屏障,阻碍了酶促反应的进行。因此,体系水分添加量为2%较为适宜。

图4 体系水分添加量对酯化率的影响
2.1.5 酶用量对酯化率的影响
固定反应压力11 MPa,反应温度55℃,反应时间15 h,水分添加量为2%,乙酸与葵花油底物比为3∶1,酶用量分别取 1%、2%、3%、4%、5%进行酯化反应,测定样品的酯化率。
如图5所示,随着酶用量的增加,酯化率随之提高后略有下降,原因是随着酶用量的增加,酶分子与底物接触的机会增加,反应速度加快,酯化反应程度提高,但当酶用量达到4%后,酯化率略有下降趋势,这是由于酶量大时,水量不足,水解慢,偏酯的生成量少,限制后续酯化反应,进而对酯化率造成影响。故酶用量选择4%最为适宜。
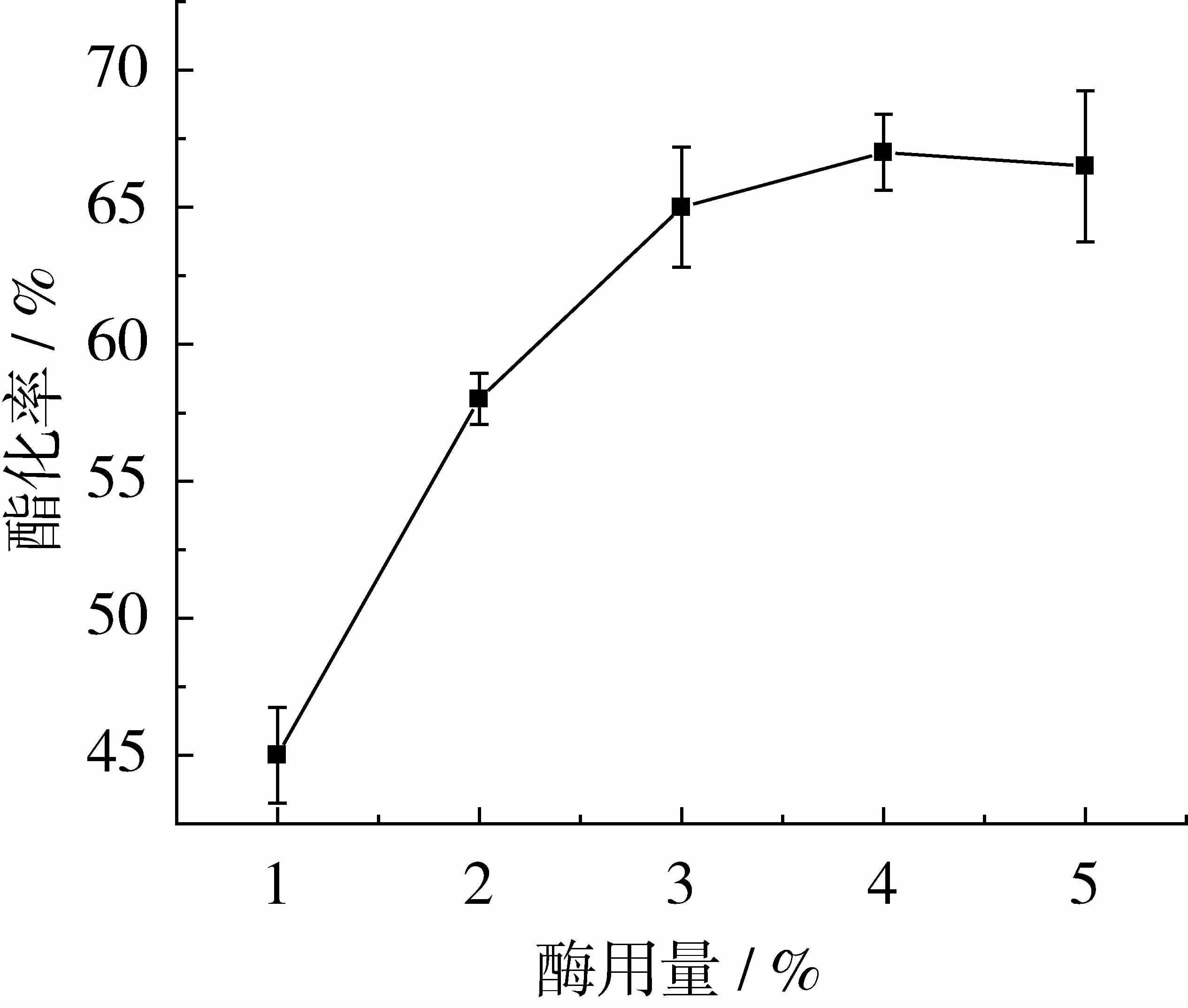
图5 酶用量对酯化率的影响
2.1.6 底物物质的量比对酯化率的影响
固定反应压力11 MPa,反应温度55℃,反应时间为15 h,水分添加量为2%,酶用量为4%,乙酸与葵花油底物比分别为 1∶1、2∶1、3∶1、4∶1、5∶1进行酯化反应,测定样品的酯化率。
底物比是影响葵花油中短链脂肪酸含量的主要因素。如图6所示,随着底物比的增加,即结合到葵花油中的乙酸含量提高,酯化率先升高后降低,当乙酸/葵花油的比例达到3∶1时,酯化率最高。当底物比超过3∶1后,酯化率降低,这是因为当羧基供体的量持续增大时,葵花油和酶的含量相应降低,可能会因底物抑制或其他(如扩散速度)的限制而影响到葵花油中的乙酸插入量。综上所述,底物比为3∶1较为适宜。
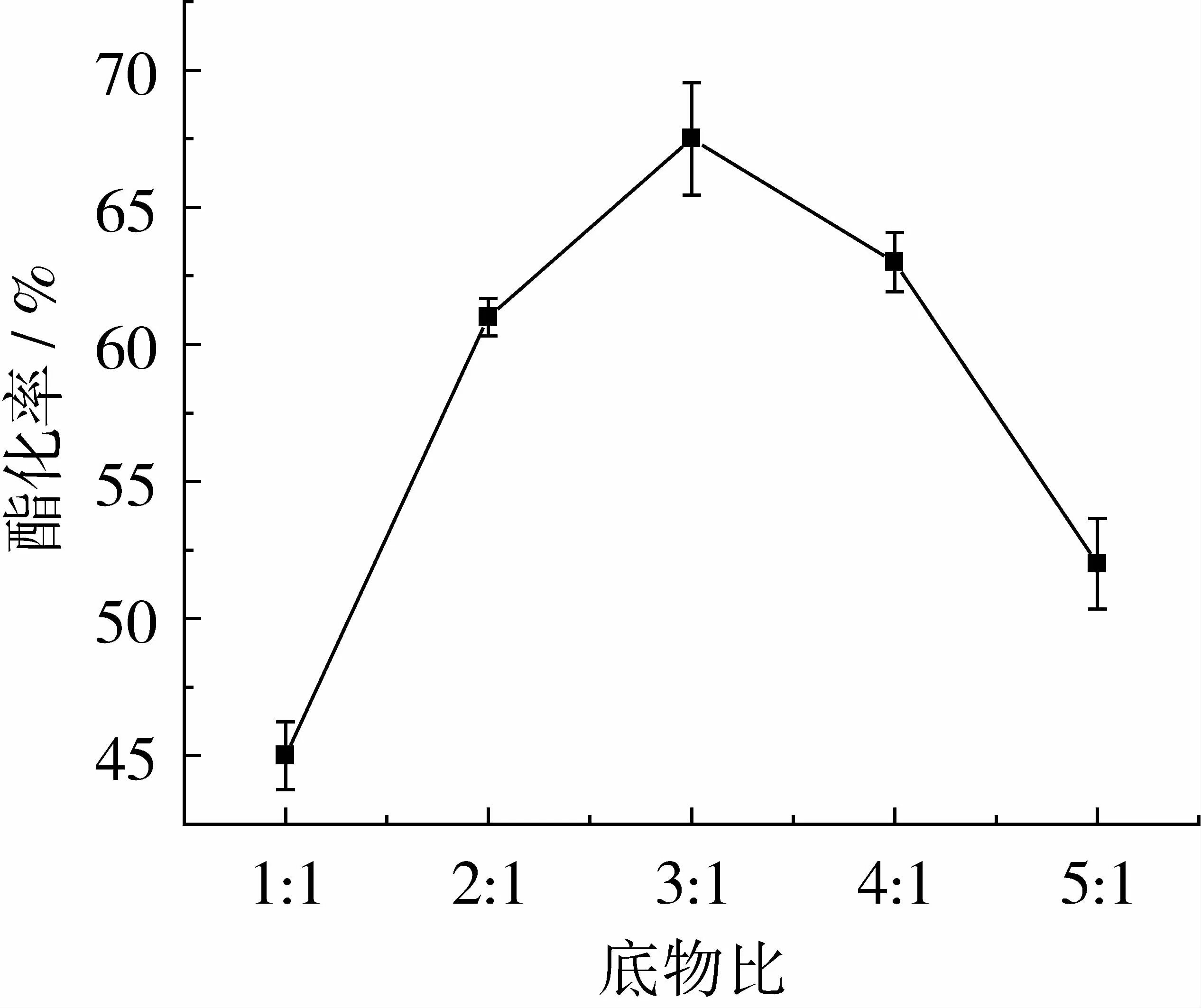
图6 底物物质的量比对酯化率的影响
2.2 最佳工艺参数的确定
由单因素试验可以看出在酯化过程中,水分添加量、酶用量、反应温度对反应的影响较大。因此,确定在水分添加量2%,酶用量4%,反应温度55℃基础上采用中心组合设计(Box-Benhnken),以水分添加量(A)、酶用量(B)和反应温度(C)为自变量,酯化率(R1)为响应值设计响应面试验。自变量水平编码见表1,试验设计方案及结果见表2。
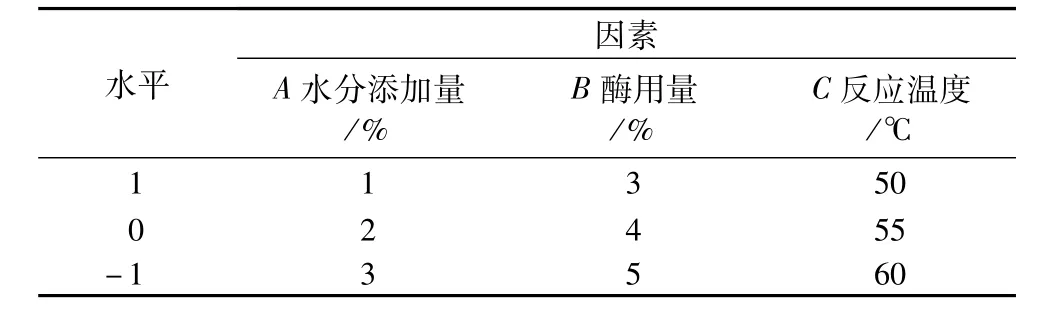
表1 因素水平编码表
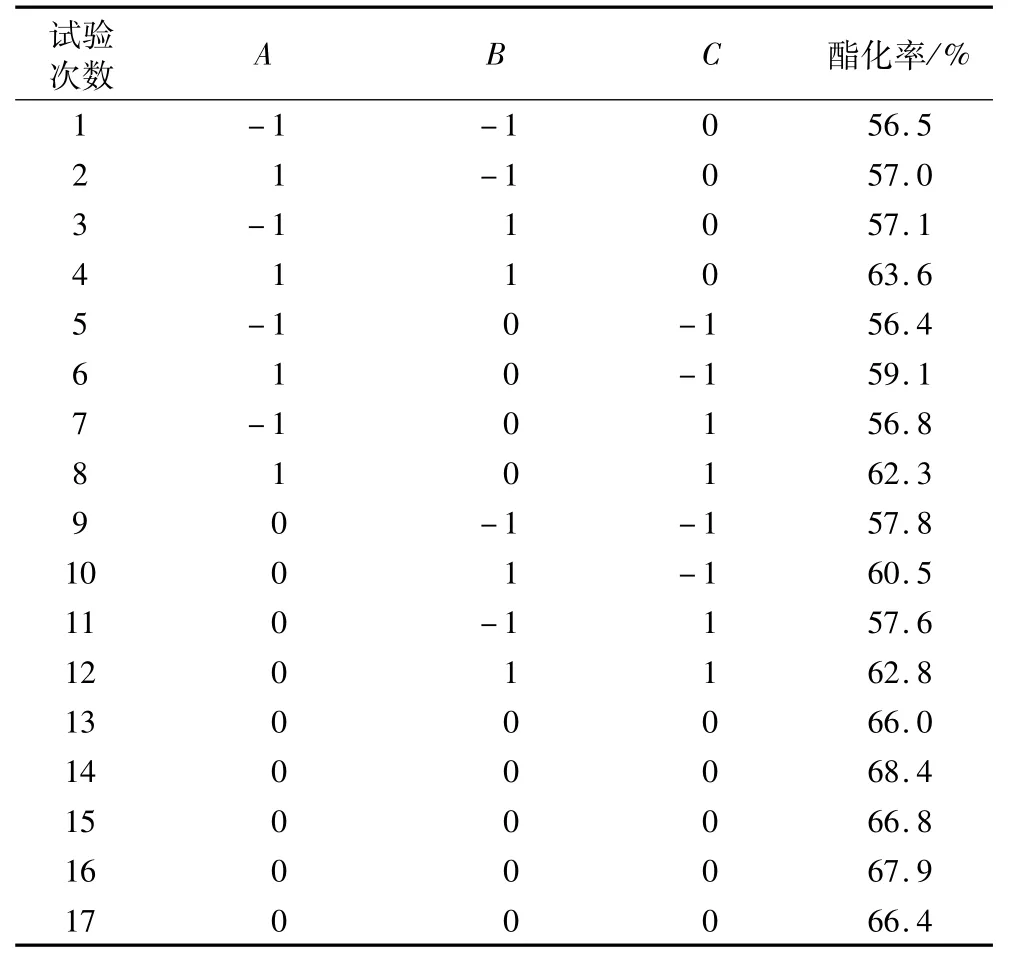
表2 响应面设计方案及试验结果
利用Design Expert7.0.0软件对试验结果进行方差分析,结果见表3(P<0.05为显著项)。
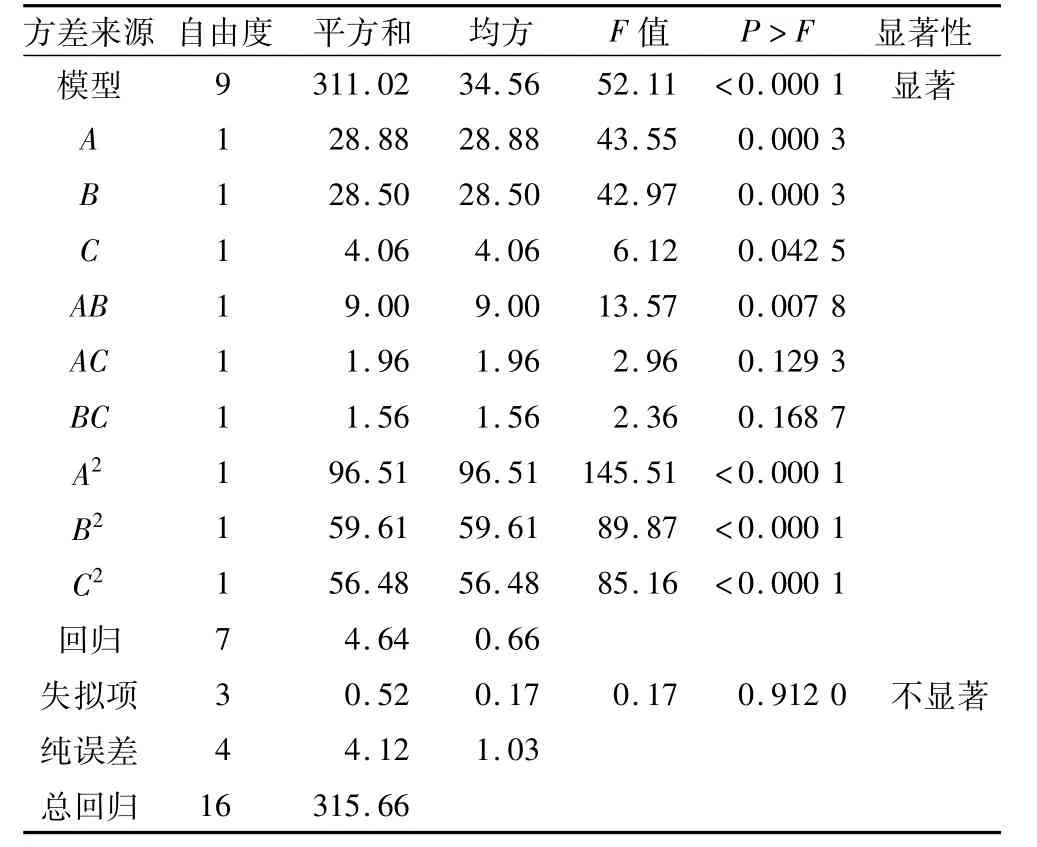
表3 方差分析结果
通过对试验数据进行多元回归拟合,得到酯化率(R1)对水分添加量、酶用量和反应温度(C)的回归方程为:
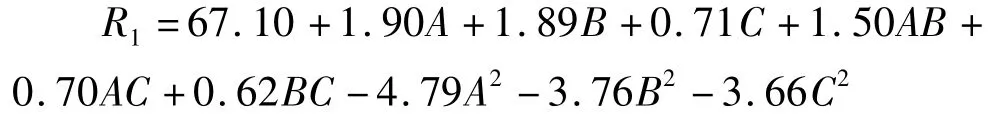
由表3可知,方程因变量与自变量之间的线性关系明显,该模型回归显著(P<0.000 1)失拟项不显著(P>0.05),并且该模型 R2=98.53%96.64%,回归模型与实际情况拟合很好,可以用该模型预测超临界CO2状态下酶法酯化的实际酯化率情况。图7~图9分别给出了酶用量与水分添加量,反应温度与水分添加量,反应温度与酶用量的交互作用对酯化率的响应曲面图。

图7 水分添加量与酶用量对酯化率影响的响应面图
将反应中的反应温度固定在0水平上,可以得到水分添加量和酶用量交互作用对酯化率的影响。由图7可以看出,加酶量不变时,随着水分含量的增加,酯化率含量呈现逐渐增加,当达到一定值后略有降低的趋势;水分添加量不变时,随着加酶量的增加,酯化率呈现先增加后降低的趋势。在水分添加量为2%~2.5%,酶用量约为4%时,酯化率在65%以上。
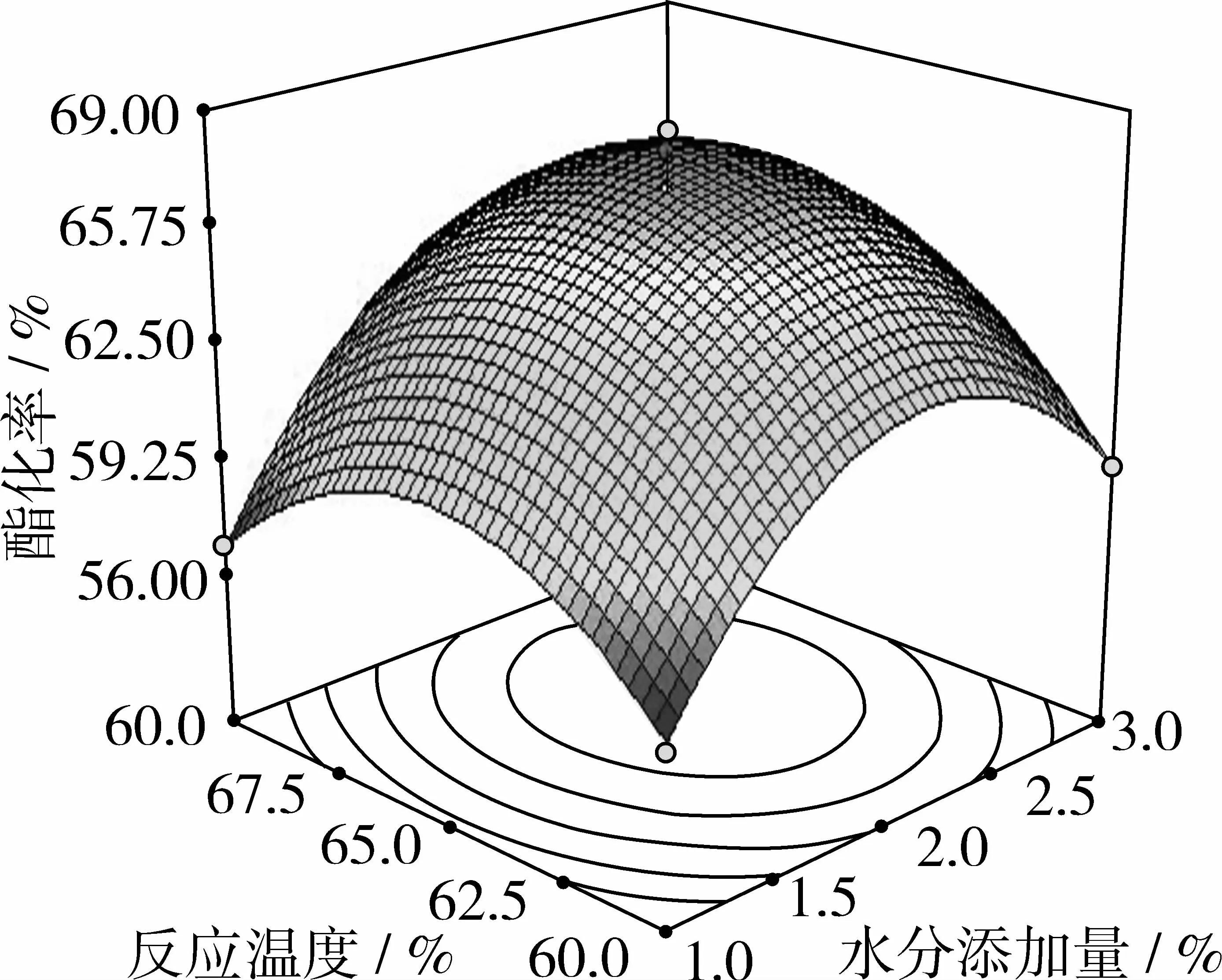
图8 水分添加量和反应温度对酯化率影响的响应面图
将反应模型中的加酶量固定在0水平上,可以得到水分添加量和反应温度交互作用对酯化率的影响。由图8可以看出,水分添加量不变时,随着反应温度的增加,乙酸酯化率呈现先增加后降低的趋势;反应温度不变时,随着水分添加量的增加,酯化率呈现先增加后降低的趋势。在水分添加量约为2%~2.5%,反应温度约为55℃时,酯化率在65%以上。
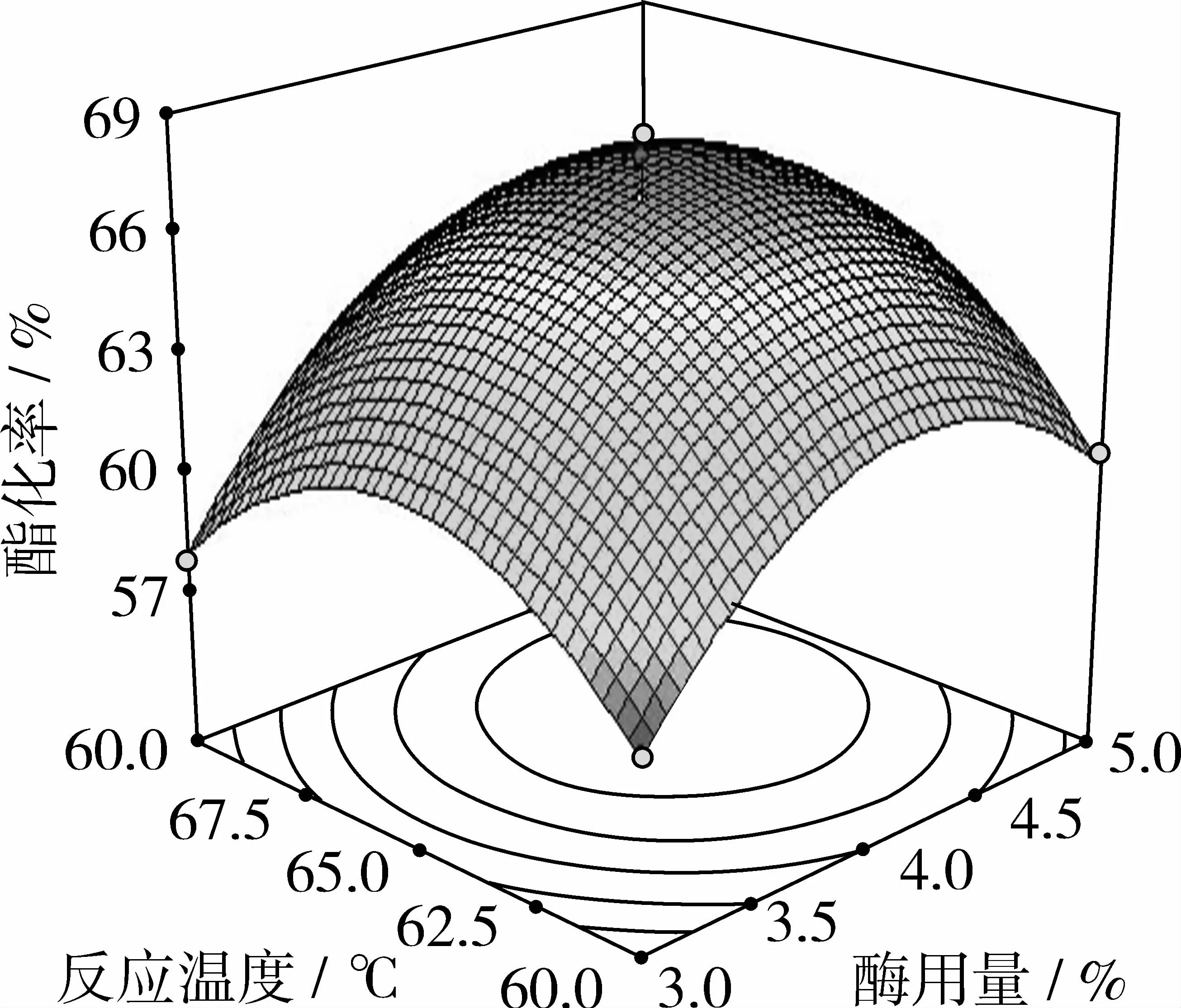
图9 酶用量和反应温度对酯化率影响的响应面图
将反应中的反应温度固定在0水平上,可以得到酶用量和反应温度交互作用对酯化率的影响。由图9可以看出,反应温度不变时,随着酶用量的增加,酯化率呈现先增加后略有降低的趋势;酶用量不变时,随着反应温度的升高,酯化率呈现先增加后降低的趋势。在加酶量为4%~4.5%,反应温度约为55℃时,酯化率在65%以上。
应用响应面优化分析方法对回归模型进行分析,寻找最优响应结果见表4。

表4 响应面寻优结果
为检验响应面方法所得结果的可靠性,按照上述整理值进行试验,得到的酯化率为65.3%,预测值与试验值之间的良好拟合性证实了模型的有效性,表明所得出的回归方程可以很好的反应水分添加量、酶用量和反应温度与酯化率的关系。
2.3 超临界状态下合成的长短链三酰甘油
在超临界状态下,用脂肪酶Lipozyme RM IM催化合成长短链三酰甘油。以酯化率为指标,以压力11 MPa,反应温度56℃,反应时间15 h,水分添加量为2.5%,乙酸与葵花油底物比为3∶1,酶用量4%的条件下合成长短链三酰甘油。在此参数下进行验证试验,试验结果显示酯化率可达65.3%(见图10,图11)。

图10 乙酸甲酯标准品标样的GC图

图11 长短链甘油酯的GC图
3 结论
在超临界CO2状态下,利用脂肪酶Lipozyme RM IM催化酯化反应合成长短链三酰甘油,通过单因素和响应面优化试验确定了最佳的制备工艺:反应压力11 MPa、反应温度56℃、反应时间15 h、体系水分添加量2.5%、酶用量4%、底物物质的量比3∶1。在最佳条件下进行酯化反应,酯化率为65.3%,用此方法制得的长短链脂肪酸三酰甘油食用安全,与普通葵花油相比,热量值降低了大约50%。
[1]Casimir C Akoh,PH D.Fat replacers[J].Food Technology,1988,52(3):47-53
[2]Ney K H.Sensogamme,eine methodische erweiterung der aromagramme[J].Gordian,1988,88(1):19
[3]董建林,曹万新,郜顺成.低热量油脂(脂肪代用品)的市场需求及研究开发现状[J].中国油脂,2000,25(3):5-6
[4]谷利伟.新一代的低热油脂 salatrim[J].食品科技,1999(2):11-12
[5]郑建仙.低热量食品[M].北京:中国轻工业出版社,2002
[6]何川,王海清.低热量油脂的制备和精炼工艺研究[J].中国油脂,2005,30(3):14-15
[7]孙志芳,高荫榆,郑渊月.功能性油脂的研究进展[J].中国食品添加剂,2005(3):4-7
[8]刘如灿,单良金,青哲,等.葵花籽油基低热量油脂的酯交换法制备工艺[J].油脂工程技术,2010(10):3-7
[9]张晶,周家春.低热量油脂Salatrim研制[J].粮食与油脂,2004(1):5-8
[10]王春玲.低热量油脂的现状和展望[J].山东教育学院学报,2009(5):89-90
[11]Cumming JH,Rombeau J L,Sakata T(eds).Physiological and clinical aspects of short-chainfatty acids[M].Cambridge:cambridge universitypress,1995
[12]石阶平,韩雅珊.两种脂肪代用品对大鼠脂质代谢的影响[J].营养学报,2002(2):11-14
[13]曹万新,孟橘,倪芳妍,等.低热量油脂的发展与应用研究现状[J].油脂化学,2011,36(6):50-54
[14]G Livesey,D Buss,P Coussement,et al.Suitability of traditional energy values for novel foods and food ingredients[J].Food Control,2000,11(4):249-289
[15]Hammond D A,Karel M,Klibanov A M,et al.Applied biochemistry enzymatic reaction in supercritical gases[J].Appl Biochem Biotechnol,1985,11(5):393-400
[16]Klemann L P,AJi K,ChrysamM,et al.Random nature of triacylglycerols produced by the catalyzed interesterification of short-and long-chain fatty acid triglyceride precursors[J].Journal of Agricultural and Food Chemistry,1994,42(2):442-446
[17]寇秀颖,于国萍.脂肪和脂肪酸甲酯化方法的研究[J].食品研究与开发,2005,26(2):46-47.
