金属卟啉催化空气氧化甲苯制取苯甲醛及苯甲醇的新工艺
2014-03-10张文明雷福琼
张文明,雷福琼
(浙江曙扬化工有限公司,浙江 衢州 324000)
0 引言
甲苯的甲基C-H 键的选择性氧化一直受到人们的关注,无论从原子经济性还是从环境保护的角度考虑都是一个极其有意义的课题。然而在化学工业上此问题仍然没有得到解决。甲苯的选择性氧化产物苯甲醛、苯甲醇与苯甲酸相比具有更高的工业附加值。苯甲醛与苯甲醇在医药、农药、食品及香料等精细化学工业上有着极其重要的应用,特别是高纯度不含氯的医药级和香料级的苯甲醛与苯甲醇在医药工业和香料工业中被用作重要的中间体及添加剂。但由于甲苯的氧化中间产物苯甲醛和苯甲醇很容易被进一步氧化为苯甲酸,从而大大降低了反应的选择性。目前工业上苯甲醛与苯甲醇的生产方法还主要是先将甲苯卤化再经过水解制得的。这种生产方法工艺条件比较复杂,对设备的腐蚀比较严重,同时在水解过程中产生大量的污染物,更为严重的是这种方法生产的苯甲醛与苯甲醇由于含氯而严重制约了其应用范围。当前工业上使用的优质苯甲醛,主要是作为甲苯直接氧化制备苯甲酸工艺过程中的很少量副产物回收得到的,产量受到很大的限制。
目前直接选择性催化空气氧化甲苯的方法研究的比较多且比较有效的方法是基于钴盐或锰盐的催化体系[1-2]。然而此催化体系存在严重的缺点,即为了提高反应的选择性往往需要羧酸作为溶剂,同时反应体系中作为引发剂的溴化物的使用对设备造成了一定的腐蚀。其他的一些新方法及工艺也在探索之中,已经取得了一定的进步,但由于条件比较苛刻,往往造成生产成本比较高,实现工业化比较困难。随着整个世界对环境保护的重视及相关法律条令的颁布实施,一种清洁有效的苯甲醛与苯甲醇生产工艺就显得更加重要。
本文介绍了在简单四苯基钴卟啉的催化下,在没有外加溶剂及反应引发剂的条件下,空气直接选择性氧化甲苯制取苯甲醛及苯甲醇的反应,考察了一系列反应条件如温度、压力、催化剂用量及空气流量对反应的转化率及选择性的影响。同时还对反应的可能机理进行了初步研究。
1 实验
1.1 仪器与试剂
UV-Vis 为Perkin-Elmer L-17 UV-Vis,IR为Perkin-Elmer Model 783,质谱为Agilent 1100C LC/MSD,1H NMR 为Bruker-80,应用CDCl3作为溶剂,TMS 作为内标,气相色谱分析采用Shimadzu GC-16A,所用柱子为0.5 mm i.d.×25 m的PEG20000 毛细管柱。
所有试剂及溶剂均为分析纯。吡咯在使用前进行了重蒸,苯甲醛在使用前进行了进一步提纯。甲苯在使用前经检测没有发现杂质及自氧化产物。对钴卟啉进行了进一步的合成及提纯,并进行了IR,UV-Vis,MS 及1H NMR 分析表征。
1.2 分子氧氧化甲苯的反应
钴卟啉催化空气氧化甲苯的活性研究是在精密自控反应釜中进行的,所使用的反应釜同文献[3]报道的相类似。向反应釜中加入350 mL 甲苯和3.5 mg 的钴卟啉,充入氮气至0.35 MPa,加热反应体系至160 ℃,然后以5 L/min 的速度通入空气并快速加热至165 ℃。用一数字测氧仪对尾气中的氧气含量进行检测。在特定的时间间隔内从体系中取出少量样品迅速进行检测。反应产物采用GC-MS 和LC-MC 进行定性分析,苯甲醛与苯甲醇含量采用GC 进行内标法定量分析,采用氯苯作为内标物,色谱柱为0.5 mm i.d.×25 m PEG20000 毛细管柱,检测器为火焰原子检测器。对反应中产生的酸采用文献报道的方法进行滴定分析[4]。
2 结果与讨论
2.1 金属卟啉催化液相空气氧化甲苯的反应
金属钴卟啉催化空气氧化甲苯反应是在一定温度(155 ℃~175 ℃)及压力(0.35~1.0 MPa)下进行的。反应不需要外加溶剂及反应引发剂。其反应式如下:
反应的主要产物是苯甲醛、苯甲醇及苯甲酸,同时还有少量苯甲酸对应的酯类。这是首次报道应用简单金属卟啉在无外加溶剂及反应引发剂的条件下直接催化空气选择性氧化甲苯。对照实验表明,在相同的反应条件下,如果不存在CoⅡTPPP,则氧化反应不会发生,这表明钴卟啉在反应中的确起到了催化作用。

图1 应用CoⅡTPP 作催化剂时反应时间对反应的影响
甲苯的氧化产物浓度随时间变化见图1,反应开始时(约1.5 h),体系中苯甲醛及苯甲醇的浓度增加比较快,在同样的时间段内,苯甲酸的浓度增加却比较慢,随着苯甲醛及苯甲醇的浓度进一步增加,苯甲酸的浓度迅速增加,这表明此时苯甲酸的浓度与苯甲醛及苯甲醇的浓度直接相关,此时苯甲醛与苯甲醇的选择性随着甲苯转化率的增加而减小。这同文献报道的钴溴催化体系相一致[5]。这也表明苯甲酸来自苯甲醛及苯甲醇的进一步氧化。图1 显示,当苯甲醛及苯甲醇的浓度积累到一定值时,便稳定下来,没有观察到下降趋势,这表明在此时间段内苯甲醛与苯甲醇的生成速度几乎等于其消耗速度。同时,有意思的是与钴锰盐催化体系相比,此催化体系对苯甲醇的选择性明显比较高。
2.2 钴卟啉与相应金属盐的催化性能对比a

表1 与钴盐的催化性能对比a
实验数据表明:在没有引发剂的情况下,用Co(OAc)2·4H2O 作催化剂,存在一定的的诱导期[6],且反应转化率及醛醇的收率都比相应的钴卟啉作为催化剂低很多(见表1),这充分表明是钴卟啉而不是其分解产物在体系中起到了催化剂的作用。应用钴卟啉作为催化剂,反应不存在诱导期。这表明钴卟啉本身可以诱导反应的进行,既起到了引发剂又起到了催化剂的作用。
2.3 反应温度对甲苯氧化的影响
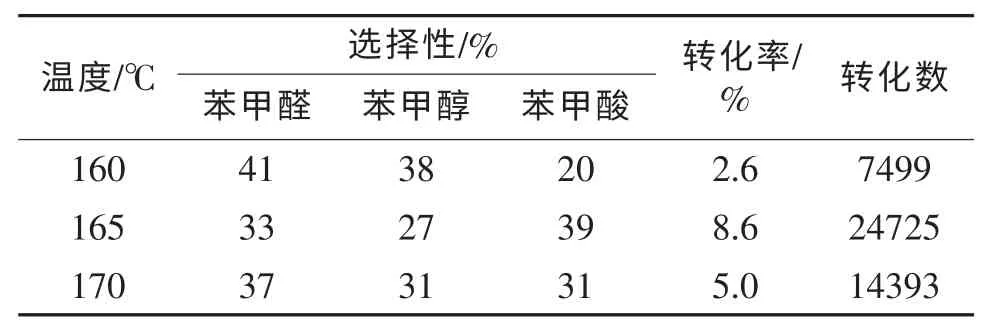
表2 反应温度对甲苯氧化的影响a
反应温度对甲苯催化氧化的转化率及选择性都有比较显著的影响(见表2)。当反应温度低于155 ℃时,反应难以进行。当反应温度为160 ℃时,反应比较慢,转化率比较低,当反应温度达到165 ℃时,催化效果最好,反应转化率、醛/醇收率及催化剂转化数均达到最高。当反应温度升高到170 ℃时反应转化率反而下降,这主要是因为温度的升高在加快了反应速度的同时也加快了催化剂被破坏的速度,从而降低了催化剂的催化循环次数。
2.4 反应压力对甲苯氧化的影响
表3 显示,随着反应压力由0.35 atm 增加到8 atm,反应速度及反应转化率都随之增加,这主要是空气压力的增加提高了反应体系中氧气的相应分压,这相应增加了氧在底物中的溶解量,从而增加了反应速度及甲苯转化率。当反应压力进一步提高到1.0 MPa 时,反应转化率反而下降,这是因为压力的升高增加甲苯自氧化的速度,反应体系中过高浓度的活性物种也使催化剂迅速失活,从而降低了反应转化率。实验数据同时表明,苯甲醛的选择性随着甲苯的转化率增加而降低,而苯甲醇的选择性却几乎不受压力影响。可能原因正在进一步研究。

表3 反应压力对甲苯氧化的影响a
2.5 催化剂用量对甲苯氧化的影响
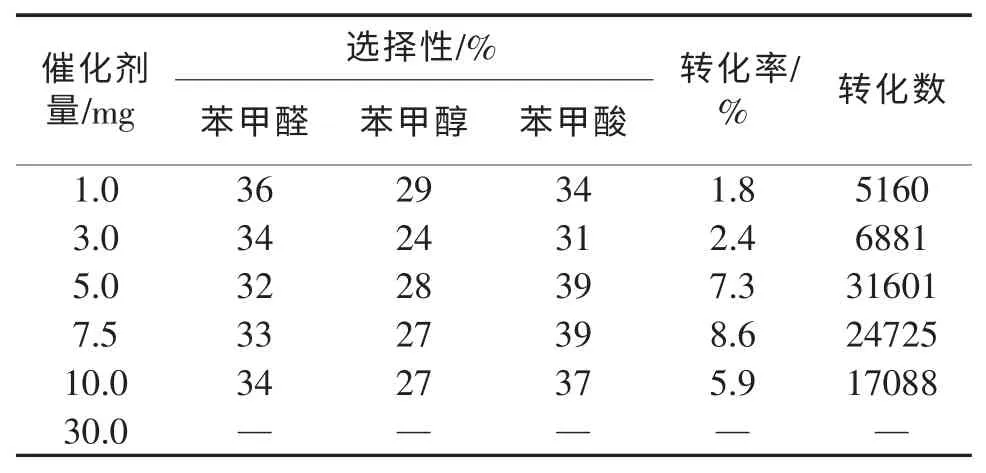
表4 催化剂用量对甲苯氧化的影响a
催化剂的量的变化影响反应的转化率(见表4)。当催化剂的量为5.0 mg 时,催化剂转化数最高,当催化剂用量增加至7.5 mg 时,反应转化率虽然有所增加,但转化数却下降。随着催化剂用量的进一步增加反而导致了转化率的下降,可能是增加了反应中活性中间体与催化剂的相互作用,从而导致催化剂迅速失活。当催化剂的量减少时,反应产率下降,转化数增加却不多。在催化剂浓度为3.4 ppm 时催化反应活性最高。低于此浓度,氧化速度随着催化剂浓度的增加而增加,当催化剂浓度高于此浓度时,反应速度随着浓度的增加反而下降,直到不发生反应。这可以理解为所谓的“催化剂-抑制剂转化”现象[7-8],这在以前我们的环己烷催化体系中也观察到类似的现象。同时发现,产物的分布受催化剂量的影响不大。
2.6 空气流量对甲苯氧化的影响

表5 空气流量对甲苯氧化的影响a
表5 显示,反应受气液扩散控制的影响。如果增加空气的流量,则由于搅拌气泡所增加的界面面积有利于传质的进行,从而增加了反应速度及转化率,因此当空气流量由10 L/h 增加至40 L/h 时,反应转化率逐步增加。但是当空气流速为60 L/h 时,反应转化率却下降,这是由于空气的流量过大,使空气在反应体系内的停留时间过短,从而造成反应速度比较慢。
2.7 可能反应机理初步分析
关于金属卟啉活化分子氧氧化烷烃的机理研究的比较多[6,9-10]。金属卟啉活化分子氧的机理应该按如下方式进行:

只有+2 价的金属卟啉能够同氧气反应。PFe3+Cl 与PMn3+Cl 在低温下不能够同氧分子反应。而钴卟啉的稳定的PM2+则能够比较容易的同氧分子反应。已经证明PCoⅢO·是一种高氧化态的物种,通过步骤(1)、(2)及(3)它可以循环不断的从底物上提取一个H 而产生R·,从而引发反应进行下去。在甲苯的分子氧氧化中,反应的决速步骤为PhCH2·的形成[11],而金属卟啉在此条件下形成的高氧化态活性物种则可以从底物PhCH3测链甲基上提取一个H 而形成R·,R·则可以同一分子氧结合形成ROO·,继而形成ROOH(步骤3),引发反应顺利进行下去,同时金属卟啉还可以有效分解过氧化物。
反应中生成的苯甲醛及苯甲醇最主要来自Haber-Wiess 循环(3)中的过氧化物的分解。而金属卟啉的氧化/还原电势低于相应的金属盐类,因此可以有效的分解过氧化物使反应在比较低的过氧化物水平下便可以顺利进行下去,从而在比较温和的条件下保证了较快的反应速度,这对提高反应选择性非常有利。步骤(4)、(5)则分别生成产物苯甲醇与苯甲醛。苯甲醛则很容易进一步自氧化生成苯甲酸。
3 结论
通过对金属卟啉催化空气氧化甲苯制取苯甲醛及苯甲醇的工艺研究,得到了如下的最佳反应条件,在温度165 ℃,压力0.8 MPa,四苯基钴卟啉3.4 ppm 及40 L/h 空气流量的最佳反应条件下,选择性催化空气氧化甲苯的转化率可以达到8.6%,同时醛醇选择性可以达到60%。同传统甲苯氧化空气制苯甲醛体系相比,此催化体系工艺反应条件简单温和、清洁无污染,产品质量好。同时通过研究表明,金属卟啉存在下的甲苯空气氧化制取苯甲醛及苯甲醇的反应经历了一个由金属卟啉引发的自由基反应历程。
[1]Partenheimer W,Methodology and scope of metal/bromide autoxidation of hydroncarbons[J].Catalysis Today,1995,23(2):69-158.
[2]Kantam M L,Sreekanth P,Rao K K,et al.An improved process for selective liquid-phase air oxidation of toluene[J].Catalysis Letters.2002,81(3-4):223-232.
[3]Guo C C,Chu M F,Liu Q,et al.Effective catalysis of simple metalloporphyrins for cylohexane oxidation with air in the absence of additives and solvents[J].Appl.Catal.A:General,2003,246:303–309.
[4]严旭辉.液相空气氧化甲苯工艺的研究[D].长沙:湖南大学,2006,30-70.
[5]S Evans,J R L Smith.The oxidation of ethylbenzene and other alkylaromatics by dioxygen catalysed by iron (III) tetrakis(pentafluorophenyl)porphyrin and related iron porphyrins[J].J Chem Soc Perkin Trans 2,2000,7:1541-1551.
[6]Grinstaff M W,Hill M G,Labinger J A,et al.Mechanism of Catalytic Oxigenation of Alkanes by Halogenated Iron Porphyrins[J].Science,1994,264 (5163):1311-1313.
[7]Black J F.The unrecognized consequences of metai -hydroperoxide complex formation[J].J.Am.Chem.Soc.,1978,100(2):527-535.
[8]Sheldon R A,Kochi J K.Metal-Catalyzed Oxidation of Organic Compound[M].New York:Academic Press,1981,301-330.
[9]Lyons J E,Ellis P E,Mayers H K.Halogenated metalloporphyrin complexes as catalysts for selective reactions of acyclic alkane with molecular oxygen[J].J Catal,1995,155(1):59-73.
[10]Bartoli J F,Battioni P,Defoor W R,et al.Synthesis and remarkable pro-perties of iron β-polynitroporphyrins as catalysts for monooxygenation reactions[J].J Chem Soc Chem Commun,1994,1:23-24.
[11]Jean Lozar,Gilles Falgayrac,Andre Savall.Kinetics of the Electrochemically ssisted Autoxidation of Toluene in Acetic Acid[J].Ind Eng Chem Res,2001,40:6055-6062.
