盐酸帕洛诺司琼在健康人体的药动学研究
2012-01-27张逸凡杨武云唐世新胡晋红
孙 军,李 珍*,张逸凡,杨武云,唐世新,胡晋红*
(1.第二军医大学长海医院药学部,上海200433;2.中国科学院上海生命科学研究院药物科学研究所药物代谢研究中心,上海201203)
盐酸帕洛诺司琼(palonosetron hydrochloride)是高效、高选择性的第二代5-羟色胺3(5-HT3)受体拮抗剂,其与5-HT3受体的亲和力是其他5-HT3受体拮抗剂的100倍,半衰期也相对较长。临床上用于预防癌症化疗药物所致急性恶心、呕吐和延迟性恶心、呕吐[1]。重庆医药工业研究院有限责任公司研制的盐酸帕洛诺司琼注射液,经国家食品药品监督管理局批准同意进行临床研究。本研究采用HPLC-MS/MS法测定帕洛诺司琼的血浆药物浓度,研究健康志愿者静脉注射不同剂量盐酸帕洛诺司琼注射液后的代谢过程,评价其在健康人体的药动学特征,为进一步的临床研究提供依据。
1 材 料
Agilent 1100液相色谱系统(包括G1311A四元泵、G1322A真空脱气机、G1367A自动进样器和G1316A柱温箱,美国Agilent公司);TSQ QuantumUltra型三重四级杆串联质谱仪,配有电喷雾电离源(ESI源)(美国Thermo Finnigan公司);盐酸帕洛诺司琼对照品(含量99.6%,批号:041205-R)和盐酸帕洛诺司琼注射液(规格:5ml∶0.25mg)购自重庆医药工业研究院;苦参碱对照品(含量100.2%,批号:81041125,江苏恒瑞医药股份有限公司);甲醇、甲酸均为色谱纯,其他试剂均为分析纯。
2 方法和结果
2.1 受试者的选择 选择健康受试者24名,性别不限,年龄18~40岁;体重指数19~24kg/m2;实验室检查(血常规、尿常规、血生化、胸片等)正常;无心、肝、肾、消化道和血液系统等疾病史;无烟酒嗜好。受试者试验前签署书面知情同意书。试验方案经第二军医大学长海医院医学伦理委员会审核批准。
2.2 试验设计 采用无对照开放平行试验设计,24名健康受试者按随机数字表法分配到低、中、高3个剂量组(0.25、0.50、0.75mg),每组各8例,进行单次静脉注射盐酸帕洛诺司琼注射液的药动学研究。
2.3 给药及样品采集 采用单剂量静脉注射给药。受试者试验前1d进食清淡晚餐后禁食12h。试验当日清晨,参考药品说明书,分别静脉注射盐酸帕洛诺司琼注射液0.25、0.50、0.75mg,2min内完成。于给药前(0h)及给药完成即刻和给药后5、15、30min,1、2、4、6、8、12、24、48、72、120、168h从前臂静脉取血3ml,置肝素化离心管中,2.0×102×g离心5min,取上清血浆,-20℃冻存,待测。
2.4 色谱和质谱条件 色谱条件 Agilent Zorbax Extend C18色谱柱(150mm×4.6mm,5μm);柱温:室温;流动相:甲醇-水-甲酸(60∶40∶0.2),流速:0.50ml/min,进样量:20μl。质谱条件 离子源为电喷雾电离源(ESI源),源喷射电压为4 000V,加热毛细管温度为320℃,鞘气(N2)流速10.5L/min,辅助气(N2)流速1.5L/min,正离子方式检测;扫描方式为选择反应监测(SRM);碰撞气(Ar)压力0.16Pa。碰撞诱导解离(CID)电压分别为30eV(帕洛诺司琼)和40eV(内标苦参碱);用于定量分析的离子反应分别为m/z 297→110,188(帕洛诺司琼),m/z249→148(内标苦参碱)。
2.5 标准溶液的配制 (1)精密称取盐酸帕洛诺司琼对照品11.22mg(相当于帕洛诺司琼10.0mg),置于25ml容量瓶中,用甲醇溶解并稀释至刻度,配制成400mg/L的帕洛诺司琼储备液,以甲醇-水(50∶50)稀释至所需浓度,得帕洛诺司琼对照品溶液。(2)精密称取10.0mg苦参碱,置于25ml容量瓶中,用甲醇溶解稀释至刻度,配制成400mg/L的储备液,以甲醇-水(50∶50)稀释得500μg/L的内标溶液。
2.6 血浆样品的处理 取血浆0.50ml加入40μl苦参碱内标溶液,100μl甲醇-水(50∶50)和200μl pH7.8的磷酸盐缓冲液,混匀,加入4ml的提取溶剂:乙醚-二氯甲烷(3∶2),涡旋混合1min后往复振荡15min,1.08×103×g离心5min;分取上清液于另一10ml具塞试管中,40℃空气流吹干,200μl流动相复溶残渣,涡旋混匀,20μl进样分析。
2.7 数据处理 采用DAS 2.0软件进行药动学数据处理。采用梯形法计算AUC0~t值,AUC0~∞=AUC0~t+ct/Ke(ct为最后一个可测时间点的血药浓度);tmax和cmax采用实测值;以血药浓度对时间作半对数曲线,取消除相时间点进行线性拟合,求算消除速率常数Ke,t1/2β=0.693/Ke;CL=D/AUC0~∞(D为给药剂量),Vd=CL/Ke;平均驻留时间(mean retention time,MRT)=一阶矩曲线下面积(AUMC)/AUC。对不同剂量的主要药动学参数与剂量进行相关性分析。
2.8 分析方法验证
2.8.1 方法的特异性 帕洛诺司琼和内标苦参碱在(+)ESI电离方式下,主要生成[M+H]+峰,分别为m/z297和249。选择性对[M+H]+峰进行产物离子全扫描质谱分析,帕洛诺司琼生成的主要碎片离子有m/z 110和188,苦参碱生成的主要碎片离子为m/z148。
取6名受试者的空白血浆0.50ml,除不加内标外,其他按2.6项下操作,进样20μl,得色谱图(见图1A);将一定浓度的帕洛诺司琼对照品溶液和内标溶液加入空白血浆中,同法操作,得色谱图(见图1B);帕洛诺司琼和内标苦参碱的保留时间分别为3.33和2.47min。取受试者给药后的血浆样品,按2.6项下操作,进样20μl,得色谱图(见图1C)。结果表明,空白血浆中的内源性物质不干扰帕洛诺司琼和内标苦参碱的测定。
2.8.2 标准曲线和定量下限 取空白血浆0.50ml,加系列对照品溶液100μl,配制成相当于帕洛诺司琼血浆浓度0.01、0.03、0.08、0.20、0.80、2.0、8.0、20.0、50.0μg/L的样品,按2.6项下操作,进样20μl。以待测物浓度为横坐标(X),待测物与内标物的峰面积比值为纵坐标(Y),采用加权(W=1/X2)最小二乘法进行回归,得回归方程:Y=0.100 9 X+0.001 0(r=0.996 8)。结果表明,帕洛诺司琼血药浓度在0.01~50μg/L范围内线性关系良好。定量下限为0.01μg/L,RSD=6.9%,RE=5.3%(n=6)。
2.8.3 方法的回收率和精密度 取空白血浆0.50ml,加系列对照品溶液100μl,配制成相当于帕洛诺司琼血浆浓度0.025、0.500和40.0μg/L的质控样品。取上述3个浓度的血浆质控样品,按2.6项下操作,于1d内测定6次,计算日内RSD;连续测定3d,计算日间RSD,结果见表1。另取空白血浆0.50ml,除不加内标外,按2.6项下操作,向获得的全部上清液中加入相应浓度的对照品溶液100μl和内标溶液40μl,涡旋混合,40℃空气流吹干,200μl流动相复溶残渣,涡旋混匀,20μl进样分析,得相应峰面积。以每一浓度两种处理方法的峰面积比值计算回收率,结果见表1。

图1 血浆中帕洛诺司琼和内标苦参碱的HPLC-MS/MS谱图Figure 1 HPLC-MS/MS photograms of palonosetron and internal standard matrine in human plasma
表1 帕洛诺司琼的回收率和精密度实验结果Table 1 Recovery rate and precision test of palonosetron(n=6,±s,%)
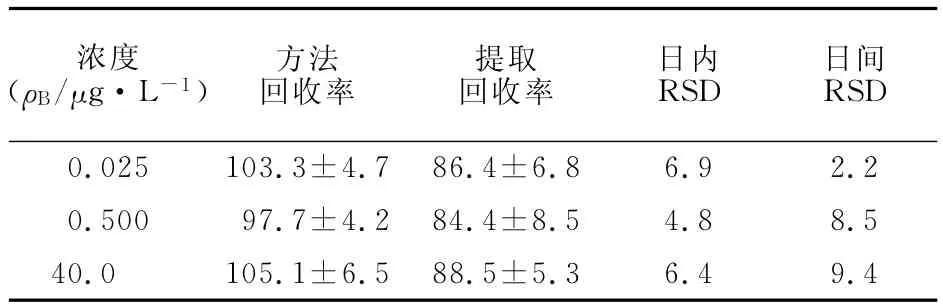
表1 帕洛诺司琼的回收率和精密度实验结果Table 1 Recovery rate and precision test of palonosetron(n=6,±s,%)
(ρB/μg·L-1) 方法回收率浓度 提取回收率日内RSD日间RSD 0.025 103.3±4.7 86.4±6.8 6.9 2.2 0.500 97.7±4.2 84.4±8.5 4.8 8.5 40.0 105.1±6.5 88.5±5.3 6.4 9.4
2.8.4 样品的稳定性考察 本研究考察了帕洛诺司琼血浆样品(0.025和40.00μg/L)于室温放置2h、-20℃放置6个月、3次冻融循环,以及萃取后室温放置24h的稳定性。结果表明,帕洛诺司琼血浆样品放置2h(RE 0.9%~4.1%)、萃取后室温放置24h(RE-8.0%~9.4%)、-20℃放置6个月(RE 5.7%~6.7%)、血浆样品经过3次冻融循环(RE-3.8%~-1.3%)均稳定。
2.9 药动学研究 24名健康受试者单次静脉注射盐酸帕洛诺司琼后平均血药浓度-时间曲线见图2。帕洛诺司琼的血浆浓度呈双指数下降,开始为迅速的分布相,随后为较慢的消除相。经过模型拟合,帕洛诺司琼在受试者体内的药动学过程符合二室开放模型,主要药动学参数见表2。帕洛诺司琼在体内的暴露量(cmax和AUC)随着剂量的增加(0.25~ 0.75mg)而增加,AUC与剂量的增加呈线性关系,t1/2、CL和Vd无剂量依赖性。

图2 静脉注射3个剂量的盐酸帕洛诺司琼注射液后的血药浓度-时间曲线Table 2 Concentration-time curves of palonosetron after administration of three doses of palonosetron hydrochloride injection by intravenous infusion
2.10 安全性评价 在试验过程中,医护人员对受试者的不良反应进行了严密观察。19名受试者在试验过程中出现轻度腹痛、腹胀、大便干燥、大便次数减少等消化道症状;6例次出现轻度乏力、恶心、头晕、头痛等症状;以上所有症状均未处理,自行缓解。这些症状的出现可能与帕洛诺司琼作用于胃肠道和中枢5-HT3受体有关。
3 讨 论
化疗引起的恶心、呕吐是肿瘤病人在化疗过程中最常见的不良反应,预防化疗所致的恶心、呕吐对改善病人生活质量并保证化疗的顺利进行具有重要意义。盐酸帕洛诺司琼是第二代5-HT3受体拮抗剂,其化学结构与第一代同类产品不同,它由一个融合的三环结构与喹核碱相连。这种结构基础决定了帕洛诺司琼与第一代5-HT3受体拮抗剂相比,与受体的结合力强30~100倍,t1/2β也较现有5-HT3受体拮抗剂明显延长。
表2 静脉注射3个剂量的盐酸帕洛诺司琼注射液后的药动学参数Table 2 Pharmacokinetic parameters of palonosetron after administered three doses of palonosetron hydrochloride injection by intravenous infusion(n=8,±s)

表2 静脉注射3个剂量的盐酸帕洛诺司琼注射液后的药动学参数Table 2 Pharmacokinetic parameters of palonosetron after administered three doses of palonosetron hydrochloride injection by intravenous infusion(n=8,±s)
Ke:消除速率常数;MRT:平均驻留时间
组别 cmax(ρВ/μg·L-1) tmax(t/h) AUC0~t(A/μg·h·L-1)AUC0~∞(A/μg·h·L-1) t1/2β(t/h) Ke(1/h) CL(L/h) Vd(V/L) MRT(t/h)0.25mg组5.57±2.97 0.03±0.00 24.3±7.6 25.0±8.0 31.0±5.6 0.023±0.004 11.0±3.6 495±208 41.7±6.2 0.50mg组6.84±5.48 0.03±0.00 48.3±14.6 50.2±16.1 33.5±5.6 0.021±0.003 11.0±4.1 513±138 45.5±9.0 0.75mg组9.75±5.78 0.07±0.08 74.7±25.4 76.8±27.2 31.1±5.0 0.023±0.003 10.7±3.1 463±91 42.4±7.9
与以往研究方法的强碱性流动相(pH 9.5)相比,本研究采用的流动相为甲醇-水-甲酸(60∶40∶2),色谱柱的适用性相对会更好一些。
文献[2]报道帕洛诺司琼在0.3~90μg/kg剂量下,在美国和日本的健康受试者中,帕洛诺司琼暴露量随着剂量增加而增加,t1/2β、CL和Vd无剂量依赖性。本研究结论与以上报道相似。静脉注射3种剂量盐酸帕洛诺司琼注射液后,其在健康人体内的消除半衰期相近,说明在0.25~0.75mg剂量范围内盐酸帕洛诺司琼呈线性药动学特征。国内外研究[3-5]表明,静脉注射盐酸帕洛诺司琼后,Vd值较大,而CL相对较低,提示帕洛诺司琼在人体内分布广泛,消除却相对缓慢,因此半衰期较长。帕洛诺司琼的长效特征除与其代谢、消除缓慢有关外,与该药与5-HT3受体结合的特点也有关[6]。鉴于以上原因,对该药短期内的频繁给药(每日连续或隔日交替)需谨慎考虑。
[1] 陈心华,刘 健,李娜妮,等.盐酸帕洛诺司琼预防高中度致吐性化疗引起恶心呕吐的临床观察[J].临床药物治疗杂志,2010,8(6):45-48. Chen XinHua,Liu Jian,Li NaNi,et al.Clinical observation of palonosetron hydrochloride in the prevention of nausea and vomitting induced by chemotherapy which can cause severe to moderate vomitting[J].Clin Med J,2010,8(6):45-48.In Chinese with English abstract.
[2] Stoltz R,Cyong J C,Shah A,et al.Pharmacokinetic and safety evaluation of palonosetron,a 5-hydroxytryptamine-3receptor antagonist,in U.S.and Japanese healthy subjects[J].J Clin Pharmacol,2004,44(5):520-531.
[3] 陈 艳,丁莉坤,孟玲燕,等.盐酸帕洛诺司琼注射液人体药动学研究[J].中国新药杂志,2007,16(10):806-809.
Chen Yan,Ding LiKun,Meng LingYan,et al.Pharmacokinetics of intravenous infusion of palonosetron hydrochloride in healthy volunteers[J].Clin J New Drugs,2007,16(10):806-809.In Chinese with English abstract.
[4] 戴媛媛,刘 鹏,陈 喆,等.注射用盐酸帕洛诺司琼健康人体药动学研究[J].中国新药杂志,2009,18(10):910-913.
Dai YuanYuan,Liu Peng,Chen Zhe,et al.Pharmacokinetics properties of palonosetron,a 5-hydroxytryptamine-3receptor antagonist,in Chinese healthy subjects[J].Chin J New Drugs,2009,18(10):910-913.In Chinese with English abstract.
[5] Shah A,DeGroot T,Apseloff G.Pharmacokinetic evaluation and safety profile of a 15-minute versus 30-second infusion of palonosetron in healthy subjects[J].J Clin Pharmacol,2006,46(10):1139-1145.
[6] Rojas C,Stathis M,Thomas A G,et al.Palonosetron exhibits unique molecular interactions with the 5-HT3receptor[J].Anesth Analg,2008,107(2):469-478.
