Nb 颗粒增韧Ti-45Al-5Nb-0.3W 合金的高温氧化行为
2023-11-22黄佳妮李慧中梁霄鹏车逸轩
黄佳妮,李慧中, ,梁霄鹏, ,车逸轩
(1. 中南大学 材料科学与工程学院,长沙 410083;2. 中南大学 粉末冶金国家重点实验室,长沙 410083;3. 中南大学 有色金属材料科学与工程教育部重点实验室,长沙 410083)
TiAl 合金具有低密度、高比模量和比强度、优良的抗氧化以及抗蠕变性能[1-2],是一种可以用于替代镍基合金的高温轻型结构材料。TiAl 合金目前在工业制造中主要应用于航空发动机涡轮叶片、矢量喷口、排气阀和活塞等零件,在服役过程中要承受高温、剧烈的空气摩擦以及循环氧化等严苛环境[3]。TiAl 合金在750 ℃以下具有较好的抗氧化性能,但在800 ℃以上,合金表面形成的氧化膜失去防护作用,致使合金的抗氧化性能降低,限制了其高温应用[4-5]。TiAl 合金的高温抗氧化性能成为当前的研究热点。通过多元合金化的方法,添加Nb、Mo、W、Si、Cr、Ta 等元素,可提高TiAl 基合金的抗氧化性能[6-8]。然而,多元合金化难以同时改善TiAl合金的力学性能与抗氧化性能[9]。金属Nb 由于其高韧性和易变形性,可以有效地提高TiAl 合金的韧性和塑性变形能力[10-13]。本课题组研究发现,采用粉末冶金法制备的摩尔分数为2%的Nb 颗粒增韧TiAl 复合材料(Nbp/TiAl)的强度和塑性明显提升,在800 ℃和850 ℃高温下,其强度-延性的乘积分别达到38.8 GPa%和46.9 GPa%[14-15]。然而,在实际应用中,长期高温和应力作用下,金属基体和增韧相之间可能发生扩散反应导致增韧效果降低,且增韧相影响材料的抗氧化性能,导致材料性能不稳定和使用寿命下降[16]。在TiAl 合金中添加适量Nb可降低氧的空位浓度,抑制TiO2生长,从而提高合金的抗氧化性能[17],但过高的Nb 含量会导致Nb2O5相和TiNb2O7相的形成,对抗氧化性能不利[18]。因此,研究Nb 颗粒增韧TiAl 基合金的抗氧化性能,使其强度、韧性和抗氧化性能协同提高具有重要的理论意义和实用价值。本文采用Ti-45Al-5Nb-0.3W合金作为基体合金,Nb 颗粒为增韧相,通过热等静压法制备Nb 摩尔分数为2%的Nbp/TiAl 合金,研究热处理后的Nbp/TiAl合金在800、850 和900 ℃空气环境中恒温暴露的氧化动力学规律以及氧化膜的显微组织与结构,揭示Nb 增韧TiAl 合金的氧化行为,为其高温应用提供理论指导和实验依据。
1 实验
将粒径为150 μm 的商用Ti-45Al-5Nb-0.3W 合金粉和摩尔分数为2%、粒径为180 μm 的Nb 粉(均由西安赛隆金属材料有限公司提供)混合,装入内腔直径和长度分别为100 mm 和200 mm 的不锈钢包套中,在500 ℃下抽真空2 h,然后密封容器。在1 250 ℃和150 MPa 下对密封好的包套进行热等静压处理(QIH-9 型热等静压机,美国热电公司),5 h后随炉冷却,获得Nbp/TiAl 合金锭坯,其直径和长度分别为85 mm 和160 mm。将其置于SX-G08163型箱式电阻炉中,在1 280 ℃分别保温4、10 和24 h 后空冷。
将保温24 h 的合金加工成尺寸为5 mm×5 mm×5 mm 的正方体,各个面打磨光亮,使用精度为0.01 mg 的电子天平分别称量每个样品的初始质量m0。将样品置于氧化铝坩埚中,再放入箱式电阻炉,在800、850 和900 ℃进行恒温氧化实验,氧化时间节点为5、10、15、20、40、60、80 和100 h。待冷却到室温后,称量氧化后样品的质量m1,计算各时间节点样品单位面积质量增量ΔM,计算公式为:ΔM=(m1-m0)/S,式中的S为样品的总面积。每个时间节点称量3 个样品,结果取平均值。
采用光学显微镜(OM, 4XC-Ⅱ型,上海光学仪器六厂)观察热处理前后合金的金相组织。使用X射线衍射仪(XRD, D/max 2550VB,日本理学株式会社)对氧化前后的样品进行物相分析,采用Cu Kα辐射,扫描速度为5 (°)/min。利用场发射扫描电子显微镜(SEM, Sirion 200,荷兰FEI)对氧化膜表面及氧化膜截面进行观察。用能量色散X 射线能谱仪(EDS, GENSIS60,荷兰FEI)和电子探针显微设备(EPMA, JXA-8230,日本电子株式会社)对氧化膜截面进行元素分析。
2 结果与讨论
2.1 Nbp/TiAl 合金的显微组织
图1所示为Nbp/TiAl 合金的原始组织以及在1 280 ℃保温4、10 和24 h 后的金相显微组织。从图看出,原始组织中Nb 颗粒清晰可见,亮色区域为富Nb 区(Nb 颗粒所在位置),富Nb 区内部可见灰色针状相。随保温时间延长,基体组织的晶粒明显长大,且富Nb 区的Nb 元素逐渐向基体扩散,使得内部的针状相溶解。保温4 h 后,富Nb 区内部灰色针状相减少(见图1(b)),且富Nb 区边界变模糊;保温10 h 后,富Nb 区边缘被层片晶团占据(见图1(c));保温24 h 后,富Nb 区转变成粗大的层片晶团,合金中已经没有明显的富Nb 区和针状富Nb相存在,Nb 颗粒消失。此时,元素扩散充分,合金的性能更加稳定。因此选择1 280 ℃保温24 h 的合金进行恒温氧化实验。
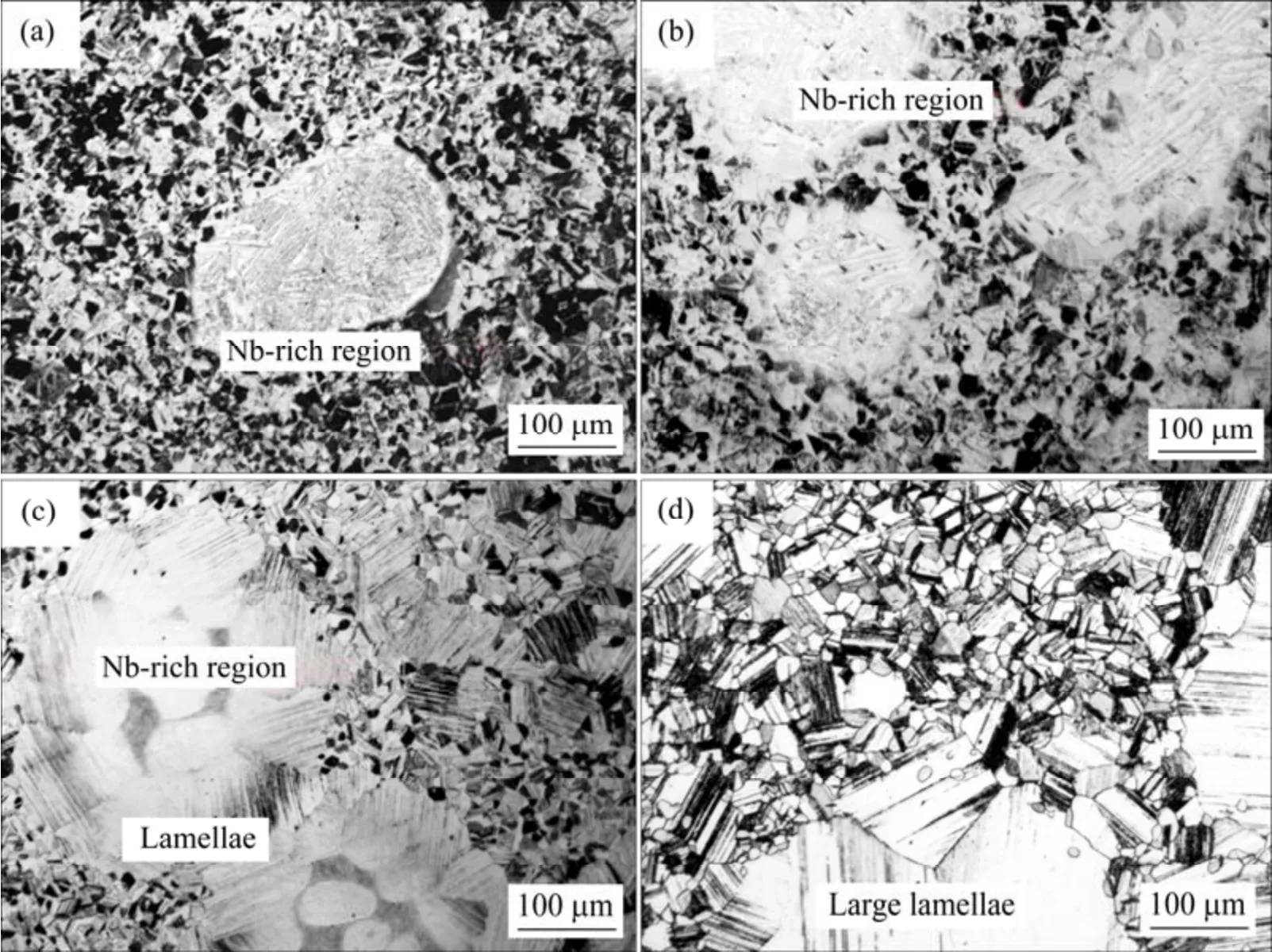
图1 Nbp/TiAl 合金热处理前后的金相组织Fig.1 OM microstructures of Nbp/TiAl alloy before and after heat treatment
图2(a)和(b)所示分别为Nbp/TiAl 合金的原始组织和在1 280 ℃保温24 h 后的SEM 图。图2(a)中左侧的亮色区域为富Nb 区(Nb 颗粒所在位置);较暗的基体为典型近γ 组织,以等轴γ 晶粒为主,存在少量α2/γ 层片晶团。合金在1 280 ℃保温24 h 后,富Nb 区的Nb 元素充分扩散,富Nb 区被粗大的层片团及片层晶界处的γ 晶粒占据,说明Nb 元素在高温下的扩散能促进α2/γ 层片团的生长和γ 相的析出。基体转变为由等轴γ 晶粒与α2/γ 层片组织共同构成的典型双态组织,从图2(b)中还观察到退火孪晶的存在。

图2 Nbp/TiAl 合金热处理前后的SEM 图Fig.2 SEM images of Nbp/TiAl alloy before and after heat treatment
2.2 氧化动力学
图3所示为Nbp/TiAl 合金在800、850 和900 ℃恒温氧化时的氧化动力学曲线。由图3(a)可知,随氧化时间延长,Nbp/TiAl 合金单位面积的质量增量ΔM逐渐减小。氧化前期(0~20 h)合金质量增加较快,800 ℃恒温氧化20 h 后合金的ΔM为1.81 g/m2,氧化100 h 后的ΔM为3.32 g/m2。质量增加速率减小说明在氧化过程中表面形成了保护性氧化膜,可抑制合金的进一步氧化。随温度升高,氧化反应加剧,850 ℃与900 ℃氧化时,恒温氧化100 h 后的ΔM分别为7.36 g/m2和17.27 g/m2。表1 所列为TiAl合金在800 ℃及900 ℃恒温氧化100 h 后单位面积的质量增量,本实验制备的Nbp/TiAl 合金的ΔM较小,表现出更优异的抗氧化性能。

表1 TiAl 合金在不同温度下氧化100 h 后单位面积的质量增量Table 1 Mass increments per unit area of TiAl alloys after 100 h exposure at different temperatures

图3 Nbp/TiAl 合金的氧化动力学曲线Fig.3 Oxidation kinetics curves of Nbp/TiAl alloy
单位面积的质量增量与氧化时间存在如下幂函数关系[23]:
式中:ΔM为样品单位面积的质量增量,g/m2;n为幂指数;k为氧化速率的常数;t为氧化时间,h。
由式(1)可知,ΔM的n次方与时间成正比,n值越大,代表合金的抗氧化性能越好。对式(1)两边取对数,可得:
为进一步分析合金在不同阶段的氧化动力学规律,将原始数据取对数,并通过拟合曲线,计算出不同阶段的氧化速率指数n。由图3(b)可知,800 ℃恒温氧化时,n值随氧化时间的延长而上升,Nbp/TiAl 合金的抗氧化能力不断提高。合金在850 ℃和900 ℃恒温氧化的氧化速率指数n均高于2,即氧化曲线(ΔM-t)呈现抛物线规律,随氧化时间延长,质量增加速率持续减小,表明生成的氧化膜的抗氧化性能持续增强。
2.3 氧化膜形貌与结构表征
图4所示为800、850 和900 ℃恒温氧化100 h后,Nbp/TiAl 合金表面的XRD 图谱。由图可知,合金表面形成了TiO2、Al2O3和NbO 等多种氧化物。TiAl 和Ti3Al 峰的存在表明合金氧化程度较轻,氧化膜较薄,X 射线可以穿透氧化膜检测到基体。随温度升高,Al2O3、Ti5Al3O2、NbO 等衍射峰的强度逐渐上升,说明高温下合金中各元素都参与了氧化过程。
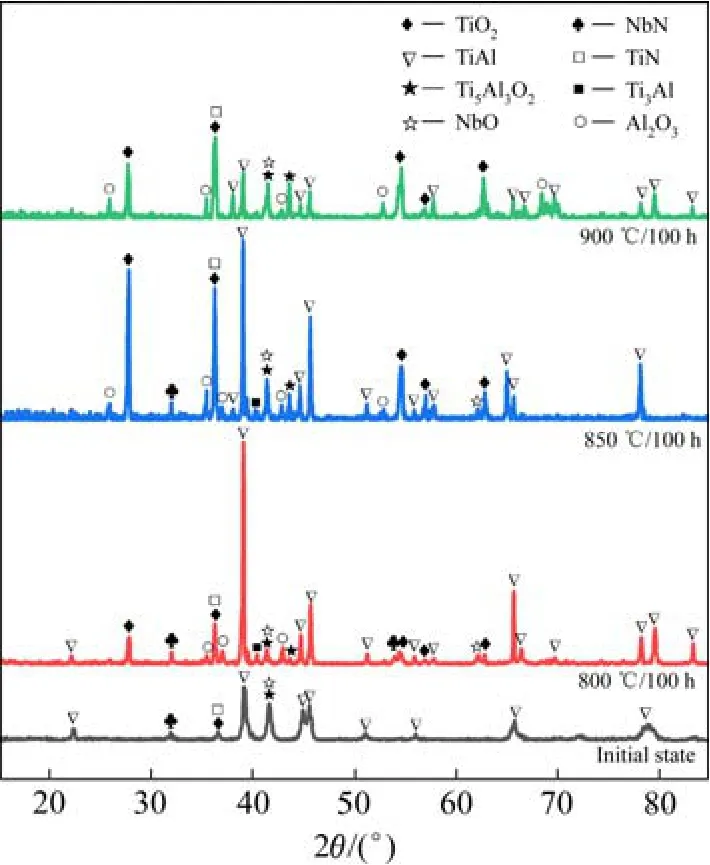
图4 Nbp/TiAl 合金的XRD 图谱Fig.4 XRD patterns of Nbp/TiAl alloy
图5所示为800、850 和900 ℃恒温氧化20 h和100 h 后,Nbp/TiAl 合金表面的SEM 形貌,图6所示为800 ℃和900 ℃氧化100 h 后氧化膜截面的SEM 形貌和EDS 元素线扫图,图中红色线段为线扫位置。从图5(a)看出,在800 ℃恒温氧化20 h 后,合金表面的氧化产物分布不均匀,细小颗粒状氧化物(黄色圆圈内)散布在方块状氧化物的缝隙中,填充空隙位置。结合图4 的XRD 结果与图6 的EDS分析可知,块状氧化物主要由Ti 和O 元素组成,是TiO2;而细小颗粒状氧化物主要包含Al 和O,是Al2O3。由此可知,氧化初期(20 h),TiO2主要呈块状分布在合金表面,而Al2O3以细小颗粒状弥散分布;氧化后期(100 h),TiO2含量增多,大量方块状TiO2均匀分布在合金表面。对比不同温度氧化100 h 后的氧化层发现,800 ℃恒温氧化100 h 后,Nbp/TiAl 合金表面氧化层颗粒尺寸较小,结构较为紧密,细小颗粒状的Al2O3占比较多(见图5(b))。相比800 ℃,850 ℃氧化后Al2O3和TiO2的尺寸都有所增大,但TiO2尺寸的增大更明显。900 ℃恒温氧化100 h 后,氧化膜表面A12O3占比减少,最外层为TiO2层,颗粒尺寸大,结构较为松散(见图5(f))。这说明高温下TiO2生成速率更快,并且更易长大,而Al2O3的生成速率相对较慢。

图5 Nbp/TiAl 合金氧化膜表面的SEM 形貌Fig.5 Surfacial SEM morphologies of Nbp/TiAl alloy oxide film
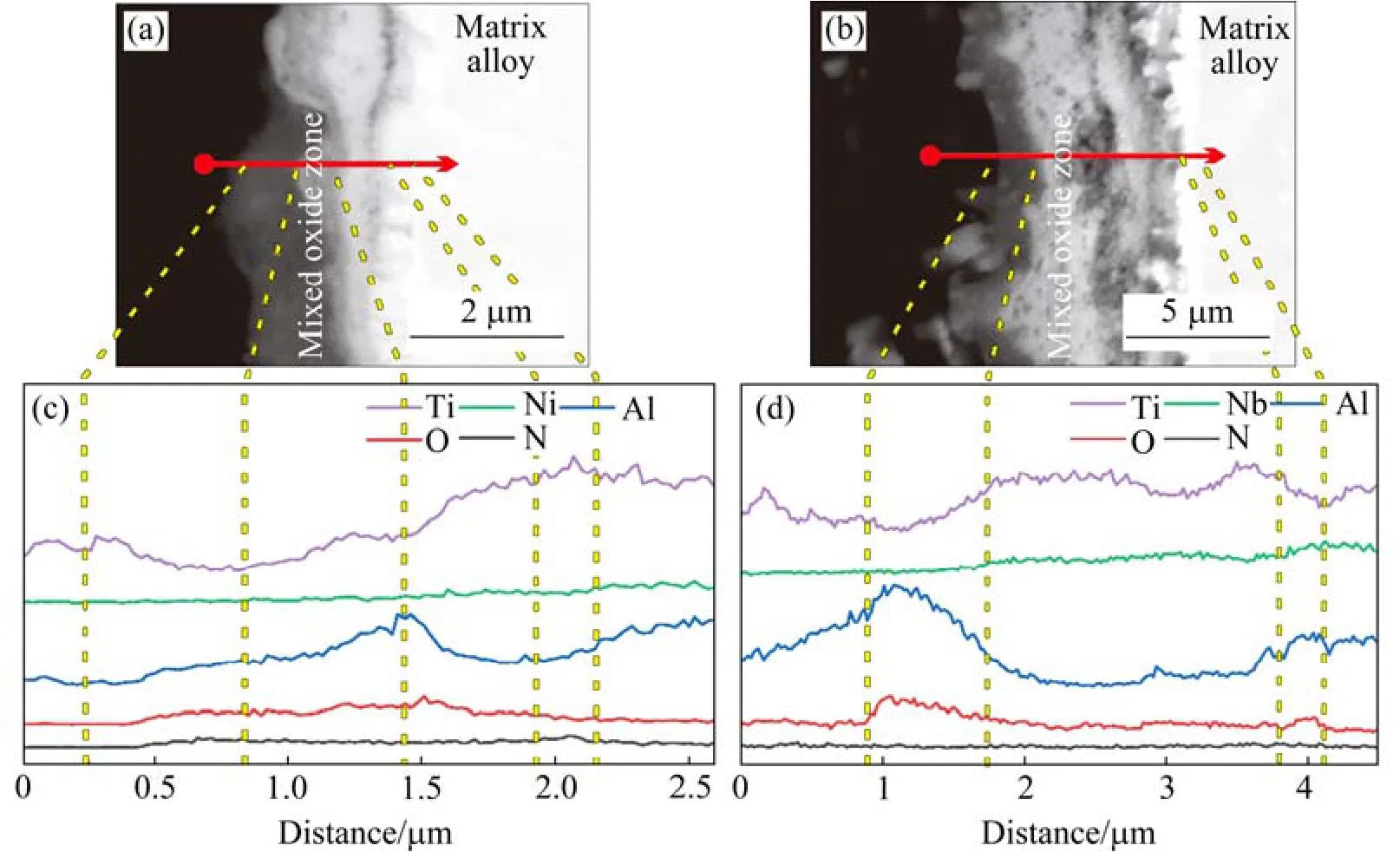
图6 Nbp/TiAl 合金氧化100 h 后氧化膜截面的SEM 形貌和EDS 元素线扫图Fig.6 SEM morphologies and EDS element line distributions of oxide film cross section of Nbp/TiAl alloy oxidized for 100 h
从图6(a)看出,800 ℃恒温氧化100 h 后,合金表面氧化膜的厚度较小,存在分层现象,由不同氧化物构成的氧化层界面呈波浪状。900 ℃恒温氧化100 h 后(图6(b)),氧化膜的厚度较大,分层结构清晰,中间亮白色氧化层最厚,但该层存在较多细小孔洞,致密性差。氧化层与基体之间存在明显的连续亮层。由图6可知,氧化膜为主要由TiO2和Al2O3,以及少量富Nb 氧化产物组成的多层结构。氧化层从外到内依次为:富含Ti 的亮层、富含Al 的暗层、富含Ti 和Al 的中间层、亮白色的交界层。从外到内O 元素浓度先增加后减小,在富含Al 的暗层达到浓度峰值,该层为α-Al2O3。Al 和O 元素在同一方向上的变化趋势较为一致,而与Ti 元素变化趋势相反。Nb 从基体到氧化层的浓度变化相对Ti 和Al更小,而在氧化膜/基体界面处与Al 一同富集,结合后续EPMA 分析以及相关文献[19]可以确定为AlNb2。
图7所示为Nbp/TiAl 合金在800 ℃恒温氧化100 h 后氧化膜截面的EPMA 面扫结果。由图可知,合金表面形成了由Ti、Al、Nb、N 和O 元素组成的氧化膜。Al 主要分布在合金基体内部、氧化膜最外层(富Al 层)和氧化膜/基体界面;Ti 主要分布在合金基体内部和氧化膜的中间层(混合层),结合图5(b)与图6(a)可以推断,所观察区域氧化膜的最外层TiO2层已经剥落;O 主要分布在氧化膜内,且在基体和氧化膜之间形成了不均匀的浓度边界,表明氧化膜具有较好的阻隔作用,能够抑制基体的进一步氧化。

图7 Nbp/TiAl 合金在800 ℃氧化100 h 后氧化膜截面的EPMA 元素面分布Fig.7 EPMA mapping results of oxide film cross section of Nbp/TiAl alloy oxidized at 800 ℃ for 100 h
由图7(f)可知,N 在氧化膜/基体界面富集,形成了一条连续的富N 带,上层区域富含Ti,下层区域同时含有Ti 和Al。氮化层的厚度一般在500 nm左右,SWADŹBA 等[24]利用透射电镜确定富N 带由TiN 和Ti2AlN 组成。从图7(d)看到,Nb 在混合层中有少量富集,而在富N 层与基体交界处明显富集,生成连续的氧化产物。Nb 在氧化膜中不仅促进了TiN 的形成和稳定,还形成了有效阻碍金属离子向外扩散和氧离子向内扩散的屏障层[25]。综合其他元素分布规律可以推断在长时间氧化后,界面处生成AlNb2相,与氮化层协同形成连续致密且与基体结合良好的氧化层结构[19]。该处O 浓度已经降至最低,说明其对抑制O 元素向基体扩散起到了关键作用。再结合图4 的XRD 结果和图6(c)的氧化膜截面EDS 元素线扫结果可以推测,Nbp/TiAl 合金在800 ℃恒温氧化100 h 后,氧化膜为从外到内依次为TiO2/Al2O3/混合层(Al2O3+TiO2+NbO 等)/富N 层(TiN+Ti2AlN+AlNb2)的多层结构。合金表面各元素通过形成连续、分层的氧化膜,降低O 的扩散速率。
2.4 氧化膜形成机理
图8所示为Nbp/TiAl 合金的氧化机理示意图。已知Nbp/TiAl 合金表面的主要氧化产物为TiO2和Al2O3。从热力学角度分析,AlO 和TiO 的标准生成自由能非常接近,因此在氧化的初期Al 和Ti 会同时氧化[26-27]。但生成的TiO 很快被氧化成TiO2,且Ti 在γ 相中的扩散系数大于Al 在γ 相中的扩散系数[28],O 在TiO2相中的扩散系数远大于在Al2O3相中的扩散系数[29],这导致Al2O3相的生长速率相对较慢[17]。TiO2快速生长,在其下方形成富Al、贫Ti 的区域,增加了Al 的活度。随时间延长,O向内扩散,在次表层生成Al2O3,起着扩散屏障的作用。然而随着Al2O3层的形成促进了Ti 的富集,导致Ti 和Al 的交替富集,最终形成由TiO2和Al2O3组成的混合氧化层。
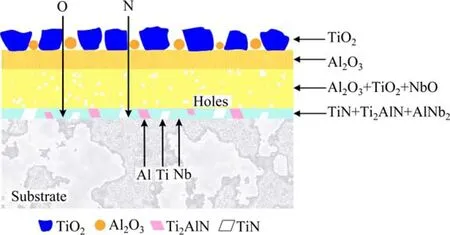
图8 氧化膜形成机理示意图Fig.8 Schematic diagram of the oxide film formation mechanism
氧化膜/基体界面形成富N 相(Ti2AlN 和TiN),这与氧和氮的分压比(PO2/PN2)有关。氧化膜形成后,会发生内氧化现象,即O 和N 离子向内渗透,Ti 和Al 离子向外迁移。当O 和N 到达氧化膜/基体界面时,由于内氧化反应的发生,PO2降低,PN2升高,使得N 活性增加,进而导致氮效应。PAN 等[30]提出了以下反应机制来解释富N 层的形成。
式中:[N]和[O]分别表示气体在溶解和分解过程中产生的N 原子/离子和O 原子/离子。
此外,氮化层到表面的距离是变化的,O 元素不断向内渗透,导致氮化层中PO2升高,氮化物进一步氧化成TiO2和Al2O3并释放[N]。
释放的[N]与从外部输送的N 相结合,扩散到基体中形成新的氮化层。所以,随氧化时间延长,富N 层向内延伸,消耗大量的Ti,促使Nb 和Al在界面处富集并发生反应生成AlNb2相[31-32]。
根据文献[33–35]的报道,在氧化膜/基体界面形成的AlNb2相能够与富Al 和Ti 的富N 层形成连续致密且与基体结合良好的氧化层,抑制金属离子和氧离子的扩散,起到显著的“扩散屏障”的作用。
3 结论
1) Nbp/TiAl 合金在800、850 与900 ℃恒温氧化均遵循近似抛物线的氧化动力学方程。氧化100 h后单位面积的质量增量分别为3.32、7.36 和17.27 g/m2。合金表面均形成具有保护性的氧化膜。
2) 合金氧化膜为多层结构,表面氧化产物主要为块状TiO2和细小颗粒状Al2O3,长时间氧化后,氧化膜表面基本被TiO2占据,最外层较为松散。氧化膜从外到内的分层结构为:TiO2/Al2O3/混合层(Al2O3+TiO2+NbO)/富N 层(TiN+Ti2AlN+ AlNb2)。
