止咳宝片的HPLC指纹图谱研究
2023-07-27吴伟峰李钰铃唐小文邓煜然孔令佳盛钊君林忠泽
吴伟峰,李钰铃,唐小文,邓煜然,孔令佳,盛钊君,林忠泽,2,3*
1.五邑大学,江门 529000;2. 特一药业集团股份有限公司,江门 529200;3.广东江门中医药职业学院,江门 529000
止咳宝片是由紫菀、橘红、桔梗、枳壳、百部、五味子、陈皮、干姜、荆芥、罂粟壳浸膏、甘草、氯化铵、前胡、薄荷素油制备而成,具有宣肺祛痰、止咳平喘的功效,可用于外感风寒所致的咳嗽、痰多清稀、咳甚而喘[1-2]。止咳宝片现执行标准为2015年版《中华人民共和国药典》一部,其中仅有薄层色谱分析定性五味子与紫菀2味药材、吗啡含量测定[3],而相关研究也多为对单味药材进行分析、测定,缺乏整体反映止咳宝片内在质量的分析方法。指纹图谱技术[4-5]是一种综合性的鉴定方法,其指对经过一定适当处理的中药或其他成分使用一定的分析手段,得到可以反映其特征性和指纹性的图谱[6-9],该图谱可整体反映中药所含的化学成分种类和数量[10-12],可对药品的质量进行全面地评价。本研究在相关研究[13-25]的基础上,用高效液相色谱法(high performance liquid chromatography,HPLC)建立止咳宝片的指纹图谱,为评价止咳宝片的整体质量提供参考。
1 仪器与试药
1.1 仪器
UltiMate 3000型高效液相色谱仪(UV-VIS检测器)、Chromeleon 7色谱数据工作站、Evolution 201紫外可见光分光光度计,均购自美国Thermo公司;KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);ML204T电子天平(万分之一,瑞士Mettler Toledo公司)。
1.2 试药
对照品:甘草苷(批号11610-201106)、柚皮苷(批号110722-201714)、橙皮苷(批号110721-201818)、白花前胡甲素(批号111711-200602)、白花前胡乙素(批号111904-201203)、五味子醇甲(批号110857-201714)、五味子乙素(批号110765-200205)、吗啡(批号171201-201825),均购自中国食品药品检定研究院;乙腈、磷酸为色谱纯,均购自上海泰坦科技股份有限公司;超纯水(用Milli-Q超纯水系统制得,法国Merck公司);甲醇等试剂均为分析纯。
对照药材:紫菀(批号120956-201807)、桔梗(批号121028-201612)、枳壳(批号120981-201605)、百部(批号121221-201604)、五味子(批号120922-201610)、陈皮(批号120969-201510)、干姜(批号120942-201606)、荆芥(批号120911-201512)、甘草(批号120904-201620)、前胡(批号120951-201706),均购自中国食品药品检定研究院;橘红进厂编码为190711005,购自安徽省亳州市药材总公司医药公司。
止咳宝片规格为0.35 g·片-1,共有20批,编号为S1~S20,其批号分别为11180611、11180612、11180621、11180622、1180623、11180624、11180625、11180626、11180627、1180628、32190601、32190602、32190603、32190604、32190605、32190606、32190607、32190608、32190609、32190610,均由特一药业集团股份有限公司提供。
2 方法与结果
2.1 色谱条件
Agilent ZORBAX SB-Phenyl色谱柱(150 mm×4.6 mm,5 μm);流速为0.5 mL·min-1;检测波长为210 nm;柱温为30 ℃。流动相为乙腈(A)-4 mL·L-1磷酸水(B),梯度洗脱,洗脱程序为0~8 min,5% A;8~25 min,5%~18% A;25~35 min,18% A;35~65 min,18%~27% A;65~110 min,27%~80% A;110~120 min,80%~90% A;120~130 min,90% A。
2.2 溶液制备
2.2.1供试品溶液 精密称取止咳宝片样品0.25 g,置于具塞锥形瓶,量取25 mL体积分数为50%的甲醇,置于具塞锥形瓶后密闭,称定质量,在超声功率500 W、超声频率40 kHz条件下超声20 min,放置至室温,再次称定质量,滴加体积分数为50%的甲醇补足质量,摇匀,滤过,取续滤液,即得。
2.2.2对照品溶液 精密称取柚皮苷、橙皮苷、白花前胡甲素、白花前胡乙素、五味子醇甲、五味子乙素、吗啡对照品适量,加一定量的甲醇,分别制成80 μg·mL-1柚皮苷、60 μg·mL-1橙皮苷、50 μg·mL-1白花前胡甲素、50 μg·mL-1白花前胡乙素、0.3 mg·mL-1五味子醇甲、1 mg·mL-1五味子乙素、10 μg·mL-1吗啡的对照品溶液;另取甘草苷对照品适量,精密称定,加入体积分数为70%的甲醇制成质量浓度为20 μg·mL-1的对照品溶液,滤过后接取续滤液,即得。
2.2.3对照药材溶液 分别将11味对照药材紫菀、橘红、桔梗、枳壳、百部、五味子、陈皮、干姜、荆芥、甘草、前胡粉碎,过40目筛。精密称取粉碎过筛的对照药材各0.25 g,分别置于具塞锥形瓶中,量取25 mL 体积分数为50%的甲醇加入后密闭,称定质量,在超声功率500 W、超声频率40 kHz条件下超声20 min,放置至室温,再次称定质量,滴加体积分数为50%的甲醇补足质量,摇匀,滤过,取续滤液,即得。
2.3 精密度实验
取同一份供试品(批号32190604),按照2.2.1项下方法制备供试品溶液,按照2.1项下色谱条件连续重复进样6次,进行HPLC分析,在指纹图谱中以10号峰为参照峰,计算得各共有峰相对保留时间的RSD值为0.01%~0.15%,相对峰面积的RSD值为0.30%~2.79%,表明仪器的精密度良好。
2.4 重复性实验
取同一份供试品(批号32190604),按照2.2.1项下的方法平行制备供试品溶液6份,按照2.1项下色谱条件进行HPLC分析,在指纹图谱中以10号峰为参照峰,计算得各共有峰相对保留时间的RSD值为0.01%~0.10%,相对峰面积的RSD值为0.55%~2.78%,表明仪器的重复性良好。
2.5 稳定性实验
取同一份供试品(批号32190604),按照2.2.1项下的方法制备供试品溶液,分别在制备后0、2.5、5、7.5、10、12.5、15、17.5、20、24、48 h按照2.1项下色谱条件进行HPLC分析。在指纹图谱中以10号峰为参照峰,计算得各共有峰相对保留时间的RSD值为0.01%~0.16%,相对峰面积的RSD值为0.19%~2.49%,表明仪器的稳定性良好。
2.6 指纹图谱的建立与相似度分析
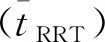

表1 相似度评价结果
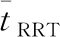
表2 20批样品的相对保留时间和相对峰面积结果

注:S1~S20分别为不同批号(11180611、11180612、11180621、11180622、1180623、11180624、11180625、11180626、11180627、1180628、32190601、32190602、32190603、32190604、32190605、32190606、32190607、32190608、32190609、32190610)的止咳宝片。

注:1~21.指纹图谱特征峰。
2.7 指纹峰归属与定性分析
精密吸取供试品溶液、对照药材溶液、对照品溶液、空白溶液(体积分数为50%的甲醇),按照2.1项下色谱条件测定,进样体积为10 μL。通过与对照药材对比分析,指认了部分峰的药材归属,3、6、7、13、14、15号峰归属甘草,5、19、20号峰归属前胡,9号峰归属枳壳,12号峰归属荆芥,16、21号峰归属五味子。另通过与对照品溶液对比分析,定性了1号峰为吗啡、7号峰为甘草苷、9号峰为柚皮苷、10号峰为橙皮苷、16号峰为五味子醇甲、19号峰为白花前胡甲素、20号峰为白花前胡乙素、21号峰为五味子乙素。见图3、图4。
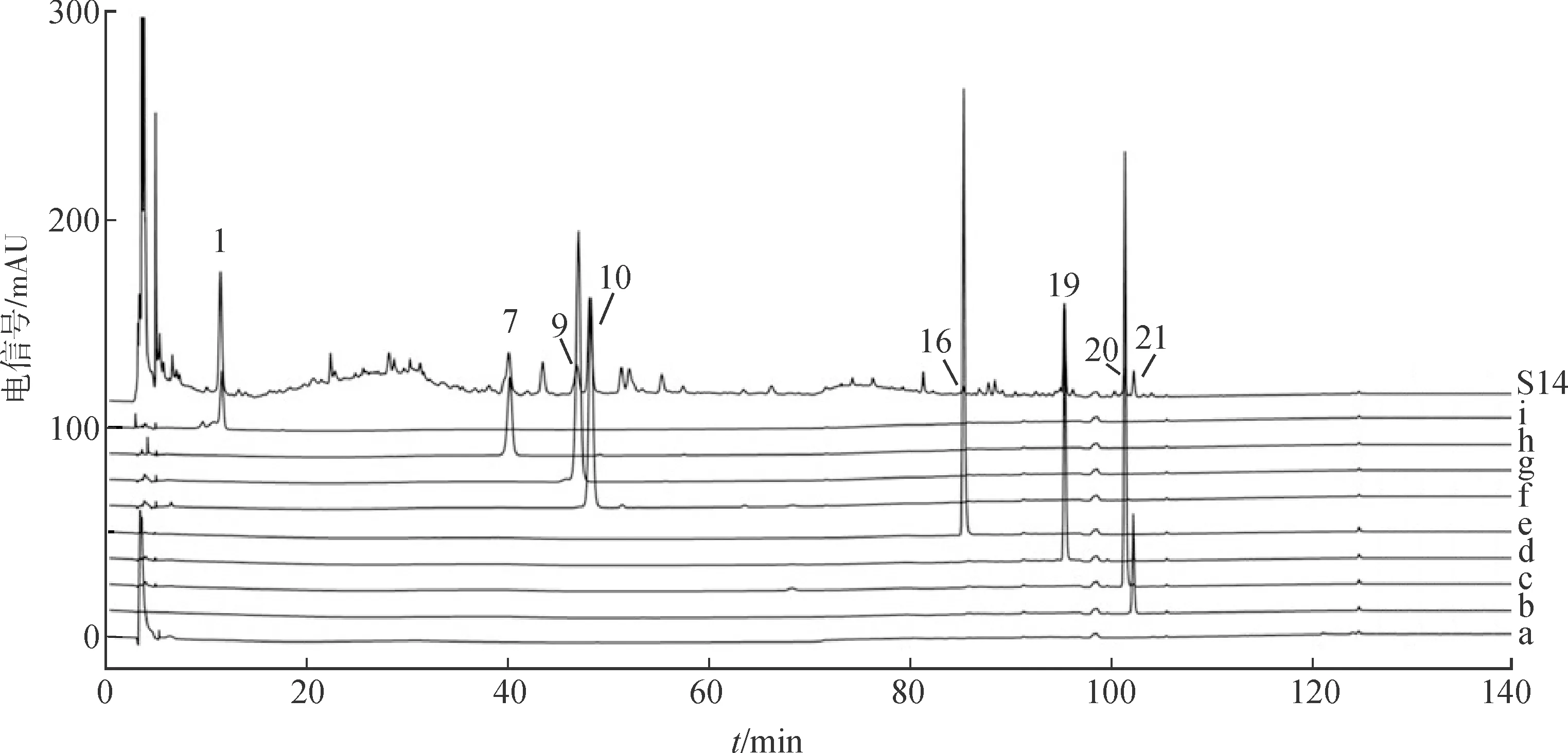
注:S14为批号32190604的止咳宝片;a.空白;b.五味子乙素;c.白花前胡乙素;d.白花前胡甲素;e.五味子醇甲;f.橙皮苷;g.柚皮苷;h.甘草苷;i.吗啡;1.吗啡;7.甘草苷;9.柚皮苷;10.橙皮苷;16.五味子醇甲;19.白花前胡甲素;20.白花前胡乙素;21.五味子乙素。

注:S14为批号32190604的止咳宝片;a.空白;j.荆芥;k.干姜;l.桔梗;m.百部;n.紫菀;o.前胡;p.五味子;q.陈皮;r.橘红;s.枳壳;t.甘草;3、6、7、13、14、15号峰归属甘草;5、19、20号峰归属前胡;9号峰归属枳壳;12号峰归属荆芥;16、21号峰归属五味子。
2.8 共有指纹峰相对保留时间规定值
根据20批止咳宝片指纹图谱中21个指纹峰的相对保留时间(以10号峰橙皮苷为参照峰),并结合方法学考察因子对指纹峰相对保留时间的影响,确定其规定值波动范围在±3%以内,分别为0.234(1号峰)、0.463(2号峰)、0.472(3号峰)、0.582(4号峰)、0.625(5号峰)、0.648(6号峰)、0.832(7号峰)、0.903(8号峰)、0.973(9号峰)、1.000(10号峰)、1.066(11号峰)、1.088(12号峰)、1.155(13号峰)、1.376(14号峰)、1.688(15号峰)、1.770(16号峰)、1.823(17号峰)、1.836(18号峰)、1.980(19号峰)、2.105(20号峰)、2.123(21号峰)。
2.9 共有指纹峰相对峰面积规定值
在20批止咳宝片指纹图谱的21个指纹峰中,单峰面积占共有峰总面积20%的共有峰有10号峰,峰面积占比小于20%但大于10%的共有峰有1号峰、7号峰,其余共有峰峰面积占比均小于10%,其中2、3号峰未达到基线分离,故将该组峰的总峰面积作为峰面积,该组合峰峰面积占比为4.80%,RSD值为8.19%。因此确定共有指纹峰相对峰面积比值为0.827(1号峰)、0.234(2、3号峰)、0.045(4号峰)、0.045(5号峰)、0.052(6号峰)、0.515(7号峰)、0.272(8号峰)、0.293(9号峰)、1.000(10号峰)、0.165(11号峰)、0.222(12号峰)、0.140(13号峰)、0.126(14号峰)、0.085(15号峰)、0.039(16号峰)、0.065(17号峰)、0.060(18号峰)、0.399(19号峰)、0.105(20号峰)、0.127(21号峰)。
3 讨论
3.1 HPLC条件选择
止咳宝片是由多味药材复方制成的,其成分众多且各自溶解度不同,在对比C18色谱柱的分离效果后,发现使用苯基色谱柱时各峰的峰形和分离度均较好。另通过对止咳宝片供试品溶液进行190~400 nm全波长扫描,考察了其最佳吸收波长,发现在210 nm处其色谱峰数较多,分离度和峰形均较好,最终确定210 nm为检测波长。因甲醇在210 nm波长处存在基线不稳的现象,故选用乙腈作为流动相的有机相,同时考察了乙腈-水、乙腈-1 mL·L-1磷酸、乙腈-1 mL·L-1冰醋酸、乙腈-4 mL·L-1磷酸等流动相系统,发现乙腈-4 mL·L-1磷酸在梯度洗脱时峰形更好,故选用该条件作为色谱条件。
3.2 止咳宝片供试品溶液制备方法选择
在考察止咳宝片的提取方法时,分别考察了加热回流提取和超声提取2种方法,并对不同提取时间(加热回流30、60、90 min,超声提取10、20、30 min)和提取溶剂(水、体积分数为50%的甲醇、甲醇)进行考察。结果表明,用体积分数为50%的甲醇作为提取溶剂、超声提取20 min获得的色谱峰响应值较高且峰形较好,故选用该方法进行提取。
4 结论
本研究建立了止咳宝片的HPLC指纹图谱,标定了21个共有指纹峰,指认了8种特征成分并对13个峰进行了药材归属,用“中药色谱指纹图谱相似度评价软件(2004A版)”对20批止咳宝片进行相似度评价,相似度为0.941~0.999,并确定了共有峰的相对保留时间比值、相对峰面积比值的范围。
综上所述,该方法简便、可靠、稳定性好,能较全面地反映止咳宝片的内在化学成分,对现有执行标准进行补充,可有效评价止咳宝片的质量。
