TiO2 在锂金属负极界面的修饰及应用
2022-11-09张华知HAFSAYoussoufi
陈 超 ,张华知 ,宋 扬 ,HAFSA Youssoufi
(1.四川化工职业技术学院应用化工学院,四川 泸州 646000;2.四川大学化学工程学院,四川 成都 610020;3.巴黎萨克雷大学ICMMO 实验室,法国 奥赛 91400)
锂金属负极具有超高的比容量(3 860 mAh/g)和较低的氧化还原电位(-3.04 V,vs.SHE),是有发展前途的高能量密度负极材料[1]。
锂金属电池在循环过程中,会因杂乱的锂成核/沉积,导致不可控的锂枝晶生长,使容量持续衰减,严重时将刺穿隔膜,产生短路,引发火灾等安全问题[2]。锂金属性质活泼,与电解质极易发生反应,不断消耗电池中的电解液和活性锂,造成容量衰减甚至失效[3]。实现均匀的锂沉积、减少锂枝晶,是锂金属负极材料应用的关键。对于锂成核/沉积的改进,已有较多研究,如优化电解液、通过锂金属负极表面改性构建固体电解质相界面(SEI)膜、构建3D 锂基体,以及采用全固态电解液,避免使用易燃的有机电解液等[4]。在锂金属负极表面构建SEI 膜,是当前一种效果较好的方法[5]。
本文作者通过机械喷涂TiO2粉末,引发并加速金属锂与TiO2的锂化反应,在锂金属表面构建LixTiO2SEI 膜[6-7],以期避免锂枝晶生成及电解液分解,提高电化学性能。
1 实验
1.1 样品制备
制备LixTiO2人工SEI 膜:将干燥后的TiO2粉末(天津产,99.9%)按照文献[6]的工艺喷涂在锂金属(天津产,99.9%)表面,然后用海绵包裹辊压机的辊轮(辊压压力为5 MPa,辊轮距离为50 μm),反复辊压到锂金属表面变黑为止。由于采用辊对辊工艺,过程规模可以扩大,也适合工业应用。所有操作均在手套箱[ω(H2O)<10-4%,ω(O2)<10-4%]或干燥室中进行。
样品制备在充满氩气的手套箱中完成。将制备的LixTiO2@Li 和Li 电极分别在碳酸二乙酯(DEC,深圳产,99.9%)溶剂中清洗干净,晾干后,用7311 SEM 专用导电胶带(日本产)粘贴在样品台上;随后,将制备的样品转移至取样瓶;最后,用封口膜封好瓶盖,将取样瓶移出手套箱[6]。
1.2 电池制备
实验制备了LixTiO2@ Li|LixTiO2@ Li 和Li|Li 对称电池,以测试TiO2改性后,对锂金属沉积的影响。以商用磷酸铁锂(LFP)电极(合肥产)为正极,Celgard 2400 膜(美国产)为隔膜,电解液为1 mol/L LiPF6/EC+DEC[体积比1 ∶1,添加10%氟代碳酸乙烯酯(FEC)和1%碳酸亚乙烯酯(VC),深圳产]。在手套箱中组装CR2025 型扣式电池,除另有说明外,电解液添加量均为40 μl。
1.3 测试分析
用Quanta 200 扫描电子显微镜(美国产)观察LixTiO2@Li 电极和循环后电极的形貌。用GERM D8 X 射线衍射仪(德国产)分析电极表面物质组成,CuKα,λ=0.154 184 nm,管流40 mA、管压40 kV,扫描速率为2(°)/min,步长为0.017°。用ESCALAB 250Xi X 射线光电子能谱(XPS)仪(美国产)测定电极表面的Ti、O、Li 等元素的键能。
用CT-4008 测试系统(深圳产)进行锂沉积性能、电池循环性寿命测试。LFP|LixTiO2@ Li 和LFP|Li 电池的测试电压为2.0~3.8 V,所有电池在1 mA/cm2的电流密度下进行测试。Li|Li 和LixTiO2@Li|LixTiO2@Li 对称电池测试的电流密度为5 mA/cm2时,沉积容量密度为5 mAh/cm2。用CHI660E 电化学工作站(上海产)进行电化学阻抗谱(EIS)测试,频率为10-2~105Hz,波形幅度为10-2~0.7 V 均方根值。
2 结果与讨论
2.1 电极制备及优化
利用金属锂的活化性质,用软海绵将适量TiO2微粉喷在锂箔金属表面,在辊压压力为5 MPa,辊轮距离为50 μm的条件下,经过多次反复机械擦拭,锂箔金属由原来的金属光泽变为黑色,白色的TiO2粉末也随之消失,说明TiO2和金属锂发生了化学反应,可通过辊对辊方法实现放大。
TiO2改性前后锂金属表面的照片,如图1 所示。

图1 TiO2 改性前后锂金属表面的照片Fig.1 Photos of the surface of lithium metal before and after TiO2 modifying
从图1(a)、(b)可知,制备LixTiO2@Li 电极后,锂金属从原始金属光泽变为黑色。LixTiO2@Li 电极表面由于人工喷涂操作的限制,仍残留白色的TiO2。为此,用DEC 溶剂洗涤制备的LixTiO2@ Li 电极,去除残留的TiO2粉末,并通过DEC 分解生成的有机产物,促进形成更致密的LixTiO2SEI 膜。这些聚合的多碳有机产物和胶水一样,将松散的LixTiO2@Li颗粒粘结在一起。从图1(c)可知,LixTiO2@Li 电极表面一致,白色TiO2的含量比初始LixTiO2@Li 少很多,说明残留的TiO2已被去除。
对LixTiO2@Li 电极的微观结构进行SEM 分析,结果如图2 所示。
从图2(a)可知,LixTiO2@Li 电极有一层致密的反应界面,约18 μm 厚。5 μm 厚的涂层可稳定锂金属负极的SEI膜,抑制锂枝晶的形成[8];从图2(b)可知,用DEC 清洗前,电极表面仍有一些分散的TiO2颗粒,由于固-固反应的限制,有明显的可见间隙;从图2(c)可知,用DEC 清洗后,由于DEC 的穿透,LixTiO2@Li 表面变得致密,间隙变少,并与金属锂发生反应,使这些颗粒粘结在一起。
2.2 电极表面物质组成分析
用XRD 分析确定电极表面的物质,结果如图3 所示。
图3 中,位于36.3°和52.2°处的强峰,均属于金属锂。LixTiO2没有明显的特征峰,主要是形成的LixTiO2为非晶态或含量较少所致;没有出现TiO2的峰,说明没有残留TiO2粉末。金属锂的特征峰消失,较大程度上是由于LixTiO2保护层的吸收效应。
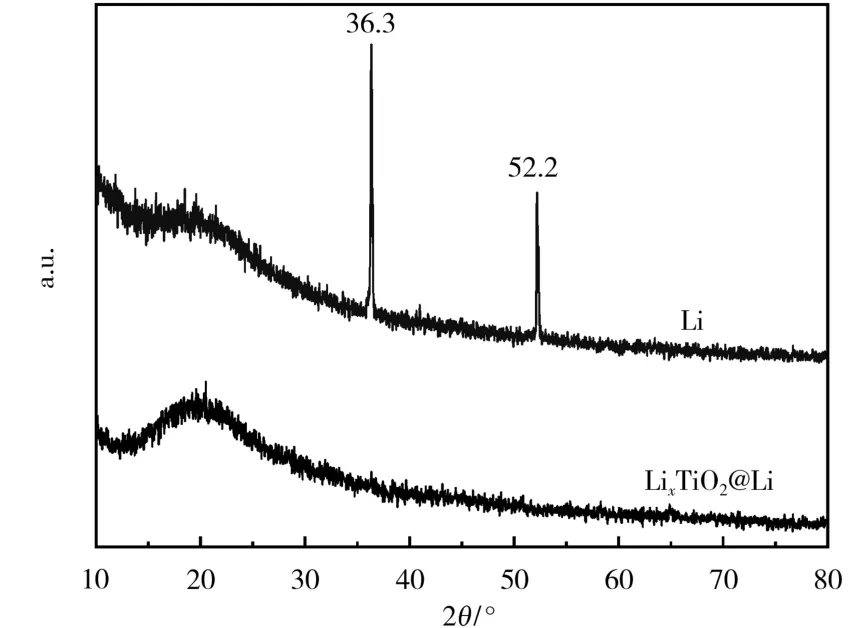
图3 LixTiO2@Li 和Li 电极表面的XRD 图Fig.3 XRD patterns of the surface of LixTiO2@Li and Li electrodes
2.3 电极表面元素键能的测定
为了确定锂金属与TiO2的反应,采用XPS 进一步分析电极表面组成,结果如图4 所示。
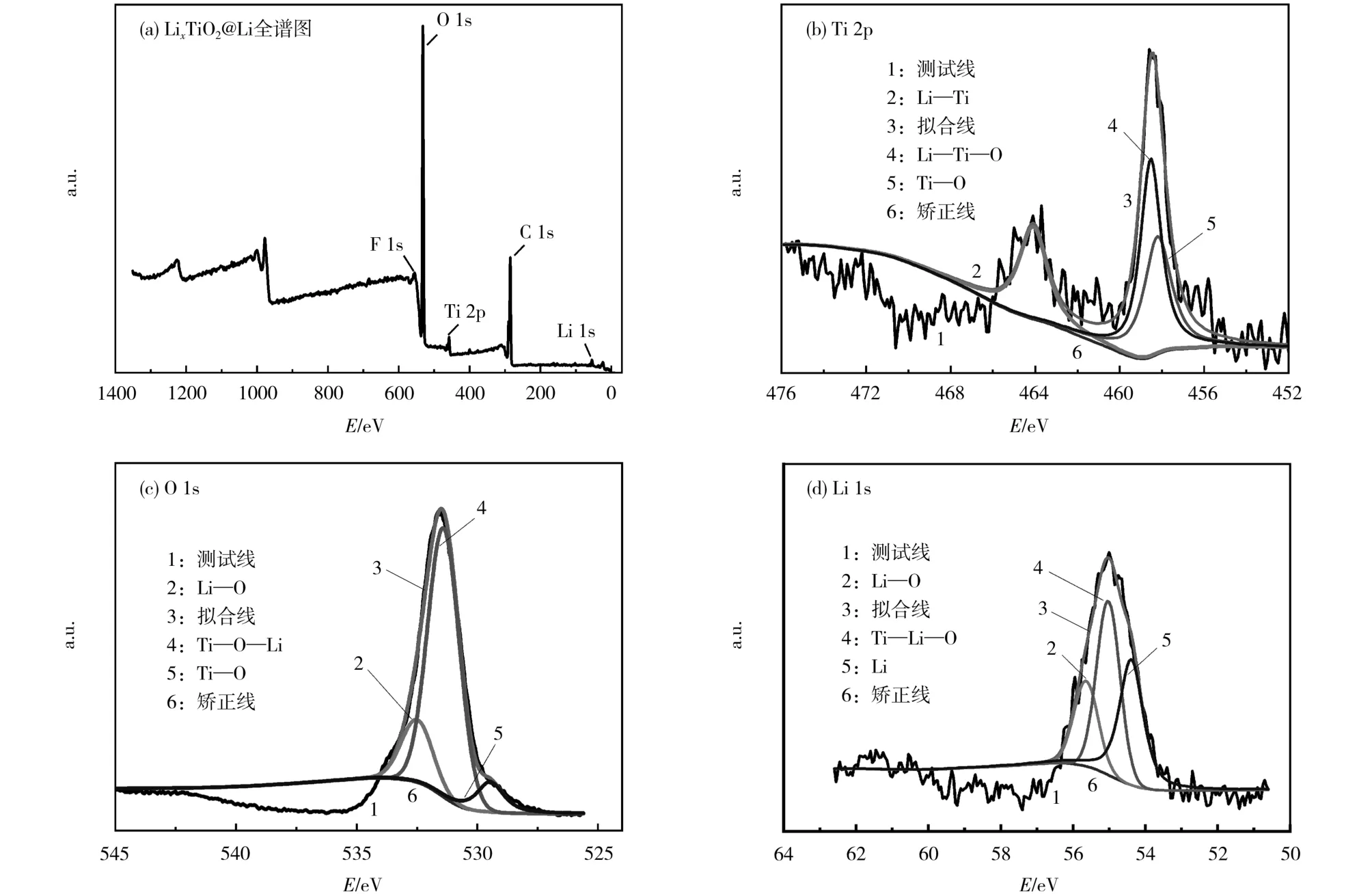
图4 LixTiO2@Li 电极表面的XPSFig.4 X-ray photoelectron spectroscopy(XPS) of the surface of LixTiO2@Li electrode
从图4(a)可知,Ti 元素的存在,表明TiO2已加入电极中。根据Ti 元素的峰值可知,除Ti—O 化学键应该来自于残留的TiO2颗粒外,在464.0 eV 和458.5 eV[9]处分别测得了Li—Ti 和Li—Ti—O 化学键[见图4(b)],说明Li 与TiO2之间发生了固-固反应。对O 元素和Li 元素进行分析,也可以得到相同的结果[见图4(c)和4(d)]。
2.4 电池性能测试
Li|Li 和锂沉积LixTiO2@Li|LixTiO2@Li 对称电池,以及LFP|Li 和LFP|LixTiO2@Li 全电池的电化学性能测试结果,如图5 所示。
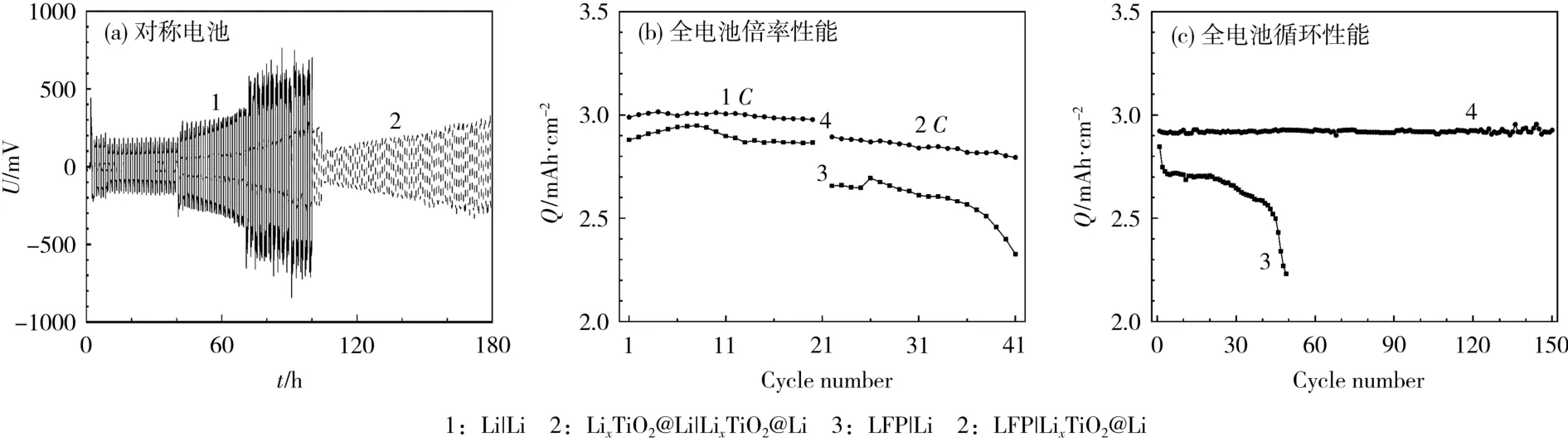
图5 TiO2 改性锂金属电池的电化学性能Fig.5 Electrochemical performance of TiO2-modified lithium metal batteries
从图5(a)可知,Li|Li 对称电池的电位在70 h 后急剧升高,100 h 后电池失效。过电位明显高于LixTiO2@Li|LixTiO2@Li 对称电池,表明锂的沉积形核(Li+得电子后被还原成锂原子,重新沉积在锂金属表面)能较大。LixTiO2@Li|LixTiO2@Li 对称电池可稳定地工作180 h,沉积电位约为200 mV,要低于Li|Li 电池的400~500 mV,说明在TiO2处理后,极化减轻。从图5(b)可知,当充放电倍率为1C(对应电流密度为3 mA/cm2)时,LFP|LixTiO2@Li 电池的放电容量密度约为3 mAh/cm2。即使充放电倍率增加到2C,容量密度也没有明显衰减,仍有2.9 mAh/cm2。充放电倍率对LFP|Li 电池的放电容量有一定影响,当倍率由1C增加到2C时,放电容量密度由2.9 mAh/cm2下降到2.6 mAh/cm2。从图5(c)可知,LFP|LixTiO2@Li 电池可稳定地循环150 次,但LFP|Li电池在循环44 次后,出现了明显的容量衰减。以上结果表明,所制备的LixTiO2SEI 膜改善了锂金属负极的性能。
用EIS 分析循环前后的电池阻抗,结果如图6 所示。
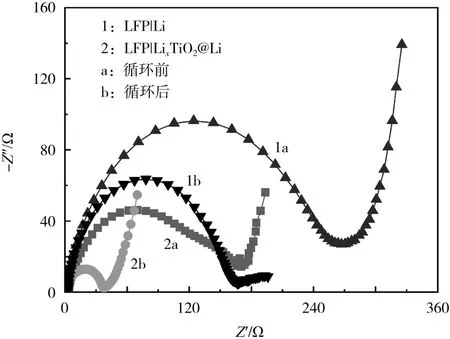
图6 LFP|Li 和LFP|LixTiO2@Li 全电池的EISFig.6 Electrochemical impedance spectroscopy(EIS) of LFP|Li and LFP|LixTiO2@Li full batteries
从图6 可知,TiO2处理后,电池阻抗比锂金属负极低,原因是构建的LixTiO2SEI 膜相比于整块的锂片具有更好的电解液润湿性。当充放电倍率为1C时,循环5 次后再次测定阻抗,与初始状态相比,LFP|Li 和LFP|LixTiO2@Li 电池的阻抗降低,得益于循环激励效应。循环后LFP|LixTiO2@ Li电池的内阻远小于LFP|Li 电池,说明LixTiO2SEI 膜阻止了金属锂表面的劣化,改善了锂沉积。
拆解循环后的LFP|LixTiO2@Li 电池,进行电极外形观察,结果如图7 所示。

图7 循环后的LixTiO2@Li 电极的照片Fig.7 Photo of LixTiO2@Li electrode after cycle
从图7 可知,LixTiO2@Li 电极经过5 次循环后,较为完整致密,可见锂沉积较为理想。由于锂枝晶的形成,裸露的金属锂变得粉碎、凌乱。
采用SEM 分析循环的锂和LixTiO2@ Li 电极的微观结构,如图8 所示。
从图8(a)可知,循环过程中,金属锂与电极发生了压碎分层。从图8(b)可知,循环后的LixTiO2@Li 电极较为致密,生成的SEI 膜厚度约为64 μm,而剩余的锂金属仍保持完整,说明仅在这一区域发生了锂化反应。循环后LixTiO2@Li 的表面与金属锂不同[见图8(c)],表面致密,并包覆了一层保护层[见图8(d)],没有发现锂枝晶,说明包覆的LixTiO2改善了锂的沉积情况。

图8 循环后电极的微观形貌Fig.8 Micromorphology of electrodes after cycle
通过XPS 分析LixTiO2SEI 膜的作用,结果如图9 所示。
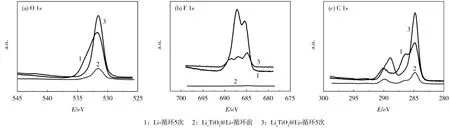
图9 循环前后Li 和LixTiO2@Li 电极表面的XPSFig.9 XPS of the surface of Li and LixTiO2@Li electrodes before and after cycle
从图9(a)可知,初始状态的LixTiO2@Li 电极的O 含量比初始状态的锂金属低[7,10],循环后,LixTiO2@ Li 电极LixTiO2SEI 膜的形成,产生了更强的O 峰。另外,从F 键能的分析来看[图9(b)],LixTiO2@ Li 和Li 的键能差异明显,说明SEI 膜主要是由LixTiO2决定。从图9(c)可知,LixTiO2@Li 电极和Li 电极循环5 次后,表面出现的含C 峰明显不同,表明涂覆TiO2后,影响了锂片表面SEI 膜的成分。
3 结论
通过机械喷涂TiO2粉末,在锂金属表面构建LixTiO2SEI膜,使金属锂与TiO2发生均匀的固-固相沉积反应。制备的LixTiO2@Li 电极的锂沉积更为致密、均匀,未发现锂枝晶。
对与商用LFP(约3 mAh/cm2)配对制备的全电池进行研究,发现LixTiO2@Li 负极电池能够以1 mA/cm2的电流密度在2.0~3.8 V 稳定循环150 次;在充放电倍率为2C的条件下,与相同条件下商用LFP 相比,容量没有出现明显的下降,电池性能比锂金属负极电池好。致谢:感谢四川大学教育部磷资源重点实验室绿色过程工程研究开发中心以及四川轻化工大学材料科学与工程学院对本工作的支持。
