非综合征性耳聋一家系TECTA基因突变分析
2022-07-04张翠荣李守霞李书瑞陈丁莉郭祥瑞陈永学刘子甲张瑞敏宋学东
张翠荣, 李守霞, 李书瑞, 陈丁莉, 郭祥瑞, 陈永学, 刘子甲, 张瑞敏, 宋学东
(1.河北省邯郸市中心医院, 河北 邯郸 0560082.山东第一医科大学附属省立医院, 山东 济南 2500213.上海交通大学电子信息与电气工程学院, 上海 201100)
耳聋已经排在全球残疾性问题的第四位[1]。听力损失会造成诸多负面影响,如人际交流障碍、不利于心理健康发展、降低就业范围、生活质量低下等。研究显示,每500~600个新生儿就有一个发生先天性听力损失,约60%的是由基因突变引起[2]。随着中国人生活水平、居住环境和医疗条件的改善与提升,环境因素致聋得到有效控制,遗传性因素则逐渐成为中国人致聋主要的致病因素[3]。The Hereditary Hearing Loss Homepage(http:// hereditary- hearingloss.org/)数据库显示,遗传性耳聋相关基因中,非综合征性耳聋(Non-syndromic hearing loss, NSHL)已发现超过80个具有致病性的耳聋基因,涉及超过1000种致病的变异和150个相关基因区域功能的改变[4]。在常染色体、性染色体和线粒体等均有耳聋相关基因的分布,与基因突变相关的耳聋具有遗传性,临床上表现出高度的遗传异质性和基因的多效性。在本研究中,我们课题组应用二代测序技术和Sanger测序的方法相结合,对邯郸地区1个耳聋家系成员进行了遗传性耳聋基因的检测,发现先证者(II∶1)与母亲(I∶2)均存在TECTA基因c.5137 T > C(p.Phe1713Leu)新发杂合突变,为耳聋家系成员遗传咨询与产前诊断提供实验和理论基础。
1 病例资料
1.1研究对象:先证者家系成员2代共3人,先证者,其父亲、母亲,其中患者2人。先证者出生后听力测试未通过,经脑干诱发电位检测结果显示,两侧波形分化差,重复性不佳,表现为高频区中度耳聋,先证者母亲表现为耳聋。本研究已通过邯郸市中心医院伦理委员会的批准,家系成员签署知情同意书,收集遗传病相关等临床资料,如先证者基本信息、母亲孕前高危因素及孕期情况、家族史和实验室检查等。由临床医师对耳聋家系全部成员进行体格检查(主要包括耳科、眼科、皮肤、消化系统等), 由护士采集耳聋家系成员的外周静脉血2~5mL,放置于EDTA抗凝的采血管,为后续的实验做准备。
1.2临床表现:先证者(II∶1),6个月,女性,出生后听力测试未通过,经脑干诱发电位检测结果显示,两侧波形分化差,重复性不佳,表现为高频区中度耳聋,视力正常,智力正常,无其他系统异常,无耳毒性药物使用史。先证者父亲(I∶1)听力正常;先证者母亲(I∶2)表现为耳聋,视力正常,智力正常,无其他系统异常,无耳毒性药物使用史。家系图谱见图1。
图1 遗传性耳聋家系图谱
1.3家系成员二代测序:先证者(II∶1)TECTA基因(NM_005422)的第15外显子(Exon15)存在c.5137 T > C(p.Phe1713Leu)杂合错义突变(详见表1和表2)。先证者母亲(I∶2)携带该突变,先证者父亲(I∶1)未发现突变。ACMG显示:中等致病的证据PM1是该突变位于TECTA基因突变热点和(或)位于已知无良性变异的关键功能区域;中等致病的证据PM2是该突变在EXAC数据库、ESP数据库和千人基因组数据库中正常对照人群中未发现的变异(或隐性遗传方式中频率极低);支持致病的证据 PP3经多种算法预测会对TECTA基因或基因产物功能造成有害影响的变异。参考数据库HGMD Pro、PubMed和ClinVar等显示TECTA基因(NM_005422)c.5137 T > C(p.Phe1713Leu)杂合错义突变,尚未见文献报道。未发现有临床意义的线粒体基因变异和CNV 变异。经MutationTaster、SIFT 和Polyphen2等软件预测,TECTA基因(NM_005422)c.5137 T>C(p.Phe1713Leu)杂合错义突变为有害。

表1 先证者(II∶1)二代测序发现TECTA基因(NM_005422)的第15外显子(Exon15)存在c.5137 T > C(p.Phe1713Leu)杂合错义突变

表2 先证者(II∶1)二代测序发现TECTA基因(NM_005422)c.5137 T > C(p.Phe1713Leu)杂合错义突变频率
1.4Sanger测序进行家系验证:Sanger测序结果验证,先证者(II∶1)TECTA基因(NM_005422)存在c.5137 T > C杂合突变,与二代测序结果一致;先证者母亲(I∶2)携带TECTA基因(NM_005422)存在c.5137 T > C杂合突变;先证者父亲(I∶1)未发现突变;先证者(II∶1)TECTA基因c.5137 T > C杂合突变来源于母亲。详见图2。
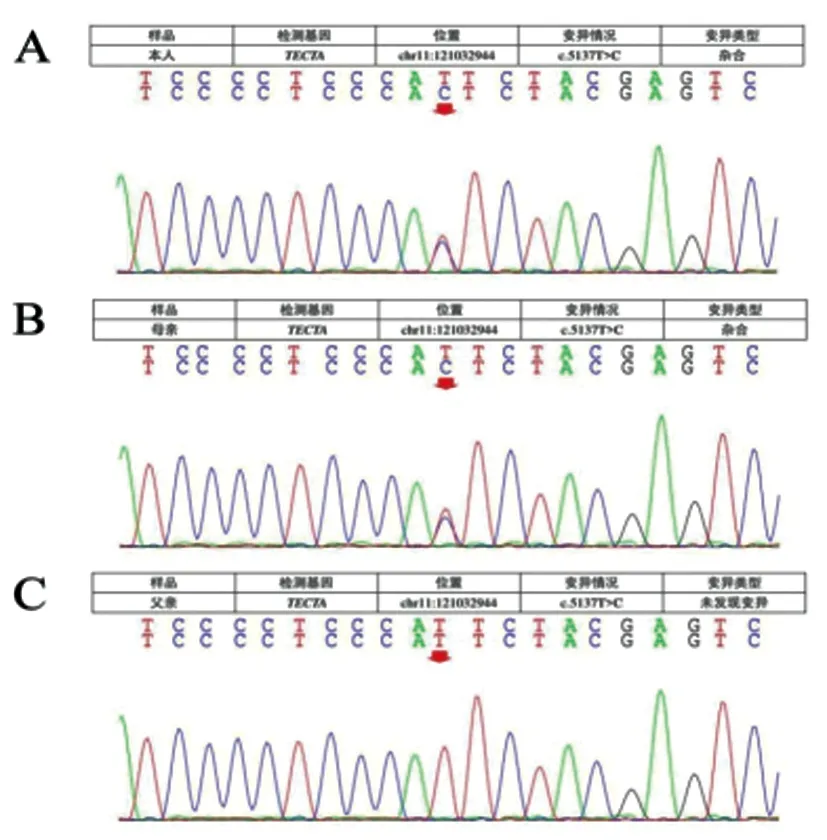
图2 Sanger测序结果验证
2 讨 论
耳聋是全世界最常见的功能残疾之一。在遗传性耳聋患者中,根据是否伴随其它器官和系统异常,又可以分为综合征和非综合征性耳聋两种,NSHL约占70%,其临床上仅出现听力损失或障碍。研究显示,已鉴定出的NSHL基因总数124(http:// hereditaryheafin910ss.org.;最后访问日期为2021年9月5日);其中常染色体隐性遗传基因78个,常染色体显性遗传基因51个(GJB2、GJB6、MYO7A、TECTA、MY03A、MY06、COL11A2、PTPRQ、TBC1D24、CEACAM6等10个基因,既是常染色体隐性又是常染色体显性遗传基因),X连锁遗传基因5个,此外还有一小部分通过母系的线粒体遗传[5]。目前临床上听力筛查与遗传性耳聋基因筛查等工作相结合,既可发现先天性的听力损失或障碍,又可预防因遗传因素导致的进行性、迟发性听力损失或药物性致聋的发生。
TECTA基因(OMIM602574)定位于染色体11q22-24,具有23个外显子,包含6465个碱基对,编码2155个氨基酸的前体蛋白,由ZA、ZP和ENT三个结构域构成[6]。研究显示,ZA结构域存在杂合突变c.3995G>T可引起高频听力损伤,ZP结构域的c.5618C>T杂合突变可致中频听力损伤,ENT结构域c.266delT的纯合突变和c.710C>T杂合突变可导致中频与高频的听力损伤[7]。TECTA基因突变具有高度的遗传异质特性,根据突变位点的不同其遗传方式可以表现为常染色体显性或常染色体隐性,可导致DFNA8/12型耳聋、DFNB21型耳聋和某些雅各布森综合征的听力损失等[8]。在一个家系成员中发现6名成员携带TECTA c.734G>A杂合突变,遵循常染色体显性遗传[9]。周赤燕[10]研究发现,先证者存在TECTA基因c.1893C>A纯合突变,先证者父母均携带TECTA 基因c.1893C>A杂合突变,但听力正常,与常染色体隐性遗传的特点相符。在本家系中,先证者(II∶1)TECTA基因c.5137 T > C杂合突变发生在ZP结构域,临床表现为先天性高频中度耳聋;先证者母亲(I∶2)携带TECTA基因c.5137 T > C杂合突变,先证者父亲(I∶1)听力正常,与常染色体显性遗传的特点相符。
目前研究显示,TECTA基因的突变多发生于国外,在中国的耳聋家系中基因突变报道的不多,如TECTA c.257-262delinsGCT、TECTA c.1893C>T、TECTA c.990C>A、TECTA c.5945C>A等[11]。中国常见的耳聋筛选基因主要是GJB2、GJB3、SLC26A4和MT-RNR1 4个基因,TECTA不是常见耳聋筛查基因,容易导致漏筛,也许是导致TECTA基因突变检出率低的原因。
综上所述,耳聋家系成员进行耳聋基因的筛查,对遗传咨询和产前诊断具有重要意义。本例家系先证者及目前均携带TECTA基因c.5137 T>C(p.Phe1713Leu)杂合突变,未见相关文献报道,可能是该家系患者致聋的原因,后续会持续追踪患儿的发育和耳聋情况,进行进一步的研究。使用二代测序与Sanger测序相结合,提高基因突变检出准确率,将提高对耳聋患者的诊断价值,有助于遗传性耳聋相关疾病的预防、早期干预或改进治疗等。
