广西地区耳聋基因突变与人工耳蜗植入术后疗效的关联性研究
2022-04-08黄兰诚林钻平唐凤珠瞿申红陆秋天黄玉英李凤提
黄兰诚, 林钻平, 唐凤珠, 瞿申红, 陆秋天, 王 涛, 黄玉英, 李凤提
耳聋是影响人类健康和生活质量的风险因素之一[1],是全球范围内备受关注的公共卫生问题。据统计,我国听力残疾者约有2 780万人,且在语前听力丧失的患者中有约60%为遗传因素所致[2]。人工耳蜗(cochlear implant,CI)是目前唯一获得国际认可,用于治疗重度-极重度感音神经性聋的生物医学装置[3],其工作原理主要是绕过耳蜗病变部位,将声学信号转化成为电信号直接刺激患者的螺旋神经节细胞和听神经,从而帮助患者获得听觉。大多数耳聋患者在CI植入术后配合规范的康复训练可获得不同程度的听力和言语功能的提高。随着研究的进展,学者们除了认识到植入年龄和CI植入术后康复治疗是影响疗效的关键因素外[4],还认为遗传因素的差异也会影响CI植入的术后疗效。鉴此,本研究旨在探讨广西地区CI植入术后疗效与致聋基因突变情况的关联性,以期为更好地评估术后康复效果及指导耳聋治疗提供依据。
1 对象与方法
1.1研究对象 选择2012年7月至2019年12月于广西壮族自治区人民医院、广西医科大学第一附属医院和中国人民解放军联勤保障部队第九二三医院行CI植入术并进行4种常见致聋基因15个突变位点筛查的语前聋患者104例,其中男61例,女43例,年龄1~20岁,平均年龄6.65岁。汉族63例,壮族34例,瑶族4例,苗族3例。所有患者及其监护人知情同意参加本研究。
1.2纳入与排除标准 纳入标准:(1)籍贯为广西,且三代人均在广西居住;(2)术前根据1997年世界卫生组织听力损失程度分级标准诊断为双耳重度或极重度感音神经性聋;(3)佩戴助听器不能有效获得听力;(4)无手术禁忌证,可耐受CI植入手术;(5)术后能有条件到正规康复机构接受系统规范的听力言语训练满1年。排除标准:(1)智力发育严重低于同龄人;(2)有明确致聋病因,如脑膜炎、耳外伤、听神经瘤等;(3)临床资料不全或术后失访者。
1.3听力学检查 所有研究对象术前由专业的听力师通过科丽纳听力设备(尔听美,丹麦)进行系统的听力学检查,检查内容包括纯音测听、声导抗、听性脑干反应(auditory brain stem response,ABR)、多频稳态听觉诱发电位(auditory steady state response,ASSR)、畸变产物耳声发射(distortion product otoacoustic emission,DPOAE)。
1.4影像学检查 所有研究对象术前需进行冠状位+轴状位颞骨CT(设备:飞利浦64排CT,荷兰)、头颅MRI平扫(设备:西门子,德国)及内耳水成像检查,以判断患者是否有中耳、内耳严重畸形及中耳炎症等病变。术后均复查颞骨CT(冠状位+轴状位)明确CI电极插入的位置。
1.5耳聋基因检测 采集受检者(包括患儿及其亲属)外周静脉血3~5 ml。应用博奥生物集团有限公司晶芯15项遗传性耳聋基因检测试剂盒(微阵列芯片法)检测4个常见致聋基因(GJB2、SLC26A4、线粒体12SrRNA、GJB3)的15个常见突变位点:GJB2(35delG、235delC、176del16、299del AT)、SLC26A4(2168A>G、IVS7-2A>G、1174A>T、1226G>A、1229C>T、1975G>C、2027T>A、IVS15+5G>A)、线粒体12SrRNA(1494C>T、1555A>G)和GJB3(538C>T)。对检出突变的患者行Sanger测序,而对未检出突变的患者标本进一步送博奥晶典生物技术有限公司行全外显子测序。根据基因突变情况分为突变组(14例)和非突变组(90例)。绘制具有罕见位点突变或新位点突变的耳聋患者的家系图。
1.6CI植入手术 所有研究对象在全身麻醉下行术侧耳后切口,并根据患者具体情况差异选择不同术式。(1)圆窗膜入路方式:磨平圆窗龛后,以显微钩针钩开圆窗膜,扩大圆窗,将CI接收器固定于耳后的骨槽内,再将CI作用电极自圆窗插入耳蜗蜗轴,以肌肉填塞固定电极。(2)鼓阶入路方式:于圆窗龛前下方行耳蜗底回开窗,再将CI电极插入鼓阶。术中检测电极神经遥感反应(neural response telemetry,NRT)。
1.7疗效评估 采用听觉行为分级标准(Categories of Auditory Performance,CAP)[5]和言语可懂评分标准(Speech Intelligibility Rating,SIR)[6]评分评估患者术后疗效。CAP详见表1,SIR详见表2。通过门诊随访或电话随访的方式在术后3个月、6个月和12个月进行CAP和SIR评估。

表1 CAP[5]

表2 SIR[6]
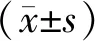
2 结果
2.1听力学检查及影像学检查结果 104例患者听力学检查结果示双侧ABR阈值>95 dBnHL。在2 kHz以下,双侧ASSR反应阈值均>100 dBHL,双侧DPOAE均未引出。术前影像学检查示双侧大前庭水管综合征(large vestibular aqueduct syndrome,LVAS)5例,双侧Mondini畸形4例,同时伴有LVAS和半规管发育不良者2例,其余无异常。
2.2基因检测结果 104例患者中有14例(13.46%)检出致聋基因突变。GJB2基因突变2例,均为汉族;其中1例为c.235delC纯合突变,1例为c.299delC杂合突变。SLC26A4基因突变10例(9.62%),有6例为汉族,3例为壮族,1例为瑶族;其中8例为c.IVS7-2A>G杂合突变,2例为c.919-2A>G/c.1614+5G>A复合杂合突变。OTOF基因c.1273C>T/c.4994T>C复合杂合突变1例(0.92%),TRIOBP基因c.5185-2A>G/c.3299C>A复合杂合突变1例(0.92%),均为汉族。未检出GJB3和线粒体12SrRNA基因突变。
2.34例新突变位点病例的基因突变家系图 在本次研究中,有4例患者检测出新位点突变。经询问家族史得知这4例患者分别来自3个家庭,有2例为双胞胎姐妹;其余2个家庭中均有2例耳聋患者(为兄弟)。根据所得信息绘制家系图,这4例患者分别为SLC26A4基因c.919-2A>G/c.1614+5G>A复合杂合突变2例(见图1);OTOF基因c.1273C>T/c.4994T>C复合杂合突变1例(见图2);TRIOBP基因c.5185-2A>G/c.3299C>A复合杂合1例(见图3)。

图1 2例SLC26A4基因c.919-2A>G/c.1614+5G>A突变患者家系图
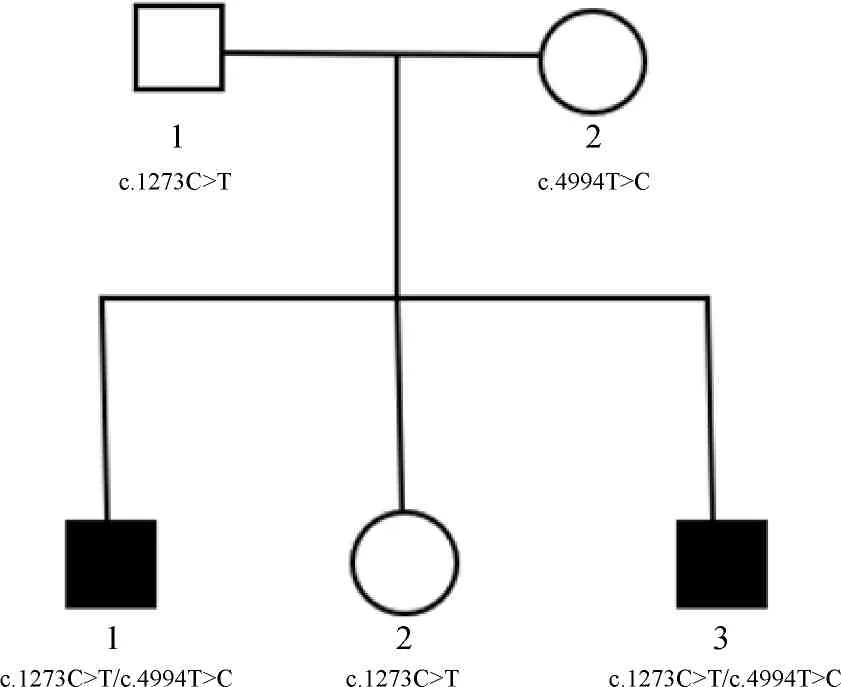
图2 1例OTOF基因c.1273C>T/c.4994T>C突变患者家系图
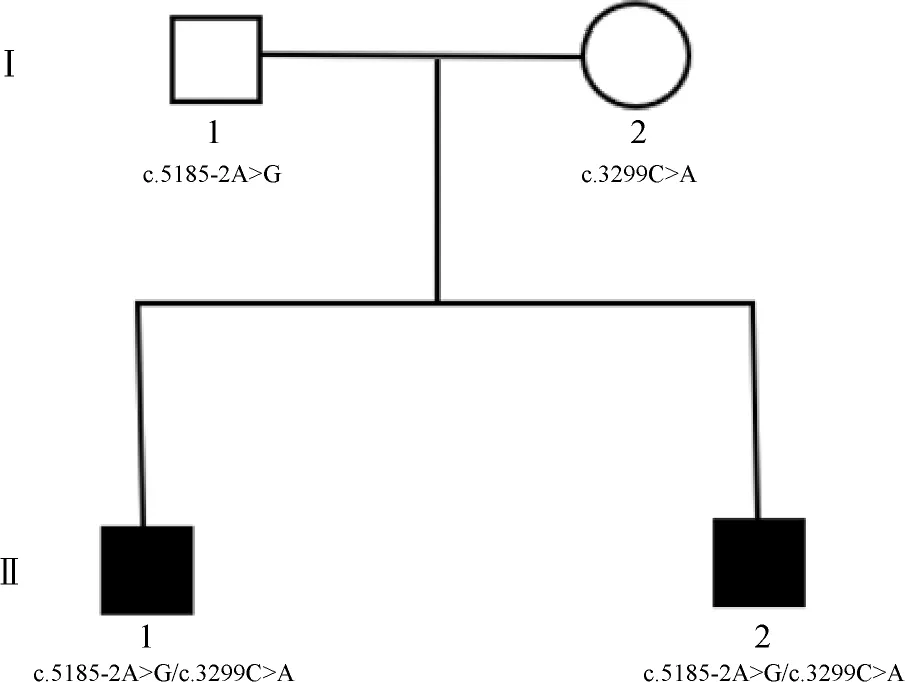
图3 1例TRIOBP基因c.5185-2A>G/c.3299C>A突变患者家系图
2.4CI植入情况 104例患者术中均顺利植入CI作用电极,其中使用澳大利亚Cochlear品牌的CI 73例,美国AB品牌的CI 13例,诺尔康品牌的CI 18例。术中检测NRT反应良好。术后未见并发症,复查颞骨CT均显示耳蜗电极在位。术后1个月开机,嘱患者及其监护人根据自身情况定期进行言语处理器调试。
2.5两组术后各时间点CAP和SIR评分比较 在术后3个月、6个月和12个月,两组术后CAP和SIR评分均呈上升趋势(P<0.05),但两组变化差异无统计学意义(P>0.05)。见表3。

表3 两组术后各时间点CAP和SIR评分比较分]
3 讨论
3.1近年来,CI对治疗重度和极重度感音神经性聋所取得的良好疗效已被广泛认可。在语前聋患者中,基因突变是致聋的关键因素,基于基因诊断水平评估患者CT植入术后疗效可进一步降低患者因术后疗效不佳而承担的经济和手术风险。本课题组前期研究主要检出GJB2和SLC26A4两种常见的耳聋基因突变,经过全外显子组测序检测出SLC26A4基因c.919-2A>G和c.1614+5G>A位点突变,且经过实验验证认为c.1614+5G>A位点是致病突变[7]。此外,在罕见耳聋基因OTOF和TRIOBP上首次发现复合杂合突变各1例,经过美国医学遗传学与基因组学学会(The American College of Medical Genetics and Genomics,ACMG)对这两种基因新发现的突变位点进行致病性分析,认为OTOF基因c.1273C>T/c.4994T>C突变[8]和TRIOBP基因c.5185-2A>G/c.3299C>A突变是致聋的主要原因[9]。经过术后随访,这些罕见基因或新位点突变的患者与常见耳聋基因突变患者术后听力言语功能均有提高。
3.2有研究表明,GJB2和SLC26A4突变患者在CI植入术后能获得良好的疗效[10],甚至认为GJB2基因突变患者术后疗效优于非基因突变的耳聋患者[11]。孔颖等[12]对42例行CI植入术并GJB2基因突变的患者进行术后随访,比较患者术后不同时间点对声母、韵母、双音节词的识别差异,结果表明该基因突变患者术后可获得显著的听力重建效果和言语功能的提高。而OTOF基因早期被认为是CI术后疗效不佳的原因之一[13],但随着OTOF基因研究的不断深入,Wu等[14]认为,OTOF基因与GJB2和SLC26A4基因在CI术后疗效上没有显著差异。对于TRIOBP基因突变的患者,将患者CI植入术前和术后的听力检查结果进行对比后认为CI植入是帮助TRIOBP突变患者有效提高听力的最佳治疗方式[15]。在本次研究中,基因突变患者均能获得令人满意的术后效果,但考虑到罕见基因突变样本量过小而未进行单独分组比较。
3.3CI植入的有效性依赖于听觉神经的完整,基因突变患者CI术后能对声音敏感是源于基因的表达部位在内耳[16-17]。GJB2是目前我国非综合征性耳聋人群最主要的致聋基因,其负责编码参与内耳非感觉上皮细胞离子传递的缝隙连接蛋白26(connexin 26,Cx26)。Cx26缺失或表达异常是致聋的关键因素[18]。SLC26A4是继GJB2后另一种常见的遗传性耳聋基因,与LVAS密切相关。本研究检出11例患者有内耳畸形,但未发现蜗神经发育不良的患者。虽然LVAS一定程度上增加了手术的难度和术后并发症出现的概率,但内耳畸形患者CI植入术后的听力和言语能力与耳蜗结构正常的患者相同[19-20]。此外,本研究检出的TRIOBP和OTOF罕见耳聋基因的表达也局限于内耳,其中TRIOBP致聋的机制是影响内耳支持细胞的刚度[21],而OTOF编码的耳畸蛋白(otoferlin)是毛细胞神经突触兴奋传递过程中钙离子的感受器[22]。根据这些基因突变引起内耳的病理改变和CI的工作原理,给予我们判断不同基因突变在CI术后效果上的理论支持。本次研究的结果也基本符合理论。
3.4在本研究中,基因突变组与非基因突变组患者CI术后经过听力言语康复训练后获得的疗效相似,罕见基因新发突变位点的患者经CI术后也能获得良好的疗效。但由于罕见基因突变样本量小,未能体现不同基因突变患者在CI术后康复疗效上的差异,应在后期的研究中扩大样本量进一步研究。此外,广西地区是少数民族聚居的地区,其耳聋基因突变谱与其他地区存在一定差异。该地区GJB2和SLC26A4的突变率低于全国水平,本研究基因检测发现SLC26A4、OTOF和TRIOBP基因上新发的突变位点,说明该地区存在耳聋基因新位点突变,有待进一步研究。
