卡瑞利珠单抗联合化疗一线治疗晚期肺鳞癌的临床疗效分析
2022-03-05郝娜李楠郭温馨刘艳粉王丽萍
郝娜 李楠 郭温馨 刘艳粉 王丽萍
肺癌是全球癌症相关死亡的首要原因[1],肺鳞癌是肺癌中常见的病理类型,晚期肺鳞癌因其表皮生长因子受体(epidermal growth factor receptor, EGFR)基因突变和间变性淋巴瘤激酶(anaplastic lymphoma kinase, ALK)融合基因重排率低,其治疗局限于放化疗,预后较差[2-3]。卡瑞利珠单抗是一种人源化IgG4 kappa单克隆抗体[4],与PD-1受体结合后阻断PD-1/PD-L1信号通路的传导,解除免疫抑制从而发挥抗肿瘤作用[5],目前已在经典霍奇金淋巴瘤、肝癌、食管癌等癌种中显示良好的抗肿瘤疗效[4, 6-7]。Camel研究中卡瑞利珠单抗联合化疗一线治疗非鳞非小细胞肺癌,mPFS长达11.3个月[8]。因此本研究的主要目的是评估卡瑞利珠单抗联合化疗一线治疗晚期肺鳞癌的安全性和有效性。
资料与方法
一、一般资料
本研究经郑州大学第一附属医院伦理委员会的批准,回顾性分析了2018年4月至2020年10月郑州大学第一附属医院收治的初诊为临床分期ⅢB~Ⅳ期驱动基因阴性的78名肺鳞癌患者的临床资料。将卡瑞利珠单抗联合化疗组归为观察组,单纯化疗组归为对照组。整理并记录两组基线资料,包括年龄、性别、ECOG评分、吸烟史、临床分期、肝转移、脑转移,差异均无统计学意义(P>0.05)(见表1)。

表1 两组基线资料比较[n(%)]
二、纳入与排除标准
纳入标准:(1)病理类型为鳞状细胞肺癌;(2)根据IASLC第八版临床分期为ⅢB~Ⅳ期;(3)基因检测提示驱动基因阴性;(4)年龄≥18岁;(5)ECOG评分为0~1分;(6)至少存在1个可测量病灶(RECIST 1.1标准);(7)无活动性脑转移 ;(8)既往未接受过抗肿瘤治疗。
排除标准:(1)有神经系统症状的脑转移;(2)有需要使用糖皮质激素的非感染性肺炎病史;(3)驱动基因表达阳性;(4)自身免疫性疾病活动期患者;(5)病例资料不完整。
三、治疗方法
1 对照组
白蛋白结合型紫杉醇 260mg·m-2第1天,卡铂AUC=6mg·mL-1·min-1第1天,静脉滴注。每21天为1个周期,规律化疗4~6个周期。若化疗期间评估疾病进展,则进入二线治疗,若化疗4~6周期后疾病评估为CR、PR或SD,则每8周复查CT、彩超等影像学检查评估疗效。
2 观察组
卡瑞利珠单抗200mg静脉滴注第1天,化疗药物应用方案同对照组,每21天为1个周期。治疗期间初次评估疾病进展但临床状态稳定的患者继续原方案治疗2周期后重新评估;治疗期间初次评估疾病进展但临床状态不稳定的患者,停止抗肿瘤治疗,给予对症支持治疗,待临床状态稳定后,进入二线治疗。若化疗4~6周期后疾病评估为CR、PR或SD,则卡瑞利珠单抗规律维持治疗,直至影像学评估疾病进展或者出现不可耐受的毒性反应,最多疗程不超过35个周期。
四、疗效评价
每2周期行影像学检查(CT、彩超、骨扫描、头颅MRI、或PET-CT等)评估疗效,评估疗效标准:根据RECIST 1.1标准,可分为完全缓解(CR)、部分缓解(PR)、疾病进展(PD)及疾病稳定(SD),ORR=CR+PR/总例数×100%,DCR=CR+PR+SD/总例数×100%。对于观察组,治疗期间,根据RECIST 1.1标准初次评估为PD且临床状态稳定的患者,原方案治疗2周期后根据iRECIST标准再次评估。
五、观察指标
主要观察指标:(1)PFS;(2)ORR,DCR;(3)观察两组皮疹、消化道反应、骨髓抑制情况等不良反应的差异。末次随访时间为2021年3月20日。
六、统计学方法
结 果
一、两组疗效比较
1 治疗两周期后评估疗效
ORR观察组高于对照组(56.4% VS 41.0%,P>0.05)。DCR对照组高于观察组(84.6% VS 92.3%,P>0.05),但差异均无统计学意义(见表2)。
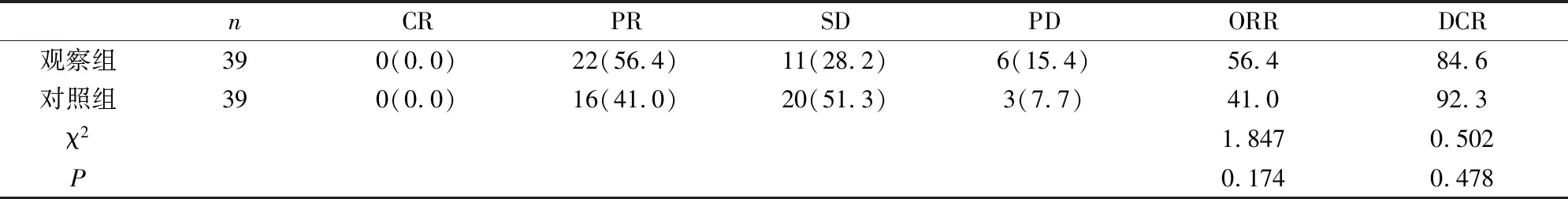
表2 两组患者治疗两周期后的疗效比较[n(%)]
2 两组PFS的比较
观察组mPFS与对照组相比,mPFS延长了2.7个月(8.00个月,95%CI:6.988~9.012 VS 5.30个月,95%CI:4.188~6.412),差异具有统计学意义(χ2=10.782,P<0.05)(见图1)。

图1 两组无进展生存期的比较
二、两组不良事件的比较
观察组最常见的不良反应是RCHs(32/39,82.1%)、骨髓抑制(24/39,61.5%)及消化道反应(18/39,46.2%);对照组最常见的不良反应是骨髓抑制(23/39,59.0%),消化道反应(16/39,41.0%)及肝功能损伤(12/39,30.8%)。与对照组相比,RCHs是卡瑞利珠单抗特异的不良反应,差异有显著统计学意义(P<0.001)(见表3)。两组3~5级不良事件发生率差异无统计学意义(均P>0.05),无治疗相关致死事件发生(见表4)。
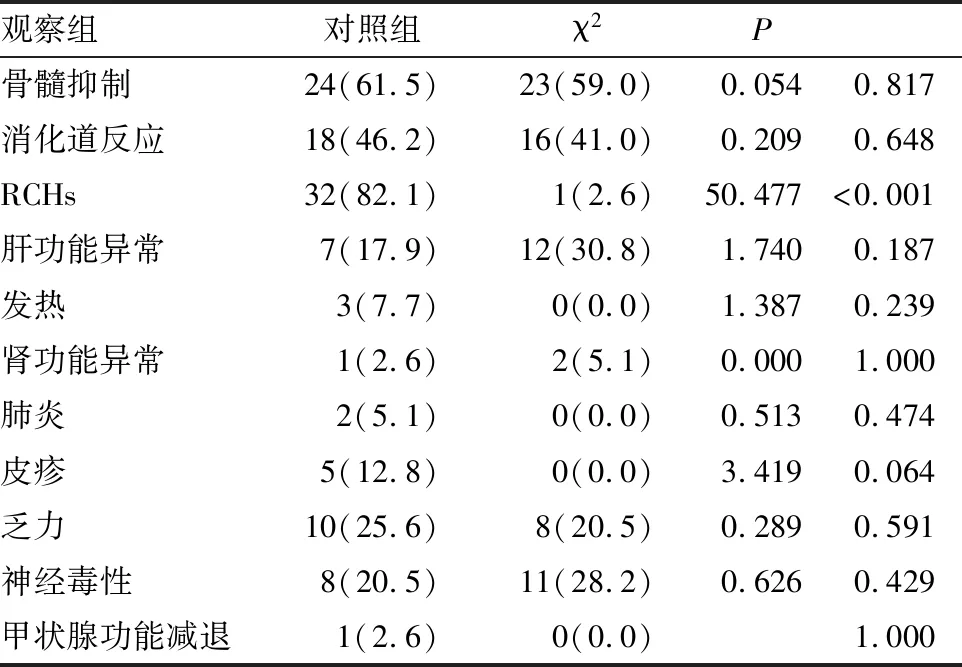
表3 两组任何级别的不良事件的比较[n(%)]

表4 两组3~5级不良事件的比较[n(%)]
讨 论
虽然既往研究表明NSCLC患者可以从PD-1/PD-L1抑制剂单药中获益,但仅限于少数人群,因此如何让更多的患者获益是亟待解决的问题。
白蛋白结合型紫杉醇属于紫杉烷类细胞毒药物,在有丝分裂中与游离微管蛋白结合,增加微管稳定性,阻止 DNA 分离,从而阻止细胞分裂,最终导致细胞死亡[9]。近来研究发现,紫杉烷类化疗药物可以通过提高肿瘤微环境中高迁移率族蛋白B1(HMGB1) 和 趋化因子CXCL11 的水平从而募集更多的CD8+T细胞到肿瘤微环境中[10],减少Treg细胞并抑制Treg细胞的功能,减少MDSCs的数量并促进MDSCs向M1样巨噬细胞分化[11]等途径发挥免疫调节的作用,这些都有利于提高免疫治疗的抗肿瘤免疫反应。本研究结果表明,与单纯化疗相比,卡瑞利珠单抗联合白蛋白结合型紫杉醇及卡铂一线治疗驱动基因阴性的肺鳞癌明显延长了患者的无进展生存期。
Keynote-407研究探讨了帕博利珠单抗联合紫杉醇/白蛋白结合型紫杉醇及卡铂一线治疗转移性肺鳞癌的疗效及安全性,与单纯化疗相比,帕博利珠单抗组明显延长了患者的PFS(mPFS,8.0 个月VS 5.1 个月 ;HR,0.57 [95% CI:0.47~0.69]),与本研究结果一致,另外Keynote-407研究最终报告已公布,与单纯化疗相比,帕博利珠单抗组OS延长了5.5个月(mOS,17.1 个月 VS 11.6 个月; HR,0.71 [95% CI:0.58~0.88]),不仅如此,还发现与帕博利珠单抗单药二线治疗肺鳞癌相比,帕博利珠单抗联合化疗一线治疗肺鳞癌临床获益更多[12]。虽然由于本研究随访时间短,样本量有限,尚无法对比,但是本研究及Keynote-407都表明对于晚期肺鳞癌,PD-1抑制剂联合化疗优于单纯化疗。周彩存等[8]开展的Camel研究进一步证实了免疫与化疗具有相辅相成的作用,研究结果表明,与培美曲塞联合铂类一线治疗驱动基因阴性的非鳞NSCLC相比,卡瑞利珠单抗联合化疗组mPFS延长至11.3个月,取得了可喜的临床疗效。这可能与种族有关,因为Camel研究纳入的是中国人群,也可能与免疫检查点抑制剂本身有关。卡瑞利珠单抗与PD-1分子有独特的结合表位,与其他PD-1抑制剂相比,其半数抑制浓度及半数效应浓度更低,在体内PD-1受体占有率更高[13],这些都使得卡瑞利珠单抗的抑瘤作用更强。但是关于已上市的帕博利珠单抗、纳武单抗、信迪利单抗、卡瑞利珠单抗等免疫检查点抑制剂疗效对比尚无头对头的研究。
另外我们发现本研究中观察组PD患者6例,其中4例存在肝转移,可能肝转移与免疫治疗预后差存在一定的关系。目前关于肝转移的NSCLC患者是否会从免疫联合化疗中获益存在争议。Impower150研究提示对于存在肝转移的非鳞NSCLC患者,与贝伐珠单抗联合化疗相比,阿特珠单抗联合化疗未显示出生存益处,但是在贝伐珠单抗联合化疗的基础上联合阿特珠单抗表现出了明显的生存益处[14],这提示免疫联合抗血管生成药物对于肺癌肝转移患者可能是一个新的选择。有研究表明抗血管生成药物具有免疫调节的作用,增加免疫治疗的疗效[15]。但是由于中央型肺鳞癌居多,抗血管生成药物风险较大,对于如何让中央型肺鳞癌肝转移患者获益是未来需要解决的问题。
安全性方面,观察组出现了RCHs这一常见的不良反应,一般发生在治疗的第一个周期内,发生率大约82.1%,都是G1~G2,未发现G4~G5级,一般停药后可自行消退,局部破溃等症状经云南白药粉末止血治疗后可缓解,这与周彩存等[8]开展的camel研究结果一致。RCHs是卡瑞利珠单抗独特的不良反应,研究表明其与生存获益相关[16]。关于RCHs发生机制,Finlay等[17]研究表明RCHs是高度特异性的脱靶结合事件,卡瑞利珠单抗可介导与VEGFR2、卷曲类受体5和UL16结合蛋白2的高选择性、低亲和力的异常结合,从而通过血管内皮细胞活化来推动血管瘤的发展。李等[18]的研究证实了Finlay的观点,发现阿帕替尼联合卡瑞利珠单抗可降低RCHs的发生率并诱导其快速消退。
本研究有以下几点局限性:1)本研究中IIIB/C期的肺鳞癌患者,未行同步或序贯放化疗,考虑到患者年龄偏大,肺功能基础差,同步放化疗联合免疫治疗可能会增加毒性反应,并且根据照射野范围大小不同,放疗后极大概率会出现不同程度的放射性肺炎,目前放疗引起的放射性肺炎没有很好的治疗预防手段,因此结合患者病情及患者和家属意愿未行同步或序贯放化疗及PD-L1抑制剂治疗,而是采用卡瑞利珠单抗联合一线化疗替代同步放化疗的手段,尽可能达到甚至超过同步放化疗为IIIB/C期患者带来的临床获益,改善患者的生存质量,相关研究目前也在探索中;2)由于本研究样本量较少,随访时间较短,未能对免疫治疗影响因素、RCHs与疗效的关系及总生存期进行分析,尚需要扩大样本量,延长随访时间进一步验证临床疗效。
综上所述,卡瑞利珠单抗联合化疗一线治疗驱动基因阴性的晚期肺鳞癌可显著延长患者的PFS,且安全性良好。
