快速测试片与国标方法测试脱盐乳清粉中金黄色葡萄球菌的对比
2021-12-16杜雅正刘洪梅安雪征
杜雅正,刘洪梅,安雪征, ,祁 娜
(1.中国食品添加剂和配料协会, 北京 100020;2.通标标准技术服务有限公司, 北京 100176)
乳清粉是干酪生产过程中的副产物,主要成分是乳糖和乳清蛋白[1-6]。脱盐乳清粉顾名思义是将乳清粉进行脱盐处理,是婴儿配方乳粉的主要原料。在我国脱盐乳清粉慢慢由进口开始转变为引进技术自主生产,通过控制脱盐乳清粉的质量,保证下游婴儿配方乳粉的安全,脱盐乳清粉营养素含量变化上基本保持稳定,蛋白质、脂肪、乳糖营养素含量很稳定,给微生物的生长提供了充足的营养物质[7-10]。目前对脱盐乳清粉每个生产环节进行风险评估和危害分析后,形成了危害分析及危害评估表,金黄色葡萄球菌污染是常见的危害之一。
自然界中葡萄球菌属至少包括有20个种。金黄色葡萄球菌属于葡萄球菌属是一种病原菌,营养要求不高,在普通培养基上生长良好,需氧或兼性厌氧,最适生长温度37 ℃,最适生长pH7.4,其会引发人或动物许多严重性感染[11-17]。典型的金黄色葡萄球菌为球形,显微镜下排列成葡萄串状。金黄色葡萄球菌无芽孢、鞭毛,大多数无荚膜,革兰氏染色阳性,是一种不利于人体的细菌。金黄色葡萄球菌在自然界中无处不在,因此,生产加工过程中受其污染的机会很多,因金黄色葡萄球菌引起的感染仅次于大肠杆菌排在第二位,引发的中毒事件很多[18-20]。因此,在各个生产企业的加工过程中对金黄色葡萄球菌进行了严格的控制管理,快速、准确的获得检测结果显得尤为重要。
对于金黄色葡萄球菌的检测,目前有国标法、测试片法、试剂盒法、生物分子学方法和免疫学方法。国标法即以GB 4789.10-2016依据的检测方法,通过Baird-Parker平板培养,其检测步骤较为繁琐,观察相对耗时,较难满足企业生产加工时食品安全的及时性检测需要以及突发性食物中毒的检测需要。免疫学方法操作简单且成本低廉,但会受到食品本身基质及非金黄色葡萄球菌的影响,在检测上有局限性。分子生物方法操作简单且灵敏度高,但在引物设计上较为复杂。测试片法是近年来使用较广的方法,通过与微生物代谢的显色反应测定食品中微生物的含量,操作较简便,价格较低廉,测试周期短,效率高[21-26]。本研究使用国标法和快速测试片法对脱盐乳清粉中金黄色葡萄球菌计数试验结果进行对比研究,旨在探求较快速准确检测脱盐乳清粉金黄色葡萄球菌的方法。
1 材料与方法
1.1 材料与仪器
乳清粉(D90)A 恒天然集团;乳清粉(D90)B爱尔兰Dairygolg公司;乳清粉(D70)C 爱沙尼亚Epiim公司,共18个批次的脱盐乳清粉进行比对研究;直径90 mm无菌培养皿、Baird-Parker琼脂平板
北京陆桥技术服务有限公司;3MTMPetrifilmTM金黄色葡萄球菌测试片[27](STX) 3M中国有限公司提供;金黄色葡萄球菌ATCC 25923菌株 上海林渊生物科技有限公司。为了保证数据结果符合国标的结果计算要求,一个稀释度的平板典型菌落数控制在20~200 CFU/g之间,如果样品的金黄色葡萄球菌菌数量小于150 CFU/g,则需添加标准菌株,制备人为污染样品。
BMJ-250恒温培养箱 28±1 ℃,上海博讯医疗生物有限公司;ME2002/E电子天平 感量为0.01 g,梅特勒-托利多国际贸易(上海)有限公司;400cc均质器、SCAN100菌落计数器 法国英特赛恩斯有限公司。
1.2 实验方法
1.2.1 菌株的准备 采用金黄色葡萄球菌标准菌株,用接种环挑取一环冻存菌株于BHI肉汤中培养24 h,混匀,做梯度稀释,为了方便读取结果,在1:10和1:100两个稀释度都有一定数量的菌落生长,选择金黄色葡萄球菌的数量控制在150~1500 CFU/g的菌悬液。
1.2.2 乳清粉样液的制备 称取25 g乳清粉至盛有225 mL生理盐水的均质袋中,用拍击式均质器拍打2 min,制成1:10的样品匀液。然后添加制备好的菌悬液1 mL到制备好的1:10乳清粉样品匀液,充分混合。
1.2.3 乳清粉样液的稀释 用1 mL微量移液器吸取1:10乳清粉样品匀液1 mL,沿管壁缓缓注入盛有9 mL稀释液的无菌试管中,振摇试管使其混合均匀,制成1:100的样品匀液。
1.2.4 接种与培养
1.2.4.1 测试片法 根据对样品污染状况的估计,按照国标方法中对于稀释度的要求,选择1:10和1:100两个稀释度的样品匀液,将测试片置于平坦表面处,揭开上层膜,使用吸管将1 mL样液垂直滴加在测试片的中央,将上层膜盖下。将压板置于上层膜中央压下,使样液均匀覆盖于圆形的培养面上。拿起压板,静置至少1 min使培养基凝固。
将测试片的透明面朝上,可堆叠至多不超过20片,置于36±1 ℃培养箱中培养,观察并记录24±2 h的结果。如果上述测试片上出现暗紫红色(典型的金黄色葡萄球菌特征),无需进行确认;如果测试片上出现黑色、蓝绿色菌落或紫红色菌落不明显,需使用确认反应片做进一步确认。将上层膜掀起,将确认反应片置入测试片的培养范围内,再将上层膜放下覆盖在确认反应片上,用手指以滑动的方式轻轻与确认反应片紧密接触并除去气泡,最后把插入确认反应片的测试片放在36±1 ℃培养箱内培养1~3 h。如出现粉红色环,判定为金黄色葡萄球菌。
1.2.4.2 国标法 根据对样品污染状况的估计,选择2~3个适宜稀释度的样品匀液(液体样品可包括原液),在进行10倍递增稀释的同时,每个稀释度分别吸取1 mL样品匀液以0.3、0.3、0.4 mL接种量分别加入三块Baird-Parker琼脂平板,然后用无菌涂布棒涂布整个平板,注意不要触及平板边缘。使用前,如Baird-Parker平板表面有水珠,可放在25~50 ℃的培养箱里干燥,直到平板表面的水珠消失[27]。
在通常情况下,涂布后,将平板静置10 min,如样液不易吸收,可将平板放在培养箱36±1 ℃培养1 h;等样品匀液吸收后翻转平板,倒置后于36±1 ℃培养 24~48 h。
1.2.4.3 样品本底试验 本实验考虑是否进行人工污染样品,对全部18个样品进行了测试,分别采用GB 4789.10-2016《食品安全国家标准食品微生物学检验金黄色葡萄球菌检验》第二法金黄色葡萄球菌平板计数法和快速测试片(3M快速测试片)检测方法进行实验和培养。
1.2.5 适应性试验 人工污染样品,选择1:10和1:100两个稀释度,吸取 1 mL金黄色葡萄球菌ATCC 25923菌悬液,加入1:10的样品匀液内,涡旋混匀以0.3、0.3、0.4 mL接种量分别加入三块Baird-Parker平板,用无菌涂布棒涂布整个平板,注意不要触及平板边缘,倒置平板于36±1 ℃培养48 h,观察标准菌株的生长状况和计数结果。
1.2.6 重复性试验 参考ISO 4833-1:2013标准中准确度的要求[28],对重复性进行考察,以短时间内同一人员使用相同场地、设备、方法测试两次,两次测试计数结果的对数值的绝对相差R≤0.25。
按照金黄色葡萄球菌测试片方法进行测试,观察两次测量结果。
1.2.7 对比试验 分别向18个样品匀液内加入1 mL金黄色葡萄球菌ATCC 25923菌株的菌悬液,涡旋混匀,制成待测样液,每个待测样液分别用GB 4789.10-2016和快速测试片的方法进行测试,获得数据结果使用t检验进行差异性分析[29-30]。
1.3 数据处理
利用Excel 2016处理数据,用SPSS Statistics 22.0进行显著性差异分析。
2 结果与分析
2.1 样品考察结果
筛选的具有代表性的18个样品分别采用两种方法测试,Baird-Parker平板和快速测试片在10-1稀释度下均无菌落生长。由此可见,全部样品需要使用标准菌株对其进行人工污染。结果见表1。
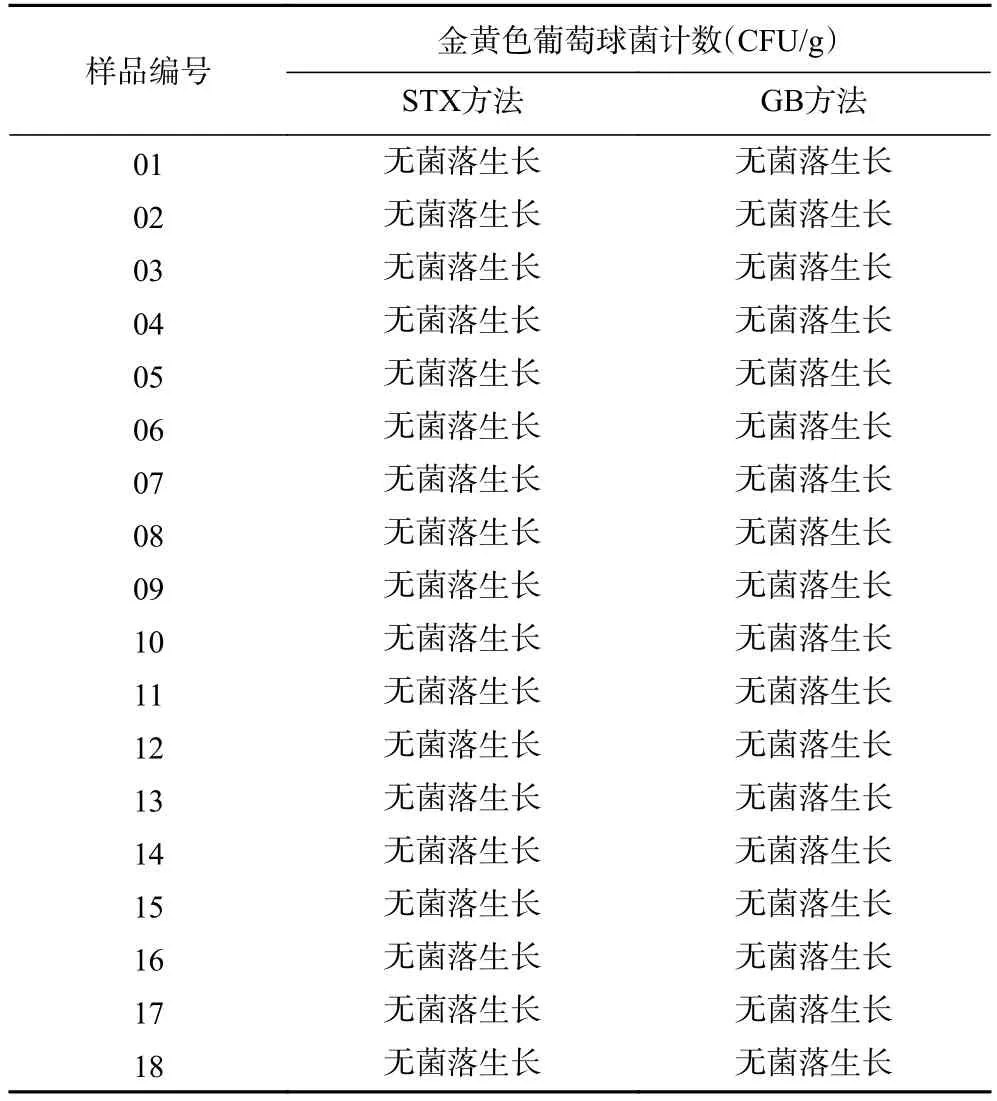
表1 脱盐乳清粉样品本底实验结果Table 1 Background test results of desalted whey powder
Baird-Parker平板和快速测试片在10-1稀释度下均无菌落生长,测试结果以<10 CFU/g报出。
2.2 适应性试验结果
通过对样品匀液进行人工污染,样品匀液中金黄色葡萄球菌的添加量范围在15~150 CFU/g,经过36±1 ℃培养48 h后,结果如表2所示。金黄色葡萄球菌分别在Baird-Parker平板和快速测试片上体现的菌落生长情况,如表3所描述,此结果可以看出金黄色葡萄球菌ATCC 25923在脱盐乳清粉样品基质下生长未被抑制,生长情况正常。
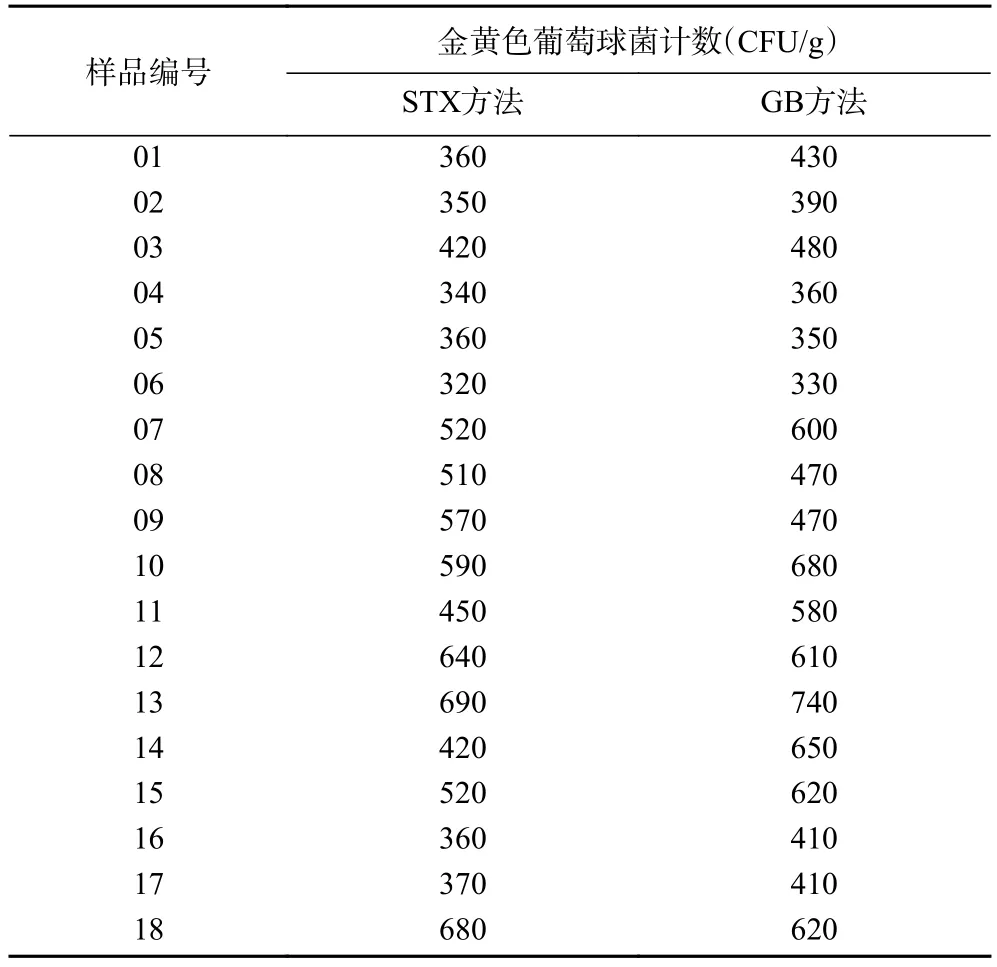
表2 人工污染测试结果Table 2 Artificial pollution test results

表3 金黄色葡萄球菌形态特征Table 3 Morphological characteristics of Staphylococcus aureus
2.3 快速测试片的重复性
在同一个实验场地,两次测试间隔1 h,使用相同的实验设备和器材,同一名实验员使用相同方法对每个样品进行重复测试,测试依据参照ISO 4833-1:2013对准确度重复性的要求,重复性限r≤0.25,结果见表4。每个样品测试结果均在可接受范围内,由此可以得出结论两次测试重复性良好。

表4 精密度测试结果Table 4 Precision test results
2.4 国标方法和快速测试片法进行对比试验结果
结果如表5所示,18份脱盐乳清粉中金黄色葡萄球菌计数的检测结果,使用Excel对数据结果进行t检验,对两组独立样本从结果看出t=0.19,金黄色葡萄球菌测试项目t≤t(0.05/2,34),说明经t检验得知该测试项目的两组结果没有显著性差异,两种方法针对该样品的检测结果具有很好的一致性。

表5 两种方法测试结果的比对Table 5 Comparison of test results of two methods
3 结论
本研究采用快速测试片法与国标方法针对脱盐乳清粉样品中金黄色葡萄球菌进行计数对比,本底实验结果显示样品中金黄色葡萄球菌计数结果均<10 CFU/g,需要人工污染样品来进行方法研究,验证标准菌株在两种方法培养基上的生长状况良好,菌落特征明显。依据ISO 4833-1:2013对重复性的要求,考虑快速测试片方法的重复性结果,将第二次和第一次测试结果值进行比较,取其lg值均在重复性限r≤0.25的范围之内,快速测试片的使用可满足标准对重复性的要求。对两种方法的对比数据进行差异性研究,使用t检验验证无显著性差异,对比结果有着良好的一致性。本实验过程中发现,按照方法培养24 h,测试片上生长的菌落直径较小,暗紫红色现象不明显,需要继续再培养12 h以上,可明显识别出来。国标方法需要进行革兰氏染色和血浆凝固酶鉴定试验,鉴定试验操作培养时间在24 h以上,观察相对耗时,测试片不需要进行单独的鉴定。综上所述,快速测试片法适用于食品配料脱盐乳清粉的金黄色葡萄球菌计数的检测,具有方法简便,产品性能稳定,检测效率高的优点。
