胰岛素自身抗体阴性外源性胰岛素抗体综合征1例报道
2021-07-29丁雄英周春欢曹政媛
刘 阳,刘 柳,丁雄英,史 昕,周春欢,曹政媛
(1.贵航贵阳医院检验科,贵州 贵阳 550004;2.贵航贵阳医院内分泌科,贵州 贵阳 550004)
注射胰岛素是临床治疗糖尿病的常用方法之一,但外源性胰岛素治疗后可能会诱发体内产生胰岛素自身抗体(insulin antibody,IA),出现高胰岛素血症,表现为血糖波动大、严重胰岛素抵抗(insulin resistance,IR)等,该组临床表现被称为外源性胰岛素抗体综合征(exogenous insulin antibody syndrome,EIAS)[1]。EIAS的主要临床特征为:(1)通过外源性胰岛素或类似物诱导;(2)常见严重的胰岛素抵抗,甚至低血糖[2];(3)IA水平随产生时间的延长逐渐下降。在实际工作中常遇见胰岛素与C肽测定结果背离的现象,需要临床根据病情、诊断和检验、检查结果综合判断。本文介绍1例采用聚乙二醇(polyethylene glycol,PEG)沉淀法[3]辅助诊断IA阴性EIAS病例,为临床提供参考。
1 病例资料
患者,女,62岁。因“发现血糖升高12年,视物模糊1周”于2019年8月6日至贵航贵阳医院住院治疗。患者12年前体检发现血糖升高,具体结果不详,未予特殊处理。10年前无明显诱因出现乏力、头昏、恶心,于贵航贵阳医院完善相关检查后明确诊断为2型糖尿病,给予二甲双胍0.5 g口服(早、晚餐时)、精蛋白生物合成人胰岛素皮下注射(早餐前16 U、晚餐前14 U)降糖至今。1周前无明显诱因出现视物模糊。
体格检查:体温36.5 ℃,脉搏78次/min,呼吸18次/min,血压19.95/11.44 kPa(150/86 mmHg)。口唇黏膜、心、肺、腹部无异常,双下肢无浮肿。专科检查:双侧下肢痛觉、温度觉、触觉、震动觉减退。辅助检查:空腹血糖、餐后2 h血糖、糖化血红蛋白、空腹胰岛素监测结果见表1;空腹C肽1.96 ng/mL(参考区间为1.1~4.4 ng/mL),IgA 2.52 g/L,IgG 12.59 g/L,IgM 0.60 g/L,类风湿因子10.3 U/mL,抗链球菌溶血素O 10.3 U/mL。糖尿病自身抗体(外院检测):抗胰岛素抗体(IgG)(免疫印迹法)阴性,抗胰岛细胞抗体(IgG)(免疫印迹法)阴性,抗谷氨酸脱羧酶抗体1.18 U/mL(参考区间为0.00~5.00 U/mL)。尿常规(干化学法):酮体±,葡萄糖±,蛋白质1+。尿微量白蛋白734.2 mg/L,尿微量白蛋白/肌酐(creatinine,Cr)比值107.42 mg/mmol Cr。大便隐血+。眼底照相示:糖尿病视网膜病变,眼底出血。血常规、粪便常规、血凝项目、肝功能、肾功能、电解质、心肌标志物、甲状腺功能、心脏彩超、腹部超声、颈部血管超声、X线片、头颅电子计算机断层扫描、心电图等均未见明显异常。
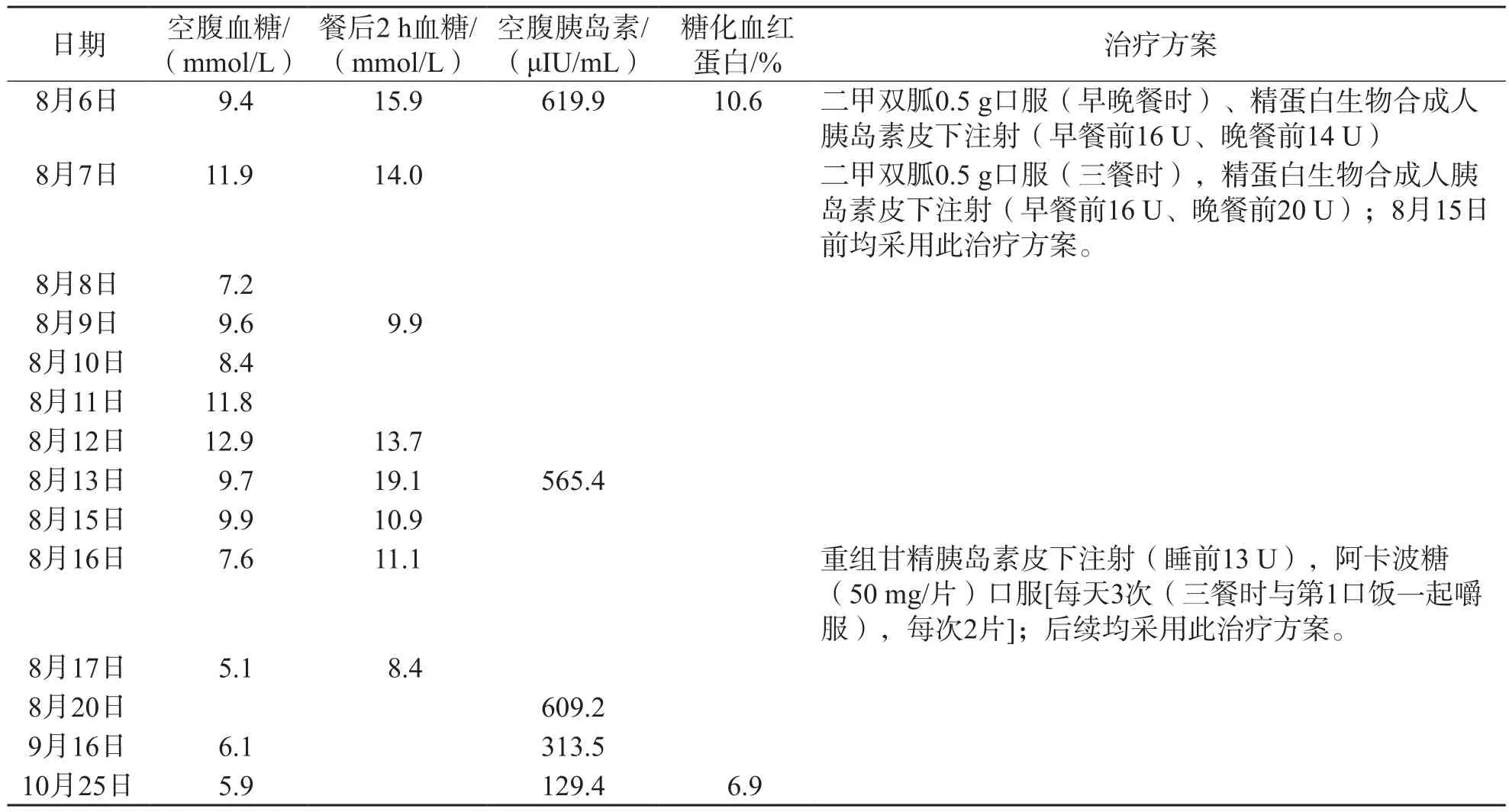
表1 患者血糖控制情况、相关检查结果及治疗方案
患者8月6日入院时的空腹血糖为9.4 mmol/L,餐后2 h血糖为15.9 mmol/L,空腹胰岛素明显升高(619.9 μIU/mL),与C肽的检测结果(1.96 ng/mL)不匹配。8月7日参考《中国2型糖尿病防治指南》(2017年版)[4]调整降糖方案后检测空腹血糖,结果为7.2~12.9 mmol/L,餐后2 h血糖为9.9~19.1 mmol/L,空腹胰岛素仍明显升高(565.4 μIU/mL)。
2 空腹胰岛素升高原因及治疗后监测结果
经过与临床科室反复沟通,发现仅增加患者胰岛素用量,血糖结果会短暂降低,随后又再次增高,而胰岛素检测结果未见明显下降,因此怀疑血清中存在某种与胰岛素亲和力高的物质影响了胰岛素的检测结果。采用PEG沉淀法处理患者血清。具体步骤:(1)配制25%PEG溶液,称取25 g PEG6000(天津致远化学试剂有限公司),加入60 mL18~25 ℃的去离子水,混匀15 min,定容至100 mL;(2)将800 μL血清样本加入800 μL 25% PEG6000溶液中,混匀10 s,然后3 030×g离心10 min;(3)取上清液,采用cobas e601电化学发光免疫分析仪(瑞士罗氏公司)及配套试剂(电化学发光法)检测胰岛素水平,同时检测未经PEG沉淀法处理的患者血清样本。按照公式:回收率=(处理后胰岛素结果×2)/处理前胰岛素结果×100%计算回收率。不同时间的患者样本采用PEG沉淀法处理后的胰岛素水平及回收率见表2。
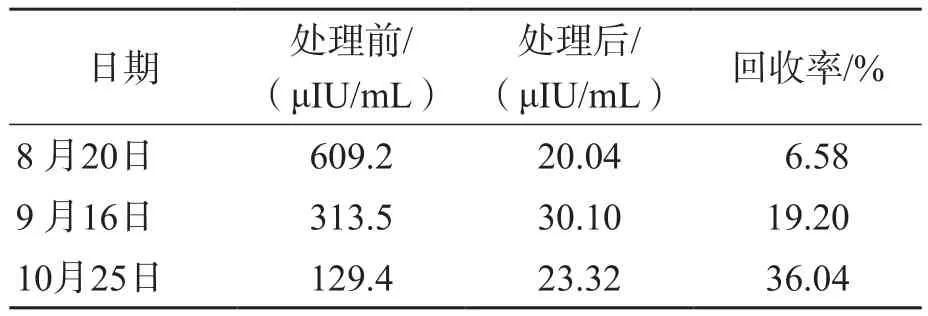
表2 采用PEG沉淀法处理前、后血清胰岛素水平及回收率
由于患者除糖尿病自身抗体3项(抗胰岛素抗体-IgG、抗胰岛细胞抗体-IgG、抗谷氨酸脱羧酶抗体)为阴性外,其他检查结果和体征均有EIAS的特征,因此临床进一步调整方案进行对症治疗:将原方案中预混人胰岛素(精蛋白生物合成人胰岛素)更换成胰岛素类似物(重组甘精胰岛素),同时搭配阿卡波糖控制餐后血糖水平。8月20日的患者血清样本采用PEG沉淀法处理后,胰岛素为40.08 μIU/mL,回收率为6.58%。经过一段时间治疗后,空腹血糖水平维持在6.0 mmol/L左右,糖化血红蛋白为6.9%,PEG沉淀法处理前的胰岛素水平明显降低,回收率由6.58%上升至36.04%。
10月28日,对患者的糖尿病自身抗体进行第2次复查,结果显示抗胰岛素抗体、抗胰岛细胞抗体均为阴性,抗谷氨酸脱羧酶抗体为1.18 U/mL,将样本送贵州省人民医院检测抗胰岛细胞抗体、抗谷氨酸脱羧酶抗体,结果均为阴性。另外,患者末梢血血糖的多次检测结果显示:空腹、餐后、睡前及凌晨均未出现低血糖结果,既往也无低血糖症状,但夜间血糖较低,空腹血糖较高。辅助检查、体格检查结果均否认胰岛素瘤及黑棘皮病可能,否认服用含巯基药物、中药及成分不明药物。
3 讨论
胰岛素自身免疫综合征(insulin autoimmune syndrome,IAS)与EIAS一般有以下区别:(1)IAS一般由内源性的胰岛素物质诱导产生,而EIAS一般由外源性胰岛素诱导产生;(2)IAS产生的抗体具有高胰岛素结合容量、低亲和力的特点,IAS患者更易发生低血糖[5],而EIAS产生的抗体通常是低胰岛素结合容量、高亲和力[6],常导致严重的IR;(3)IAS与EIAS产生的抗体特征不同[7],通常外源胰岛素所致抗体的滴度相对较低,可自愈[8]。结合上述特征,本例患者倾向诊断为EIAS。
在胰岛素水平相同时,IAS患者体内的胰岛素可结合更多抗体,但不紧密,在外部因素刺激的情况下易分离;而EIAS患者结合抗体数量少,且紧密,易出现高胰岛素结果,采用PEG沉淀法可以去除抗体和抗体包裹的大分子物质,仅剩游离胰岛素。见图1。

图1 IAS与EIAS产生的抗体在外部因素刺激时的变化
本研究采用PEG沉淀法的主要作用是去除胰岛素-免疫球蛋白复合物[9]。糖尿病自身抗体多为IgG类,但有少数IgE、IgM类抗体的报道[10]。由于这些抗体相对分子质量均大于IgG类抗体,所以采用PEG沉淀法可去除胰岛素-免疫球蛋白复合物的干扰。因为这类物质可能保留了免疫学活性,但丧失了降低血糖的生物学性质。检测剩余未被抗体结合的游离胰岛素,其结果越低,说明患者体内胰岛素与抗体结合越接近饱和。此时若加大胰岛素注射剂量,则可能出现低血糖风险。
由于本例患者急需进行眼部手术,因此只能将原本完全停用胰岛素、更换为口服降糖药的治疗方案改为使用长效胰岛素+口服药物控制餐后血糖的方案。可能由于不同胰岛素制剂的来源及结合位点不同,患者血糖控制尚可,胰岛素回收率上升,表明IR正在缓解。
总之,糖尿病的发展过程是各组织、器官由量变到质变的过程,因此某些定性检验方法会因待测物尚未达到检测“阈值”而出现假阴性结果。在EIAS的诊疗过程中无需等患者出现胰岛素抗体阳性甚至低血糖症状[8]后再进行干预,血清胰岛素与C肽出现背离现象、IR、PEG处理后胰岛素回收率降低等有助于早期诊断EIAS。