没食子酸在大鼠体内的药物动力学特征及生物利用度研究
2021-07-05朱钰璞张维敏王四旺
朱钰璞,张维敏,武 坤,王四旺,余 喆,李 骅*
(1.空军军医大学基础医学院学员大队,西安 710032;2.解放军第518医院药剂科,西安 710043;3.空军军医大学药学系中药与天然药物学教研室,西安 710032;4.空军军医大学药学系药物化学与药物分析学教研室,西安 710032)
没食子酸(3,4,5-三羟基苯甲酸,gallic acid,GA)又名五倍子酸,是一种天然多酚类化合物,广泛存在于丹皮、赤芍、广枣、费菜等活血化瘀中药材中,亦富含于柠檬、石榴、葡萄以及绿茶、红茶等预防心血管疾病的药食中[1-3],是众多中成药中的主要有效成分[4-6]。研究显示,没食子酸不仅具有显著的抗炎、抗菌、抗氧化、抗肿瘤、抗动脉粥样硬化以及神经保护和心脏保护活性[7-11],且具有良好的安全性。急性毒性实验表明,当没食子酸给药剂量达到小鼠体内给药的最高限度时仍未观察到小鼠有死亡或急性中毒的现象[12]。没食子酸单体单剂量给药后的药物动力学行为已有相关文献报道,如Shahrzad S等[13-14]通过高效液相色谱法(HPLC)考察了人单剂量口服没食子酸单体后的药物代谢动力学特性,王晓莉等[15]对大鼠单剂量灌胃没食子酸后的体内药物动力学特征进行了初步探究。本实验拟通过建立测定大鼠血浆中没食子酸的HPLC法,研究大鼠单次灌胃不同剂量及静脉注射没食子酸后的药物动力学特征和绝对生物利用度,为没食子酸及其相关制剂的开发及临床应用提供数据支持。
1 仪器与材料
1.1仪器 LC-2010A HT型高效液相色谱系统(日本Shimadzu公司);ME235S型微量分析天平(德国Sartorius公司);TDZ5-WS型台式低速离心机(上海卢湘仪离心机仪器有限公司);Certrifuge 5417R台式高速冷冻离心机(德国Eppendorf公司)。
1.2试药 没食子酸原料药(质量分数≥99.0%,西安金绿生物工程技术有限公司,批号160903);没食子酸对照品(质量分数≥99.0%,中国食品药品检定研究院,批号11831-200803);4-乙酰氨基酚(质量分数≥98.0%,国药集团化学试剂有限公司,批号20141128);甲醇为色谱纯(美国Honeywell公司);水为去离子水;聚乙烯吡咯烷酮K30(PVP K30,巴斯夫新材料有限公司);微晶纤维素(山东聊城阿华制药股份有限公司);交联羧甲基纤维素钠(明台化工股份有限公司);磷钨酸钠(上海阿拉丁生化科技股份有限公司);十二烷基硫酸钠(安徽山河药用辅料股份有限公司);0.45 μm聚偏四氟乙烯膜(杭州科百特过滤器材有限公司)。
1.3实验动物 雄性SD大鼠,体质量为320~350 g,购自空军军医大学实验动物中心,合格证号:SCXK(军)字第2012-0007号。
2 方法与结果
2.1色谱条件 色谱柱:Woburn Bio-technologies Stamsil ODS-BP色谱柱(250 mm×4.6 mm,5 μm);柱温:30 ℃;流动相:甲醇-冰醋酸-水(5∶1.9∶93.1);流速:1.0 mL·min-1;检测波长:272 nm;进样量:20 μL。
2.2对照品溶液和药液的配制 精密称取没食子酸对照品10 mg,置于10 mL棕色量瓶中,加体积分数为50%的甲醇(含体积分数为1%的冰醋酸)使溶解,定容至刻度,制成质量浓度为1.00 mg·mL-1的对照品母液;将对照品母液按比例稀释,制成没食子酸系列对照品溶液(质量浓度为0.05~20.00 μg·mL-1),4 ℃冷藏待用。精密称取4-乙酰氨基酚对照品10 mg,置于10 mL棕色量瓶中,加体积分数为50%的甲醇(含体积分数为1%的冰醋酸)使溶解,定容至刻度,制成质量浓度为1.00 mg·mL-1的内标母液;将内标母液稀释,制成4-乙酰氨基酚质量浓度为40 μg·mL-1的内标供试溶液,4 ℃冷藏待测。精密称取没食子酸原料药适量,分别用蒸馏水制成没食子酸质量浓度为10、5 mg·mL-1的药液。
2.3血浆样品的处理 精密吸取血浆200 μL,置于离心管中,加体积分数为50%的甲醇(含体积分数为1%的冰醋酸)100 μL,2.2项下制备的内标供试溶液(40 μg·mL-1)50 μL,1 mol·L-1盐酸100 μL,乙酸乙酯1.5 mL,用涡旋振荡器充分振摇5 min,以4 000 r·min-1离心15 min,吸取上清液,重复以上步骤,合并上清液,氮气吹干。用200 μL流动相复溶,再以12 000 r·min-1离心,取上清液20 μL进样。
2.4分析方法的确证
2.4.1专属性考察 取大鼠空白血浆[4,16],按照2.3项下方法处理后进样分析,获得空白血浆色谱图、空白血浆添加没食子酸、4-乙酰氨基酚(内标)色谱图以及大鼠给药后含药血浆的色谱图,见图1。由图1可知,没食子酸和内标峰保留时间分别为7.0、13.3 min,二者分离度良好且无内源性杂质峰干扰,表明本实验色谱条件适宜,提取处理方法合适,专属性较强。
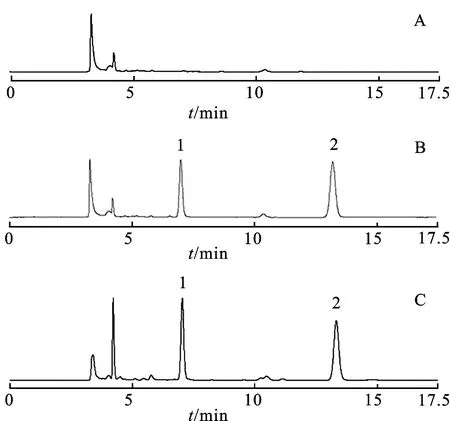
图1 没食子酸专属性实验典型色谱图
2.4.2标准曲线的建立及定量下限 取200 μL空白血浆,加入2.2项下制备的没食子酸对照品溶液(质量浓度为0.05~20.00 μg·mL-1)100 μL,除不加100 μL 体积分数为50%的甲醇(含体积分数为1%的冰醋酸)外,其余按照2.3项下方法处理,得相应系列质量浓度(0.025~10.000 μg·mL-1)的血浆对照品溶液,分别进样进行色谱分析。以没食子酸质量浓度(x)为横坐标、没食子酸与4-乙酰氨基酚峰面积之比(y)为纵坐标,进行回归分析,得标准曲线方程y=0.421 1x+0.022 5(r=0.999 9),结果表明,没食子酸质量浓度在0.025~10.000 μg·mL-1范围内线性关系良好,定量下限为0.025 μg·mL-1。
2.4.3精密度和回收率实验 取200 μL空白血浆[4,16],分为日内与日间2组,分别加入没食子酸对照品适量,配制成质量浓度分别为0.078、0.625、2.500、8.000 μg·mL-1的含药血浆样品溶液,加入内标4-乙酰氨基酚溶液,按照2.3项下血浆样品处理方法提取处理,日内组每日测定5次,日间组每日测定1次并连续测定5 d,记录没食子酸与4-乙酰氨基酚峰面积,代入回归方程计算其质量浓度。同法测定相对回收率。测定结果见表1。由表1可知,所有样品的日内精密度RSD值小于2.58%,日间精密度RSD值小于3.40%,平均相对回收率大于97.43%,符合生物样品的质量控制要求。
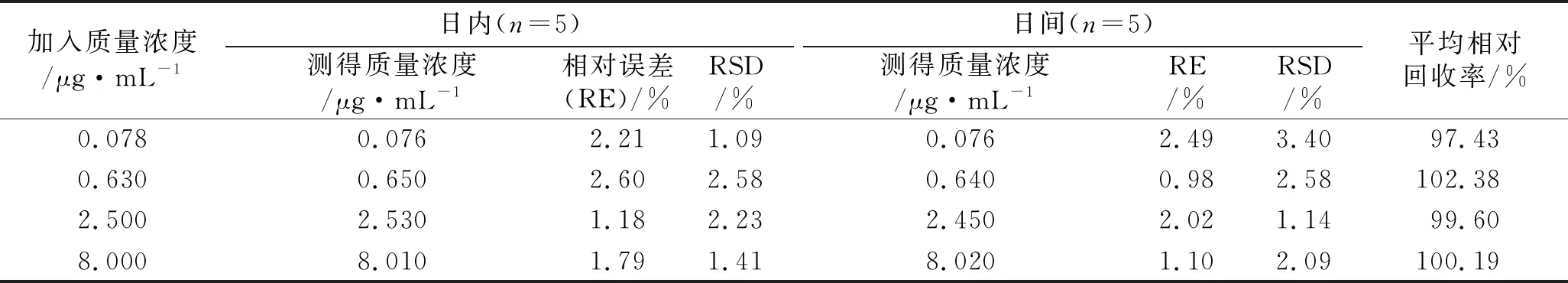
表1 没食子酸在大鼠血浆内的精密度、准确度和相对回收率测定结果
取200 μL大鼠空白血浆,加入没食子酸对照品适量,配制成质量浓度分别为0.078、0.625、2.500、8.000 μg·mL-1的含药血浆样品溶液,加入内标4-乙酰氨基酚溶液,按照2.3项下血浆样品处理方法提取处理,进样后记录没食子酸峰与4-乙酰氨基酚峰面积比A1。另取2.2项下制备的相应质量浓度的对照品溶液直接进样,记录没食子酸峰与4-乙酰氨基酚峰面积比A2。按公式计算绝对回收率(Rabs),Rabs=A1÷A2×100%。结果表明,各组平均回收率分别为87.31%、88.79%、90.02%、91.56%,且在待测质量浓度范围内RSD值均小于5%,符合生物样品的质量控制要求。
2.4.4稳定性实验 为了覆盖预期样本所处的不同实验环境和条件,按照2.4.3项下方法配制没食子酸质控样品,按照2.3项下方法处理并测定没食子酸质量浓度[4,16-17]。结果表明,短期(室温下2 h)、长期(-80 ℃储存1个月)、反复冻融(冻-融循环3次)稳定性实验中没食子酸质量浓度RSD值均小于15%,符合生物样品的质量控制要求。
2.5药物动力学实验 将32只雄性SD大鼠随机分为4组,每组8只,实验前禁食12 h,不禁水。其中3组大鼠灌胃(10 mL·kg-1)给予没食子酸,剂量分别为50、100、200 mg·kg-1;另一组为静脉给药组,经尾静脉注射(2 mL·kg-1)给予没食子酸10 mg·kg-1。灌胃给药后于0、10、30、60、90、120、180、300、420、540、600 min,静脉给药后于0、2、5、10、20、30、45、60、90、120、180、240、300 min,分别从大鼠眼眶后静脉丛采血400~500 μL,置于肝素化处理过的抗凝管中,以4 000 r·min-1离心15 min,分离血浆,按照2.3项下方法处理并测定没食子酸质量浓度。绘制得到大鼠血药质量浓度-时间曲线,见图2。

图2 不同剂量没食子酸在大鼠体内的平均血药质量浓度-时间曲线
运用DAS2.1软件对血药质量浓度-时间参数进行非房室模型的统计矩法拟合,获得没食子酸单次不同剂量给药后的主要药物动力学参数,见表2。依据公式:绝对生物利用度(Fabs)=(AUC非静脉×D静脉)÷(AUC静脉×D非静脉),计算不同剂量给药后没食子酸在大鼠体内的Fabs,其中,AUC非静脉为非静脉给药途径药时曲线下面积,D静脉为静脉给药途径给药剂量,AUC静脉为静脉给药途径药时曲线下面积,D非静脉为非静脉给药途径给药剂量,结果见表2。
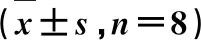
表2 不同剂量没食子酸在大鼠体内的药物动力学参数
3 讨论
3.1样品处理方法的优化 前期预实验时对比了有机溶剂(乙腈、甲醇)沉淀法、强酸(1 mol·L-1盐酸、体积分数为10%的三氯乙酸)沉淀法等直接沉淀样品蛋白的方法,样品经处理后进样分析所得色谱图杂质峰较多,且强度较强,对目标峰造成一定干扰。后改用1 mol·L-1盐酸预处理样品溶液,再用乙酸乙酯分别萃取2次,合并萃取液经氮气吹干的方法[4]。采用该预处理方法进样分析所得色谱图,干扰峰较少,响应信号全面,能够满足实验需求。
3.2色谱条件的优化 本实验采用与没食子酸分子结构及保留时间相对接近的4-乙酰氨基酚为内标,采用甲醇-水洗脱系统对没食子酸和4-乙酰氨基酚进行洗脱分离,当甲醇-水的比例为5∶95时,没食子酸和4-乙酰氨基酚色谱峰均与内源性响应信号峰分离良好[4]。由于结构中强极性基团与反相色谱柱填料硅胶中的羟基之间的相互作用,没食子酸和4-乙酰氨基酚在测定过程中均存在不同程度的拖尾现象,本实验在洗脱系统中加入适量竞争性的有机酸(体积分数为1.9%的冰醋酸),可使硅胶羟基吸附达到饱和,从而有效改善峰形,增加峰对称性。预实验考察了依利特、Woburn、Kromasil等反相色谱柱的分离效果,结果显示,Woburn Stamsil ODS-BP C18(250 mm×4.6 mm,5 μm)色谱柱的分离效果较好,故选用其为正式实验分析测试柱。没食子酸及4-乙酰氨基酚供试品经二极管阵列检测器扫描后均显示在272 nm波长处有强吸收,故确定色谱检测波长为272 nm。
3.3没食子酸的药物动力学研究 没食子酸不同剂量灌胃给药后,10 min即可在血浆样品中被检出,但血药质量浓度约在90 min才达到最大值。Konishi Y等[18]研究表明,没食子酸跨肠上皮细胞膜转运方式为细胞旁路通道转运,非极化且与pH值无关,推测没食子酸的吸收速率受胞膜孔道数量及紧密连接蛋白表达程度的影响[19]。大鼠灌胃50、100、200 mg·kg-1没食子酸后,Cmax随剂量升高而成比例递增,分别为(0.83±0.15)、(1.71±0.29)、(3.13±0.56) μg·mL-1,AUC0~t随剂量增加而成比例递增,分别为(137.07±24.75)、(262.55±22.05)、(501.64±31.64) mg·min·L-1,而MRT0~t、CL及t1/2相对恒定,表明在给药剂量范围内,没食子酸在大鼠体内呈现典型的线性药物动力学特征。此外,不同剂量没食子酸灌胃后Vd分别为(78.52±8.51)、(89.60±10.53)、(83.56±10.64) L·kg-1,说明其在组织中可以广泛分布。静脉注射没食子酸后,血药质量浓度在分布相下降迅速,至90 min后以较缓慢的速度从体内消除,其CL约为0.061 L·min-1·kg-1。根据2.5项下公式计算得出没食子酸的Fabs较低,平均值约为14.71。文献报道[20],大鼠口服没食子酸后腹主动脉没食子酸质量浓度与门静脉中的质量浓度几乎相同,药物受肠道菌群及肝药酶的影响较小。因此,与没食子酸的首过效应相比,肠道上皮细胞膜的透过性更可能是影响没食子酸生物利用度的因素,这也提示我们在未来开发基于没食子酸的新药时应设计更加适合其吸收的新型递药系统。
