可再生能源电解制氢技术及催化剂的研究进展
2021-06-26郭博文罗聃周红军
郭博文,罗聃,周红军
(中国石油大学(北京)新能源与材料学院,北京102249)
能源是人类生存、生活与发展的重要基础,面对全球性的能源危机和环境污染等问题,开发可持续利用的清洁新能源已成为世界各国的一致选择。在新一轮能源变革中,氢能以其来源丰富、清洁无污染、可再生、可存储、运输方便、用途广泛等优势,成为世界各国开发新能源技术的首选,甚至被称为21世纪的“终极能源”[1]。我国一直以来致力于推动传统能源向低碳清洁能源转型,以氢能为核心的绿色产业布局已逐渐清晰。2019年《政府工作报告》明确指出“推动充电、加氢等设施建设”,国家部委、各省市政府相继出台氢能政策及发展纲要,大力支持氢能产业发展;与此同时,各大传统能源和电力央企也纷纷布局氢能产业,推动全产业链发展,中国氢能产业迎来前所未有的发展机遇。
氢能全产业链覆盖较长,包括上游制氢、中游储运、下游用氢,涉及化工、电力、交通运输等多个领域。其中,上游制氢是整个产业的关键环节,中国制氢工业仍面临着局部产能严重不足、原料依赖化石能源技术、温室气体排放较高等问题。目前,世界范围内超94%的氢气来源于化石燃料(煤炭、石油、天然气等)重整,虽然该路线技术成熟、成本低廉、可大规模制备氢气,但从环境和资源角度考虑并不是最佳选择。电解水是一种绿色环保、生产灵活的制氢技术,其产品纯度高,技术相对成熟,并且可利用光伏发电、风电等可再生能源实现氢气的大规模制备[2-4]。根据中国氢能源及燃料电池产业创新战略联盟预测[5],2050年之后70%的氢气将来源于可再生能源,未来可再生能源电解水制氢技术或将成为主流。然而电解水制氢目前也面临着瓶颈,其中综合制氢成本较高是制约该技术发展的主要问题。目前来看,电解水制氢的成本包含电费、运营费和资产折旧费等,其中电费成本占比高达70%~80%;从总成本来看,电解水制氢是天然气重整、煤制氢等技术路线的3~4倍,阻碍了该技术的大规模推广[5]。
通过可再生能源转化技术降低电费成本、开发高性能电催化剂降低电解水能耗是降低电解水制氢成本的主要途径。过去十年里,中国的可再生能源产业链建设以及清洁能源发电装机规模已处于国际领先地位。根据国家能源局公布的数据显示,截至2020年底,我国可再生能源发电装机总规模达到9.3亿千瓦时,占总装机的42.4%,已连续多年稳居全球首位;发电量达2.2万亿千瓦时,占全社会用电量的29.5%,但基于能源绿色低碳转型的背景考虑,所占比例仍较低[6]。原因来自多方面:①我国资源分布问题导致可再生能源发展并不均衡,存在产能过剩及弃光、弃风、弃水现象;②可再生能源发电并网仍存在诸多问题,限制其大规模发展;③缺乏有效的可再生能源消纳方式。将西部地区的可再生能源发电与电解水制氢系统偶联可有效解决上述问题,电解水装置可参与电厂的调峰,消纳富余的电能,避免资源浪费;更重要的是调峰电价大幅低于沿海城镇工业电价,极大降低了电解水成本,增加了该制氢路线规模应用的可行性。由此可见,利用可再生能源发电实现电解水制氢有望成为我国低碳可持续发展、能源结构优化、保障国家能源安全的重要途径。
当前,我国电解水制氢技术从氢源供给角度考虑仍占比较低,电力来源成本以及核心部件的开发是导致其能耗较高、限制其发展的关键[7]。研究者们提出多种合理路径以解决上述问题,如利用可再生能源电力以解决制氢电力成本问题,开发高性能析氢催化剂以降低电解水制氢能耗等,积累了大量经验并取得了丰硕的成果[8-12]。现有的研究或专注于基础研究,或聚焦于工业应用,但是考虑到目前我国发展低碳能源、优化能源结构、加快发展氢能产业的需求,非常有必要将可再生能源与氢能两大领域结合讨论、共同推进。因此,本综述详细地论述了现阶段可再生能源发电与电解水制氢耦合的核心技术问题,从基础研究的催化剂领域出发,转向可再生能源电解制氢的工业应用项目,总结研究进展的同时提出合理化建议,希望为推动我国传统能源向低碳清洁能源转型、解决可再生能源消纳问题及加速氢能产业化进程提供参考依据。
1 电解水制氢技术
电解水制氢是一种成熟的工业制造氢气的技术,通过电能供给能量,使得电解槽内水分子在电极上发生电化学反应,分解成氢气和氧气。水分解反应主要包括阴极析氢(hydrogen evolution reaction,HER)和阳极析氧(oxygen evolution reaction,OER)两个半反应。目前,根据电解质的不同,电解水制氢技术可分为三类,分别是碱性电解水制氢(alkalinewater electrolysis,AWE)、质子交换膜电解水制氢(proton exchangemembranes,PEM)、固体氧化物电解水制氢(solid oxide electrolytic cells,SOEC)[13-14]。三类电解水制氢技术的相关参数对比详见表1。其中,碱性电解水技术最为成熟,具有技术安全可靠、制造成本低、操作简单、运行寿命长等优点,但其电解效率较低,一般为60%~75%;质子交换膜技术具有反应无污染、装置结构紧凑、转化效率高等优点,但其质子交换膜和铂电极催化成本较高,导致其尚未实现大规模应用;固体氧化物技术因其工作温度高达600~1000℃,使其转化效率较高,但高温限制了材料选择,该技术尚处于研究阶段。
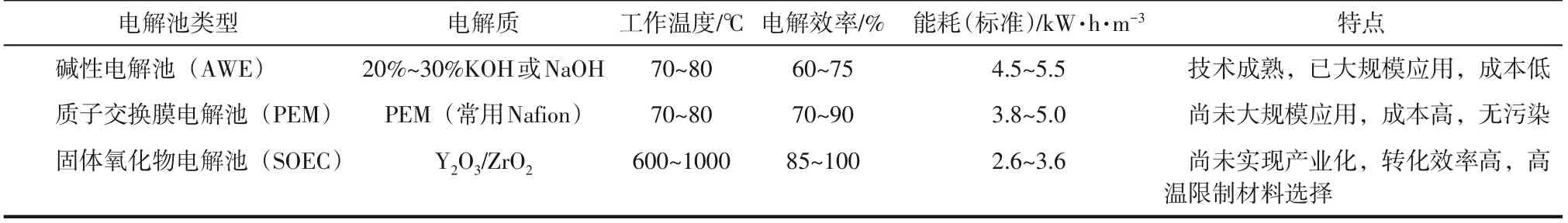
表1 三类电解水制氢技术的相关参数对比
1.1 碱性电解水制氢
碱性电解水制氢技术的主反应在电解槽中进行,槽内装填电解质溶液,通过隔膜将槽体分为阴、阳两室,各电极置于其中。如图1碱式电解水主要部件及原理所示[15],当在一定电压下电流从电极间通过时,在阴极上产生氢气,在阳极上产生氧气,从而达到水电解目的。该技术一般在低温(70~80℃)下进行,以KOH和/或NaOH水溶液为电解质(质量分数20%~30%)。电解槽中的隔膜为石棉,电极一般采用镍基材料,产生的氢气纯度约为99%,经分离后的氢气需配合脱附剂以除去其中的水分和碱雾。通常电解槽的最大工作电流密度小于400mA/cm2,能耗为4.5~5.5kW·h/m3(标准)。为避免氢气/氧气渗透多孔石棉隔膜而引起爆炸危险,必须平衡阳极和阴极侧之间的压力。此外,碱性电解槽无法快速启动,并且加载响应缓慢,通常需要降低电压、增大电流来提高转化效率。其中,降低电压的主要方法是开发高性能电极材料和隔膜材料,并进一步优化槽体结构[16]。

图1 碱式电解水主要部件及原理
碱性电解槽是该技术的核心部件,衡量其性能优劣的关键是电极材料的使用寿命和能耗。理论上,铂系贵金属是作为电极材料的理想选择,如具有优异析氢催化活性的Pt/C和具有析氧催化活性的贵金属氧化物(RuO2、IrO2、RhO2等)。但贵金属储量低、成本高、耐腐蚀性差,不具备大规模应用的条件。在实际工业生产中,为降低设备和生产成本,国内外广泛采用镍、镍网或镍合金作为碱性电解槽阴极的活化涂层,因为该类催化剂相比于贵金属催化剂成本低廉、制备简单、耐腐蚀性好,较适合大规模生产及应用。此外,具有尖晶石结构的氧化物,如NiCo2O4[17]、CoFeO4[18]等复合金属氧化物也可用于碱性电解槽阳极活化涂层。由于催化剂是碱性电解水制氢技术的核心材料,科研人员将催化剂的制备作为研究重点,积累了大量经验并取得了一定的成果,关于催化剂的研究进展将在第2节重点讨论。
此外,电解液和隔膜作为整个电解系统的主要构成部分,二者的优劣同样影响碱性电解水制氢的效率。碱性电解液可选用KOH或NaOH溶液,阴极与阳极被浸置在电解液中,通过OH-作为载流子来实现电极间的电荷传递。研究表明,质量分数为30%的KOH溶液可保证优良的电解效率,一方面是因为KOH溶液的电导率大于NaOH溶液;另一方面是电解液浓度过低或过高会影响参与电荷转移的离子数量和离子迁移阻力[19-20]。隔离膜的设置是为了允许电解液通过,同时防止产生的氢气和氧气互相扩散,并且膜材料需要较强的耐腐蚀能力。石棉[Mg3(Si2O5)(OH)4]是早期的碱式电解水隔离膜,但由于耐腐蚀性差、产品纯度低、易致癌等原因被取代。NiO网孔负载ZrO2、NiTiO3等石棉替代物和高分子聚合物与特定无机类材料交联形成的复合隔膜已相继被开发,但生产成本、电解效率、产品纯度等方面仍需优化。离子交换膜是一种允许特定离子透过的薄膜,也可用于电解水隔离膜,但存在膜开裂等问题,需要不断改进[21]。
碱性电解水制氢工艺已处于成熟阶段,广泛应用于储能、冶金、制药、食品等行业。国外拥有众多碱性电解水制氢设备生产单位,如挪威Hydro公司、德国Lurgi公司、美国德立台公司等。我国可生产出多种不同型号和不同规格的电解水制氢设备,技术指标已达到国际先进水平,代表性单位包括中船重工第七一八研究所、苏州竞力制氢设备有限公司等。目前,国内碱性电解水制氢设备单台最大产气量为1000m3/h。国内外碱性电解槽大多采用双极型结构,较适宜大量生产,且系统结构紧凑,对于电极材料的选择也并无较大区别。碱性电解水制氢整个系统结构较为简单、成本低、寿命长、稳定性好,而且工作温度较低,无需使用贵金属催化剂。然而,现阶段使用的催化剂多集中于Ni基合金以适应碱性腐蚀环境,电解效率有待提升。虽已开发出多种性能优异的新型催化剂,但从制备工艺和生产成本等多方面考虑并未能实现工业应用。当前,碱性电解水制氢的最大挑战在于高能耗,同时受制于电力成本的约束,利用廉价的可再生能源发电资源是其大规模应用的有效途径。与此同时,开发出成本低廉、性能优异的电极材料有助于进一步降低成本和能耗,也是推动该技术进步的重点工作。
1.2 质子交换膜电解水制氢
质子交换膜电解水技术与碱性电解水制氢技术原理不同,区别在于PEM技术采用高分子聚合物阳离子交换膜代替了AWE技术中的隔膜和液态电解质,起到隔离气体和离子传导的双重作用[22]。如图2所示,PEM技术的核心部件仍是电解槽,其由PEM膜电极、双极板等部件组成。其中,膜电极是水电解反应的场所,由质子交换膜和黏合在质子交换膜上的阴阳极催化剂组成,决定了电解池的性能;双极板将多片膜电极串联在一起,且彼此隔开,双极板两侧的阳极和阴极流道起到物质输运的作用,收集并输出产物H2、O2和H2O,同时在反应过程中起传导电子的作用[23-24]。
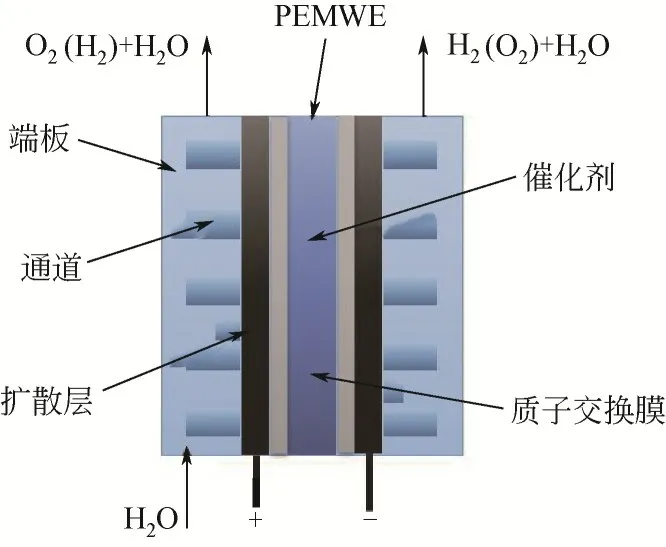
图2 PEM电解池结构
相比于碱性电解水制氢技术,PEM电解水制氢具有以下优点:①PEM采用的固体聚合物电解质膜可保证膜两侧承受较大的压差,且只对氢离子有单向传导作用,能够直接将氢气和氧气隔离开,避免串气,保证了安全性和产物纯度;②PEM电解质膜厚度可小于200μm,电极间距小,能够降低工作电压和能耗,而且使得电解槽的结构更加紧凑;③纯水作为PEM电解池的电解液,对槽体几乎无腐蚀,且电解反应产物不含碱雾[25]。
目前,对于PEM电解水制氢的主要研究方向在阴阳极端板、阴阳极扩散层、质子交换膜和阴阳极催化剂。端板可通过材料选择、优化工艺等方式提高传质效率并降低成本。Lettenmeier等[26]以不锈钢为端板分别涂覆Ni层、Ti层和Ni/Ti层作为保护层,发现Ni修饰的Ti涂层可降低接触电阻,并保持运行1000h的高稳定性,为解决Ti基端板成本高的问题提供了新的思路。Toghyani等[27]分别使用不同形状流道端板进行实验,发现双通道蛇形流道表现出最优性能。扩散层同样需对材料和结构进行优化,实现端板和催化剂间的高效传质,其中阳极扩散层必须具有较高的抗氧化和耐腐蚀能力。Grigoriev等[28]通过实验和模拟确定了最优扩散孔径和孔隙率,在1A/cm2下分别为20μm和25%~40%。
质子交换膜是PEM技术中非常关键的部件,研究集中在不同的质子交换膜对PEM电解池性能的影响、退化机理以及新型膜材料的研发。Fouda-Onana等[29]探究了温度、电流密度对全氟磺酸膜退化的影响,发现水中F元素含量可作为评价全氟磺酸膜寿命的指标。阳极催化剂需抵抗腐蚀和氧化环境,目前多使用RuO2或IrO2,其中RuO2在复杂的电解水阳极环境中稳定性较差,IrO2活性略低但稳定性有提升;阴极催化剂则采用Pt、Pt/C等,商业上比较成熟,文献报道的MoS2、WO3纳米棒、Mo2C、Pd/CNTs等催化剂效果并不能与Pt系催化剂媲美[30-31]。近年来,研究人员开发了多种高性能阴阳极催化剂,具体关于阴极析氢催化剂的研究进展将于第2节统一讨论。
美国作为最早进行PEM技术研究的国家,其PEM技术仍代表着国际最高水平。1982年,美国通用电气公司(GE)为美国海军研制了电解水制氧装置原型机;近年来研制的PEM电解水制氧装置应用于航天领域,以满足航天员的耗氧需求。在民用方面,欧美国家致力于消纳可再生能源PEM电解水制氢技术的研究,代表性企业为美国的Proton Onsite、英国的ITMpower、加拿大的Hydrogenics、德国Siemens等。近年来,国内多家单位正在开展PEM电解水技术研究,如中国航天员中心、中船重工第718所、航天科技集团811所、中科院大连化物所等。2012年,航天员中心研制的PEM电解制氧试验装置随“天宫1号”发射入轨,并在轨稳定运行。目前,国外PEM技术研发及商业应用均优于我国,无论是电解质膜的开发还是铂系电极的应用,加拿大Hydrogenics研发的PEM电解水制氢装备“HYLYZER 600”,单堆产氢量达400m3/h(标准)。
PEM电解水制氢技术作为一项新兴的储能技术,具备工作电流密度高、电解效率高、反应无污染、装备质量轻、结构紧凑等优点,在实际生产中应用越来越广泛。随着PEM电解水技术的不断突破,与可再生能源发电技术进行深度耦合,可使其成为电网调峰的理想能量存储转换装置,发展前景广阔。
1.3 固体氧化物电解水制氢技术
固体氧化物电解水(SOEC)是一种在高温状态下电解水蒸气制氢技术,基本原理如图3所示。通过电极反应将电能转化为化学能,水从阴极侧进入,反应生成H2和O2-;O2-通过电解质层进入阳极侧,失电子后产生O2。该技术工作温度在600~1000℃,主要结构包括阴极、阳极和电解质层。阴极通常使用Ni/YSZ多孔金属陶瓷,阳极为含稀土元素的钙钛矿(ABO3)氧化物、电解质层为氧离子导体(YSZ或ScSZ等)[32]。
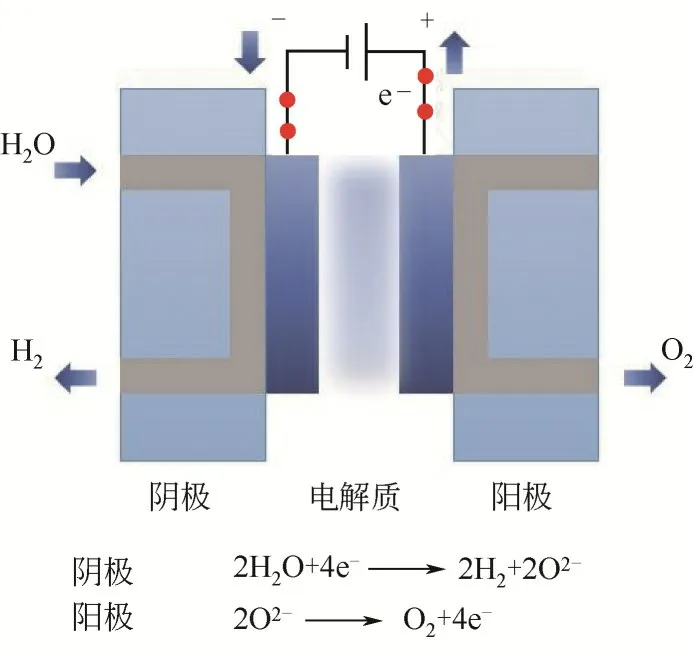
图3 固体氧化物电解池原理
固体氧化物电解技术具有高效、简单、灵活、环境友好等优势。①氢气转化率高。从电解水能量转化效率考虑,实验室电解制氢效率接近100%,因为高温操作降低了水的理论分解电压,即有效降低了反应过电势,降低了能耗。②操作灵活且规模可控。将多个电解池片耦合可成倍地提高单位时间的产氢量。③可逆操作。SOEC具有在电池和电解池模式间可逆运行的优势。然而,从整体能量使用率来看,SOEC技术的高温条件会造成热能的损失以及水资源的过量使用,同时增大了对电解池材料的要求,使得该技术目前只能在特定的高温场合下应用,短期内无法大规模投入实际应用[33]。
固体氧化物电解水制氢技术的核心部件同样是电解池,包括电解质、阴极和阳极。高温环境对关键部件构成要求较高,如电极、电解质应具有较好的反应活性和电导率;组成材料要具有优良的热稳定性、化学稳定性和耐久性。下文分别介绍电极材料和电解质的主要研究进展。
固体氧化物电解池中,对阳极材料的主要要求是高温条件性质稳定、与电解质材料兼容、较高的离子电子导电率等。钙钛矿结构的混合氧化物(如LSM,即LaMnO3掺入Sr2+形成的离子电子混合导体)在早期被广泛用作阳极材料,但存在离子电导率低的问题,通常需要添加离子导电材料(如氧化钇掺杂的氧化锆)以制成复合阳极材料来提高离子电导率[34]。近几年,一系列镧-锶-钴-铁体系的混合离子电子导体(锶掺杂的钴酸镧LSC、铁酸镧LSF、钴部分取代的铁酸镧LSCF等)表现出较高的离子电导率,且氧扩散能力较好,但稳定性有待提升[35-36]。此外,复合材料的制备同样可显著提升阳极材料性能。Chen等[37]通过浸渍法制成了NNO-SSZ复合材料,在Ni-YSZ/SSZ/NOO-SSZ固体氧化物电解池中具有优良的氧化还原催化活性。
固体氧化物电解池对阴极材料同样要求较高,比如需要具备优良的导电性、高温稳定性和催化活性。典型的催化材料为Ni-YSZ金属陶瓷,但Ni容易被氧化,其他钛酸盐/CeO2复合材料、La1-xSrxCr1-yMnyO3等也可作为新型阴极材料。Xu等[38]报道的载Fe的LSCM(La0.75Sr0.25Cr0.5Mn0.5O3-δ)复合材料可用于高温电解,这是由于Fe的负载显著提高了电极性能。Li等[39]研发了载有金属纳米粒子的钒酸掺杂复合阴极,这种La0.7Sr0.3VO3(LSV)表现出良好的性能和潜力,缺点是电催化活性较低。
电解质在SOEC中起到传递氧离子和分离两极氧化性和还原性气体的作用,对其材料的主要要求是具有较高的离子电导率和高温稳定性。目前,因为YSZ电解质的电阻率相比电极材料高几个数量级,决定整个电解池的反应速率,为降低电解能耗,需研发新材料或电解质薄膜以解决关键问题。为进一步提高电解效率并增大产氢量,通常需将单体电池连接组成电堆使用[32]。
在当今能源转型的背景下,固体氧化物电解技术具备高效、灵活、环保等优势,可以与可再生能源或核能结合,实现能量的转化和存储,已成为国际能源领域的研究热点。美国Idaho国家实验室致力于高温固体氧化物电堆技术的研发,完成了15kW的高温电解实验,进行了4kW高温电解设计和运行,处于世界领先水平[40-41];德国Juelich研究中心实现了SOEC模式的9000h和可逆电堆8100h的长期运行实验[42-43];法国原子能委员会(CEA)开发了易于工业生产的低质量电堆,提高了产氢效率和电堆的紧凑性[44];中国清华大学核能与新能源技术研究院(INET)开展的核能制氢技术课题于2010年被列为国家重大专项,2014年实现了10片电堆的高效稳定运行。法国研究机构设计出一种高温电解水蒸气系统,700℃高温条件下氢气生产率达90%,并且可回收排出气体热量。此外,该系统可最大化利用热能实现低温制氢,1m3(标准)氢气的能耗为3.9kW·h,而且设备紧凑、成本较低。相对而言,我国SOEC的研究尚处于起步阶段,对于电极催化剂的研发和电解效率的提升等仍落后于国外。目前,各国研究的重点工作是电极材料的研发和电堆性能的优化,以解决电极材料中毒、分层问题,并降低电堆内阻以保证其长时间运行。因此,为进一步推广固体氧化物电解技术,需重点从材料研发和电堆系统开发等方面展开工作。
2 电解水制氢催化剂
电解水可分阴极析氢(HER)和阳极析氧(OER)两个半反应。电解液不同,则水分解反应表达方式不同,如式(1)~式(5)。
在酸性电解液中
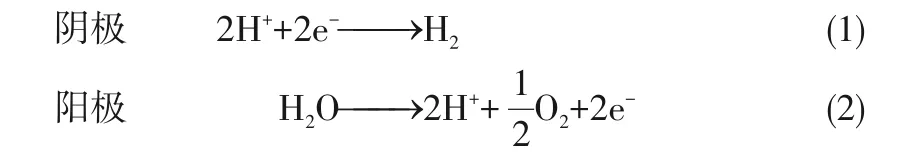
在中性或碱性电解液中
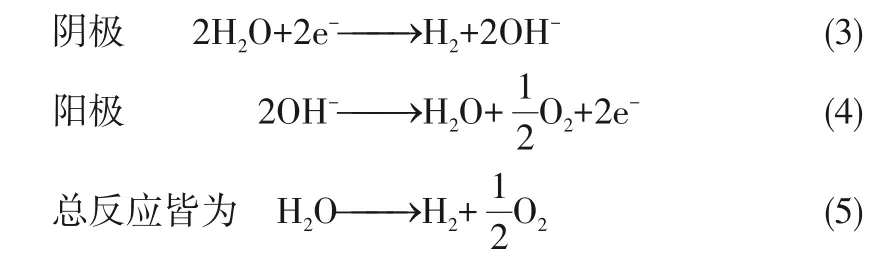
HER的发生可能基于Volmer-Heyrovsky机理或Volmer-Tafel机理[45]。但无论HER反应的途径如何,氢吸附的自由能(ΔGH*)仍旧是目前评价催化活性的重要指标,一般认为理想的HER催化剂ΔGH*应接近于零。图4给出了HER反应交换电流密度j0和ΔGH*之间的关系,其中j0表示反应速率,通常用“火山形”曲线来表示HER催化剂的反应活性[46]。
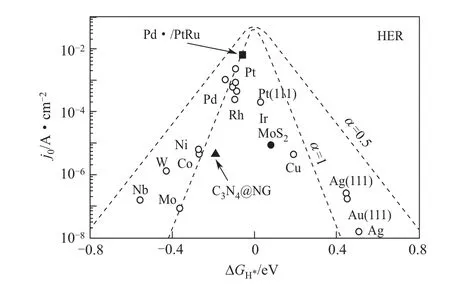
图4 HER反应中不同催化剂j0和ΔG H*之间的关系[38]
如图4所示,顶端的Pt、Pd、Ir等贵金属催化剂ΔGH*更接近零,j0值较大,即活性最优,因此被认为是目前最佳析氢催化剂。然而,贵金属因储量低、价格昂贵,限制了其大规模应用。此外,Co、Ni、Mo等过渡金属储量更为丰富,但其存在与活性氢结合较强的问题,导致后续活性氢脱附困难,影响了整体的反应速率。目前,开发高效的HER催化剂主要集中于两个方向,一是降低贵金属使用,设计出结构合理、性能高效的HER催化剂;二是开发非贵金属基催化剂,如过渡金属材料、掺杂合金复合材料等。表2为本文综述的三类析氢催化剂的相关信息对比,包括贵金属基电催化剂、过渡金属基电催化剂和单原子析氢催化剂。
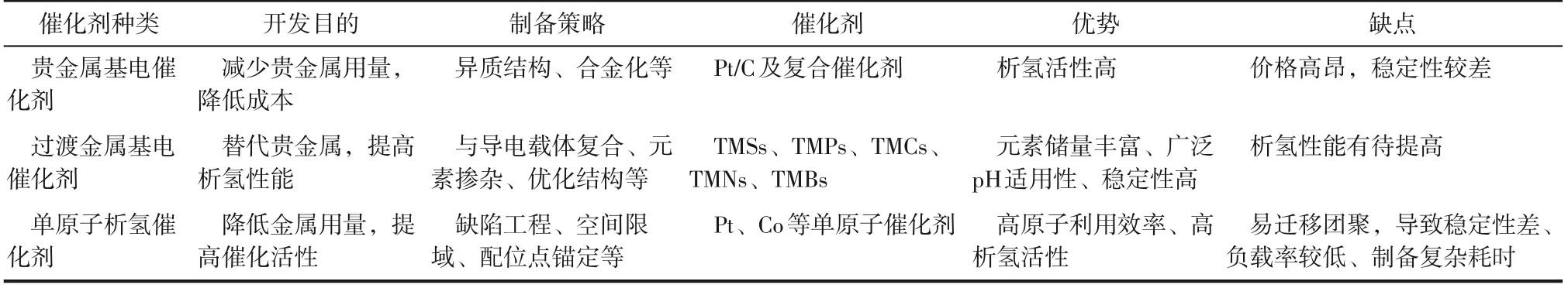
表2 三类析氢催化剂的相关信息对比
2.1 贵金属基电催化剂
2.1.1 异质结构催化剂
Markovic等[47]在Pt电极上沉积氢氧化镍纳米簇,在1mol/LKOH碱性溶液中HER催化活性显著提高,自此构建异质结构催化剂便受到广泛关注。因为异质结构催化剂一方面可降低贵金属的使用,另一方面在异质界面处形成的协同效应可进一步提升HER反应速率。Huang等[48]通过对金属Pt-Ni纳米线在空气中进行退火,制备了NiOx/Pt-Ni异质结构催化剂。Pt-Ni合金中的Ni被氧化成NiOx壳,聚集在纳米线的外表面上。通过使用Pt3Ni纳米线作为前体,获得了具有适当NiOx密度的NiOx/Pt3Ni,在0.1mol/L和1mol/LKOH溶液中HER活性均优于市售Pt/C。随后,他们通过硫化分离了Pt-Ni纳米线前体的成分,构建了Pt3Ni2/NiS界面纳米线[49]。衍生的硫化物/金属异质结构在碱性条件下电流密度37.2mA/cm2时的过电势为70mV,是市售Pt/C的9.7倍以上。Zhang等[50]制备了一种Pt修饰的Ni3N纳米片电催化剂。除了两种组分之间的协同作用外,这种杂化纳米结构中的Ni3N还可以提高电子传导速率。结果显示,Pt质量分数为15%的Ni3N/Pt复合材料在碱性条件下表现出优异的HER活性,电流密度200mA/cm2时的过电势为160mV,塔菲尔斜率为36.5mV/dec,24h工作后电流保持率为82.5%。这项工作为进一步提高异质结构催化剂的催化性能提供了有效的策略。除Pt以外,其他贵金属(如Ru和Pd)也已用于构建异质结构催化剂[51-52]。
尽管由于异质结构材料的出现促进了HER性能提升,但仍存在较大的开发空间,主要表现为贵金属Pt等含量仍较高,且难以精确控制界面以调节其催化性能。近年来,出现的单原子催化剂(single-atom catalysts,SACs)为降低Pt的负载量提供了新的思路。
2.1.2 合金催化剂
双金属合金催化剂的协同效应可有效提升催化性能,该思路同样适用于电解水制氢催化剂的制备。非贵金属(Co、Ni和Cu)和贵金属(Pd、Ru和Pt)的结合有效地降低了贵金属的使用量,重要的是,通过表面改性与界面工程构筑的合金催化剂可大幅度提升纳米催化效率。
2020年,Luo等[53]报道了IrMo合金纳米催化剂的合成及其在碱性电催化反应中的应用。IrMo0.59催化剂的HER活性相较于商业Pt/C和单质Ir性能分别提高了5倍和10倍。密度泛函理论(density functional theory,DFT)计算表明,IrMo合金上的Mo位点可以有效地优化H2O和OH的吸附自由能,从而提高催化反应动力学。同年,Zhang等[54]报道了一种二维双金属烯氢化物纳米片催化剂。在合成过程中,甲醛释放H原子,稳定了铑钯双金属烯,形成RhPdH双金属氢化物二维纳米片。所获得的催化剂展现出优异的HER催化性能,在电流密度为10mA/cm2条件下,过电势仅为40mV;此外,该催化剂还展现出优异的稳定性,在100mA/cm2的电流密度下可稳定工作10h以上。2019年,Huang课题组[55]合成了富含纳米通道的RuCu纳米片(RuCu NSs)。在不同退火处理条件下,催化剂的HER/OER活性有所差异。研究证明RuCu NSs/C-350℃展现出高OER活性,而RuCu NSs/C-250℃的HER活性最优。在全水解时,RuCu-NSs/C的起始电位较小;在不同浓度的酸/碱溶液中,电流密度达到10mA/cm2时所需要的过电位远低于纳米粒子和商用电催化剂。
2.2 过渡金属基电催化剂
迄今为止,寻找廉价、储量丰富、高活性的电催化剂来替代贵金属基催化剂仍旧是科研重点,其中过渡金属基电催化剂展现出优异的催化性能,有望成为贵金属基催化剂的潜在替代者。将过渡金属(铁、钴、镍、钼等)与非金属元素(氧、硫、磷、碳、氮等)复合是一种显著提高催化性能的方法,且取得了较大进展。表3列出几类典型过渡金属基电催化剂的相关信息,具体内容将分别讨论。

表3 几类过渡金属基电催化剂的相关信息对比
2.2.1 过渡金属硫化物
过渡金属硫化物(transition metal sulfides,TMSs)具有成本低、储量丰富和稳定性高等特点,是一种极具应用前景的析氢催化剂,其中比较有代表性的是二硫化钼(MoS2)。现阶段报道的提升HER活性的方式主要有与导电载体复合、元素掺杂、调控活性位点、调节晶相等。
将催化剂与导电基底结合是提升HER催化活性的常用方法。其中具有高导电性的多孔结构碳材料(如石墨烯、碳纳米管、碳纸等)是使用较多的导电基底,这些材料一方面可作为催化剂载体提高导电性,另一方面活性金属通过在载体表面的负载可暴露更多的活性位点,提高分散性的同时可避免颗粒团聚。2017年,Guo等[56]报道了一种由双层MoS2纳米片和负载CoS2纳米颗粒的氧化石墨烯(RGO)组成的三层复合材料(CoS2@MoS2/RGO)。MoS2和CoS2提供了丰富的催化活性位点,石墨烯作为导电基底亦发挥了协同效应,因此所制备的CoS2@MoS2/RGO具有优异的析氢反应活性:电流密度在10mA/cm2下过电势为98mV,塔菲尔斜率为
37.4mV/dec。
通过合理掺杂可调控催化剂的电子结构和活性位点,最终提升HER性能。Zhao等[57]报道了一种钴掺杂MoS2催化剂,实现了HER和OER活性的双提升。该工作的设计理论源于元素掺杂(如O、Fe、Co、Ni)可有效地改变MoS2的电子结构并调整Mo的电子密度,从而降低氢吸附自由能以提高HER性能,为设计过渡金属双功能电催化剂提供了合理的思路。
通过设计不同纳米结构的催化剂以最大限度提高活性位点数量,是提升过渡金属硫化物HER性能的常规手段。Shang等[58]针对MoS2层状结构易于堆叠而导致边缘活性位点数量减少的问题,设计了纳米柱结构催化剂。沿化学惰性(002)面垂直定向堆叠的结构相比于MoS2块体和随意堆叠的MoS2结构具有更优的HER活性,其电化学活性表面积提高了约25倍。
由于MoS2具有不同晶相结构,研究表明2H-MoS2到1T-MoS2的转变将直接影响催化剂的导电性和活性。Yang等[59]利用氩气和磷蒸气的混合气体对2H-MoS2块体进行简单的退火处理,获得稳定的1T-2H MoS2异质结构。其中磷原子不仅掺入S-Mo-S层,还嵌入到MoS2的晶格中,导致MoS2从2H相转变到1T相,该异质结构在碱性电解质中的HER性能大幅度提升。
值得注意的是,虽然当前报道的过渡金属硫化物HER性能不断提升,但相比于贵金属催化剂仍存在差距,合理设计催化剂结构、调控活性位点、构建双功能催化剂仍是未来工作的重点。
2.2.2 过渡金属磷化物
过渡金属磷化物(transitionmetal phosphides,TMPs)是一种新型半导体材料,具有较低的能带隙,因其含量丰富、稳定性高和导电性好等优势而备受关注。重要的是,在电催化反应中很多TMPs不受酸碱影响,而且磷原子可以作为路易斯碱来捕获带正电荷的质子,这使得被吸附的H(Had)的ΔGH*接近于零,具备作为析氢反应催化剂的潜力,近年来TMPs已被大量用作碱性条件下的HER催化剂[60-61]。
2005年,Liu等[62]利用密度泛函理论预测Ni2P有望成为Pt的优良替代品,结果显示P的存在会降低Ni表面活性位点浓度,使之具有适中的氢吸附自由能,同时P也是整个反应的重要参与者,自此科研人员展开了对磷化镍纳米材料的析氢性能研究。Ni2P纳米材料的研究集中于两方面,一是调控Ni2P的纳米形貌(如纳米颗粒、纳米片以及纳米线阵列等),并研究不同结构对HER性能的影响;二是讨论镍与磷元素比例对催化性能的影响。2017年,Wan等[63]证实NixPy纳米粒子的HER活性取决于退火处理后磷化镍的元素比例,不同元素比的NixPy纳米粒子在H2SO4和NaOH溶液中具有截然不同的HER活性。
与磷化镍类似,磷化钴(CoP)同样被证明是一种高活性及高稳定性的HER催化剂。Zhang等[64]报道了一种由碳纳米管(CNT)/二维CoP纳米片制备的异质结构(CoP/CNTs)。研究表明CoPNS/CNTs催化剂在CoP纳米片的多孔结构、CNT与CoPNSs间的高活性界面、高暴露的催化活性位点的共同作用下,降低了HER反应的能垒,提高了电荷转移速率。在1.0mol/L的KOH溶液中,10mA/cm2时的过电势为68mV,并可稳定运行长达24h。
过渡金属中铁储量最为丰富,成本相对较低,且具有广泛的pH适用范围,被认为是HER催化剂理想候选者之一[65-67]。2020年,Chen等[68]报道了生长在钛箔表面的FeP纳米片(FeP/Ti),其表面存在的天然氧化层阻碍了析氢反应的进行,浓硫酸去除后HER活性显著提高。
2.2.3 过渡金属碳化物
过渡金属碳化物(transition metal carbides,TMCs)凭借诸多优势,如类贵金属的电子结构、高电导率、低成本、广泛的pH适用性、高催化活性及稳定性等,受到了广泛关注。为提升过渡金属碳化物的HER性能,研究人员往往从以下几方面入手,构造特定纳米结构以暴露活性表面、与导电碳或多孔碳杂化以促进电子/离子传输、杂原子掺杂以调节电子构型优化活性位点、异质界面工程协同促进性能提升。
通常制备TMCs需要较高的温度,因为高温可使碳或与碳合金化的金属取代本体材料中的氧。程序升温还原(TPRe)法是利用富碳气体(CH4/H2、CO/H2、C2H6/H2等)与金属氧化物固体之间进行气固反应,是制备TMCs的常用方法。然而,过量的含碳气体会产生积炭,覆盖活性位点,导致催化剂失活;此外安全性也是必须考虑的问题。近年来,化学气相沉积法等为TMCs制备提供了新途径,在形貌上基于TMCs的一维材料和二维过渡金属化合物等均表现出优异的HER性能。Tang等[69]通过对MoMOF进行原位掺碳,开发了一种由石墨化炭壳包裹的MoC电催化剂(nanoMoC@GS)。MoC的超微纳米结构及超薄石墨化炭壳优异的导电性和丰富的孔隙率,使nanoMoC@GS在酸性和碱性介质中均表现出高效的HER活性。
碳基载体,如碳纳米管(CNTs)、石墨烯(GO)、还原氧化石墨烯(RGO)、多孔碳等常被用来支撑TMCs。碳基载体不仅可以改善纳米级TMCs的分散性,避免其团聚或烧结,还可以利用界面相互作用影响活性位点的电子构型,降低纳米晶体间的电阻,促进电解质的运输。Tao等[70]利用石墨烯、钼酸铵和六硝基钴酸钠合成了双金属碳化物纳米骨架Co6Mo6C,该材料由具有三维多孔表面的纳米多晶组成。Co6Mo6C具有较小的起始过电位(15mV),在电流密度为10mA/cm2时过电位为154mV。
2.2.4 过渡金属氮化物
过渡金属氮化物(transition metal nitrides,TMNs)因具有类金属单质的物理化学性质和独特的电子结构而备受关注。通过氮与过渡金属结合,可以使过渡金属d带电子密度增加,表现出类贵金属Pt的电子特性。此外,TMNs具有优异的导电性和耐腐蚀性,适用于酸性或碱性条件下的电催化水分解。
Xie等[71]报道了原子厚度的金属氮化钼(MoN)纳米片,表现出优异的析氢活性。理论计算表明,原子级厚度的MoN纳米片表现出金属特性,可以有效促进电子传输。虽然一元TMNs在电化学水分解中已具有良好的导电性和活性,但由于一元TMNs具有稳定的M—H键合强度,无法达到最优的氢吸脱附状态,最终导致活性未能与Pt基催化剂媲美。一种简单方法是引入另一种金属来减弱或增强M—H键,从而改变电子性能。Yan等[72]通过电沉积工艺结合NH3气氛中退火,在大孔泡沫镍(NF)表面原位合成了多孔镍钴氮化物纳米片NiCo2N。从金属氢氧化物到金属氮化物的转变可以有效地增强OER和HER的电催化性能;更重要的是,镍的掺入进一步提高了氮化钴的催化活性。
TMNs与碳材料的复合已被证实在酸性/碱性溶液中都具有较高的HER活性。Shao等[73]利用金属有机骨架(metalorganic framework,MOF)合成了氮化钼@氮掺杂碳多孔纳米八面体(MoN-NC)。该催化剂在10mA/cm2的电流密度下过电势低至62mV,并拥有较低的塔菲尔斜率(54mV/dec)和较大的交换电流密度(0.778mA/cm2)。TMNs和其他过渡金属化合物(如碳化物、硫化物、氧化物等)的复合材料同样被用作水分解电催化剂。Bagchi等[74]报道了一种碳载体支撑的碳化钼和氮化钼纳米复合材料,该结构中碳化钼和氮化钼纳米颗粒尺寸范围是8~12nm。该复合结构中,组分间的协同作用平衡了M—H强度,因此展现出优良的HER催化活性。
2.2.5 过渡金属硼化物
过渡金属硼化物(transition metal borides,TMBs)近几十年来一直被用于电解水,但最近才真正被视为替代贵金属催化剂的候选者。相比于其他非贵金属电催化剂(如金属磷化物和金属硫化物),TMBs的合成方法简便、制备过程能耗较低,兼具低成本、广泛pH适用性等优势。2017年,Li课题组[75]在有机溶剂中使用LiBH4还原Fe2+制备了FeB2纳米颗粒,该颗粒可作为优异的水分解双功能电催化剂。在碱性电解液中,FeB2电极在电流密度达到10mA/cm2时HER过电势为61mV,OER过电势为296mV,塔菲尔斜率分别为87.5mV/dec和52.4mV/dec。密度泛函理论计算表明,富硼表面具有适当氢结合能,实现吸附和解析氢中间体的平衡,因此有利于HER反应。
金属硼化物的成功促使研究人员开发了多元硼化物以及其他金属掺杂用于电化学水分解,研究表明掺入第二种元素后,金属硼化物的电催化性能得到了极大地提高。Gupta课题组[76]成功地合成了在宽pH范围内具有HER高催化活性的非晶态Co-Ni-B纳米催化剂。Liang等[77]将泡沫镍交替浸入镍前体和还原溶液中,实现了泡沫镍上快速化学沉积非晶态Ni-B纳米颗粒膜。这种3D催化电极(Ni-B/Ni)实现了高效水分解制氢。另外,这种交替浸渍沉积技术可实现催化剂负载量的调节,普遍适用于其他导电基底。
催化剂结构、形态以及表面积的控制对于电化学性能方面起着重要作用。因此,优化合成方法以获得独特的纳米结构,使其具有大量的活性位点和较高的表面积,是提升催化性能的主要方法之一。Lu等[78]通过NaBH4在室温下对Ti网上的CoO纳米线阵列进行处理,导致纳米线表面上原位形成CoB纳米粒子,最终制备成CoB@CoO纳米阵列。该材料在1.0mol/L KOH环境中,电流密度达50mA/cm2时的HER、OER过电势分别为102mV和290mV,并且仅需1.67V的电压即可提供50mA/cm2的水分解电流。
2.3 单原子析氢催化剂
单原子催化剂(single-atom catalysts,SACs)是指活性金属以单个原子的形式存在于载体表面形成的催化剂,单个原子与载体的结合将形成新的电子形态,因而表现出优异的催化活性和原子利用效率。单原子催化剂为从原子和分子层面阐明催化剂构效关系提供了基础,同时构建了多相催化和均相催化间的桥梁。
如上文所述,Pt由于其接近零的氢吸附自由能被认为是最好的析氢反应催化剂,然而高昂的成本和有限的储量限制了Pt催化剂的商业应用。解决上述问题存在两个思路,一个是开发高活性且地球元素丰度高的非贵金属催化剂(上文已详细介绍);另一个是提高Pt原子的利用效率以减少Pt消耗。单原子催化剂的出现可最大化提高金属利用率并降低经济成本,为HER催化剂的开发提供了新策略。单原子催化剂的主要合成策略有缺陷工程、空间限域、设计配位点锚定等。
为了便于比较,表4列出了本文综述的不同种类电催化剂析氢关键性能参数信息。

表4 不同种类电催化剂析氢性能比较
2.3.1 贵金属单原子催化剂
提高贵金属催化剂(Pt、Ru、Pd、Ir等)的原子利用率和反应活性,是构建高效HER单原子催化剂的目标之一。虽然已报道的贵金属SACs有极高的催化活性,但是较高的表面能易导致单原子的迁移与团聚,极大地影响了催化活性及稳定性。设计合理的载体是解决上述问题的有效途径。Luo等[79]将Pt单原子负载于泡沫镍表面并生长于CoP基纳米管阵列上(PtSA-NT-NF)。该催化剂在磷酸盐缓冲溶液(pH=7.2)工作环境中,无论低电流密度还是高电流密度的性能均优于市售Pt/C。Bao等[80]证实了单原子金属掺杂可激发MoS2中硫原子的催化活性。与MoS2相比,Pt单原子掺杂的MoS2纳米片(Pt-MoS2)可大幅度提升HER活性;密度泛函理论计算表明,掺入Pt单原子可调节硫原子对H的吸附行为,从而提高HER性能。该文章进一步计算了多种金属单原子掺杂MoS2材料的HER活性,并获得了基于电流密度和氢吸附自由能关系的火山曲线,为设计单原子掺杂催化剂提供了理论指导。Chen等[81]合成了一种钌原子级分散的碳基纳米线(Ru-NC),并发现RuCxNy是该材料的活性中心。在0.1mol/L KOH中,Ru-NC-700在电流密度为10mA/cm2时过电势仅有-47mV,塔菲尔斜率仅为14mV/dec,在-10mV下只有20.7Ω的电荷转移电阻,均优于商业铂电极(-125mV、39mV/dec、136Ω)。该催化剂同时展现了极佳的耐久性能,10000次循环测试以后性能未发现明显降低。Cao等[82]将单原子Ru负载于MoS2表面(SA-Ru-MoS2),引起MoS2的相变,同时产生了硫空位,进一步提升了MoS2的HER性能。密度泛函理论计算结果证实S空位、单原子Ru与相变后的MoS2调控了催化剂的电子结构,进而提升了性能。
2.3.2 非贵金属单原子催化剂
尽管过渡金属催化剂研究已取得了很大的进展,但相较于Pt等贵金属催化剂,传统过渡金属催化剂的HER性能仍有待提高。单原子催化剂得益于低配位环境和独特的电子结构,为设计高活性非贵金属催化剂提供了更多选择。Wang等[83]利用金属-有机骨架制备了单原子钨催化剂(W-SACs)。通过高角度环形暗场扫描透射电子显微镜(HAADF-STEM)和X射线吸收精细结构(XAFS)光谱分析证明了钨的原子级分散,并通过密度泛函理论计算揭示了W1N1C3可能有利于催化反应的进行。在0.1mol/LKOH溶液中,W-SAC在10mA/cm2的电流密度下具有85mV的过电位和53mV/dec的Tafel斜率,HER活性接近商业Pt/C。Liu等[84]开发了组装/浸出新策略(assembly/leaching),即将钴纳米盘首先组装于二维MoS2表面,浸出后获得扭曲1T相MoS2表面负载的钴单原子催化剂(SA Co-D 1T MoS2)。该研究发现在Co与MoS2间的晶格失配及Co—S间形成强共价键的共同作用下,单原子催化剂载体MoS2会发生由2H相向扭曲1T相的转变,上述现象阐释了金属单原子与载体之间的相互作用,对高负载量单原子催化剂的设计至关重要。
2020年,Sun等[85]报道了一种在酸性、碱性和中性介质中都表现出高催化活性的单原子催化剂,为Mo掺杂Co9S8的HER/OER双功能催化剂(Mo-Co9S8@C)。该材料首先通过水热法合成Co9S8,再通过部分氧化表面的硫原子锚定Mo原子(Mo质量分数为0.99%)。Mo-Co9S8@C催化剂界面展现独特的电子结构,有利于水分子的吸附、氧自由基的形成和产物释放。
通过上述实例证明SACs在电催化领域具有极大应用前景。提高金属原子利用率可减少金属消耗,对于降低催化剂成本和促进可持续开发至关重要。此外,暴露的活性位点、独特的电子结构以及与载体间的强相互作用使SACs具有更强的电催化活性。同时,SACs简单的结构有助于精确识别活性位点,为原子尺度研究电化学过程和机理提供了理想平台。为了满足基础研究和实际应用的需求,SACs仍面临着诸多挑战,比如:如何在不引起聚集的条件下提高SACs的金属负载量;如何实现SACs的大规模制备;如何精确控制金属原子的结构和配位环境以改善催化性能;如何在原子尺度下建立SACs的构效关系并阐明催化机理等,上述问题仍需要科研人员深入研究和探讨。
3 可再生能源发电驱动电解水技术
生产低碳的氢能源已成为贯彻落实党的十九大精神、构建“清洁低碳、安全高效”能源体系、推动能源供给侧结构性改革的重要举措。目前,生产低碳的氢能源主要有两种技术路线:一是采用天然气重整或煤气化结合碳捕集与封存技术(carbon capture and storage,CCS)制氢;二是通过低碳的电力驱动电解水制氢。
3.1 可再生能源发电驱动电解水制氢
3.1.1 生产低碳的氢能源技术路线对比
天然气重整制氢技术较为成熟,其制氢成本受制于天然气价格。2018年中国超越日本成为全球第一大天然气进口国,天然气对外依存度高达45%,面对国际局势日益紧张、贸易摩擦升级、全球新冠疫情蔓延以及我国“富煤、缺油、少气”的资源特点,发展天然气制氢技术有待进一步评价。
我国煤化工产业高速发展,使得煤制氢技术相对成熟且可大规模制备氢气,但生产过程中不可避免地造成二氧化碳排放,需结合碳捕集与封存技术(CCS)。然而,当前我国CCS技术尚处于探索和示范阶段,需进一步推动技术进步以降低能耗和成本,未来或可作为提供低成本、大规模的氢源路线之一。
通过低碳的电力驱动电解水制氢主要是指利用可再生能源发电来驱动电催化水分解产生氢气,其中电力来源包括光伏、风电、水电、核电等。我国可再生能源丰富,开发力度居世界前列,据国际能源署(IEA)最新报告显示,2020年我国可再生能源装机容量在全球占比首次达50%,尽管政府决定于2020年底逐步取消对风能和太阳能项目的补贴,但预计可再生能源新增产能(2021年增加45%,2022年增加58%)仍将远高于2017—2019年平均水平,这与我国2060年实现“碳中和”的长期目标不无关系[86]。
综合考虑,可再生能源与氢能的耦合是实现能源高质量、高效率、可持续发展的必然选择,是未来突破可再生能源电力制氢技术瓶颈的重要途径。
3.1.2 可再生能源电力制氢问题
可再生能源电力制氢作为推动氢能产业绿色、经济、高效发展的重要方式之一,仍面临着严峻的挑战和诸多问题。①可再生能源发电运行问题。光伏、风电等可再生能源受季节、气候的影响存在随机、间歇、不均衡等问题,发电并网波动性较大,影响安全运行;而且资源分布和开发力度的不同导致现阶段可再生能源存在大量弃光、弃风现象[87]。②可再生能源发电制氢成本问题。受技术进步、规模化经济、供应链竞争日益激烈的推动,过去十年间,可再生能源发电成本急剧下降,但与化石燃料发电相比仍需要综合考虑,价格竞争力是解决可再生能源消纳问题的关键,并且最终影响制氢成本。③可再生能源发电并网问题。鉴于我国可再生能源资源丰富地区主要集中于西部,而电力使用量较大段则位于东部和南部,如何解决并网、输送、消纳三方的协调问题是目前面临的最大挑战。④可再生能源电力制氢利用问题。我国风力、光伏资源丰富,大量弃风、弃光的地区却不是氢能利用的急需地区,必然存在氢气的运输问题,如何实现安全可靠、低成本地运输氢气和合理利用氢气成为氢能产业亟待解决的问题之一[8]。
3.1.3 可再生能源电力制氢优势
发展可再生能源制氢技术是解决可再生能源发电和氢能综合利用的有效途径,具有如下优势。①解决可再生能源发电运行问题。大量弃风、弃水、弃光导致的弃电是发展电解水制氢的有利条件,在可再生资源丰富的地区建造电解槽制氢装置可有效解决可再生能源发电运行问题,是最为环保的能源利用方式。②实现合理消纳可再生能源。生产低成本氢必须获得充足的低成本电力,以确保电解槽能够长时间运行,随着太阳能发电和风力发电的成本降低,未来光伏和风电等可再生能源平价上网为电网电力制氢提供更多选择。③实现能源高效环保利用。基于成本和环保的角度考虑,利用可再生能源发电驱动电解水制氢,一方面可实现氢能低成本、大规模制备;另一方面可有效解决全球性碳排放问题,实现清洁能源的高效利用。
总之,可再生能源电解制氢技术是推进我国能源绿色低碳转型的重要途径,主要技术路线包括光伏发电制氢、风力发电制氢、生物质发电制氢等。表5为可再生能源电解制氢技术路线对比,简要概述了现阶段各种技术的主要优势和存在问题,并给出一些发展建议,详细内容将分小节讨论。

表5 可再生能源电解制氢技术路线对比
3.2 光伏发电制氢
3.2.1 光伏发电制氢概述
太阳能是当前最受青睐的可再生能源之一,围绕其展开的技术研究和应用是人类对能源利用的永恒主题。随着人类对氢能需求的增大,以水为原料利用太阳能大规模制氢已成为世界各国共同努力的目标。利用太阳能制氢的方法有光电化学或光催化分解水制氢、光伏发电与电解水制氢、太阳能热化学分解水制氢等。其中,光伏发电制氢技术因国家对光伏发电产业的推动、光伏发电成本的降低以及以燃料电池为代表的各种氢能利用技术的迅猛发展,已成为实现可再生能源高效利用、能源结构优化、促进清洁能源发展的重要途径。
目前,光伏发电制氢技术根据太阳能光伏板与电解槽之间的连接方式可以分为间接连接和直接耦合两种系统。间接连接系统是当前主要采用的方式[88-89],其主要部件包括光伏阵列、蓄电池、转换器、电解槽。基本设计方式是通过蓄电池蓄能,利用转化器调节输出电压、电流,最终满足电解槽要求。该系统优势在于可发挥电解槽的性能,使其在稳定的电压下运行;缺点是转化器等电子设备增加了系统成本,同时伴随电能传递损失,降低了系统效率[90]。直接耦合系统是通过对光伏阵列与电解槽之间的最佳结构匹配,省去蓄电池和转换器等设备,优势是系统简单且减少了故障出现次数,有效地减少了维护成本。研究表明,充分考虑当地气候、日照、温度等气象条件,通过合理地设计光伏阵列、电解槽的构成方式,直接耦合链接较传统的间接链接方式更能达到提高太阳能电解水制氢效率的目的[91]。
光伏发电制氢技术优势明显,主要体现在以下几方面:①光伏发电具有随机性、波动性、阶段性供电等问题,增加了电网调度难度,同时面临增加储能问题,将光能和电能利用电解水制氢转化为氢能,实现了能量的有效利用和存储,是解决该问题的有效途径;②光伏发电制氢工艺简单、运行维护难度低,制氢规模可根据场地和需求进行模块化组合,分布式可再生能源制氢供应燃料电池也是未来重要发展方向,可实现能量的高效、灵活应用;③光伏发电是可再生能源替代传统能源的重要方式,电解水制氢是实现清洁能源开发的重要手段,二者的结合符合国家发展绿色清洁能源战略要求,绿色低碳更符合全球能源替代和环境治理的需求。
3.2.2 光伏发电制氢国内外进展
随着氢能在全球的需求日益增多,光伏发电制氢技术被视为未来新能源最具潜力的发展方向之一,日本、德国、法国、荷兰、澳大利亚等国家均已开展大型光伏制氢项目的研究或投入。日本政府高度重视氢能发展,提出建设“氢能社会”的愿景,与氢能相关的氢燃料电池技术等在全球也处于领先地位。2020年3月,日本企业集团东芝公司宣布其福岛氢能研究领域(FH2R)项目正式投产,项目配备20MW的光伏发电系统以及10MW的电解槽装置。澳大利亚BOC制氢项目配备220kW电解槽和100kW太阳能阵列,实现可再生氢的大规模供应。2019年12月,法国宣布新一批氢能源公交车正式启用,该公交车搭载太阳能电池板,通过光伏制氢产生动力。
自2013年我国实行度电补贴政策以来,国内光伏行业得到了快速发展,近年来迎着氢能上升为国家能源战略的机遇,各大企业纷纷布局光伏制氢项目。2019年12月,由中国科学院李灿院士团队主导的太阳能燃料生产示范工程在兰州新区精细化工园区落地。该项目由光伏发电、电解水制氢、二氧化碳加氢合成甲醇三大系统单元组成,通过装机规模为10MW的光伏发电单元向2台功率为1000m3/h的电解槽供电实现电解水制氢。2020年4月,宁夏宝丰能源集团开工建设太阳能电解水制氢储能及综合应用示范项目,同时配套建设光伏电站及下游加氢站,建成后合计年产氢气1.6亿标方,可减少煤炭资源消耗25.4万吨/年,减少二氧化碳排放约44.5万吨/年。
3.2.3 光伏发电制氢项目问题及建议
光伏发电制氢技术的发展首先受制于光伏发电技术的进步,目前光伏发电仍存在诸多问题:①光伏发电的最大问题仍是上网问题,自身电力不稳定,没有电网的协助前期无法满足应用要求,因此电网配套问题将决定光伏发电发展速度,采用间接连接和直接耦合电解水制氢则需要综合评价;②我国已经连续第五年在光伏新增规模上领跑全球,但其最核心技术均起源于外国,这无疑对未来光伏产业的发展带来严重挑战,同样制约着光伏制氢技术进步;③由于西北地区弃光限电严重,目前全国的光伏发展重心已经逐步转移到了中东部,其分布式、集中式装机都呈现出爆发式增长的态势,如何与氢能产业发展同步、高效推进,将成为光伏制氢技术无法回避的问题。
实现光伏发电制氢高效利用,需要在以下几方面寻求突破。①解决光伏发电上网成本问题。随着我国下调光伏补贴电价,未来光伏产业如何发展将决定光伏发电制氢的命运,建议我国部分光照资源优势的地区逐步扩大规模,先行示范。②解决核心技术问题。在光伏和氢能核心技术领域加大科研投入比例,依托现有示范项目进行技术攻关,提升核心竞争力。③探索合理布局的示范项目。光伏发电具备分布式、灵活性建设优势,鉴于氢燃料电池产业高速发展带动的氢气需求用量增多,可进一步探索小规模光伏发电制氢示范路线,为未来构建氢能社会提供更多选择。
3.3 风力发电制氢
3.3.1 风力发电制氢概述
风力发电制氢是利用风力驱动产生电能,再通过电解水制氢技术生产氢气,最终输送至氢能应用终端。该技术主要分为并网型风电制氢和离网型风电制氢两类。并网型是指将风电机组直接接入电网,利用电网电力实现电解水制氢,多应用于大规模风电场;离网型是指将风电机组产生的电能直接输送至电解水制氢装置,无需经过电网分配,多应用于分布式制氢或燃料电池技术[92]。
风力发电制氢系统的主要优势在于以下几方面。①保证电力高效利用。风力发电机组首先可保证向电网供电,当电网客户端用电量较少时,剩余电能输送至电解水装置,把电能转变为氢能存储起来;当电网负荷过重、风电机组超负荷运行时,又可将氢气和氧气通过氢氧联合发电系统进行循环发电,将电能供给电网,最终实现电力的高效利用,起到“削峰填谷”作用。②实现能量可持续存储。由于风资源存在随机性、间歇性及无规律性等问题,导致风电电能品质差,大多数情况被迫弃风;而且电能存储较难,传统的电化学储能、电磁储能及物理储能技术无法满足未来发展需求,且运行成本较高,电解水制氢的引入有效解决了上述问题,实现了能量的可持续存储。③氢能综合利用。氢作为清洁、易存储、易传输的二次能源,既可以融入现有的燃气供应网络,实现电力到燃气的互补转化,又可以直接供应至氢能终端应用系统,符合未来纯绿色能源发展的需求。④优化能源结构。大容量、不稳定风电并网时会引起电网电压的大幅度波动,为调控和抑制这种波动,需要建造比风电场总容量大2~3倍的“调压控制电站”以解决输电稳定性问题,而这些调控电站却需要更多的传统能源来支持,综合考虑反而增大了传统能源的使用,无益于能源结构的优化[93-94]。
3.3.2 风力发电制氢国内外进展
欧洲和美国对风电制氢技术发展较为重视。欧洲启动了INGRID氢储能项目,以提升可再生能源的利用效率,维护电网安全和稳定。德国制定了“Power to gas”发展计划,将氢气作为能源载体或原料供应至氢燃料电池汽车,并打算2022年之前全面废除核电,扩大可再生能源占比。2011年10月,在德国柏林建成的氢气储能和利用项目(“风氢混合电站”)正式启用。2004年,美国能源部国家可再生能源实验中心(NREL)与Xcel能源公司合作推出了Wind2H2计划,以助力科研人员掌握可再生能源电解制氢关键技术问题。
我国风电制氢技术研发起步较晚,近年来在国家政策指导、可再生能源技术突破和氢能产业蓬勃发展的推动作用下,一些风电制氢综合示范项目先后落地。2014年4月,由中国节能环保集团公司负责的国家863计划“风电直接制氢及燃料电池发电系统技术研究与示范”项目启动,该项目制氢功率为100kW,燃料电池发电为30kW。2015年4月,由河北建投新能源有限公司投资,与德国McPhy、Encon等公司合作建设的沽源风电制氢综合利用示范项目,包括200MW容量风电场、10MW电解水制氢系统和氢气综合利用系统三部分,对风电消纳、氢气综合利用具有重要意义。
3.3.3 风力发电制氢存在的问题及建议
当前,我国风电制氢技术发展主要面临的问题如下。①技术方面。电解水制氢技术对电能的要求较高,而风电不可避免的随机性、不稳定性使得电力供应频繁波动,对制氢设备的高效利用、使用寿命、产品纯度均造成影响,如何实现最优电能匹配以提高设备利用率需要进一步加大技术投入。②应用方面。当前氢气大规模利用单位仍为化工企业,考虑到运输和存储成本,企业通常采用传统制氢方式自供应氢气;另一方面,虽然高纯氢气用户较多,但用量较小,氢燃料电池行业处于起步阶段,暂不具备大规模应用条件。③科研方面。当前风电制氢示范项目中诸多问题仍未得到有效解决,如系统在线动态优化控制、风氢热电联产、并网风氢系统与电网相互作用机理探究等,未来需进一步加大科研投入力量以推动产业发展。
针对当前风电制氢存在的上述问题,给出以下几点建议。①寻求关键技术突破。针对风电的间歇性和波动性问题,电解水制氢技术可寻求自身技术突破,进一步开发低成本、高效率的碱性电解水制氢技术,同时加大质子交换膜、固体氧化物电解水制氢技术投入,以适应生产条件。②推动海上风电制氢项目发展。当前风电制氢仍采用并网型方式,考虑输电线路的容量问题,风电厂和氢气用户距离不宜太远;从区域方面考虑,现阶段对氢气需求量较大的企业大都分布在沿海地区,以往风电机组均建设在内陆,未来需大力推进海上风电项目,可同时解决电力运输和氢能储运方面等存在的问题。③注重综合性评价。在社会、环境及经济各方面进行综合研究,建立一套多能源转换利用的综合效益评价指标体系,实现对风电制氢运行模式及经济性优化。
3.4 其他可再生能源发电制氢技术
利用可再生能源发电驱动电解水制氢,除光伏发电制氢、风力发电制氢,还有水力发电制氢、生物质发电制氢等。
3.4.1 水力发电制氢
水力发电制氢是指通过水力发电产生的电力驱动电解水制氢,该技术暂不适合全国推广,因为我国水力资源分布不均,具有较强的地域性,目前可优先在水力资源丰富的省市进行试点。水力发电制氢的核心优势仍然是解决可再生能源消纳问题。据统计,作为“西电东送”的主要能源基地四川省和云南省,由于经济规模总量小、消纳能力不足等原因,水电弃水问题日益突出,两省近五年累计弃水量接近三峡水电站两年的发电量[96]。通过将水电与电解水制氢技术耦合,可充分利用富余水电并将富余电力储存起来,实现水电规模性消纳,进一步提升水电产业的综合经济效益。截止目前,国内仍未有专门的水电制氢项目落地,主要原因是发展水电制氢需要综合当地经济发展水平,且现阶段规模化氢能产业尚未成熟。未来水电制氢需要多方合力推动,一是政府出台相应政策以促进发展,二是氢能全产业链需要配套完善,三是要合理布局,考虑技术、成本各方面问题。
3.4.2 生物质发电制氢
在国家一系列利好政策推动下,生物质发电技术蓬勃发展。利用生物质能发电有其独特优势,例如,秸秆直燃可实现CO2零排放,燃烧后的灰渣可加以综合利用;垃圾焚烧实现了垃圾处理的无害化、减量化;沼气发电效率高、建站简单、投资少;生物质气化污染排放较低、小规模效率高、规模灵活。上述技术优势明显,但成熟度和经济性仍是限制其发展的关键,并未大规模推广。因此,将生物质发电与电解水制氢技术结合,严重依赖于我国生物质发电技术的突破。随着我国城镇化发展的进度加快,未来生物质发电与氢能的耦合将在小规模、示范性、灵活性方面发力,成为该领域未来的发展方向之一[95]。考虑到电解水制氢技术对电力成本的严重依赖性,推动二者的技术耦合首先需各方在生物质发电方面下功夫。例如,政府可借鉴风电、光伏所积累的经验进行合理的专项电价补贴;电网公司给予生物质发电足够重视,做好相关规划和产业推动工作;生物质发电企业通过技术设备升级等方式提升企业在环保层面的核心竞争力。总之,生物质能与氢能作为我国可再生能源和清洁能源的代表,二者的结合必将为我国建设成为环境节约型和资源友好型社会做出突出贡献。
4 结语
能源低碳化和氢能产业化已成为世界能源的发展趋势,需要国家引领、企业合作、产业协同等各方面推动。本综述聚焦氢能和可在生能源两大领域,从氢能产业链上游制氢技术出发,简述了电解水制氢技术的核心问题,重点综述了电解水制氢催化剂的研究进展,从基础研究展开讨论并转向实际工业应用。结合当前我国可再生能源亟待解决的消纳问题以及探索生产低碳氢能的需求,论述了可再生能源发电与电解水制氢技术耦合的重要性,并列举了风力、光伏、水力等可再生能源发电制氢项目的开发进展及现阶段存在的问题,并给出一些建议。最后为实现我国传统能源向低碳清洁能源转型、可再生能源高效利用、氢能产业高质量发展总结出以下几点结论。
(1)在制氢技术方面,继续推动电解水制氢技术的发展是实现低碳氢供给的重要途径,可有效解决我国氢气制备严重依赖化石能源及氢气产能不足的问题。
(2)在电解水制氢方面,需要不断优化现有的电解水制氢技术,在降低成本、减小能耗、提高效率等方面下功夫,对核心关键部件,如电解槽、隔膜、电极材料等加大研发投入力度,以解决限制其发展的关键问题。
(3)在电解水析氢催化剂方面,一方面要降低贵金属的使用,设计出结构合理、性能高效的HER催化剂,如单原子催化剂;另一方面要开发非贵金属基催化剂,重点加大对过渡金属基电催化剂的研发,早日实现对Pt/C等贵金属催化剂的替代,降低成本、提升性能。
(4)在优化能源结构方面,积极探索出可再生能源发电与电解水制氢耦合的合理路径,有效解决可再生能源消纳问题,实现不同能源网络之间的协同优化,促进清洁能源发展。
