参芪固本方破壁饮片与传统汤剂联合鹤蟾片治疗ⅢB、Ⅳ期非小细胞肺癌的疗效及安全性研究
2021-06-11王雄文乔翠霞张俊萍邓运宗王红玲熊绍权罗秋月方灿途李陆振王斌田华琴梁燕玲周岱翰成金乐
王雄文, 乔翠霞, 张俊萍, 邓运宗, 王红玲, 熊绍权, 罗秋月,方灿途, 李陆振, 王斌, 田华琴, 梁燕玲, 周岱翰, 成金乐
1.广州中医药大学第一附属医院,广东 广州 510405;2.河南中医药研究院附属医院,河南 郑州 450000;3.河南中医药大学第三附属医院,河南 郑州 450000;4.成都中医药大学附属医院,四川 成都 610000;5.广州中医药大学附属中山医院(中山市中医院),广东 中山 528400;6.佛山市中医院,广东 佛山 528000;7.中山中智药业,广东 中山 528400
2020年全球新发肺癌病例数220万,死亡数179万,占所有肿瘤发病率的第二位和死亡率的第一位,而我国肺癌的发病率及死亡率均居所有肿瘤首位[1]。非小细胞肺癌(Non-small Cell Lung Cancer,NSCLC)是肺癌发病的主要类型,占比85%[2]。现阶段晚期NSCLC治疗路径明确,对于驱动基因阴性的晚期NSCLC的患者,化疗是治疗的基石[3],联合PD-1免疫治疗可获得更好的疾病控制率(Disease Control Rate,DCR)及生存时间(Overall Survival,OS)。而驱动基因阳性患者以针对性靶向治疗为主,综合治疗方案也与无进展生存时间(Progression-Free Survival,PFS)相关。含铂双药化疗会导致骨髓抑制及肝肾功能损伤等毒副作用[4],同样靶向治疗及PD-1免疫治疗可能也会因副作用致使治疗中断,影响疗效。中医认为肺癌的病机与“瘀”“痰”“毒”“虚”有关,晚期肺癌证型以“正气亏虚”为主[5],其中正气虚又包括气虚、血虚、阴虚、阳虚等证,涉及脏腑主要为肺、脾、肾,其在疾病发生发展过程中可互为影响。参芪固本方及鹤蟾片均是周岱翰教授治疗肺癌的经验方[6],前者有健脾固肾、益气补血的功效;后者是国内第一个批准生产并进入药典的治肺癌的中成药,有解毒除痰,凉血祛瘀,消癥散结的疗效,二者联用有扶正祛邪,攻补兼施之功。
参芪固本方破壁饮片是中山市中智药业集团研制的新型中药饮片,通过现代粉碎技术将传统中药饮片加工至D90<45 μm的粉体,不添加成型技术制成的30-100目的干燥颗粒状饮片,其优点是保留了原中药饮片的全部成分,可使其成分利用率提高至60%~90%,大部分中药破壁饮片剂量为其传统剂量的1/2~1/4,甚至1/8,即可产生与传统饮片相近或更强的药效作用[7]。
本研究设计参芪固本方破壁饮片或传统汤剂联合鹤蟾片治疗ⅢB、Ⅳ期非小细胞肺癌,分析二者疗效及安全性差异。
1 材料与方法
1.1 研究对象
病例来自于广州中医药大学第一附属医院、河南中医药研究院附属医院、河南中医药大学第三附属医院、成都中医药大学附属医院、广州中医药大学附属中山医院、佛山市中医院6家医院2016年6月至2019年6月就诊患者共73例,随机将研究对象进行分组,传统汤剂组33例,破壁饮片组40例。研究对象皆知情同意研究方案并签署知情同意书,试验已通过所在单位或地区伦理学相关机构的批准(编号:CTXY-150012-4)。
1.2 筛选标准
1.2.1 纳入标准
(1)符合中华人民共和国医政司编写的《常见恶性肿瘤诊治规范》中的肺癌诊断标准,经过病理组织学或细胞学证实的ⅢB/Ⅳ期非小细胞肺癌患者(NSCLC分期参照AJCC,第七版标准),中医辨证属于脾虚痰湿证或气阴两虚证(中医辨证标准参照周岱翰教授主编的《中医肿瘤学》);(2)年龄18~80岁;(3)预期生存期超过4个月;(4)患者不宜或不愿意行手术、放化疗及靶向治疗者;(5)一个月内未接受手术、放化疗、靶向治疗等治疗者;(6)患者愿意接受本方案治疗、依从性好者;(7)无合并主要器官疾病及功能障碍,血、尿、粪三大常规、肝肾功能及心功能基本正常;(8)体力状况评分(Performance Status,PS)0~3分;(9)神志清楚,可客观配合完成疾病及身体状况的检查和评估;(10)自愿加入本研究,签署知情同意书的患者。
1.2.2 排除标准
(1)入组前已经接受一周及以上类似参芪固本方补益类中药、中成药治疗的患者;(2)合并精神病患者,妊娠期或哺乳期妇女;(3)重复癌未愈者;(4)依从性差者;(5)严重感染;(6)研究者认为不适宜参加本研究的其它情况。
1.2.3 剔除标准
(1)不符合纳入标准而被误纳入者;(2)符合纳入标准而纳入后未曾用药者,或无任何复诊记录者;(3)自行中途换药或加用非规定范围内联合用药,特别是合用对试验药物影响较大的药物,影响药物有效性和安全性判断者。
1.3 治疗方法
1.3.1 分组 试验组:参芪固本方破壁饮片联合鹤蟾片,参芪固本方破壁饮片(30 g/次),每日2次,冲服;鹤蟾片,5片/次,每日3次,口服。对照组:参芪固本方传统汤剂联合鹤蟾片,每天1剂(120 g/剂),煎两次,每次200 ml,每日2次;鹤蟾片服用方法同上。
1.3.2 治疗周期 筛选期V1(2周,-14天~0天),治疗期V2(30天±3天)、V3(90天±3天),随访期V4(试验用药后20个月)。其中,治疗期V2、V3各进行一次疗效评价。
1.3.3 合并用药 观察期间禁止使用其他补益类中草药及中成药;若患有其他合并疾病所必需继续服用药物或进行其它治疗,必须在病例报告表中记录药品通用名或其它疗法名、用量、使用原因、使用次数和时间等,以便总结时加以分析和报告;试验过程中因不良事件需使用的合并用药,应详细记录在病例报告表中。
1.4 疗效标准与观察指标
1.4.1 主要疗效指标
(1)体力状况积分(PS)、中医症状积分(参考《中医虚证辨证参考标准》);(2)骨髓抑制发生率。
1.4.2 次要疗效指标
(1)生存期;(2)肿瘤标志物(CEA、Cyfra21-1、CA153、CA125、SCC)。
1.5 统计学方法
2 结果
2.1 一般资料
2016年6月至2019年6月期间来自6家医院符合纳排标准病例共73例,随机分为传统汤剂组33例,破壁饮片组40例。两组一般情况见表1,两组患者基线情况差异无统计学意义。

表1 基线资料情况Table 1 Basic characteristics
2.2 主要疗效指标比较
2.2.1 体力状况积分(PS)
破壁饮片组与传统汤剂组患者PS评分在访视期V2和访视期V3差异没有统计学意义(P>0.05,V2 P=0.873;V3 P=0.976),具体结果如表2。
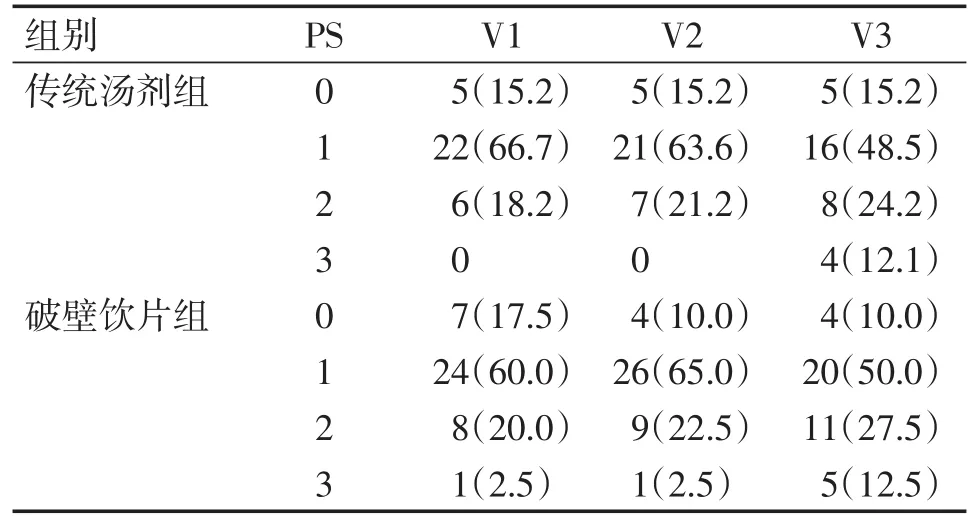
表2 两组体力状况积分情况比较[n(%)]Table 2 Comparison of PS between the two groups and comparison before and after treatment
2.2.2 中医症状积分
破壁饮片组与传统汤剂组两组在访视期V2、V3内脾虚证主证积分差异均没有统计学意义(P>0.05);传统汤剂组在治疗前后脾虚证主证积分差异没有统计学意义(P>0.05),破壁饮片组脾虚证主证积分治疗前后差异没有统计学意义(P>0.05),具体如表3。
表3 两组脾虚证主证积分比较及治疗前后比较(±s)Table 3 Comparison of main syndrome scores of the spleen deficiency syndrome between two groups and comparison before and treatment

表3 两组脾虚证主证积分比较及治疗前后比较(±s)Table 3 Comparison of main syndrome scores of the spleen deficiency syndrome between two groups and comparison before and treatment
注:①两组脾虚证主证积分在访视V1时P=0.94;②在访视V2时P=0.71;③在访视V3时P=0.44;④是表示访视V1与访视V2之间对照的P值;⑤是表示访视V1与访视V3之间对照的P值。
脾虚证主证积分组别P⑤P④(V1-V3)0.12 0.30传统汤剂组破壁饮片组V1①1.30±0.79 1.38±0.80 V2②1.26±0.71 1.29±0.81 V3③1.12±0.68 1.30±0.78(V1-V2)0.36 0.13
破壁饮片组与传统汤剂组在各访视期V2、V3内痰湿证主证积分差异均没有统计学意义(P>0.05);传统汤剂组在V3时痰湿证主证积分下降,差异具有统计学意义(P=0.01);破壁饮片组痰湿证主证积分在治疗前V2、V3时统计分析差异均有统计学意义(P=0.00,P=0.00),具体见表4。
表4 两组痰湿证主证积分比较及治疗前后比较(±s)Table 4 Comparison of the main syndrome scores of the phlegm-dampness syndrome between two groups and comparison before and after treatment

表4 两组痰湿证主证积分比较及治疗前后比较(±s)Table 4 Comparison of the main syndrome scores of the phlegm-dampness syndrome between two groups and comparison before and after treatment
注:①两组在访视V1时P=0.96;②在访视V2时P=0.07;③在访视 V3时P=0.06;④(V1-V2)是表示访视V1与访视V2间对照的P值;⑤(V1-V3)是表示访视V1与访视V3间对照的P值。
痰湿证主证积分组别P④P⑤(V1-V3)0.01 0.00传统汤剂组破壁饮片组V1①2.24±1.35 1.65±1.25 V2②2.07±1.44 1.09±0.87 V3③1.59±1.17 0.93±0.78(V1-V2)0.30 0.00
破壁饮片组与传统汤剂组在各访视期V2、V3内气虚证主证积分差异均没有统计学意义(P>0.05);传统汤剂组在治疗后V3时气虚证主证积分下降,差异具有统计学意义(P=0.04);破壁饮片组气虚证主证积分在治疗后V2、V3期统计分析差异均没有统计学意义(P>0.05),具体如表5。
表5 两组气虚证主证积分比较及治疗前后比较(±s)Table 5 Comparison of the main syndrome scores of the Qi-deficiency syndrome between two groups and comparison before and after treatment

表5 两组气虚证主证积分比较及治疗前后比较(±s)Table 5 Comparison of the main syndrome scores of the Qi-deficiency syndrome between two groups and comparison before and after treatment
注:①两组在访视V1时P=0.84;②在访视V2时P=0.32;③在访视V3时P=0.94;④(V1-V2)是表示访视V1与访视V2之间对照的P值;⑤(V1-V3)是表示访视V1与访视V3之间对照的P值。
气虚证主证积分组别P④P⑤(V1-V3)0.04 0.40传统汤剂组破壁饮片组V1①1.15±0.97 1.04±1.06 V2②1.02±1.15 0.95±0.94 V3③0.80±1.00 1.06±0.96(V1-V2)0.49 0.28
破壁饮片组与传统汤剂组在各访视期V2、V3内阴虚证主证积分差异没有统计学意义(P>0.05);传统汤剂组在治疗后V2、V3时阴虚证主证积分均见下降,差异有统计学意义(P=0.01,P=0.02);而破壁饮片组阴虚证主证积分在治疗V2、V3期统计分析差异没有统计学意义(P>0.05),具体如表6。
表6 两组阴虚证主证积分比较及治疗前后比较(±s)Table 6 Comparison of main syndrome scores of Yin deficiency syndrome between two groups

表6 两组阴虚证主证积分比较及治疗前后比较(±s)Table 6 Comparison of main syndrome scores of Yin deficiency syndrome between two groups
注:①两组在访视V1时P=0.20;②两组在访视V2时P=0.65;③两组在访视V3时P=0.60;④表示访视V1与访视V2之间对照的P值;⑤是表示访视V1与访视V3之间对照的P值。
阴虚证主证积分组别P④P⑤(V1-V3)0.02 0.87传统汤剂组破壁饮片组V1①1.33±1.40 1.04±1.18 V2②0.96±0.98 1.11±0.95 V3③0.96±0.93 1.11±1.11(V1-V2)0.01 1.00
2.2.3 骨髓抑制情况
由于统计数据V2部分不完整,因此剔除V2时段的统计数据,仅对两组治疗前V1及治疗后V3时段比较,以及各组治疗前后进行比较,经统计学分析,传统汤剂组及破壁饮片组治疗前后均无明显骨髓抑制,差异没有统计学意义(P均>0.05),见表7。
表7 两组治疗前后骨髓抑制情况比较(±s)Table 7 Comparison of bone marrow suppression between the two groups
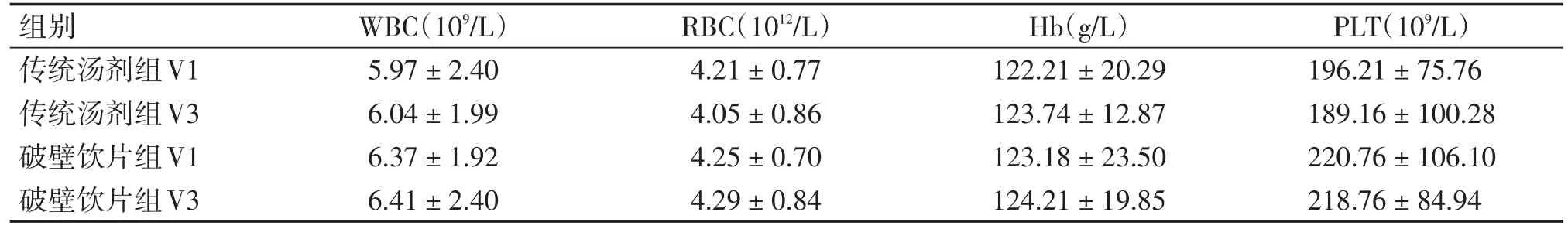
表7 两组治疗前后骨髓抑制情况比较(±s)Table 7 Comparison of bone marrow suppression between the two groups
组别传统汤剂组V1传统汤剂组V3破壁饮片组V1破壁饮片组V3 WBC(109/L)5.97±2.40 6.04±1.99 6.37±1.92 6.41±2.40 RBC(1012/L)4.21±0.77 4.05±0.86 4.25±0.70 4.29±0.84 Hb(g/L)122.21±20.29 123.74±12.87 123.18±23.50 124.21±19.85 PLT(109/L)196.21±75.76 189.16±100.28 220.76±106.10 218.76±84.94
2.3 次要疗效指标
2.3.1 生存分析
随访跟踪患者的生存情况,其中参芪固本方破壁饮片组1例患者失访,截止随访结束存活25例,死亡14例,传统汤剂组1例患者失访,截止随访结束存活16例,死亡16例。通过Kaplan-Meier法绘制生存曲线,经Log-rank检验,两组中位生存期差异无统计学意义(P=0.859),具体结果如表8及图1。
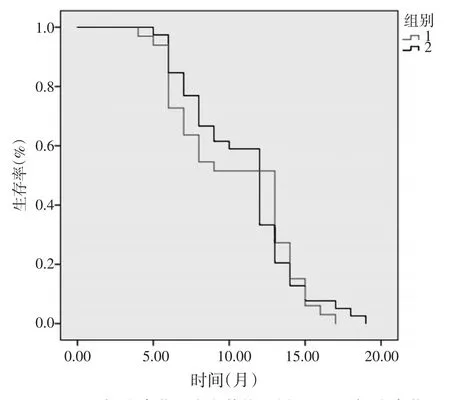
图1 两组患者总生存期曲线图Figure 1 The survival curve of the two groups of patients
表8 两组生存期比较(±s)Table 8 Comparison of the median survival time between the two group
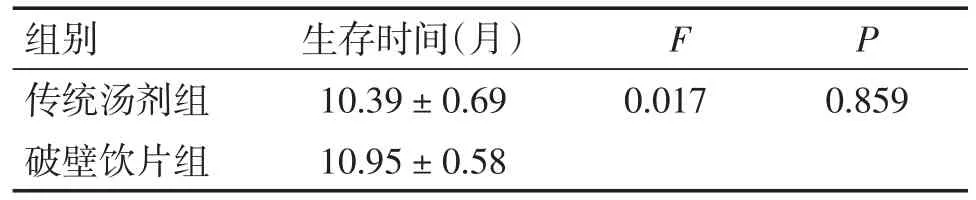
表8 两组生存期比较(±s)Table 8 Comparison of the median survival time between the two group
组别传统汤剂组破壁饮片组生存时间(月)10.39±0.69 10.95±0.58 F P 0.0170.859
2.3.2 肿瘤标志物变化
经统计分析发现,破壁饮片组与传统汤剂组在治疗前后,肿瘤标志物CEA、Cyfra21-1、CA153、CA125、SCC差异没有统计学意义,提示两种剂型在改变肿瘤标志物方面疗效相当。具体结果见表9。
表9 两组治疗前后肿瘤标志物变化(±s)Table 9 Changes of tumor markers in the two groups before and treatment
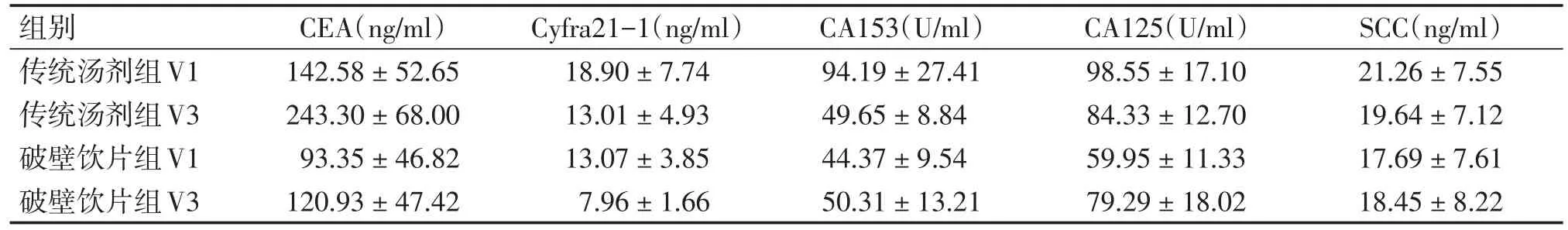
表9 两组治疗前后肿瘤标志物变化(±s)Table 9 Changes of tumor markers in the two groups before and treatment
组别传统汤剂组V1传统汤剂组V3破壁饮片组V1破壁饮片组V3 CEA(ng/ml)142.58±52.65 243.30±68.00 93.35±46.82 120.93±47.42 Cyfra21-1(ng/ml)18.90±7.74 13.01±4.93 13.07±3.85 7.96±1.66 CA153(U/ml)94.19±27.41 49.65±8.84 44.37±9.54 50.31±13.21 CA125(U/ml)98.55±17.10 84.33±12.70 59.95±11.33 79.29±18.02 SCC(ng/ml)21.26±7.55 19.64±7.12 17.69±7.61 18.45±8.22
表10 两组治疗前后肝肾功能比较(±s)Table 10 Comparison of liver and kidney function between the two groups before and ofter treatment
组别传统汤剂组V1传统汤剂组V2传统汤剂组V3破壁饮片组V1破壁饮片组V2破壁饮片组V3 ALT(U/L)23.96±11.38 27.96±17.52 27.06±11.81 22.00±12.59 22.98±13.23 25.59±15.00 AST(U/L)29.65±13.01 28.97±13.65 26.67±11.05 23.84±11.59 25.33±11.12 31.84±19.48 TBIL(umol/L)14.76±9.58 15.45±12.90 19.25±4.19 13.32±4.35 13.24±4.95 14.00±6.87 GGT(U/L)49.07±46.87 62.83±14.65 65.05±53.29 40.93±8.67 54.06±12.82 43.95±37.46 BUN(umol/L)64.61±27.71 64.02±25.74 70.53±38.11 62.90±15.00 61.48±21.17 64.12±21.75 SCr(mmol/L)9.58±3.32 5.63±1.30 6.00±1.18 4.65±1.79 22.62±17.04 8.26±3.00
2.4 安全性评价
经统计学分析,治疗前后各访视期内抽血查肝肾功能,两组肝肾功能各指标均在正常范围内,未见明显的肝肾毒性,且两组治疗前后及组间比较差异均没有统计学意义(P均>0.05)。
3 讨论
本研究参芪固本方联合鹤蟾片同用治疗ⅢB、Ⅳ期NSCLC,扶正抑瘤,攻补兼施,研究结果显示参芪固本方破壁饮片组与传统汤剂组在治疗期V2(30天±3天)、V3(90天±3天)中医症状积分方面、体力状况评分(PS)方面、相关肿瘤标志物等方面均未见明显差异。同时,结果表明两个治疗组V3访视期(90天±3天)治疗前后自身对照比较,破壁饮片能更好地改善痰湿证积分,而传统汤剂改善阴虚证积分更优。生存分析显示治疗Ⅳ期为主的晚期肺癌患者皆获得超过10个月的生存时间,但两组比较亦未见明显差异。在安全性方面,两组均未见明显的肝肾功能损害,均未见骨髓抑制的发生。
参芪固本方是国医大师周岱翰多年临证实践的经验方,方中以党参、黄芪为君,健脾补中、益气养血;臣以淫羊藿、女贞子,补肾强精生血;佐以白术、茯苓健脾除湿,既助党参补脾胃之气,又增强脾之运化,以助后天之源;以五味子为使药,载药入脾肾,全方共奏健脾补肾、益气养血之功。固护脾胃,则气血生化有源,精血可得化生,正气得复;补中有疏,气血得以调达,可助驱邪外出[6]。鹤蟾片治疗肺癌的研究获得1986年卫生部“全国中医药重大科技成果乙等奖”,是二十余年来临床常用于治肺癌的中成药,主要由干蟾皮、仙鹤草、浙贝母、猫爪草、鱼腥草等药物组成,具有“除痰、消癥、散结”等功效,其联合化疗,可减毒增效,延长患者生存期[7]。林伟波[8]通过临床研究发现参芪固本方破壁饮片与传统汤剂均可改善大肠癌化疗后出现的骨髓抑制等以虚证为主的部分证候。经治疗后,患者外周血白细胞、红细胞及血红蛋白等计数相对增多,同时还可以调节人体免疫功能,大约1/3剂量的参芪固本方破壁片即可达到近似于参芪固本方传统饮片疗效。黄裕芳[9]通过临床研究,发现参芪固本方破壁饮片及传统饮片均可明显改善肿瘤患者化疗后骨髓抑制的临床症状,如神疲乏力、食欲减退等,较大程度上改善了患者生活质量,且两种剂型效果相当。
中药材资源宝贵,将剂型调整为破壁剂型,解决了中药煎煮不便的问题,也提高了中药材的有效利用率。而基于以上研究结果分析认为,参芪固本方破壁饮片可用于晚期肺癌的综合治疗,且疗效不劣于传统汤剂,因此,可作为传统中医汤剂的替代。本研究也存在不足,基线数据没有充分考虑驱动基因情况,以及并未把瘤体变化作为疗效指标等,今后的研究再进一步完善。
