微导管微导丝技术治疗患儿极细小动脉导管未闭的临床应用
2021-05-06耿文磊胡海波吕建华刘垚徐亮徐仲英张戈军潘湘斌
耿文磊 胡海波 吕建华 刘垚 徐亮 徐仲英 张戈军 潘湘斌
动脉导管未闭(patent ductus arteriosus,PDA)是常见先天性心脏病之一,在先天性心脏病新生儿中的发生率约10%[1]。对直径较大或有血流动力学意义的PDA行经导管介入封堵治疗已经成为临床常规,技术上安全成熟;对无明显血流动力学意义的细小PDA是否行介入治疗,目前临床存在一定争议,但因其感染性心内膜炎(infective endocarditis,IE)的概率较正常人明显增高,因此在技术安全的前提下仍然主张介入治疗[2]。对于极细小PDA(直径<1 mm),由于常规泥鳅导丝无法通过PDA的原因,临床上封堵成功率低,国内外对此类型PDA介入封堵的经验尚不足,目前尚缺乏一种安全、有效的介入技术来解决极细小PDA介入封堵问题。2017年4月10日至2019年12月20日,中国医学科学院阜外医院尝试应用Amplatzer ductal occluder(ADO)Ⅱ封堵器配合微导管微导丝轨道技术对12例患儿极细小PDA进行了介入封堵治疗,现报道如下。
1 对象与方法
1. 1 研究对象
2017年4月10日至2019年12月20日,应用美国AGA公司第Ⅱ代PDA封堵器(ADO Ⅱ)治疗患儿极细小PDA共12例。入选标准:年龄大于6个月;体重>5 kg;术前超声心动图提示PDA直径<3 mm,术中造影示PDA直径<1 mm。排除标准:患者合并其他急性疾病,如急性感染等;合并其他严重心脏畸形;对对比剂过敏。
1. 2 介入封堵方法
(1)微导丝、微导管建立半轨道法:全身麻醉下穿刺右股动脉,置入5 F Terumo儿童穿刺鞘管,送入5 F猪尾导管行降主动脉造影,明确PDA的位置、大小、形态;然后将4 F ADO Ⅱ封堵器专用输送鞘管送入PDA主动脉侧附近,借鉴现有冠状动脉介入技术和微导丝(BMW, 雅培),将0.014 in(1 in=2.54 cm)BMW微导丝(直径约0.356 mm)预装入1.9~2.4 F微导管(外径0.627~0.792 mm)内,一起送入4 F输送鞘管管腔内并远端出头。小幅度调整输送鞘管位置、方向,操控微导丝微导管寻找PDA主动脉侧入口并通过PDA,然后在微导管保护下将微导丝、微导管一同跨肺动脉瓣送入右心室-右心房-上腔或下腔静脉,建立微导丝、微导管半轨道(不使用圈套器),在半轨道支撑下,再沿微导丝、微导管轨道导入4 F输送鞘管通过PDA,然后经股动脉入径导入和释放ADO Ⅱ封堵器,完成逆向经股动脉入径行PDA介入封堵。
(2)微导丝、微导管建立全轨道法:如果上述半轨道法4 F输送鞘管仍然无法获得有效支撑不能通过PDA狭窄端进入肺动脉(推送中切忌暴力强行通过),则选择穿刺右股静脉,送入5 F Terumo儿童穿刺鞘管,经股静脉送入5 F MPA2导管及圈套器,在上腔或下腔静脉抓取有微导管保护的微导丝,不拉出体外,建立全轨道,借用全轨道的支撑力,送4 F输送鞘管从主动脉侧通过PDA最狭窄端进入肺动脉,然后采用经股动脉入径逆行封堵PDA。也可以将微导管微导丝拉出体外后,利用冠状动脉延长导丝技术,由股静脉侧送入4 F输送鞘管,从肺动脉侧通过PDA进入降主动脉,然后完成顺行经股静脉入径PDA介入封堵。无论哪种方法,封堵术后都要应用5 F MPA2导管进行升主动脉-降主动脉连续测压,排除PDA封堵术后造成的弓降部压差,如果压差>20 mmHg(1 mmHg=0.133 kPa)可考虑介入回收封堵器。
1. 3 术后随访
术后24 h、1个月、3个月、6个月门诊复查超声心动图、心电图、X线胸片,主要观察术后患者左心形态及是否存在残余分流。
1. 4 统计学分析
所有数据应用SPSS 18.0进行统计学分析。计量资料以均数±标准差(±s)表示。计数资料以频数表示。术前、术后心功能比较采用配对t检验。以P<0.05为差异有统计学意义。
2 结果
2. 1 患儿基线资料及介入封堵相关资料
12例患儿中男性4例,女性8例;年龄(3.7±1.5)岁;身高(103.1±13.9)cm;体重(16.4±5.4)kg。12例患儿均为单纯PDA,无其他合并心血管畸形,均经超声心动图明确诊断,2例患儿(病例1、病例3)为外院封堵未成功的病例,临床及术中资料见表1。
2. 2 介入封堵结果
术中12 例患儿造影测量P D A 最窄处直径(0.8±0.1)mm, PDA长度(17.1±6.1)mm。PDA按照Krichenko分型均为C型(长管型)。
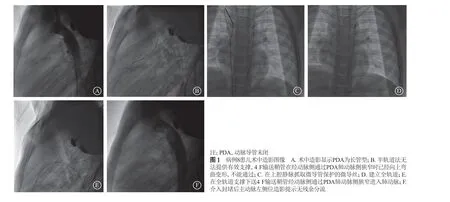
12例患儿全部封堵成功,技术成功率12/12。共释放ADO Ⅱ封堵器12枚,其中3 mm×4 mm 6枚,3 mm×6 mm 6枚。采用穿刺股动脉、股静脉建立全轨道法经股静脉入径顺行介入封堵1例,经股动脉入径逆行介入封堵5例;采用穿刺股动脉建立半轨道法经股动脉入径逆行介入封堵6例。12例术后即刻全部无残余分流,即刻完全封堵率达12/12。病例8患儿的术中造影图像见图1。
2. 3 随访结果
术后24 h、1个月、3个月、6个月复查超声心动图、心电图、X线胸片,均无残余分流,未发生封堵器移位及其他并发症。超声心动图评估显示,封堵术前与封堵术后左心室舒张末期内径[(32.1±4.1)mm比(32.5±4.4)mm,t= - 0.375,P=0.715]、左心房前后径[(19.2±3.0)mm比(20.4±2.9)mm,t= - 1.529,P=0.155]、左心室射血分数[(70.4±3.4)%比(69.4±4.1)%,t=0.588,P=0.569]比较,差异均无统计学意义。
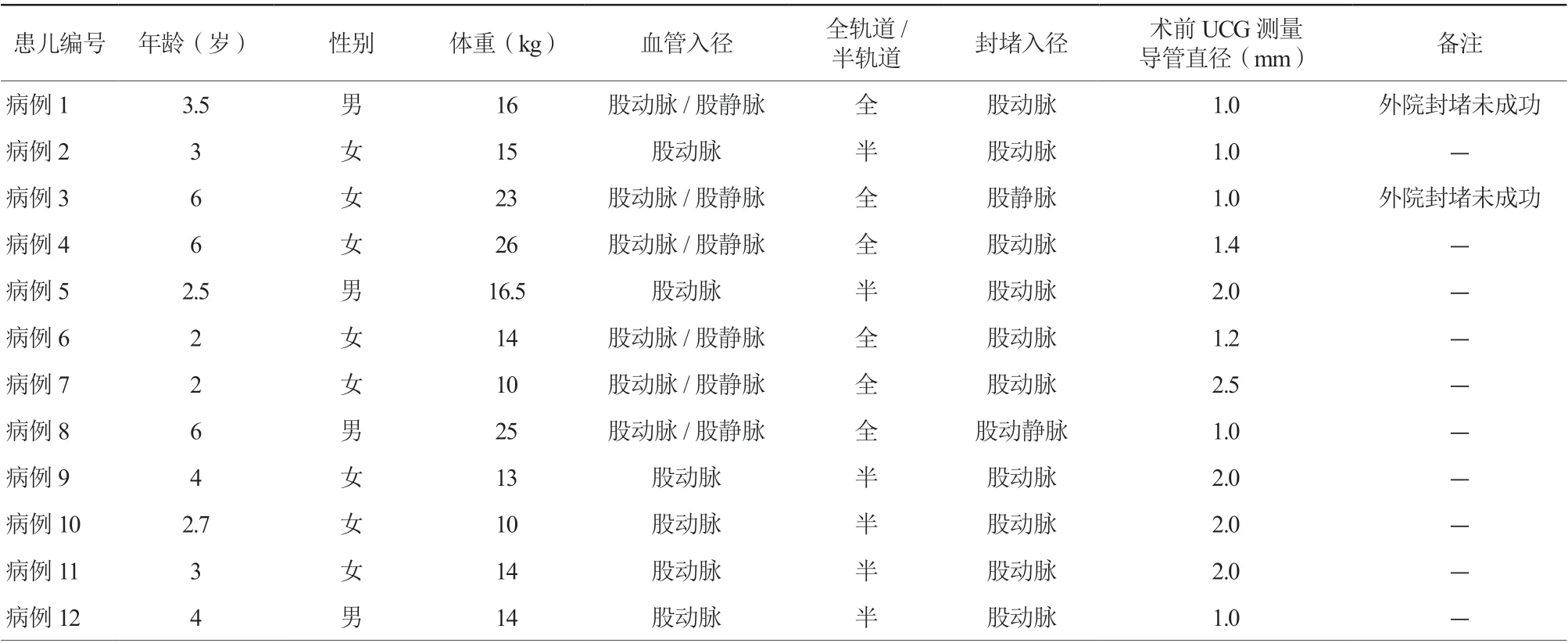
表1 患儿介入封堵相关资料
3 讨论
IE是PDA患儿的主要不良结局之一。早年文献报道PDA患儿每年IE的发生率为0.14%~0.45%[3-4],近期流行病学统计数据报道正常儿童IE的发生率约为0.43/100 000[5],可见PDA患儿IE的发生率较正常儿童高。细小PDA一般指左向右分流量较小,没有明显血流动力学意义,心脏负荷无明显增加的PDA[6]。临床上习惯将最窄处直径<1 mm的PDA定义为极细小PDA。细小PDA患儿每年IE的发生率约为0.01%[6],虽然发生率较低,但一旦发生IE死亡率约为2.8%[5],并且有学者认为IE的发生率与PDA大小可能无关,仅与PDA存在与否相关[7]。
细小PDA临床听诊可无杂音,临床上又称为“沉默”型PDA,此类型也存在发生IE的风险,临床报道并不少见[8-9]。现今关于细小PDA是否应进行介入封堵仍存在争议[10-11]。美国心脏协会的相关指南建议对患儿细小PDA行介入封堵(Ⅱb类推荐)[12]。有学者认为无论PDA大小,都应该早发现早治疗,以预防IE的发生[11]。笔者认为,如果介入封堵治疗技术安全有效,细小PDA也应该早发现早治疗。随着介入封堵技术及器械的发展,尤其是弹簧圈及ADO系列封堵器的临床应用,对于细小PDA行介入封堵已十分安全、成熟。ADO Ⅱ是封堵长管型PDA最佳器械之一,已经广泛应用于国内外,并且封堵效果良好[13-14]。
对于极细小PDA的介入封堵治疗,既往采用的方法都有不足之处。(1)Cook可控弹簧圈法:存在残余分流、弹簧圈移位、异位栓塞等问题,且普通弹簧丝直径0.035 in,对泥鳅导丝不能通过的极细小PDA就不能用这种方法进行封堵[2]。(2)诱导血栓形成法:即将4~5 F导管头端插入PDA内,阻断血流,诱导PDA内血栓形成。这种方法疗效不确定,远期有再通的风险[15]。
本研究所涉及12例患儿PDA直径造影测量均小于1 mm,原来对此类极细小PDA处理方法为先尝试用直径0.035 in普通泥鳅导丝通过PDA,但如果导丝通过失败就无法置入输送鞘管,只能放弃封堵。另外如果泥鳅导丝通过失败,普通Cook可控弹簧圈同样也无法通过,无法完成封堵。有学者尝试采用4 F或5 F导管堵塞PDA口部,诱导PDA内血栓形成,但该方法疗效不定,可能再通。针对以上问题我们采用了冠状动脉介入治疗所使用的BMW微导丝(直径0.356 mm)和1.9~2.4 F微导管(外径为0.627~0.792 mm),微导丝微导管可顺利通过直径<1 mm的PDA。但操作时需要注意几点:(1)建轨道时,微导丝必须要有微导管在外保护,否则微导丝的切割效应容易损伤心脏或瓣膜,特别是在建立轨道时;(2)微导丝微导管依次送入4 F输送鞘管内,建立轨道后4 F输送鞘管直接通过PDA;(3)操作务必轻柔,切忌使用暴力通过PDA,以免造成PDA断裂出血,尤其是PDA最窄部,需要建立半轨道或全轨道增加支撑力,4 F输送鞘管才能通过。
本研究所针对的均为患儿PDA,经介入封堵后可降低患儿IE的发生率,解决部分家长的心理顾虑。本研究初步表明,该技术安全可靠,可完成绝大部分极细小PDA的介入封堵治疗,值得进一步临床推广。
