肺腺癌中关键RNA结合蛋白预后评估模型的构建*
2021-04-28杨文娟马青梅马梦婷刘欣跃
杨文娟,马青梅,马 莉,马梦婷,张 倩,刘欣跃
兰州大学第二医院检验医学中心,甘肃兰州 730030
肺癌的发病率居各大癌症之首,也是引起癌症患者死亡的主要原因[1]。据世界卫生组织报道,2018年肺癌发病和死亡人数分别为210万例、180万例,肺腺癌占所有肺癌的40%~55%,发病率逐年上升[2]。目前,尚缺乏对肺腺癌进行有效诊断和预后评估的分子标志物,导致大多数患者临床确诊时已处于晚期且5年生存率较低。因此,迫切需要分析肺腺癌预后的风险因素,以及确定肺腺癌的预后分子标志物。
RNA结合蛋白(RBPs)是一类具有RNA结合域的蛋白总称,包括信使RNA(mRNA)、长链非编码RNA(lncRNAs)、微小RNA(miRNAs)和核糖体RNA(rRNAs)等,参与剪接、修饰、转运、定位和翻译等一系列生物学过程。此外,RBPs在维持细胞生理稳态,尤其是发育和应激反应等方面也发挥重要功能[3]。GERSTBERGER等[4]已筛选出1 542种RBPs,然而目前仅有少数研究探讨了RBPs的生物学功能及致病机制。研究报道称大多数肿瘤中均有RBPs表达失调的现象,可能与肿瘤的发展、迁移、预后等过程密切相关[5-6]。本文对肺腺癌患者RNA测序数据进行生物信息学分析,挖掘差异表达RBPs,探讨RBPs对肺腺癌患者生存预后的影响。
1 资料与方法
1.1一般资料 从癌症基因组图谱(TCGA)数据库中下载526例肺腺癌组织和59例正常组织的RNA测序数据。为了扩大正常组织的样本数,下载基因型-组织表达(GTEx)数据库中288例正常组织的RNA测序数据。以上TCGA和GTEx数据库中肺腺癌和正常组织的测序数据均来自UCSC数据库(https://xenabrowser.net/datapages/)。
1.2GO功能注释和京都基因与基因组百科全书(KEGG)富集分析 为了明确差异表达RBPs在肺腺癌发生发展中的作用,使用R软件Clusterprofiler包对差异表达RBPs进行功能富集分析,包括GO功能注释[生物学过程、细胞学组分(CC)和分子生物学功能(MF)]和KEGG通路富集(BP)分析。
1.3生存分析 收集从UCSC数据库中下载的500例肺腺癌患者的临床信息,采用Perl软件合并肺腺癌患者差异表达RBPs的表达和生存数据。通过单因素和多因素Cox回归分析筛选关键RBPs。根据风险评估公式:风险评分=Exp1×Coe1+Exp2×Coe2+Expi×Coei(i、Exp和Coe分别表示关键RBPs的数目、表达值和系数值),建立关键RBPs生存分析的预后模型。R软件将关键RBPs的表达及生存数据随机分为试验组(252例)和验证组(248例),根据风险评分分为高风险组和低风险组,并绘制受试者工作特征曲线(ROC曲线),计算曲线下面积(AUC)。此外,绘制验证组关键RBPs的ROC曲线并计算AUC值,对试验组风险评估模型进行验证。
1.4关键RBPs筛选和验证 采用Kaplan Meier-plotter数据库(https://kmplot.com/analysis/)验证关键RBPs对肺腺癌预后总生存期(OS)的影响;采用人类蛋白质图谱(HPA)数据库(https://www.proteinatlas.org/)对关键RBPs在肺腺癌中的表达进行验证,进一步验证构建预后模型的有效性。
1.5统计学处理 采用Perl软件对下载的肺腺癌和正常组织的RNA测序数据进行整理及合并,得到基因表达矩阵文件。根据已知的1 542个RBPs列表,用R软件(3.6.1)获取肺腺癌及正常组织中RBPs的表达矩阵。以|log2FC|>1且错误发现率<0.05为标准,R软件Limma包筛选肺腺癌和正常组织中差异表达RBPs,Ggplot2包绘制差异表达RBPs的表达分布图。
2 结 果
2.1肺腺癌中差异表达RBPs的筛选和富集分析 本研究共纳入526例肺腺癌组织、347例正常组织的RNA测序数据。按照|log2FC|>1且错误发现率<0.05的标准,用R软件Limma包筛选出375个差异表达RBPs。差异表达RBPs的GO分析结果表明,差异表达RBPs主要参与RNA代谢、lncRNA的代谢过程和RNA剪切等BP;MF主要为RNA的催化活性、核糖体结构组成部分和核糖核酸酶活性;核糖体、线粒体基质和核糖体亚单位等的CC。此外,差异表达RBPs参与核糖体、mRNA的监控通路、RNA的转录和剪切体等KEGG通路。见表1。
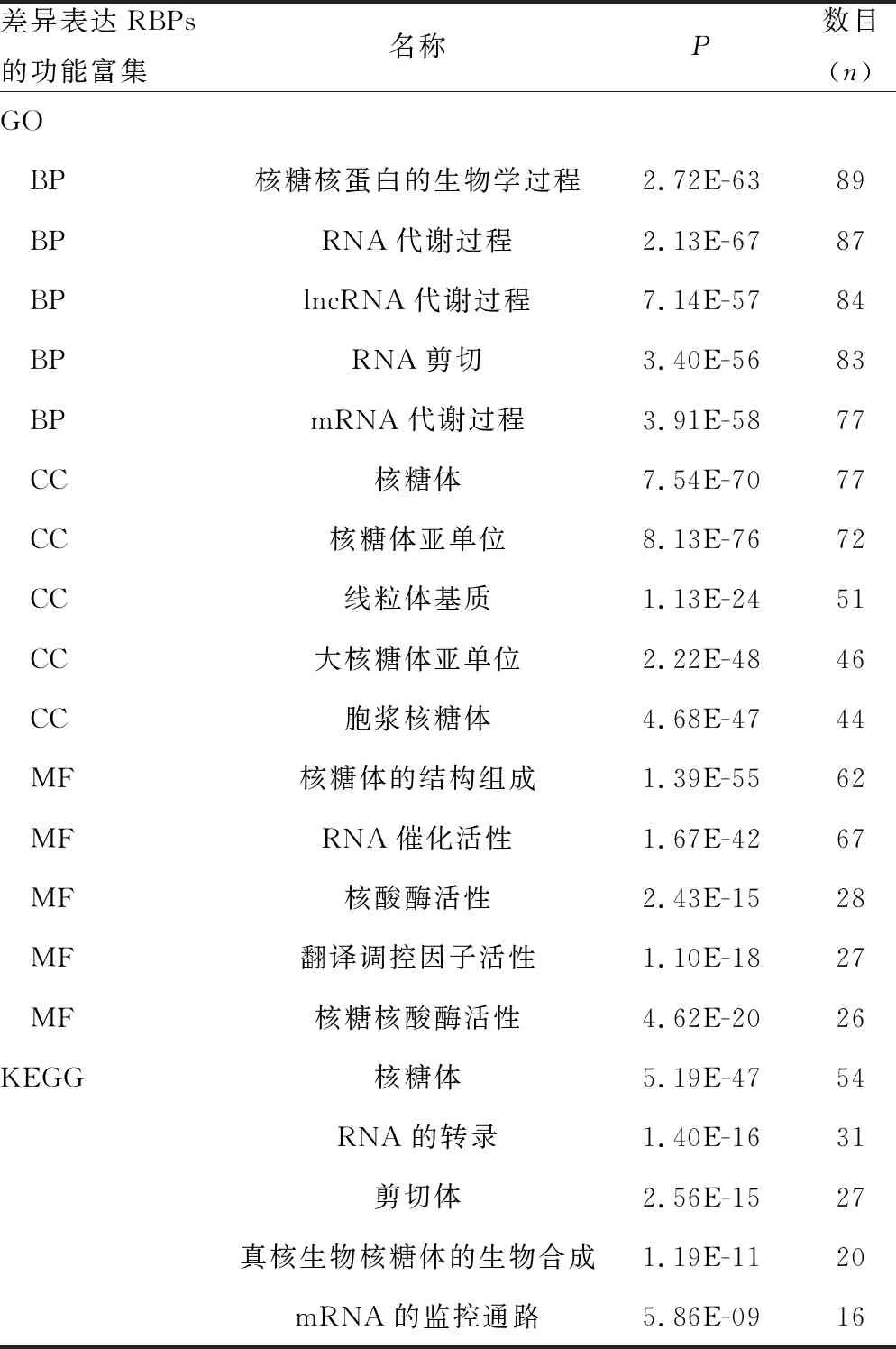
表1 差异RBPs的功能富集表
2.2生存预后模型的构建 对375个差异表达RBPs进行单因素Cox回归分析,获得26个RBPs。对上述26个RBPs进行多因素Cox回归分析,得到8个关键RBPs(WDR3、SMG9、DARS2、CARHSP1、LARP6、GAR1、INTS7和EXO1),它们是影响肺腺癌患者OS的独立预后因素。将包含8个关键RBPs的表达及生存数据的肺腺癌患者,随机分为试验组和验证组。按照风险评估公式:风险评分=(0.696×WDR3)+(0.764×SMG9)+(0.591×DARS2)+(0.675×CARHSP1)+(0.301×LARP6)+(0.526×GAR1)+(0.498×INTS7)+(-354×EXO1),建立肺腺癌患者生存预后的风险评估模型。在试验组中,8个关键RBPs的风险评分模型的AUC为0.761,且高风险肺腺癌患者的OS较低风险者短,表明该模型对肺腺癌患者OS可进行良好的预测。在验证组中,高风险肺腺癌患者OS较低风险者短,AUC为0.666。本研究成功构建了具有较高的灵敏度和特异度的肺腺癌RBPs预后评估模型,见表2、图1~2。

表2 多因素Cox回归分析筛选关键RBPs

注:A为高、低风险患者的生存曲线图;B为风险评分的OS的ROC曲线图;C为风险评分分布图:D为生存状态图。

注:A为高、低风险患者的生存曲线图;B为风险评分的OS的ROC曲线图;C为风险评分分布图:D为生存状态图。
2.3关键RBPs的列线图 为了定量预测肺腺癌患者1、3、5年的生存率,构建8个关键RBPs的列线图。在总点轴和各基因预后轴之间画1条垂直线,进而估算1、3和5年的生存率,为肺腺癌患者的临床决策提供依据。见图3。
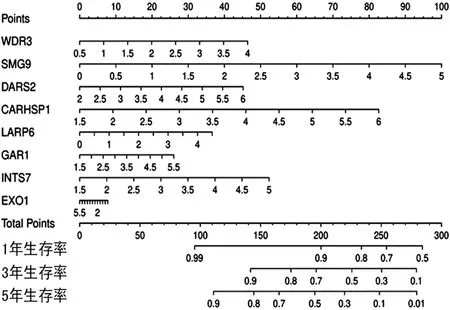
图3 预测肺腺癌患者1、3、5年总体生存时间的列线图
2.4关键RBPs的预后和表达验证 通过Kaplan Meier-plotter数据库明确肺腺癌患者中8个预后关键RBPs与OS的关系,发现高表达WDR3、DARS2、CARHSP1、LARP6、GAR1、INTS7和EXO1基因的肺腺癌患者预后更差(P<0.05);而SMG9对预后OS的影响无统计学意义(P>0.05)。为了进一步明确上述关键RBPs在肺腺癌中的表达情况,HPA数据库免疫组化结果表明在肺癌组织中SMG9、DARS2、CARHSP1、LARP6、GAR1基因表达较正常组织高。然而,HPA数据库尚缺乏WDR3、INTS7和EXO1基因的免疫组化表达数据。见图4、5。
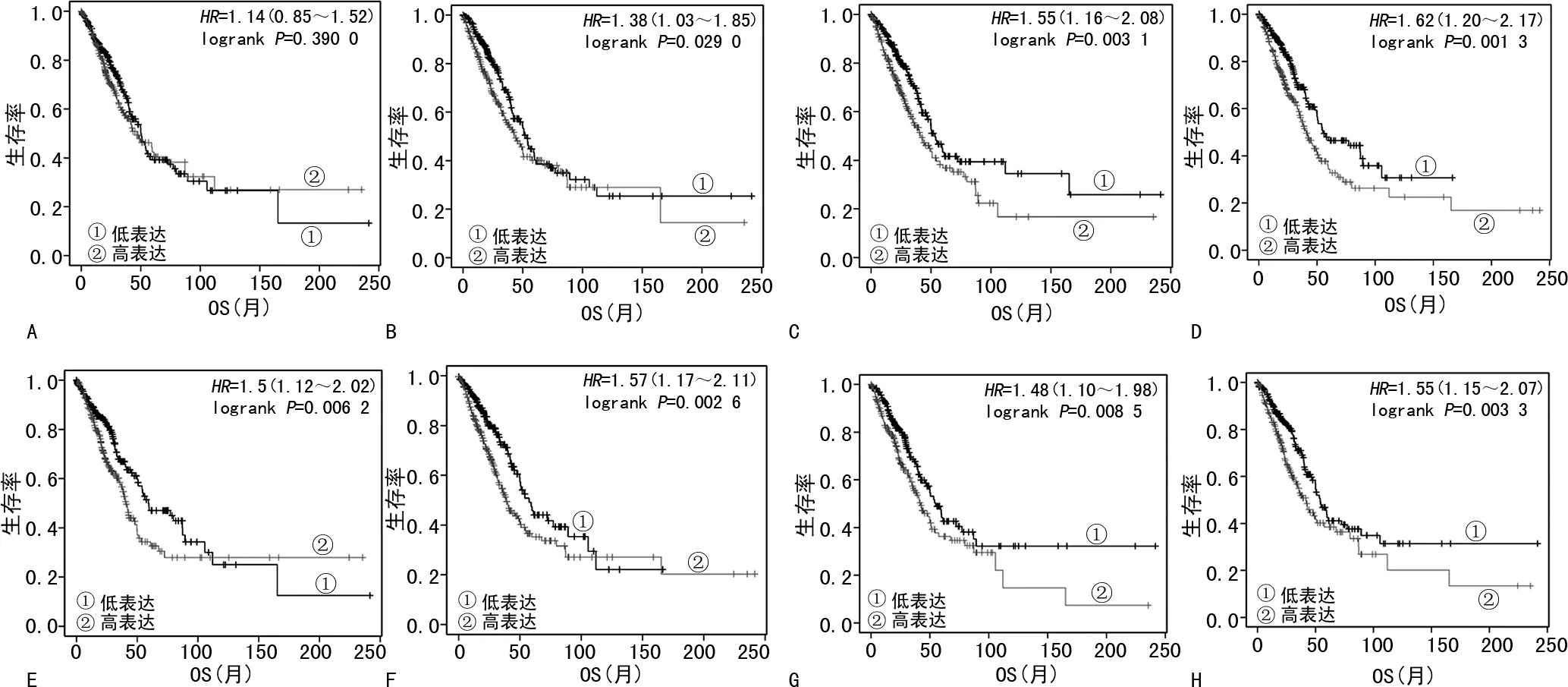
注:A~H分别为SMG9、WDR3、DARS2、CARHSP1、LARP6、GAR1、INTS7、EXO1高表达者和低表达者Kaplan Meier生存分析图。

注:A为SMG9基因在正常组织中低表达;B为SMG9基因在肺腺癌组织高表达;C为DARS2基因在正常组织未检测到;D为DARS2基因在肺腺癌组织高表达;E为CARHSP1基因在正常组织低表达;F为CARHSP1基因在肺腺癌组织中度表达;G为GAR1基因在正常组织高表达(25%~75%);H为GAR1基因在肺腺癌组织高表达(>75%);I为LARP6基因在正常组织低表达;J为LARP6基因在肺腺癌组织高表达。
3 讨 论
本研究从UCSC数据库中下载肺腺癌和正常组织的RNA测序数据,R软件筛选差异表达的RBPs,获得375个差异表达RBPs。通过单因素和多因素Cox回归分析得到8个关键RBPs,成功构建了肺腺癌患者RBP预后风险评估模型,且验证组结果表明该模型具有较好的预后预测意义;构建的列线图进一步直观定量地描述了肺腺癌患者1、3、5年生存率。Kaplan Meier-plotter数据库表明WDR3、DARS2、CARHSP1、LARP6、GAR1、INTS7和EXO1 7个关键RBPs高表达的肺腺癌患者的总体生存率较低表达患者低。使用HPA数据库验证SMG9、DARS2、CARHSP1、LARP6、GAR1等基因在肺癌组织中高表达,与本研究所得结果一致。上述结论均表明,本研究建立的关键RBPs预后评估模型,对肺腺癌患者调整治疗策略、预后标志物的探索有一定的意义。
目前,已有研究者对预后关键RBPs在肿瘤中的作用展开了多项研究。在西班牙人群中展开的研究发现WDR3基因可增加甲状腺癌的风险,且在甲状腺癌细胞中WDR3表达上调[7]。研究表明DARS2基因可延长肝细胞肝癌的细胞周期并抑制肝细胞肝癌细胞的凋亡[8];DARS2也参与膀胱癌的发生、发展和转移等过程[9]。胡仁旺等[10]发现LARP6的异常表达可影响胃癌患者的OS和无进展生存期。研究表明GAR1在胃癌组织中尚无表达差异,而在结肠癌组织中表达上调,可能在结肠癌的发生发展中起着重要作用[11]。INTS7在转录调控中起着重要作用,且具有高度突变性。前列腺癌的侵袭性与INST7的过表达有关[12];INTST7被证实在胃癌、膀胱癌和肺腺癌中均为过表达[13]。EXO1基因异常表达可能影响前列腺癌患者的预后生存及进展[14];ZHENG等[15]发现,乳腺癌患者OS较短,与EXO1基因的表达上调有关。不同肿瘤细胞的增殖、侵袭及肿瘤患者的预后与关键RBPs的异常表达有关,未来可通过干扰上述RBPs的表达,改善肺腺癌患者的预后生存情况。
综上所述,本研究成功构建了肺腺癌关键RBPs预后评估模型,为进一步探索RBPs对肺腺癌的影响提供了新思路,有助于临床开发新的靶向治疗药物,预测患者预后生存时间。然而,本研究尚存在一定的局限性,仍需要大量测序数据及相应的前瞻性临床试验进一步验证。
