复方斑蝥胶囊联合经导管肝动脉化疗栓塞术治疗肝细胞癌疗效及安全性评价*
2021-02-24蒋洪春谭盛葵
唐 芬,蒋洪春,谭盛葵
(1.广西壮族自治区南溪山医院,广西 桂林 541002;2.桂林医学院,广西 桂林 541010)
肝细胞癌(HCC)为原发性肝癌的主要病理类型,占85% ~90%[1],发病症状不典型且隐匿,肿瘤恶性程度高,增殖速度快,浸润性较强,侵犯范围广,病程短,且病死率和术后复发率高,严重威胁患者的生命安全[1]。目前,临床治疗HCC仍以手术切除为主,但超过70%的患者确诊时已为中晚期,手术疗效不佳,加之HCC患者对放射治疗(简称放疗)、化学治疗(简称化疗)的敏感性差,且存在诸多药品不良反应,极易产生耐药性[2]。经导管肝动脉化疗栓塞术(TACE)是公认的治疗中晚期HCC的首选治疗策略,通过栓塞剂阻断病灶供血动脉,促使肿瘤细胞缺血性死亡,从而缓解病情,延长患者生存时间[3]。斑蝥素可通过对脱氧核糖核酸(DNA)和核糖核酸(RNA)的合成产生阻碍效应,并高度亲和肝癌细胞,促使其有效凋亡,能明显改善TACE术后的肝功能损伤,且无明显骨髓抑制作用,安全性良好[4]。作为纯中药制剂的复方斑蝥胶囊,有破血除瘀、攻毒蚀疮功效,在肝癌、直肠癌、妇科恶性肿瘤及肺癌治疗中广泛应用,能延缓肿瘤进展[5]。本研究中探讨了TACE术联合复方斑蝥胶囊治疗HCC的疗效,以及对血清肿瘤标志物、血管新生指标、药物安全性和生存率的影响。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:参照《内科学》中HCC的诊断标准[6],且经影像学手段、血清甲胎蛋白测定及病理学检查确诊;至少有1个可测量病灶;经评估不具有手术指征;巴塞罗那分期(BCLC)为B~C级;经肝功能Child-Pugh分级为A~B级;经美国东部肿瘤协作组(ECOG)评分低于3分;年龄35~70岁;预计生存期大于3个月。本研究经广西壮族自治区南溪山医院医学伦理委员会批准,患者签署知情同意书。
排除标准:3个月内进行介入治疗或其他相关治疗;对本研究中的治疗方案存在禁忌证;凝血功能障碍;肝肾功能障碍;存在出血倾向;妊娠期和哺乳期。
病例选择与分组:选取广西壮族自治区南溪山医院2015年3月至2018年3月收治的HCC患者122例,按随机数字表法分为对照组和观察组,各61例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。详见表1。
1.2 方法
对照组患者予TACE治疗,利用经皮穿刺导丝引入导管技术(Seldinger技术),经皮股动脉穿刺介入手术,向肿瘤供血动脉缓慢注入混合药物[注射用洛铂(海南长安国际制药有限公司,国药准字H20050308,规格为每瓶以无水物计50 mg)30~50 mg+注射用吡柔比星(深圳万乐药业有限公司,国药准字H10930105,规格为每支按C32H37NO12计10 mg)30~50 mg],具体药物剂量根据瘤体直径、肿瘤染色情况及患者耐受性调整,注射完毕,合并有(门)动静脉瘘者,瘘口用明胶海绵颗粒(和)或无水乙醇补充栓塞,再行碘油栓塞治疗。观察组患者在此基础上加用复方斑蝥胶囊(贵州益佰制药股份有限公司,国药准字Z52020238,规格为每粒0.25 g)治疗,于TACE手术当天口服0.75 g,每日2次,连续服用12周。治疗过程中,经影像学复诊,若发现新病灶或残存病灶间隔1个月以上,则再次进行TACE治疗。
1.3 观察指标与疗效判定标准
疗效判定[7]:按实体瘤疗效评价标准,分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)4个等级。CR,经影像学检查显示所有病灶动脉期强化消失,持续至少4周,无新病灶出现;PR,全部存活肿瘤最大径总和缩小≥50%,持续至少4周,无新病灶出现;SD,全部存活肿瘤最大径总和缩小<50%或增大25%;PD,全部存活肿瘤最大径总和增大≥25%,有新病灶出现。客观缓解(ORR)=CR+PR,疾病控制(DCR)=CR+PR+SD。
血清生化指标:分别于治疗前及治疗4周后采集患者空腹静脉血各5 mL,室温静置30 min,离心(3 000 r/min)10 min,分离血清,冷藏于-80℃冰柜中备检。采用酶联免疫吸附试验(ELISA)测定血清甲胎蛋白(AFP)、癌胚抗原(CEA)、糖类抗原 19-9(CA19-9)、糖类抗原 125(CA125)、血管内皮生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)及血小板内皮细胞黏附分子 -1(PCEAM-1)水平。
不良反应[8]:统计患者治疗期间不良反应发生情况。
随访生存分析:随访3年,记录术后1,2,3年的无瘤生存率。
1.4 统计学处理

表1 两组患者一般资料比较(n=61)Tab.1 Comparison of the patients′general data between the two groups(n=61)
2 结果
结果见表2至表5。两组患者均获得随访,截止随访时间为术后6~36个月,随访中位时间为18个月。观察组术后1,2,3年的无瘤生存率分别为85.25%(52/61),73.77% (45/61),62.30% (38/61);对 照 组 分 别 为78.69% (48/61),68.85% (42/61),57.38% (35/61)。组间比较,差异无统计学意义(P>0.05)。

表2 两组患者临床疗效比较[例(%),n=61]Tab.2 Comparison of clinical efficacy between the two groups[case(%),n=61]
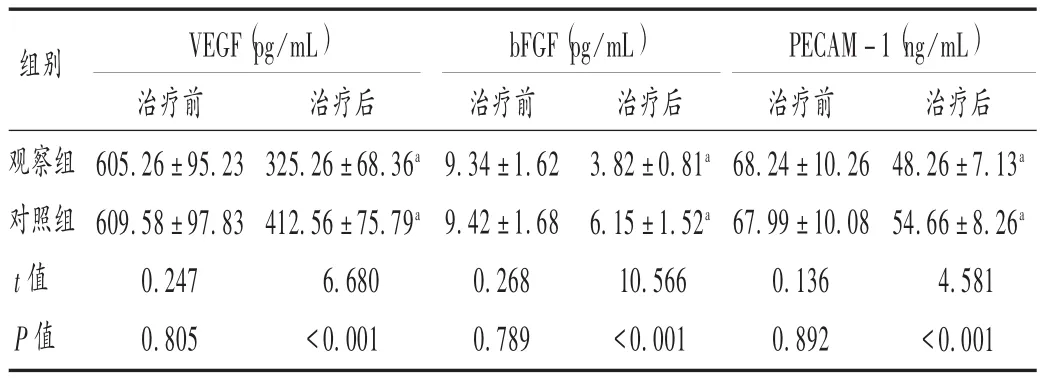
表3 两组患者血清VEGF,bFGF,PECAM-1水平比较[例(%),n=61]Tab.3 Comparison of serum VEGF,bFGF and PECAM-1 levels between the two groups[case(%),n=61]

表4 两组患者药品不良反应发生情况比较[例(%),n=61]Tab.4 Comparison of incidence of adverse drug reactions between the two groups[case(%),n=61]
3 讨论
对于HCC,目前国内外治疗均采用BCLC分期标准合理运用局部治疗联合全身治疗策略,以期最大程度提高疗效[9]。TACE虽是中晚期HCC的首选治疗方式,但无法彻底栓塞肿瘤的供血动脉,临床肿瘤病灶完全坏死率相对偏低。TACE术后栓塞的肿瘤组织周围缺氧细胞能产生多种生长因子,可促进肿瘤癌细胞的生长和转移,是造成TACE术后复发及转移的主要原因[10]。
中医辨证治疗可从全方位、多靶点治疗HCC,抗肿瘤效果明确,安全性高。中医理论认为,HCC可纳入“积”“肝积”“瘕”等范畴,病因在于素体正气不足,七情伤志,饮食失调,外感邪毒六淫,聚集于五脏而俱损,气血瘀滞,痰结湿聚、热毒内蕴,而成肝积;以正气不足为本,以气滞、血瘀、痰凝、热毒为标。中医治法应以扶正祛邪、益气活血、祛痰化瘀、清热解毒为主[11]。复方斑蝥胶囊为中药复方制剂,其中斑蝥、刺五味抗癌、止痛,山茱萸、人参扶正祛邪、益气养阴,黄芩行气活血,半枝莲清热解毒,熊胆粉祛瘀解毒,莪术健脾益气,三棱补益肝肾,诸药合用,共奏扶正祛邪、补肝益肾、健脾益气、行气活血、抗炎止痛、抗肿瘤等功效[12]。
本研究结果显示,观察组ORR和DCR显著高于对照组(P<0.05)。现代药理学研究表明,斑蝥可增强机体免疫作用,并能通过刺激淋巴细胞、巨噬细胞分泌大量白细胞介素,进而使肿瘤细胞凋亡,并能抑制肿瘤血管的新生,继而降低蛋白质合成浓度,避免肿瘤细胞对氨基酸的过度摄取,同时,斑蝥提取物可起到阻止肿瘤转移、抗氧化作用,能有效修复机体损伤,减轻不良反应;女贞子、刺五味可对机体起修复和保护作用,减轻化疗不良反应,增强机体免疫功能;半枝莲有明显抗肿瘤、抗氧化、抑制肿瘤增殖及诱导其凋亡等功效;人参不仅能阻碍肿瘤增殖、转移及浸润过程,还可抑制肿瘤血管新生,增强机体抗肿瘤能力;全方能通过影响肿瘤细胞分裂周期酶对肿瘤细胞的凋亡起到抑制作用,并能阻碍肿瘤血管新生,破坏肿瘤细胞骨架,且能明显减轻胃肠道反应,刺激骨髓细胞DNA合成,增强骨髓细胞的增殖活性[13]。
表5 两组患者治疗前后血清肿瘤标志物水平比较(±s,n=61)Tab.5 Comparison of serum tumor markers levels before and after treatment between the two groups(±s,n=61)

表5 两组患者治疗前后血清肿瘤标志物水平比较(±s,n=61)Tab.5 Comparison of serum tumor markers levels before and after treatment between the two groups(±s,n=61)
组别AFP(ng/mL) CEA(μg/L) CA19-9(U/mL) CA125(U/mL)观察组对照组t值P值治疗前564.26±86.23 571.64±89.18 0.465 0.643治疗后85.26±12.26a 123.15±34.68a 8.045<0.001治疗前4.23±0.58 4.36±0.61 1.206 0.230治疗后2.08±0.35a 2.83±0.41a 10.866<0.001治疗前73.26±12.66 74.31±12.59 0.459 0.647治疗后28.66±5.26a 38.79±6.89a 9.127<0.001治疗前84.26±16.23 84.79±15.89 0.182 0.856治疗后30.26±5.18a 39.26±6.82a 8.208<0.001
血清肿瘤标志物是肝癌筛查、早期预测术后复发的有效指标,AFP,CEA,CA19-9,CA125 等指标已广泛应用于肝癌筛查[14]。本研究中加用复方斑蝥胶囊治疗后,HCC 患者的 AFP,CEA,CA19-9,CA125水平均下降,且观察组下降幅度显著大于对照组(P>0.05)。可见,联合治疗策略能通过抑制血清肿瘤标志物水平延缓病情进展,减少术后复发风险。观察组患者的血清VEGF,bFGF,PECAM-1水平与治疗前相比受到明显抑制,且上述新生血管指标水平均低于对照组(P<0.05)。王霞等[15]检测肝细胞癌灶和外周血的VEGF水平发现,VEGF高水平时,肝内转移能力提高,微转移灶形成加快,可作为预测肝癌转移的特异性血清生化标志物;bFGF对内皮细胞有丝分裂、细胞外基质降解和诱导内皮细胞脱离基质向肿瘤区转移均有促进效应。HCC属典型的多血供肿瘤,VEGF阳性表达过多,则bFGF表达也相应增多[16]。周焕城等[17]研究发现,PECAM-1参与肝癌发病过程,其高水平表达可能对肝癌细胞中的信号途径起到调控作用,进而影响肝癌细胞的侵袭、繁殖能力。本研究结果表明,复方斑蝥胶囊可能通过下调VEGF,bFGF,PECAM-1等新生血管指标水平以抑制肝癌细胞的侵袭、繁殖能力,达到延缓病情进展的目的。
由表4可知,加用复方斑蝥胶囊治疗能明显减少HCC患者TACE术后的不良反应,提示本品用药安全性良好。王涛等[18]报道,加用复方斑蝥胶囊治疗癌症能有效改善患者消化道不良反应、血液系统毒性和肝肾功毒性,与本研究结果一致。分析两组患者治疗后1,2,3年的无瘤生存率发现,TACE联合复方斑蝥胶囊治疗并未提高治疗后1,2,3年的无瘤生存率。CHAO等[19]研究发现,TACE联合复方斑蝥胶囊治疗BLCL B级患者,能明显延长中位生存期,延缓疾病进展时间。本研究中,联合治疗方案并未提高治疗后1,2,3年的无瘤生存率。其原因可能与本研究中纳入样本量不足和随访时间不够长有关,故临床仍需开展大样本量、长期随访观察研究,以期进一步验证本研究中的结论。
综上所述,TACE联合复方斑蝥胶囊治疗HCC疗效确切,能明显抑制血清肿瘤标志物及肿瘤血管新生,降低肿瘤细胞的增殖、侵袭及转移能力,延缓病情进展,安全性高。
