小红蒜总萘醌质量标准的研究
2020-12-13郭朋程陈婕妤刘思雨叶祥睿邱明丰
郭朋程,陈婕妤,刘思雨,叶祥睿,苏 靖,邱明丰
(上海交通大学药学院,上海 200240)
冠心病发病率及危险因素水平逐年上升,并日趋年轻化,已经成为“人类健康第一杀手” 的心血管疾病。傣药小红蒜又名红葱、红葱头、百步还阳,其性凉,味苦,有活血散瘀、消肿止痛、止血、清热解毒、利尿除湿之功效[1-3],是傣医治疗冠心病的主要药物,分布于我国海南、广西、云南等省[4-5]。现代研究表明,小红蒜主要有效成分为萘醌衍生物[6-9],其醇提物中的总萘醌能显著增加冠状动脉血流量,直接舒张血管,抑制苯肾上腺素和氯化钾对血管环的预收缩作用[10-12],以异红葱乙素、红葱乙素、红葱甲素为主。因此,本实验在前期工艺基础上制备小红蒜总萘醌,并在性状、检查、定性鉴别、定量测定等方面进行研究,以期为该药材质量标准的制定和相关制剂的研发奠定基础[13]。
1 材料
MiniQ超纯水机(美国Millipore公司);UV-759紫外可见分光光度计(上海奥谱勒仪器有限公司);Agilent 1200高效液相色谱仪(美国Agilent公司);硅胶GF254薄层层析预制板(青岛海洋化工厂分厂);ZF-20D暗箱三用紫外分析仪(上海骥辉科学分析仪器有限公司);KQ-250DB数控超声波清洗仪(昆山超声仪器有限公司)。异红葱乙素(批号DFZY-17110)、红葱乙素(批号DFZY-17111)、红葱甲素 (批号DFZY-17112)对照品(成都瑞芬思生物科技有限公司)。小红蒜对照药材(批号20160116,西双版纳傣族自治州食品药品检验所)、原料药(批号20150909,云南金发药业有限公司)均经上海交通大学药学院王梦月副教授鉴定为鸢尾科植物红葱Eleutherine plicataHerb.的干燥鳞茎。小红蒜总萘醌 (自制,批号20190402、20190412、20190426)。甲醇、乙腈为色谱纯;其余试剂均为分析纯。
2 方法与结果
2.1 性状 本品为黄褐色粉末,气微,味苦。
2.2 TLC定性鉴别 取3批本品粉末,每批约0.02 g,精密称定,置于10 mL量瓶中,甲醇定容至刻度,摇匀,即得供试品溶液;取对照药材适量,粉碎后过60目筛,取粉末约0.5 g至10 mL量瓶中,甲醇定容至刻度,超声30 min,冷却至室温后甲醇定容至刻度,摇匀,滤过,取续滤液,即得对照药材溶液;取异红葱乙素、红葱乙素、红葱甲素对照品各约10 mg,精密称定,置于同一10 mL量瓶中,甲醇定容至刻度,摇匀,即得对照品溶液。
方法1:取对照品溶液约5 μL、对照药材及3批供试品溶液各约10 μL,点于同一硅胶GF254薄层板上,以环己烷-甲苯-乙酸乙酯-甲酸(5 ∶5 ∶3 ∶0.1)为展开剂,展开,取出,晾干,置于紫外光灯(254 nm)下检视,结果见图1,可知供试品在对照品相应位置有相同斑点。
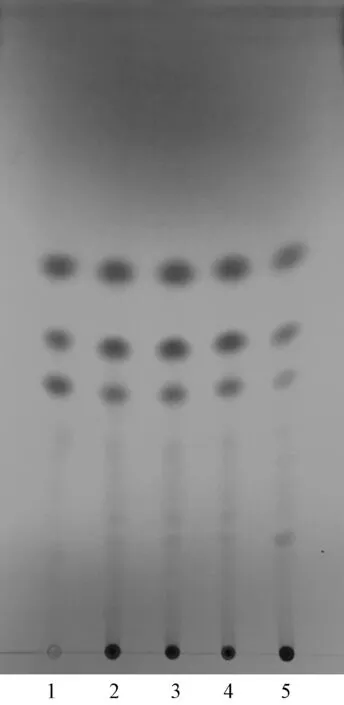
图1 小红蒜总萘醌TLC色谱图(Ⅰ)Fig.1 TLC chromatogram of total naphthoquinones in E.plicata(Ⅰ)
方法2:取对照品溶液约5 μL、对照药材及3批供试品溶液各约10 μL,点于同一硅胶GF254薄层板上,以二氯甲烷-乙酸乙酯-甲酸 (12 ∶1 ∶0.2)为展开剂,展开,取出,晾干,置于紫外光灯(254 nm)下检视,结果见图2,可知供试品在对照品相应位置有相同斑点。
综上所述,2种方法下TLC斑点均较清晰,分离度良好。
2.3 检查
2.3.1 干燥失重 取3批本品,按照2015年版《中国药典》 四部0831干燥失重测定法[14]进行测定,测得干燥失重分别为3.91%、4.03%、2.34%,均小于5%,符合相关规定。
2.3.2 水分 取3批本品,按照2015年版《中国药典》 四部0832水分检测法[14]进行测定,测得含水量分别为2.15%、3.56%、2.06%,均小于4%,符合相关规定。
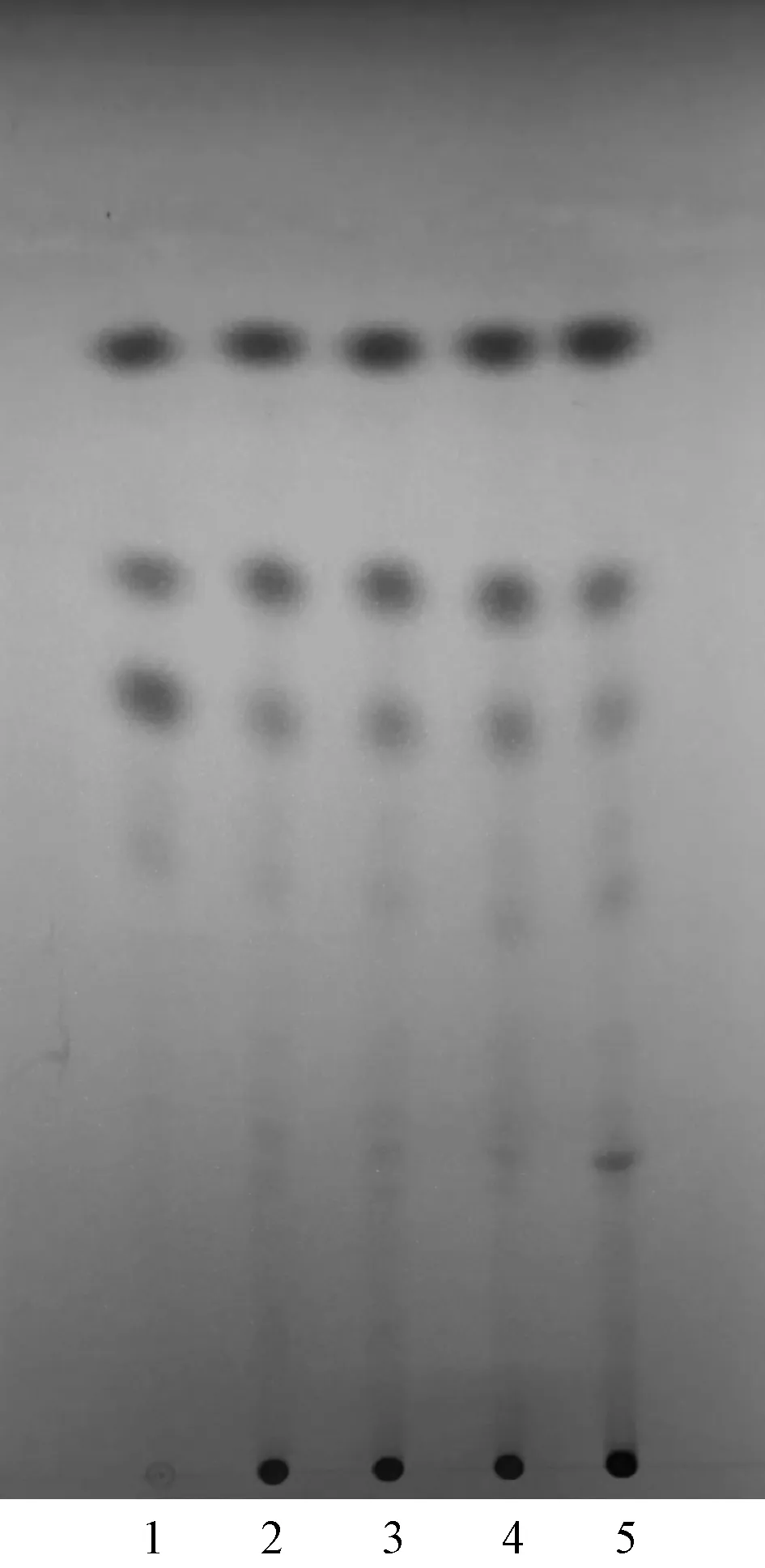
图2 小红蒜总萘醌TLC色谱图(Ⅱ)Fig.2 TLC chromatogram of total naphthoquinones in E.plicata(Ⅱ)
2.3.3 炽灼残渣 取3批本品,按照2015年版《中国药典》 四部0841炽灼残渣检查法[14]进行测定,测得炽灼残渣分别为0.15%、0.16%、0.19%,均小于0.2%,符合相关规定。
2.3.4 树脂残留物 取3批本品,按照2015年版《中国药典》 四部0861残留溶剂测定法[14]进行测定,测得苯、甲苯、二甲苯、苯乙烯质量分数均小于0.000 1%,正己烷、二乙烯苯质量分数均小于0.001%,符合相关规定。
2.4 总萘醌含有量测定
2.4.1 对照品溶液制备 精密称取异红葱乙素对照品10.0 mg,置于5 mL量瓶中,甲醇稀释至刻度,摇匀,精密吸取1 mL至25 mL量瓶中,甲醇稀释至刻度,摇匀,即得(0.08 mg/mL)。
2.4.2 供试品溶液制备 将本品研细,精密称取12.5 mg,置于25 mL量瓶中,甲醇稀释至刻度,摇匀,即得。
2.4.3 线性关系考察 取适量对照品溶液,甲醇依次稀释至1、2、4、5、8、10 μg/mL,于208 nm波长处测定吸光度。以溶液质量浓度为横坐标(X),吸光度为纵坐标(A)进行回归,得方程为A=0.101 8X+0.085 7 (r=0.999 4),在1~10 μg/mL范围内线性关系良好。
2.4.4 精密度试验 精密量取4 μg/mL对照品溶液适量,按“2.4.3” 项下方法测定吸光度6次,测得其RSD为0.31%,表明仪器精密度良好。
2.4.5 稳定性试验 精密量取供试品溶液1 mL至10 mL量瓶中,甲醇稀释至刻度,摇匀,于0、2、4、8、12 h按“2.4.3” 项下方法测定吸光度,测得其RSD为0.93%,表明溶液在12 h内稳定性良好。
2.4.6 加样回收率试验 取总萘醌含有量已知的本品6份,每份约6.0 mg,精密称定,置于25 mL量瓶中,精密加入含等量总萘醌的对照品溶液,甲醇稀释至刻度,摇匀,精密移取0.1 mL至10 mL量瓶中,按“2.4.3” 项下方法测定吸光度,计算回收率,结果见表1。
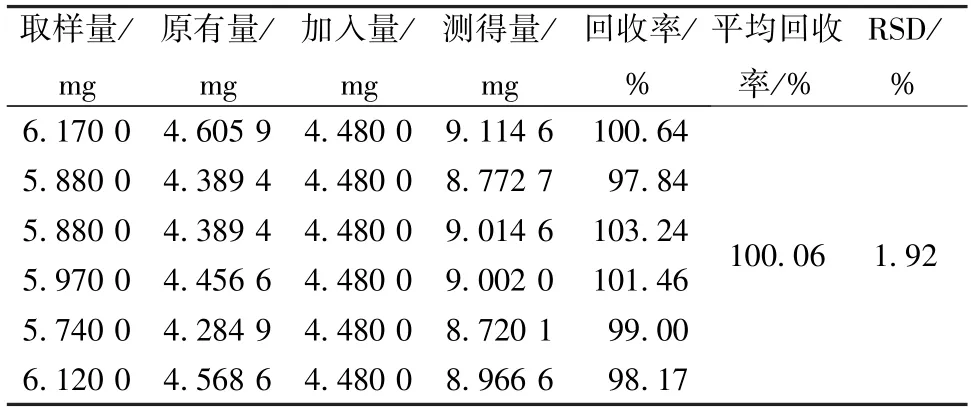
表1 总萘醌加样回收率试验结果(n=6)Tab.1 Results of recovery tests for total naphthoquinones(n=6)
2.4.7 分析结果 精密称取3批本品,按“2.4.2”项下方法制备供试品溶液,每批平行3份,分别精密量取1 mL至10 mL量瓶中,按“2.4.3” 项下方法测定吸光度,计算含有量,结果见表2。
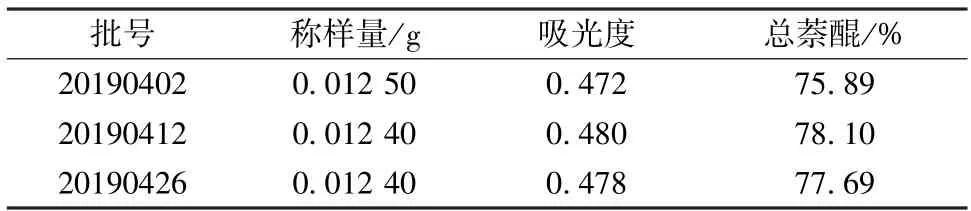
表2 总萘醌含有量测定结果(n=3)Tab.2 Results of content determination of total naphthoquinones (n=3)
2.5 异红葱乙素、红葱乙素、红葱甲素含有量测定
2.5.1 色谱条件与专属性考察 Agilent TC-C18(2)色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)-0.1% 磷酸 (B),梯度洗脱 (0~25 min,40%A;25~30 min,40%~80% A;30~35 min,80%A);体积流量1 mL/min;柱温40 ℃;检测波长254 nm;进样量10 μL,色谱图见图3。由此可知,各成分色谱峰与相邻峰的分离度均大于1.5,理论塔板数按各成分计均大于3 000,表明该方法专属性良好。积为纵坐标(Y)进行回归,结果见表3,可知各成分在各自范围内线性关系良好。

图3 各成分HPLC色谱图Fig.3 HPLC chromatograms of various constituents

表3 各成分线性关系Tab.3 Linear relationships of various constituents
2.5.2 对照品溶液制备 分别精密称取异红葱乙素、红葱乙素、红葱甲素对照品10.00、9.60、4.96 mg,置于5 mL量瓶中,甲醇稀释至刻度,振荡溶解,摇匀,分别精密吸取1、3、2 mL至10 mL量瓶中,甲醇稀释至刻度,摇匀,即得(0.200 0、0.576 0、0.198 4 mg/mL)
2.5.3 供试品溶液制备 精密称取小红蒜总萘醌对照品12.5 mg,置于25 mL量瓶中,甲醇定容至刻度,摇匀,滤过,即得。
2.5.4 线性关系考察 取对照品溶液5、2.5、1.25、0.5、0.25 mL至10 mL量瓶中,甲醇依次稀释至不同质量浓度,在“2.5.1” 项色谱条件下进样测定。以溶液质量浓度为横坐标(X),峰面
2.5.5 精密度试验 取含0.050 0 mg/mL异红葱乙素、0.144 mg/mL红葱乙素、0.049 6 mg/mL红葱甲素的对照品溶液,在“2.5.1” 项色谱条件下进样测定,测得三者峰面积RSD分别为0.73%、0.97%、0.68%,表明仪器精密度良好。
2.5.6 稳定性试验 取同一份供试品溶液,分别于0、2、4、8、12、24 h,在“2.5.1” 项色谱条件下进样测定,测得异红葱乙素、红葱乙素、红葱甲素峰面积RSD分别为1.96%、1.63%、1.73%,表明供试品溶液在24 h内稳定性良好。
2.5.7 重复性试验 取同一批本品,按“2.5.3”项下方法平行制备6份供试品溶液,在“2.5.1”项色谱条件下进样测定,测得异红葱乙素、红葱乙素、红葱甲素含有量RSD分别为1.96%、1.63%、1.73%,表明该方法重复性良好。
2.5.8 加样回收率试验 精密称取小红蒜总萘醌对照品6.0 mg,置于25 mL量瓶中,精密加入含等量异红葱乙素、红葱乙素、红葱甲素的对照品溶液,甲醇稀释至刻度,平行6份,在“2.5.1” 项色谱条件下进样测定,计算回收率,结果见表4。
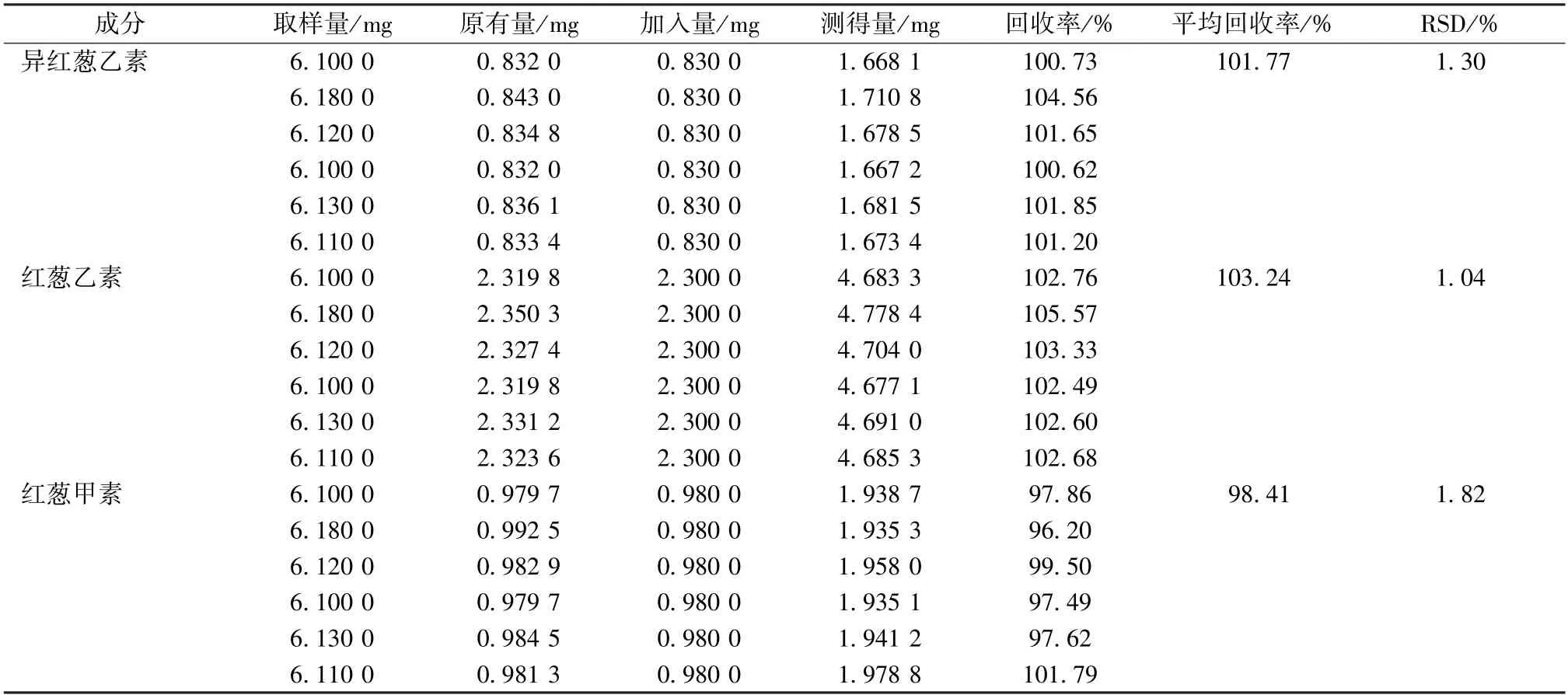
表4 异红葱乙素、红葱乙素、红葱甲素加样回收率试验结果(n=6)Tab.4 Results of recovery tests for isoeleutherin,eleutherin and eleutherol (n=6)
2.5.9 分析结果 精密称取3批本品,按“2.5.3”项下方法制备供试品溶液,每批平行3份,在“2.5.1” 项色谱条件下进样测定,计算含有量,结果见表5。

表5 异红葱乙素、红葱乙素、红葱甲素含有量测定结果(n=3)Tab.5 Results of content determination of isoeleutherin,eleutherin and eleutherol (n=3)
3 讨论
本实验根据紫外扫描情况,确定检测波长为254 nm;考察了流动相甲醇-0.1% 磷酸、乙腈-0.1%磷酸的分离效果,发现后者优于前者,并对其梯度洗脱比例进行优化。最终,确定为“2.5.1” 项下色谱条件。
小红蒜总萘醌是治疗冠心病傣药小红蒜的有效部位,主要含有异红葱乙素、红葱乙素、红葱甲素,具有巨大开发潜力。根据本实验结果,初步建议小红蒜总萘醌干燥失重不得超过5%,含水量不得超过4.0%,炽灼残渣不得超过0.2%,树脂残留物(苯、甲苯、二甲苯、苯乙烯)质量分数均不得超过0.000 1%,正己烷、二乙烯苯质量分数均不得超过0.001%,萘醌类成分质量分数不得低于70%,异红葱乙素、红葱乙素、红葱甲素总质量分数不得低于60%。
