利用酪蛋白酸钠的分子伴侣特性抑制蛋清蛋白的热聚集研究
2020-10-27何大博仝其根
何大博, 仝其根,2,*
(1.北京农学院 食品科学与工程学院, 北京 102206;2.食品质量与安全北京实验室, 北京 100022)
蛋清蛋白富含多种必需氨基酸,具有易吸收,价格低廉的特点,由于其良好的凝胶特性广泛应用于食品工业[1],但其在加热过程中极易产生聚集。在蛋白饮料的生产过程中,蛋清蛋白经过热处理后形成体积较大的聚集物,从而产生沉淀,影响产品品质,这限制了蛋清蛋白在蛋白饮料中的应用。因此,控制蛋清蛋白的热聚集具有十分重要的意义。
分子伴侣是指在特定的变性条件下可以防止蛋白质展开和聚集的一系列蛋白质[2]。分子伴侣可以与蛋白质变性之后表面暴露的疏水基团相结合[3],从而抑制蛋白质的热聚集。分子伴侣只与蛋白底物中的易优先聚集结构进行结合,并不与未变性的蛋白以及已经发生聚集的蛋白相结合[4]。其中酪蛋白及酪蛋白酸钠的分子伴侣特性已应用于食品中的多种蛋白质[5]。来源于牛乳以及骆驼乳的酪蛋白可以防止乙醇脱氢酶发生热聚集,主要是由于其较强的表面疏水性[6];κ-酪蛋白以及酪蛋白酸钠可以抑制乳清蛋白热聚集,且随着酪蛋白酸钠浓度的增加,抑制效果不断增强,聚集体的体积逐渐减小[7];β-酪蛋白可以发挥分子伴侣的作用抑制β-乳球蛋白形成不溶性聚集物[8]。酪蛋白可以抑制鸡蛋中含量较高的卵白蛋白以及卵转铁蛋白的热聚集[9-11],而蛋清蛋白为包含多种蛋白质的复杂体,对单一蛋白质的作用效果不足以证明其有效性[12-14],因此本文在前人研究的基础上采用蛋清蛋白这一复杂体作为底物,进一步证明酪蛋白酸钠对蛋清蛋白热聚集的抑制作用。
基于上述问题,1)通过测定热处理蛋白溶液的浊度以及上清液中可溶性蛋白含量,研究酪蛋白酸钠对蛋清蛋白热聚集的抑制效果;2)通过测定热处理蛋清蛋白溶液的粒径分布、分子量分布、聚集形态以及蛋清蛋白的热聚集过程,进一步对酪蛋白酸钠的分子伴侣特性进行研究。希望本研究能为酪蛋白酸钠在蛋清蛋白饮料中的应用提供理论依据,扩展蛋清蛋白在食品工业中的应用。
1 材料与方法
1.1 材料与试剂
鸡蛋,北京德青源科技股份有限公司;酪蛋白酸钠(BR),上海麦克林生化科技有限公司;BCA试剂盒(A045-3),南京建成生物工程研究所;磷酸盐缓冲液(pH=7.20,10 mol/L)、十二烷基硫酸钠,北京索莱宝科技有限公司;6×上样缓冲液,北京全式金生物科技有限公司;三羟甲基氨基甲烷(Tris)、甘氨酸,美国Novon公司;过硫酸铵、TEMED(四甲基乙二胺),美国sigma公司;丙烯酰胺、甲叉丙烯酰胺,百灵威科技有限公司。
1.2 仪器与设备
DYY-6D型电泳仪,北京六一仪器厂;T6型紫外可见光分光光度计,北京普析通用仪器有限公司;酶标仪,赛默飞世纪科技有限公司;BT-9300H型激光粒度仪,丹东百特仪器有限公司;LGJ-18型冷冻干燥机,北京松原华兴科技发展有限公司;HX-HH600A4型水浴锅,深圳市力通世纪科技有限公司;GPC-1525型凝胶色谱仪,沃特世科技有限公司;H-7500型透射电镜,日立有限公司。
1.3 实验方法
1.3.1冻干蛋清蛋白质的制备
冻干蛋清粉的制备参考文献[15]的方法。新鲜蛋清与超纯水按体积比1∶1混合,4 ℃下磁力慢速搅拌1 h;使用1 000 MW截留分子量透析膜4 ℃透析48 h,每隔12 h换水一次;8 000 r/min离心30 min除去不溶物,取上清液进行冷冻干燥;干燥的蛋清蛋白粉置于-20 ℃冰箱备用。
色谱柱:DB-5型石英毛细柱(30 m×0.25 mm,0.25 μm),J&W;升温程序:180 ℃保持1 min,以20 ℃/min升至280 ℃,保持4 min;载气(He)流速1.2 mL/min,压力2.4 kPa,进样量0.5 μL;分流比:10∶1。
1.3.2浊度的测定
将25 mg蛋清蛋白粉以及酪蛋白酸钠(5、10、15、20、25 mg)溶于5 mL磷酸盐缓冲液(pH=7.2, 0.01 mol/L),配置成不同酪蛋白酸钠添加量(1、2、3、4、5 mg/mL)的混合蛋白溶液;4 ℃放置12 h使其充分溶解。将混合蛋白溶液置于90 ℃水浴锅中加热30 min,取出后迅速放入冰水浴中,冷却至室温;使用紫外可见光分光光度计测定540 nm处蛋白溶液的吸光值。
1.3.3上清液中总蛋白含量的测定
按1.3.2方法,将25 mg蛋清蛋白粉以及酪蛋白酸钠(5、10、15、20、25 mg)溶于5 mL磷酸盐缓冲液(pH =7.2,0.01 mol/L),配置成不同酪蛋白酸钠添加量的混合蛋白溶液,4 ℃放置12 h使其充分溶解。将蛋白溶液置于90 ℃水浴锅中加热30 min,取出后迅速放入冰水浴中,冷却至室温。取冷却之后的蛋白溶液,10 000 r/min离心30 min;迅速分离上清液以及沉淀,取上清液;使用BCA法总蛋白定量测定试剂盒测定上清液中蛋白质含量;使用酶标仪测定562 nm下溶液的吸光值。以仅添加等量酪蛋白酸钠的热处理溶液(90 ℃,30 min)作为空白;将蛋白质溶液替换为蒸馏水调零;将56.3 g/L的BSA蛋白质标准品用蒸馏水稀释至不同质量浓度(2 500、1 000、500、250、100、50、25、0 μg/mL),在562 nm下测定吸光值制作标准曲线。根据标准曲线计算上清液中的蛋清蛋白含量。
1.3.4还原性SDS-PAGE分析
向1.5 mL离心管中加入100 μL蛋白样品、20 μL上样缓冲液,其中包含0.1 mol/L Tris-HCl(pH=6.8)、0.01 mol/L DTT、0.1 g/mL甘油、0.01 g/mL SDS、0.01 g/L巯基乙醇、0.01 g/L溴酚蓝,充分混匀,沸水浴5 min,4 ℃条件下12 000 r/min离心5 min,除去不溶物。分离胶体积分数为12.5%,浓缩胶体积分数为6%,样品的上样量为20 μL。浓缩胶电压为80 V,分离胶电压为200 V。电泳结束后,使用0.25 g/L考马斯亮蓝R-250染色液染色30 min,含体积分数10%冰醋酸及8%乙醇的脱色液脱色48 h。
1.3.5体积排阻色谱分析
使用体积排阻-高效液相色谱法(SE-HPLC)检测热处理蛋清蛋白溶液中可溶性聚集物的变化[16],使用TSK G4000SWXL凝胶色谱柱进行色谱分析。流动相为0.05 mol/L磷酸盐缓冲液(pH=7.0,0.3 mol/L NaCl),流速为0.5 mL/min,检测器波长为280 nm,样品使用0.45 μm滤膜过滤,上样量为20 μL。
1.3.6粒径的测定
将不同比例的蛋清蛋白以及酪蛋白酸钠溶于磷酸盐缓冲液(pH=7.2,0.01 mol/L),4 ℃放置12 h使其充分溶解。将蛋白溶液置于90 ℃水浴锅中加热30 min,迅速放入冰水浴中冷却至室温。使用激光粒度仪测定冷却至室温下蛋白溶液中的粒度分布。
1.3.7透射电镜分析
使用透射电镜在加速电压为80 kV时观察蛋白质的聚集形态,将不同比例的蛋清蛋白以及酪蛋白酸钠溶于磷酸盐缓冲液(pH=7.2,0.01 mol/L),4 ℃放置12 h使其充分溶解。将蛋白溶液置于90 ℃水浴锅中加热30 min。迅速放入冰水浴中冷却至室温。使用磷酸盐缓冲液(pH=7.2,0.01 mol/L)稀释500倍。向封口膜上滴加30 μL的蛋白样品以及30 μL 0.02 g/mL硅钨酸溶液,将覆有碳膜的铜网置于混合液滴上方,负染15 min,室温下自然干燥12 h。
1.4 统计学分析
所有实验至少重复3次,数据处理及作图使用Microsoft Excel 2007及Origin 8.0。使用SPSS 19.0进行单因素方差分析,Duncan多重范围检验均值之间的显著性差异(P<0.05)。
2 结果与分析
2.1 酪蛋白酸钠对蛋清蛋白热处理溶液浊度的影响
浊度可以反映蛋白溶液中的颗粒大小以及数量,是描述蛋白质聚集程度的宏观指标[17]。酪蛋白酸钠的添加量对蛋清蛋白溶液浊度的影响见图1。与对照组相比,当酪蛋白酸钠的添加量为1 mg/mL时,溶液的浊度无显著变化;当酪蛋白酸钠的添加量超过2 mg/mL时,溶液的浊度显著降低;随着酪蛋白酸钠添加量的继续增加(3、4、5 mg/mL),溶液的浊度呈现略微上升的趋势。实验结果表明,酪蛋白酸钠的添加量大于1 mg/mL时可以有效抑制蛋清蛋白质的热聚集。但由于酪蛋白酸钠的溶解性较低,当其添加量超过一定值时,酪蛋白酸钠会造成混合溶液浊度的增加[18]。因此,当酪蛋白酸钠添加量较高时(4、5 mg/mL),溶液浊度再不能作为判断酪蛋白酸钠对蛋清蛋白热聚集的抑制程度的唯一指标[19]。

不同字母代表差异显著(P<0.05)。图1 酪蛋白酸钠添加量对热处理蛋清蛋白溶液浊度的影响Fig.1 Effect of different addition amounts of sodium caseinate on turbidity of heat-treated egg white protein solution
2.2 热处理蛋清蛋白溶液上清液中可溶性蛋白含量分析
为进一步探究酪蛋白酸钠对蛋清蛋白热聚集影响,排除酪蛋白酸钠溶液浊度的干扰,对经过热处理蛋白溶液上清液中的蛋清蛋白含量进行了测定(见图2)。离心之后上清液中保留的蛋清蛋白含量越多,表明酪蛋白酸钠对蛋清蛋白不溶性热聚集的抑制效果越强[20]。对于酪蛋白酸钠添加量较低(1 mg/mL)的蛋清蛋白溶液,离心得到的上清液中的可溶性蛋白含量与对照组相比,无明显差异;随着酪蛋白酸钠添加量的增加,上清液中保留的可溶性蛋白含量逐渐增加;高添加量的酪蛋白酸钠(4、5 mg/mL)对热聚集抑制效果的变化增幅相比于低添加量(2、3 mg/mL)的酪蛋白酸钠的抑制效果的变化增幅减小。实验结果进一步表明,酪蛋白酸钠的添加可以抑制蛋清蛋白的热聚集,且随着酪蛋白酸钠添加量的增加,其对蛋清蛋白热聚集的抑制效果逐渐增强;过量添加的酪蛋白酸钠对蛋清蛋白热聚集的抑制效果的提升不显著。这与浊度的结果(图1)基本一致,随着酪蛋白酸钠质量浓度的增加,上清液中蛋清蛋白的含量无显著变化,这表明较高浓度的酪蛋白酸钠对蛋清蛋白热聚集的抑制无效果。酪蛋白酸钠热处理溶液的浊度是由酪蛋白酸钠的溶解性较低造成的[6],这也可能是造成高添加量酪蛋白酸钠对热聚集的抑制效果没有显著增强的原因。据前人研究,酪蛋白以及酪蛋白酸钠可以抑制多种单一蛋白的热聚集,如牛血清蛋白、过氧化氢酶、醇脱氢酶、胰岛素、卵转铁蛋白及溶菌酶,当底物蛋白浓度与本研究相近时,酪蛋白酸钠的有效添加量均低于1 mg/mL[10,21-22],酪蛋白酸钠以及酪蛋白作用于蛋清中的卵白蛋白和卵转铁蛋白时[9,11],其有效添加量均高于上述蛋白,本研究中酪蛋白酸钠的有效添加量为2 mg/mL(图2),这可能是由不同蛋白种类与结构之间的差异造成的;且对于酪蛋白酸钠抑制混合蛋白热聚集的有效浓度均高于蛋白底物的浓度[23],这与本研究结果一致。

不同字母代表差异显著(P<0.05)。图2 酪蛋白酸钠的添加量对热处理蛋清蛋白溶液上清液中蛋清蛋白含量的影响Fig.2 Effect of different addition amounts of sodium casei nate on soluble protein content in supernatant of heat-treated egg white protein solution
2.3 热处理蛋清蛋白溶液上清液中可溶性蛋白组分分析
2.3.1酪蛋白酸钠对不同热处理温度下蛋清蛋白热聚集效果的影响
为了对酪蛋白酸钠抑制蛋清蛋白热聚集的过程进一步说明,以及测定蛋清蛋白中各组分的聚集趋势,本研究使用还原SDS-PAGE电泳测定了蛋清蛋白溶液经过热处理之后上清液中的可溶性蛋白含量(见图3),以及酪蛋白酸钠的添加对蛋清蛋白热聚集的影响(见图4)。在图3中,当温度上升至75 ℃时,上清液中卵转铁蛋白、卵黏蛋白以及溶菌酶的含量明显降低;当温度上升至80 ℃时,卵白蛋白的含量明显降低;当温度上升至85 ℃时,卵类黏蛋白的含量明显降低。这表明在蛋清蛋白的热处理过程中,首先发生聚集的是卵转铁蛋白、溶菌酶以及卵类黏蛋白,其次是卵白蛋白,卵黏蛋白。在图4中,添加酪蛋白酸钠后,当温度上升至75 ℃时,卵转铁蛋白条带颜色变浅,推测蛋清蛋白热聚集物粒径降低,可能是由于酪蛋白酸钠与蛋清蛋白表面的疏水基团相结合,从而抵制了蛋清蛋白的热聚集。溶菌酶条带在温度上升至80 ℃后强度降低;卵白蛋白条带在85 ℃时颜色明显变浅。结果表明,酪蛋白酸钠的添加可以抑制蛋清蛋白各组分的热聚集温度,抑制其热聚集,且可以抑制蛋清蛋白中的各组分在75 ℃以下产生的热聚集。酪蛋白酸钠以及酪蛋白可以抑制鸡蛋中单一的卵转铁蛋白、卵白蛋白以及溶菌酶的热聚集[8],但是在本研究中对于卵白蛋白的热聚集的抑制效果较弱。鸡蛋中包含了多种相互作用的蛋白质[24],混合体系中的蛋白质相比于单一组分热聚集的温度更低,更容易形成聚集体;不同蛋白质组分具有不同的结构以及等电点,这些蛋白之间的相互作用力会对热聚集产生一定的影响[15,25-26]。

图3 不同温度下热处理蛋清蛋白溶液上清液SDS-PAGE电泳分析Fig.3 SDS-PAGE analysis of supernatant of heat-treated egg white protein solution at diverse temperatures

图4 添加酪蛋白酸钠时在不同温度下热处理蛋清蛋白溶液的上清液SDS-PAGE电泳分析Fig.4 SDS-PAGE analysis of supernatant of heat-treated egg white solution at diverse temperatures with addition of sodium caseinate
2.3.2酪蛋白酸钠添加量对蛋清蛋白热聚集效果的影响
使用还原SDS-PAGE电泳探究不同酪蛋白酸钠添加量对蛋清蛋白各组分的热聚集的影响(见图5)。随着酪蛋白酸钠的增加,蛋清蛋白各组分的条带颜色加深;当酪蛋白酸钠的质量浓度分别为1、2、3 mg/mL时,溶菌酶、卵转铁蛋白、卵白蛋白的条带颜色相比于对照组明显加深。这表明在蛋清蛋白混合体系中,酪蛋白酸钠对溶菌酶、卵转铁蛋白、卵白蛋白的有效热聚集抑制质量浓度分别为1、2、3 mg/mL。当酪蛋白酸钠质量浓度为1 mg/mL时,主要是蛋清蛋白中的溶菌酶的热聚集有所抑制,但由于蛋清蛋白中的溶菌酶含量较低[27],因此其浊度与上清液中蛋清蛋白含量的变化不显著(见图1、图2);当酪蛋白酸钠添加量较高时,蛋清蛋白中含量较多的卵白蛋白以及卵转铁蛋白[27]的热聚集得到了抑制,因此浊度与上清液中的可溶性蛋白含量发生了显著变化(见图1、图2)。对于仅添加酪蛋白酸钠样品的上清液,当酪蛋白酸钠质量浓度较低时(1、2、3、4 mg/mL),随着酪蛋白酸钠添加量的增加,各组分的条带颜色逐渐加深;当酪蛋白酸钠添加量较高时(5 mg/mL),上清液中包含的可溶性酪蛋白酸钠含量无显著变化。这进一步印证了当酪蛋白酸钠添加量较高时,其浊度与上清液中可溶性蛋白含量变化不显著的原因是酪蛋白酸钠的溶解度较低,在热处理过程中发挥分子伴侣特性的组分是有限的。
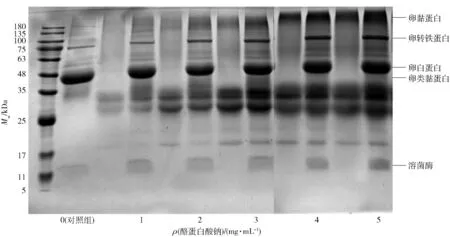
图5 不同酪蛋白酸钠的添加量下热处理蛋清蛋白溶液上清液SDS-PAGE结果分析Fig.5 SDS-PAGE analysis of supernatant of heat-treated egg white protein solution with different addition amounts of sodium caseinate
2.4 酪蛋白酸钠对蛋清蛋白溶液热聚集物溶解性的分析
浊度、上清液中可溶性蛋白含量的测定以及还原SDS-PAGE电泳结果表明,酪蛋白酸钠抑制了蛋清蛋白不溶性聚集物的形成,促进了可溶性聚集物的形成。为进一步验证,测定了不同酪蛋白酸钠添加量对热处理蛋清蛋白溶液粒径分布以及分子量分布的影响(见图6)。使用动态光散射技术测得的蛋白溶液的粒径分布能够较好地反映蛋白在溶液中的聚集状态。与对照组相比,酪蛋白酸钠的添加使得粒径分布整体发生了明显的左移,表明随着酪蛋白酸钠添加量的增加,蛋清蛋白的粒径降低。对照组在0.76、2.00以及55.36 μm附近有3个明显的粒径峰,酪蛋白酸钠的添加使得55.36 μm附近的粒径峰完全消失;随着酪蛋白酸钠添加量的增加,2.00 μm附近的粒径峰变小且左移,0.76 μm附近的粒径峰逐渐增大且左移。由此可知,随着酪蛋白酸钠添加量的增加,参与热聚集的蛋清蛋白越来越少。研究表明,酪蛋白由于缺乏游离巯基残基而缺少三级结构与四级结构,可以与其他蛋白表面的疏水基团结合从而防止蛋白质发生聚集以及变性[6]。因此,推测蛋清蛋白热聚集物粒径的降低可能是由于酪蛋白酸钠与蛋清蛋白表面的疏水基团相结合,从而抑制了蛋清蛋白的热聚集。图6(b)为使用体积排阻色谱法对添加酪蛋白酸钠的蛋清蛋白溶液中可溶性聚集体的分析。将不同酪蛋白酸钠添加量的蛋清蛋白溶液90 ℃条件下加热30 min,样品离心之后取上清液进行色谱分析。随着酪蛋白酸钠添加量的增加,样品峰右移且峰面积逐渐增加。表明溶液中的可溶性聚集物的分子量逐渐减小,且可溶性蛋白含量逐渐增加。综上,酪蛋白酸钠的添加可以抑制蛋清蛋白不溶性聚集物的形成,促进可溶性聚集物的形成。蛋白溶液粒径分布及分子量分布的变化与浊度的变化相一致,二者共同说明酪蛋白酸钠可以抑制蛋清蛋白的热聚集。
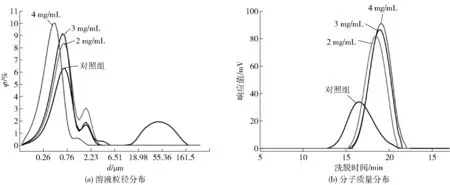
图6 不同酪蛋白酸钠添加量对热处理蛋清蛋白溶液粒径以及分子质量分布的影响Fig.6 Effect of different addition amounts of sodium caseinate on particle size and molecular weight distribution of heat-treated egg white protein solution

图7 酪蛋白酸钠及不同酪蛋白酸钠有效添加量下蛋清蛋白的热聚集体形态Fig.7 Aggregated morphology of sodium caseinate and egg white protein at different addition amounts of sodium caseinate
2.5 热处理蛋清蛋白聚集形态分析
使用透射电镜对经过热处理(90 ℃,30 min)的酪蛋白酸钠、不同酪蛋白酸钠添加量的蛋清蛋白的聚集形态进行观察(如图7)。酪蛋白酸钠在一定条件下会形成大型的稳定胶束(40~300 nm)[28-29]。经过加热的酪蛋白酸钠溶液(见图7(a)),形成了由蛋白颗粒组成的大型胶束;未添加酪蛋白酸钠的蛋清蛋白溶液(见图7(b))经过热处理之后形成了体积较大且结构紧密的聚集体;当酪蛋白酸钠的添加量为2、3 mg/mL时(图7(c)、7(d)),蛋清蛋白热聚集物的体积减小,且部分蛋清蛋白吸附于酪蛋白胶束内;当酪蛋白酸钠添加质量浓度为3 mg/mL时(图7(e))放大观察,蛋清蛋白形成了体积较小且较为稀疏的结构;当酪蛋白酸钠的添质量浓度为4 mg/mL时(图7(f)),蛋清蛋白形成了体积较小的聚集体,且与酪蛋白胶束内的球状颗粒交联。结果表明,酪蛋白酸钠的添加不仅抑制蛋清蛋白的热聚集,并且使聚集体的结构更加松散细小。
3 结 论
研究结果表明,酪蛋白酸钠的添加可以有效抑制蛋清蛋白的热聚集。当酪蛋白酸钠的添加质量浓度高于2 mg/mL时,热处理(90 ℃,30 min)蛋清蛋白溶液(5 mg/mL)的浊度显著降低,上清液中保留的可溶性蛋清蛋白含量增加。由于酪蛋白酸钠的溶解性较低,当其添加质量浓度高于4 mg/mL时,其对蛋清蛋白的抑制效果无显著变化。酪蛋白酸钠的添加抑制了蛋清蛋白经过热处理后不溶性聚集物的形成,促进了溶液中可溶性聚集物的形成,使得结构紧密的大聚集体转变为结构疏散且体积较小的热聚集物。
