培美曲塞与贝伐单抗联合应用维持治疗晚期肺腺癌的临床疗效
2020-06-27王鹏李莉
王 鹏 李 莉
1 滨州市人民医院肿瘤二科 山东 滨州 256610 ;2 滨州医学院附属医院妇产科
近年来肺癌发病率呈增长趋势,成为威胁人类健康的一大杀手。肺癌占全球恶性肿瘤发病率的12.7%,死亡率占18.2%,均高居首位[1];肺癌中非小细胞肺癌(non-small cell lung cancer,NSCLC)比例占87.05%,确诊时大多为晚期,估计每年全球有超过一百万人死于此病[2-3]。对晚期NSCLC非鳞状细胞癌治疗策略层出不穷,行一线诱导化疗后的维持化疗亦是近年肺癌治疗上的一新观点[4]。
贝伐单抗是针对血管内皮生长因子(vascular endothelial growth factor, VEGF)的重组人源化单克隆抗体,近年来被用于包括肺癌在内的多种实体瘤治疗。回顾性分析已经显示贝伐单抗应用于铂类为基础的非鳞癌NSCLC患者时,在无疾病进展生存和总生存上是有所获益的[5-6]。培美曲塞是人工合成的抗叶酸药物,其作用机制为破坏细胞内叶酸依赖性的正常代谢过程,抑制嘌呤、嘧啶的合成从而阻碍细胞复制使细胞分裂在S期即停止,从而达到抗肿瘤效应。最新研究表明培美曲塞对大肠癌、肺癌、乳腺癌等实体肿瘤具有一定疗效[7]。为了探讨在培美曲塞基础上加用贝伐单抗对晚期肺腺癌患者维持治疗疗效,本研究回顾性分析对肺腺癌一线含铂类方案化疗获益后,应用上述两药联合治疗,观察疗效及安全性。
1 资料与方法
1.1 病例选择 入组54例患者均为2017年1月至2019年5月一线含铂类方案化疗获益的晚期驱动基因阴性肺腺癌患者,均有病理明确诊断。两药联合组中男 13 例,女14例;年龄为46~88岁,平均年龄为(64.58±7.81) 岁。对照组中男14例,女13例,年龄为47~87 岁,平均年龄为(65.24±7.26) 岁。两组患者的一般资料比较,差异无统计学意义, 具有可比性。所有参与本研究的患者在实验前对本次研究目的及过程均有充分的了解,患者表示自愿参与本次实验,并签署知情同意书,符合医学伦理学要求并经伦理委员会审批通过。肺癌分期采用第八版TNM分期,全部系IV期并多发转移病例。入组患者KPS评分及ECOG评分均较好。所有患者均接受PC方案(培美曲塞 500 mg/m2d1,顺铂75 mg/m2d1, Q3w)或PC+贝伐单抗(7.5 mg/kg, Q3w)方案化疗4至6周期,疾病获得控制后,所有患者均有可测量的肿瘤病灶,肝肾功及血常规均正常。同时所有患者未行其他抗肿瘤治疗。
1.2 治疗方法 患者在一线诱导方案化疗结束后,第21天开始进行培美曲塞维持化疗,具体方案:培美曲塞 500 mg/m2,静滴1 d,Q3w;培美曲塞用药前1周开始口服金施尔康补充叶酸,直至全部化疗周期结束。在用培美曲塞前1周应用VitB121 000 μg肌肉注射。用培美曲塞前1天、当天及第2天口服地塞米松4 mg bid。贝伐单抗(上海罗氏制药有限公司)7.5 mg/kg,静滴1 d,Q3w。培美曲塞维持化疗第2个周期后进行临床评价,每3周重复维持化疗直至疾病进展,主要观察PFS、DCR,同时记录药物不良反应及血清VEGF表达与疗效间关系。其中,“近期疗效” 参照NCCN制定的RECIST标准对两治疗组患者进行近期疗效评价,疗效分为完全缓解(complete remission, CR) 、部分缓解(partial remission, PR) 、稳定(stabilization, SD)、进展(progress, PD),客观有效率(objective response rate, ORR) = (CR + PR) /总例数。疾病控制率(Disease control rate, DCR) = (CR + PR + SD) /总例数。不良反应:依据美国NCCN化疗毒性评价标准。VEGF测定方法:开始维持化疗前及维持化疗4周期后第2天抽血行VEGF检测。标本采集后3 000 r/min离心15 min取上清,所有标本均采用深圳晶美生物公司VEGFELISA试剂盒进行检测。
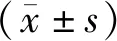
2 结果
2.1 两组患者近期疗效比较 两药组ORR显著高于单药组(P<0.01),且两药组DCR显著高于单药组(P<0.05),见表1。
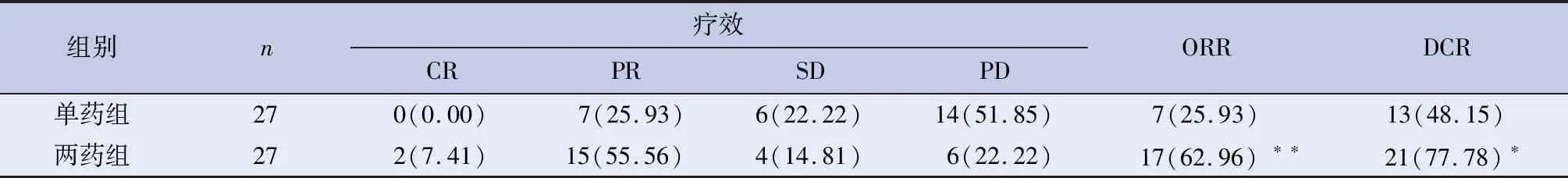
表1 两组患者近期疗效/n(%)
注:与单药组比较,*P<0.05,**P<0.01。
2.2 两组患者不良反应发生情况比较 两组不良反应比较,除两药组患者高血压发生率明显高于单药维持治疗组(P<0.01)外,其余不良反应比较,差异均无统计学意义,见表2。

表2 两组患者不良反应比较
注:与单药组比较,**P<0.01。
2.3 近期疗效评价 培美曲塞组中位PFS为3.9个月,培美曲塞+贝伐单抗组中位PFS为7.8个月。两组患者PFS对比采用生存分析 Kaplan Meier法,行Log rank检验,差异有统计学意义,说明培美曲塞联用贝伐单抗能提高晚期NSCLC患者的近期疗效,见图1。
2.4 血清VEGF表达与疗效间关系 开始维持治疗前,两组患者血液VEGF平均值比较,P>0.05。经化疗药物维持治疗后,两组患者血液VEGF水平均下降。维持治疗4周期后,两药组有效病例27 例,PD病例0 例,与治疗前比较,两药组患者治疗后血清 VEGF 水平明显下降(P<0.01),而单药组中有效病例16例,无效病例11例,有效和无效患者治疗前后血清VEGF水平差异无统计学意义,考虑样本含量小,故可能存在误差。与单药组比较,两药组患者治疗后血清 VEGF 水平明显下降(P<0.01),见表3。

表3 两组治疗前后血清VEGF水平比较 单位:ng·L-1
注:与治疗前比较,**P<0.01;与单药组比较,##P<0.01。
3 讨论
众所周知,肿瘤生长、扩散的先决条件为血管生成,而贝伐单抗能与血管内皮生长因子A(VEGF-A)结合,并阻断VEGF-A与血管内皮生长因子受体(VEGFR)的结合,从而对 VEGF 表达产生抑制,同时控制肿瘤的生长。 此外,它还具有降低组织间隙压力、促进肿瘤血管正常化等作用,达到临床抗肿瘤疗效。由此可见, 监测患者血清 VEGF 水平变化可以预测贝伐单抗治疗晚期肿瘤的疗效。本研究结果显示,培美曲塞联合贝伐单抗对疾病的控制率明显升高,较单药维持治疗明显延长无疾病进展生存时间;在药物毒副作用及不良反应方面,比如白细胞减少、血小板减少、贫血、恶心呕吐和高血压、出血等较轻且均可耐受,且两组比较中除高血压外,其余差异均无统计学意义。由此可见,贝伐单抗可增加患者高血压的发生风险,在治疗过程中需密切观察,积极对症处理。治疗过程中,患者血清 VEGF水平亦发生变化,在维持治疗4周期后,培美曲塞+贝伐单抗组血清VEGF水平与治疗前比较,患者治疗后血清 VEGF水平明显下降,差异有统计学意义;而培美曲塞单药组中,未发现血清VEGF水平变化有统计学差异。总之,培美曲塞与贝伐单抗联合维持治疗驱动基因阴性晚期肺腺癌,显示有较好的有效性和安全性;同时,可明显延长晚期肺腺癌患者无疾病进展生存时间[8-10]。
在化疗靶向治疗时代,驱动基因阴性的晚期非鳞NSCLC治疗策略是依据组织学分型,Zinner等[12]研究显示,非鳞癌患者培美曲塞联合顺铂较吉西他滨联合顺铂组生存时间明显延长(11.8月vs10.4月,HR=0.81),因而指南推荐晚期非鳞NSCLC优选培美曲塞联合铂类治疗。同时,Karayama等[12]研究显示,在驱动基因阴性非鳞NSCLC中培美曲塞维持治疗给患者带来进一步生存获益;并且在AVAPERL研究中,将患者经过贝伐单抗联合培美曲塞+顺铂治疗后随机分为贝伐单抗联合培美曲塞组和贝伐单抗单药组,结果显示,双药联合组维持治疗可提高患者PFS(7.4月vs3.7月,P<0.001)。近年,免疫检查点抑制剂治疗在肺癌领域研究同样鼓舞人心。Zhang等[13]研究,对比帕博利珠单抗联合培美曲塞铂类在驱动基因阴性非鳞IV期NSCLC中疗效,无论PD-L1表达状态高低,培美曲塞铂类联合帕博利珠单抗能延长患者PFS(8.8月vs4.9月)。基于该研究结果,目前NCCN指南上述三药联合作为1类推荐治疗晚期非鳞NSCLC。随着免疫治疗药物的不断创新与完善,晚期NSCLC患者将有越来越多的治疗选择;而对于临床医生,针对不同患者群体,把握合适的治疗时机并选择适宜的联合方案才能进一步提高患者的整体疗效。
