熔融尿素法提取羊毛角蛋白机制
2020-03-11萨如拉赵雪梅宮川刚棚桥光彦
萨如拉,赵雪梅,宮川刚,棚桥光彦
(1.赤峰学院 生命科学学院,内蒙古 赤峰 024000; 2.日本岐阜大学 应用生物科学部,岐阜县 岐阜市501-1193)
近年来,随着人口增加和经济的发展,资源消耗越来越多,温室效应、热带雨林减少、酸雨等环境问题日趋严重。如何通过生物质资源的有效利用来减轻环境负担引起广泛关注。
除木质资源外,生物质资源还包括大量的蛋白质、纤维等资源。羊毛在纺织过程中会产生大量废弃物,如羊毛屑和落毛,羊毛屑和落毛中掺杂垃圾和异物,染色时会出现着色浓淡不均匀等,不适合作为工业原料。另外,每年大量生产的含羊毛衣料等纺织品产生的废弃物——羊毛纤维大部分被焚烧或填埋处理,没有得到有效利用,不仅污染了环境,也浪费了大量的蛋白质资源[1]。羊毛角蛋白是天然蛋白质,有优良的生物相容性和亲肤性,无毒无刺激,且富含多种氨基酸,在纺织、生物医用材料和化妆品等领域具有广阔的开发空间和巨大的应用价值[2-3]。
为了减轻环境负担,进行可持续性开发,有必要开发废弃羊毛的有效利用方法。目前羊毛角蛋白的提取主要有酸碱法[4]、还原法[5]、离子液体法[6]、氧化法[7]等,但这些方法存在高温、溶剂昂贵且危险、溶剂难去除、周期长、效率低、不适宜工业化生产等缺点[2]。熔融尿素法是一种新型的羊毛角蛋白提取技术,羊毛的整个溶解过程只使用尿素,不添加其他任何化学试剂,最终尿素还可回收循环利用,是一种高效、经济、安全、快速、环保、适合工业化生产的技术。但是,尿素溶解羊毛的机制还未见详细的报道,鉴于此,以羊毛为原料,采用熔融尿素法溶解羊毛并提取角蛋白,同时测定角蛋白的分子质量。另外,以标准化合物为原料,替代羊毛角蛋白中的官能团及化学键与尿素进行反应,分析官能团及化学键的变化及相应的反应路径,为阐明羊毛角蛋白在熔融尿素中溶解原理提供新的依据。
1 材料和方法
1.1 材料、试剂及仪器设备
材料:羊毛购买于日本毛绒株式会社。标准化合物:香草醛、香草醇、香草酸、乙酰香草醛、甲酰香草酸、4-乙酰-3-甲酰芥子酸、水杨酰苯胺、3,3-二羟基二苯二硫醚、苯胺、酪氨酸。试剂:尿素、乙酸乙酯、氯化钠、硫酸钠、丙酮、丙烯酸酯,化学试剂均为分析纯。仪器设备:高温油浴锅、十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)仪、日本岛津气相色谱质谱联用仪(GCMS)-QP5050A、日本电子核磁共振装置(CP/MAS13C-NMR) ECA 500MHz。
1.2 试验方法
1.2.1 溶解羊毛角蛋白的分子质量测定 准确称量10 g尿素放入试管,然后放入150 ℃恒温油浴锅中让尿素完全熔融,在熔融尿素中加入1 g羊毛,反应20 min后取出试管,加入5 mL蒸馏水(防止尿素迅速凝固),放入透析袋中透析24 h、过滤,沉淀物为非水溶性角蛋白,滤液为水溶性角蛋白[8]。将水溶性角蛋白用10% SDS-PAGE法测定其分子质量。
1.2.2 尿素与标准化合物的化学反应
1.2.2.1 标准化合物的选择 为了分析熔融尿素溶解羊毛的反应机理,分别选用香草醛、香草醇、香草酸、乙酰香草醛、甲酰香草酸、4-乙酰-3-甲酰芥子酸、水杨酰苯胺、3,3-二羟基二苯二硫醚、苯胺、酪氨酸等标准化合物来替代羊毛角蛋白中的官能团及化学键(为适应GC-MS分析,所选用的化合物都带苯环),与尿素进行化学反应。标准化合物对应的官能团及化学键见表1。标准化合物的化学结构见图1。

表1 标准化合物对应的官能团、化学键Tab.1 Functional groups, chemical bonds corresponding to standard compounds

图1 标准化合物的化学结构Fig.1 Chemical structure of standard compounds
1.2.2.2 尿素与标准化合物的化学反应及分析方法 于干燥试管中加入2 g尿素,在150 ℃油浴锅中加热至尿素熔融,再加入0.2 g标准化合物,150 ℃反应20 min,取出试管加入8 mL的蒸馏水,冷却至室温,加入乙酸乙酯10 mL,进行3次分液。有机层由20 mL的食盐水脱水1次,再使用硫酸钠脱水,过滤除去硫酸钠、浓缩,加入丙酮(1 mg/mL)溶解,进行GC-MS分析。水层冷冻干燥,加入吡啶和无水乙酸各10 mL,放置24 h进行乙酰化、浓缩,GC-MS分析。
GC-MS分析条件:进样温度230 ℃,气化室温度300 ℃,初始温度为100 ℃,保持5 min,以10 ℃/min速率上升至300 ℃,保持5 min,分析时间为30 min[9]。
测定仪器为GCMS-QP5050A;电离模式: EI (电子电离);电压:70 eV;毛细管柱:DB-5MS (J&W),0.25 mm(I.D.)×30 m(L)×0.5 μm(有机层);毛细管柱:Rtx-5Amine(水层);载气:He;测定方法: 扫描。
另外,使用13C-NMR对酪氨酸与尿素反应物的有机层(溶媒为重丙酮)进行分析[10-11]。
2 结果与分析
2.1 溶解羊毛角蛋白的分子质量测定结果
熔融尿素溶解羊毛的SDS-PAGE电泳结果如图2。水溶性角蛋白的分子质量为75 ku,一般低分子角蛋白分子质量为40~60 ku,所以溶解羊毛角蛋白仍然保持着较高分子状态。因此,可以判断水溶性角蛋白的一级结构没有被破坏,只是空间结构被破坏。

图2 溶解羊毛角蛋白的SDS-PAGE电泳结果Fig.2 SDS-PAGE electrophoresis results of dissolved wool keratin
2.2 尿素与标准化合物的反应结果
香草醛和尿素与香草醛反应产物的有机层的气相色谱(GC)比较与峰对应化合物结构如图3,香草醛与尿素的化学反应路径如图4。GC色谱中,保留时间6.0~7.0 min时出现了香草醛失去醛基的化合物峰,保留时间12.0~13.0 min时出现了香草醛峰。尿素中带有独立电子对的氮攻击香草醛羰基碳导致醛基从香草醛脱离。

图3 香草醛和尿素与香草醛反应产物的有机层GC色谱比较与峰对应化合物结构
Fig.3 Comparison of organic layer GC of vanillin and urea and vanillin reaction products and structureof peak-corresponding compounds

图4 香草醛与尿素的化学反应路径Fig.4 Chemical reaction pathway of vanillin and urea
香草酸和尿素与香草酸反应产物的有机层GC色谱比较与峰对应化合物结构如图5,香草酸与尿素的化学反应路径如图6。香草酸也在保留时间6.0~7.0 min时出现了失去羧基的化合物峰,保留时间在15.0 min时出现了香草酸峰。由于尿素中带有独立电子对的氮夺走香草酸羧基的氢而导致羧基的脱离。
乙酰香草醛和尿素与乙酰香草醛反应产物的有机层GC色谱的比较与峰对应化合物结构如图7,乙酰香草醛与尿素的化学反应路径如图8。乙酰香草醛和尿素反应后出现了3个峰,在保留时间6.0~7.0 min时出现了香草醛失去醛基的化合物峰,在保留时间12.0~13.0 min时出现了香草醛的峰,在保留时间14.0~15.0 min时出现了乙酰香草醛的峰。这说明乙酰香草醛和尿素的反应是逐步进行的,虽然醛基和乙酰基都会脱离,但反应性能更高的乙酰基先脱离,醛基后脱离。乙酰基的脱离与醛基相同,尿素中带有独立电子对的氮攻击香草醛羰基碳而导致乙酰基的脱离。
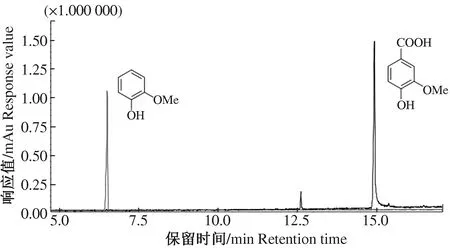
图5 香草酸和尿素与香草酸反应产物的有机层GC色谱比较与峰对应化合物结构Fig.5 Comparison of organic layer GC of vanillic acid and urea and vanillic acid reaction product and structure of peak-corresponding compounds
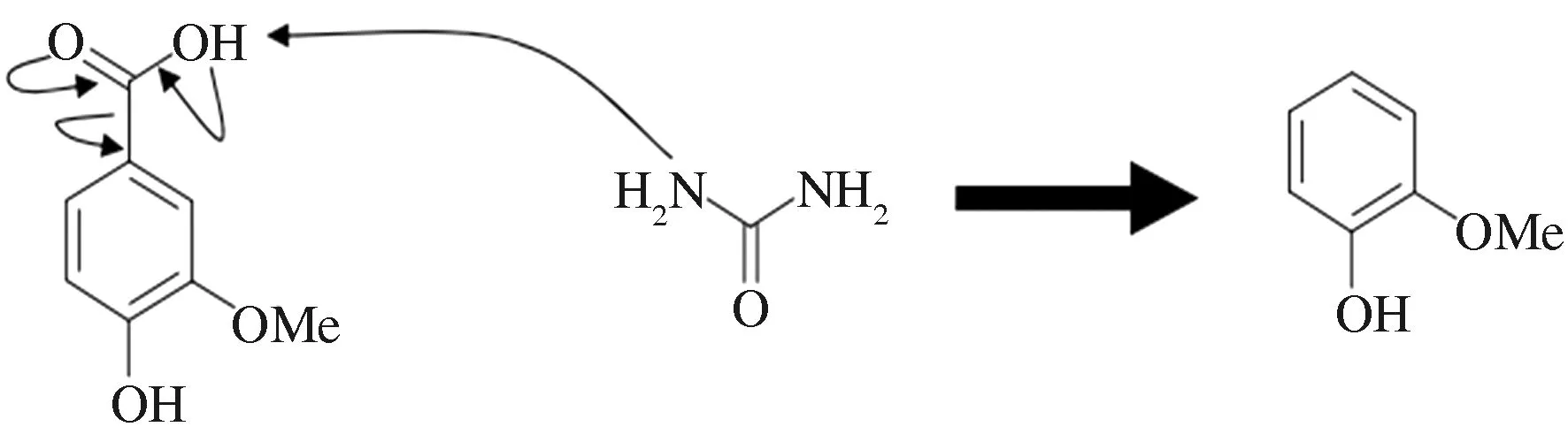
图6 香草酸和尿素的化学反应路径Fig.6 Chemical reaction pathway of vanillic acid and urea
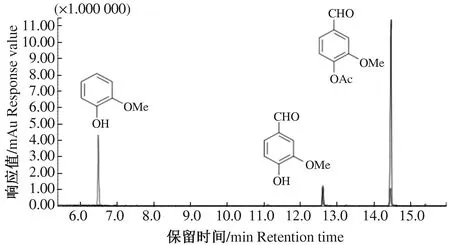
图7 乙酰香草醛和尿素与乙酰香草醛反应产物的有机层 GC色谱比较与峰对应化合物结构Fig.7 Comparison of organic layer GC of acetyl vanillin and urea with acetyl vanillin reaction products and structure of peak-corresponding compounds
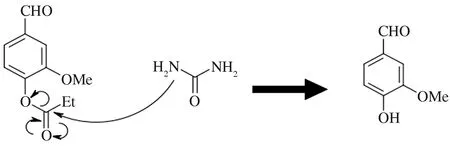
图8 乙酰香草醛与尿素的化学反应路径Fig.8 Chemical reaction pathway of acetyl vanillin and urea
4-乙酰-3-乙基芥子酸盐和尿素与4-乙酰-3-乙基芥子酸盐反应产物的有机层GC色谱比较与峰对应化合物结构如图9,4-乙酰-3-乙基芥子酸盐与尿素的化学反应路径如图10。4-乙酰-3-乙基芥子酸盐与乙酰香草醛相同也失去了乙酰基,在保留时间21.5~22.0 min时出现了4-乙酰-3-乙基芥子酸盐失去乙酰基的化合物峰,保留时间22.0~22.5 min出现了4-乙酰-3-乙基芥子酸盐的峰。乙酰基的脱离过程与乙酰香草醛相同。
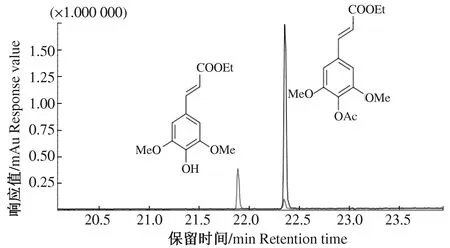
图9 4-乙酰-3-乙基芥子酸盐和尿素与4-乙酰-3-乙基芥子酸盐反应产物的有机层GC色谱比较与峰对应化合物结构Fig.9 Comparison of organic layer GC of 4-acetyl-3-ethyl succinate and urea and 4-acetyl-3-ethyl succinate reaction product and structure of peak-corresponding compounds

图10 4-乙酰-3-乙基芥子酸盐和尿素反应的化学反应路径Fig.10 Chemical reaction pathway of 4-acetyl-3- ethyl succinate with urea
香草醇和尿素与香草醇反应产物的有机层GC色谱比较与峰对应化合物结构如图11,香草醇与尿素的化学反应路径如图12。在保留时间13.0 min时出现了香草醇的醇羟基被氨基取代的化合物峰,紧接着出现香草醇的峰,最后在保留时间21.0 min时出现香草醇和尿素反应产物的峰。其反应路径为:香草醇酚羟基氧的独立电子对依次被挤出去,导致醇羟基被脱离;尿素中的氮攻击不稳定的第7位碳,最终尿素与香草醇结合;脱离羟基的氧攻击尿素香草醇化合物的羧基碳而导致尿素的一部分被脱离,形成了香草醇的醇羟基被氨基置换的化合物。

图11 香草醇和尿素与香草醇反应产物的有机层GC色谱比较与峰对应化合物结构Fig.11 Comparison of organic layer GC of vanillyl alcohol and urea and vanillyl alcohol reaction products and structure of peak-corresponding compounds

图12 香草醇和尿素的化学反应路径Fig.12 Chemical reaction pathway of vanillyl alcohol and urea
苯胺和尿素与苯胺反应产物的有机层GC色谱的比较与峰对应化合物结构如图13,苯胺与尿素的化学反应路径如图14。GC色谱中保留时间5.0 min前出现苯胺的峰,15.0 min附近出现了苯胺与尿素结合的化合物峰。苯胺氨基的氮向尿素羰基碳攻击而合成了尿素与苯胺结合的化合物。

图13 苯胺和尿素与苯胺反应产物的有机层GC色谱比较与峰对应化合物结构Fig.13 Comparison of organic layer GC of aniline and aniline and urea reaction product and structure of peak-corresponding compounds

图14 苯胺与尿素的化学反应路径Fig.14 Chemical reaction pathway of aniline and urea
酪氨酸和尿素与酪氨酸反应产物的有机层GC色谱的比较与峰对应化合物结构如图15,酪氨酸与尿素的化学反应路径如图16。通常酪氨酸几乎不溶于丙酮,不出现在GC色谱中,但与尿素反应后保留时间23.0 min附近出现了与环化尿素结合的酪氨酸峰。尿素与酪氨酸反应产物的有机层13C-NMR分析结果如图17,从图17可以确定尿素与酪氨酸反应产物的结构。酪氨酸氨基的氮向尿素羰基碳攻击而导致尿素向酪氨酸结合,尿素氨基氮向酪氨酸羧基的羰基碳攻击而形成环化结构。

图15 酪氨酸和尿素与酪氨酸反应产物的有机层GC色谱比较与峰对应化合物结构Fig.15 Comparison of organic layer GC of tyrosine and urea and tyrosine reaction products and structure of peak-corresponding compound
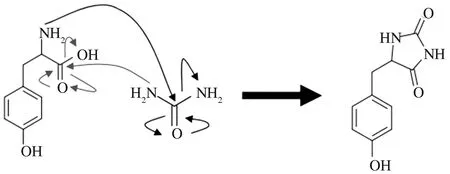
图16 酪氨酸与尿素的化学反应路径Fig.16 Chemical reaction pathway of tyrosine and urea
尿素与香草酸甲酯、水杨酰苯胺、3,3-二羟基二笨二硫醚没有产生化学反应,即肽键及二硫键没有断裂。
尿素与香草醇反应产物的水层GC-MS分析结果与峰对应化合物结构如图18。保留时间7.5 min附近检测出尿素的二聚体,所有标准化合物与尿素反应产物的水层都相同,既没有原料转变的化合物,也没有原料本身,有必要改善试验方法进行进一步的研究。
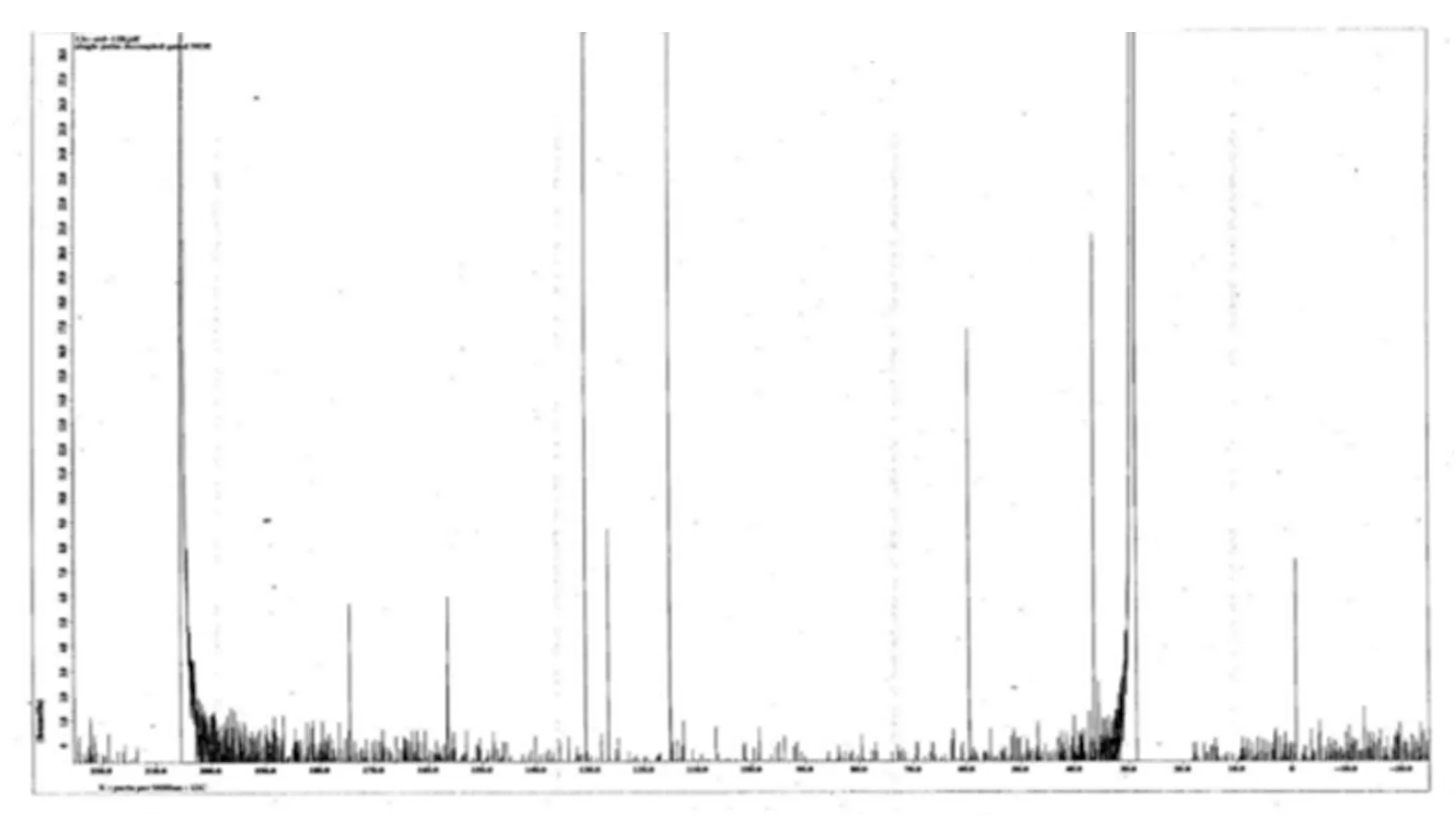
图17 尿素与酪氨酸反应产物的有机层13C-NMR分析结果Fig.17 Organic layer 13C-NMR analysis of urea and tyrosine reaction products

图18 尿素与香草醇反应产物水层GC-MS分析结果与峰对应化合物结构Fig.18 GC-MS analysis of aqueous layer of urea and vanillin reaction products and structure of peak-corresponding compounds
3 结论与讨论
为了探明熔融尿素中羊毛溶解的机制,首先进行了溶解羊毛角蛋白的分子质量测定,其次,选用一些标准化合物,替代羊毛角蛋白中的官能团与化学键,与尿素进行化学反应,分析了反应过程中化学键、官能团的变化及相应的反应路径。
通过SDS-PAGE测得的溶解羊毛角蛋白分子量为75 ku,一般低分子角蛋白分子质量为40~60 ku[12],由此可以判断熔融尿素中溶解后的羊毛角蛋白保持较高分子状态。标准化合物与尿素的反应中,尿素与官能团及化学键产生多种化学反应。主要化学反应为醛基、芳香环连接的羧基、乙酰基从标准化合物脱离;醇羟基、氨基、碳键连接的羧基与尿素结合;含有肽键和二硫键的化合物与尿素不产生化学反应,说明蛋白质的一级结构没有被破坏,与分子质量测定结果一致。因此,羊毛在熔融尿素中溶解的主要途径是以氢键的断裂、官能团的脱离及尿素与官能团的结合等方式来完成的。另外,酪氨酸的氨基和羧基均跟尿素反应形成环化结构,才能溶于有机溶剂中,并从GC-MS的分析中能检测。所有标准化合物与尿素反应产物的水层中,既没有原料转变的化合物,也没有原料本身,因此下一步有必要改善试验方法进行进一步的研究。王丽静等[2]采用熔融尿素法在150 ℃处理羊毛30 min提取角蛋白,所得分子质量为 45.3~66.2 ku。房启海等[3]采用熔融尿素法在160 ℃处理50 min提取角蛋白,所得分子质量为25~37 ku。本研究中采用熔融尿素法150 ℃处理20 min,得到角蛋白的分子质量为75 ku。这些结果表明,提取温度和提取时间极有可能影响角蛋白的分子质量。王丽静[2]等采用ATR-FTIR 测试结果表明,熔融尿素法提取角蛋白分子结构中仍然保留有二硫键,这与本研究结果一致。
综上所述,本研究选用未知分子质量的标准化合物进行了试验,虽然解释了一些官能团的脱离、结合、化学键的反应及分子质量的大小等问题,但未解决羊毛角蛋白最终能否降解成氨基酸或短肽、尿素与氨基酸的详细化学反应路径等问题。为了全面解释羊毛在熔融尿素中的溶解机制,有必要选用分子质量已知的蛋白质及20种氨基酸为原料与尿素进行化学反应,分析反应过程及产物,更有必要优化试验方法及试验条件。
随着纤维产业的废弃物、破旧的衣料等蛋白质纤维日益增加,如何利用废物纤维蛋白质成为一个重要的课题,本研究利用熔融尿素法可以从废弃的蛋白质纤维中大量提取纤维蛋白质,为下一步纤维蛋白的有效利用(比如加工成蛋白质饲料或有机氮肥料等产品)提供了参考。
