小剂量激素联合免疫抑制剂在Ⅰ、Ⅱ型重症肌无力患者中的疗效观察及对细胞免疫水平的影响研究①
2019-11-20孙静洁
孙静洁 王 琪
(兰州大学第二医院,兰州730000)
重症肌无力(Myasthenia gravis,MG)是一种由神经、肌肉接头部位传递功能障碍引起的自身免疫性疾病,临床表现为部分或全身骨骼肌无力或易疲劳,且活动后症状加重,经休息后症状减轻[1]。数据报道显示:重症肌无力患病率为(77~150)/100万,年发病率为(4~11)/100万,女性发病率略高于男性[2]。临床研究表明:重症肌无力发病机制复杂,普遍认为与自身免疫有关,其严重影响患者的身体健康及生活[3]。糖皮质激素(GCS)是MG患者中常用的治疗药物,在多数患者中能取得良好的治疗效果,但是部分患者用药时出现病情加重,再加上长时间大剂量给予GCS药物,其安全性较低,激素并发症较多[4,5]。硫唑嘌呤在体内几乎全部转变成6-巯基嘌呤而起作用。它可通过对RNA代谢的干扰而具有免疫抑制作用。如小剂量长期存在于培养基中,可抑制致敏的淋巴细胞在体外的杀伤细胞作用。硫唑嘌呤在重症肌无力的治疗中,尤其是对于类固醇激素治疗不佳者,比较多用且有较好的治疗效果。目前小剂量激素与硫唑嘌呤片联合用于重症肌无力的治疗,临床效果及对细胞免疫水平的影响研究较少[6,7]。因此,本文采用随机对照方法开展研究,探讨小剂量激素联合免疫抑制剂在Ⅰ、Ⅱ型重症肌无力患者中的临床效果及对细胞免疫水平的影响,现报道如下。
1 资料与方法
1.1一般资料 选择2016年5月~2018年2月来本院治疗的Ⅰ、Ⅱ型重症肌无力患者84例作为研究对象,电脑抽取随机数字法分为对照组(n=42)和观察组(n=42)。纳入标准:①符合重症肌无力诊断标准[8];②近3个月未给予其他方法治疗,能在医嘱下完成相关检查、治疗。排除标准:①存在药物禁忌症或其他硫唑嘌呤片治疗禁忌症;②合并难以控制的高血压、心脏病、溃疡病、糖尿病或感染者;③合并精神异常或伴有恶性肿瘤者。本研究均在医院伦理委员会监管下完成,两组临床资料差异无统计学意义(P>0.05),具有可比性。
1.2方法
1.2.1治疗方法 对照组:给予溴吡斯的明与泼尼松治疗。每次取溴吡斯的明(上海中西三维药业有限公司,国药准字H31020867)60 mg,4次/d口服;醋酸泼尼松(上海信谊药厂有限公司,国药准字H31020675)30 mg,1次/d口服;观察组:在对照组基础上联合硫唑嘌呤治疗,予以硫唑嘌呤片(上海信谊药厂有限公司,国药准字 H31021422)每次50 mg,2次/d口服[9,10]。
1.2.2观察指标 (1)重症肌无力症状评分。采用通用重症肌无力症状评分量表对两组治疗前、治疗2周后复视、面肌、咀嚼、吞咽、睑下垂、发音、左上肢、右上肢、头部、左下肢、右下肢及呼吸肌功能进行评估,每项总分100分,得分越高,治疗效果越理想[11,12]。(2)细胞免疫水平。两组治疗前、治疗2周后次日早晨取空腹静脉血5 ml,4 500 g离心20 min,血清后采用流式细胞仪测定两组CD3+、CD4+、CD8+、CD4+/CD8+水平[12-14]。(3)药物安全性。统计并记录两组治疗后消化道症状、高血压、体重异常、感染及高血脂发生率。

2 结果
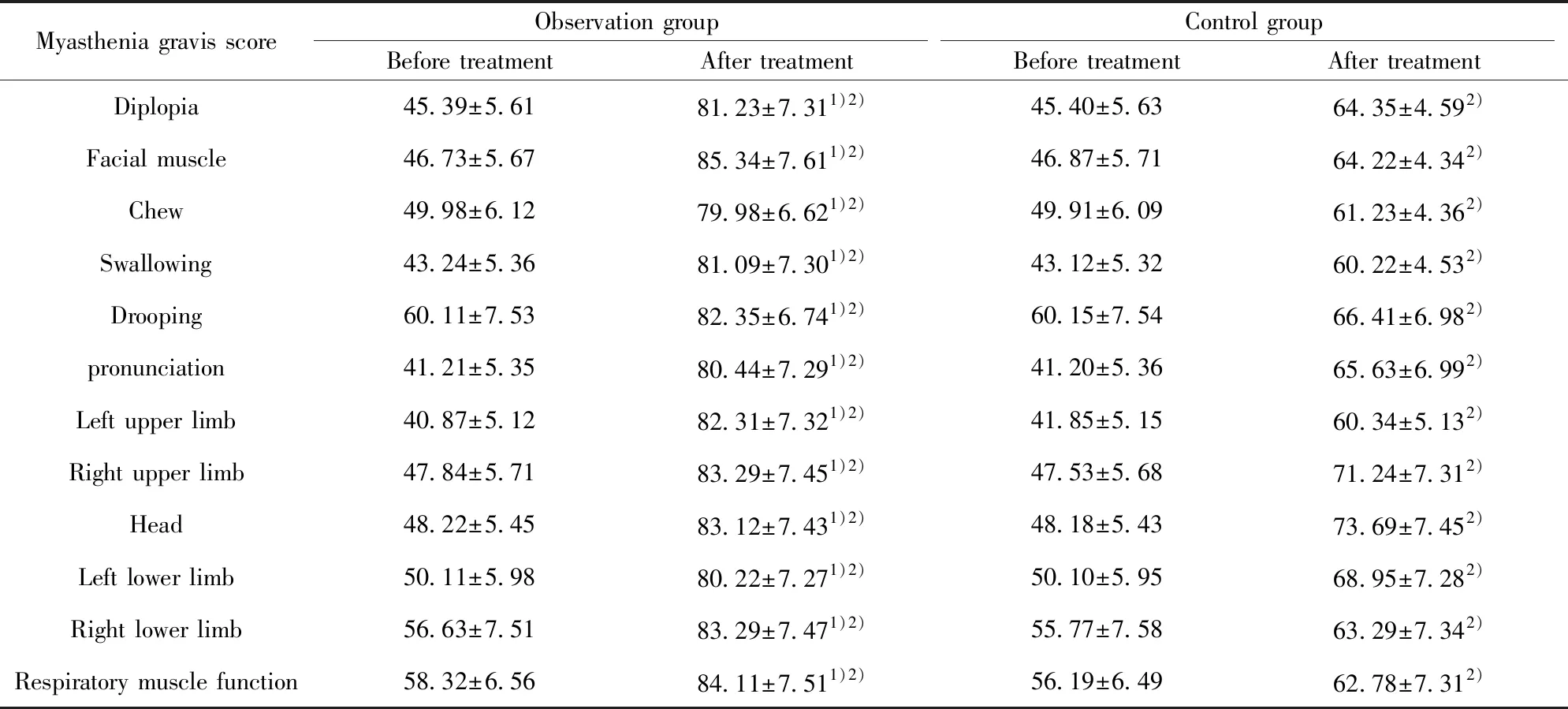
2.1两组重症肌无力症状评分比较 两组治疗前重症肌无力症状评分差异无统计学意义(P>0.05),见表1;观察组治疗后复视、面肌、咀嚼、吞咽、睑下垂、发音、左上肢、右上肢、头部、左下肢、右下肢及呼吸肌功能评分均高于对照组(P<0.05),见表2。
2.2两组T淋巴细胞水平比较 两组治疗前T淋巴细胞水平差异无统计学意义(P>0.05);观察组治疗后CD3+、CD4+、CD4+/CD8+水平均低于对照组(P<0.05);观察组治疗后CD8+水平高于对照组(P<0.05),见表3。
表1 两组临床资料比较
Tab.1 Comparison of clinical data between two groups

Clinical informationObservation groupControl groupt/χ2PGenderMale18171.221>0.05Female2425Age(years)36.79±4.5536.17±4.362.109>0.05Course(years)7.53±1.237.55±1.263.291>0.05Clinical stageRelief period22210.784>0.05Acute phase2021Pathological typingNormal thymus18171.295>0.05Thymic hyperplasia1618Thymoma87


Myasthenia gravis scoreObservation groupBefore treatmentAfter treatmentControl groupBefore treatmentAfter treatmentDiplopia45.39±5.6181.23±7.311)2)45.40±5.6364.35±4.592)Facial muscle46.73±5.6785.34±7.611)2)46.87±5.7164.22±4.342)Chew49.98±6.1279.98±6.621)2)49.91±6.0961.23±4.362)Swallowing43.24±5.3681.09±7.301)2)43.12±5.32 60.22±4.532)Drooping60.11±7.5382.35±6.741)2)60.15±7.5466.41±6.982)pronunciation41.21±5.3580.44±7.291)2)41.20±5.3665.63±6.992)Left upper limb40.87±5.1282.31±7.321)2)41.85±5.1560.34±5.132)Right upper limb47.84±5.7183.29±7.451)2)47.53±5.6871.24±7.312)Head48.22±5.4583.12±7.431)2)48.18±5.4373.69±7.452)Left lower limb50.11±5.9880.22±7.271)2)50.10±5.9568.95±7.282)Right lower limb56.63±7.5183.29±7.471)2)55.77±7.5863.29±7.342)Respiratory muscle function58.32±6.5684.11±7.511)2)56.19±6.4962.78±7.312)
Note:Compared with the control group,1)P<0.05;compared with before treatment,2)P<0.05.



GroupsCD3+CD4+CD8+CD4+/CD8+Observation groupBefore treatment67.41±5.5343.42±5.3518.85±2.302.30±0.53After treatment56.74±3.4125.63±4.6929.41±4.350.87±0.12t12.18410.89312.18510.834P0.0000.0000.0000.000Control groupBefore treatment67.34±5.5143.12±5.3118.84±2.292.29±0.51After treatment60.86±4.5933.98±5.0923.45±3.311.45±0.32t11.2819.88413.29514.093P0.0000.0000.0000.000tobservation group vs control group10.89315.39512.10512.189Pobservation group vs control group0.0000.0000.0000.000
表4 两组安全性比较[n(%)]
Tab.4 Comparison of safety between two groups[n(%)]

GroupsnGastrointestinal symptomsHypertensionAbnormal weightInfectionHyperlipidemiaObservation group421(2.38)0(0.00)1(2.38)1(2.38)0(0.00)Control group420(0.00)1(2.38)0(0.00)2(4.76)1(2.38)χ2/1.2940.7810.9980.2852.125P/0.3920.5780.1250.0770.493
2.3两组安全性比较 观察组与对照组治疗后消化道症状、高血压、体重异常、感染及高血脂发生率差异无统计学意义(P>0.05),见表4。
3 讨论
重症肌无力发病机制复杂,普遍认为是一种自身免疫系统疾病,严重影响患者健康及生活[15]。目前,临床上对于重症肌无力多以药物治疗、血浆置换、手术治疗为主,不同治疗方法各有优缺点,但是患者选择何种治疗方法存在争议[16,17]。近年来,硫唑嘌呤片在重症肌无力患者的治疗,得到应用,且效果理想。本研究中,观察组治疗后复视、面肌、咀嚼、吞咽、睑下垂、发音、左上肢、右上肢、头部、左下肢、右下肢及呼吸肌功能评分均高于对照组(P<0.05),由此说明:将硫唑嘌呤片用于重症肌无力患者的治疗中能改善患者症状,利于患者恢复。硫唑嘌呤片是重症肌无力患者中常用的治疗药物,可以通过对RNA代谢的干扰而具有免疫抑制作用,且小剂量药物即可产生明显的细胞免疫抑制作用,而大剂量的药物则能抑制体液免疫[18,19]。临床研究表明:硫唑嘌呤片用于MG患者中通过抑制相关各细胞因子的产生与表达从而抑制T细胞的活化[20]。硫唑嘌呤片用于重症肌无力患者中能抑制TNF-α的产生,且硫唑嘌呤片浓度越高,TNF-α表达水平越低[21,22]。临床上,将小剂量激素联合硫唑嘌呤片用于重症肌无力患者的治疗中,效果理想,能发挥不同药物优势,并且两种药物的联合使用并未增加并发症发生率,药物安全性较高[23,24]。本研究中,观察组与对照组治疗后消化道症状、高血压、体重异常、感染及高血脂发生率差异无统计学意义(P>0.05),说明小剂量激素联合硫唑嘌呤片用于重症肌无力患者的治疗,并发症发生率较低,有助于提高患者依从性和耐受性。
重症肌无力的发生、发展是一个多因素过程,常伴有免疫水平的异常,由细胞免疫途径、乙酰胆碱受体抗体途径介导产生的自身免疫性疾病,患者发病后机体内T辅助细胞水平、分泌的细胞因子水平将会出现异常,从而造成血清调节性T细胞介导多种细胞因子、T细胞依赖抗体增高[25]。目前,Tregs在临床MG发病中的作用引起医学界广泛关注,CD4+细胞、CD8+T细胞及CD4+/CD8+细胞均被视为Tregs的代表[26,27]。对于正常人而言,CD3+、CD4+、CD8+、CD4+/CD8+水平处于动态平衡状态,但是对于重症肌无力患者由于机体免疫水平持续升高,导致机体免疫发生失衡,表现为CD3+、CD4+、CD4+/CD8+水平升高及CD8+水平降低[28,29]。临床上将小剂量激素联合硫唑嘌呤片用于重症肌无力患者中,有助于降低患者机体细胞免疫水平,促进患者早期恢复[30]。本研究中,观察组治疗后CD3+、CD4+、CD4+/CD8+水平均低于对照组(P<0.05);观察组治疗后CD8+水平均高于对照组(P<0.05),说明小剂量激素联合硫唑嘌呤片在重症肌无力患者的治疗中有助于调整机体的免疫紊乱,改善患者的病况。
综上所述,小剂量激素联合硫唑嘌呤片用于Ⅰ、Ⅱ型重症肌无力患者的治疗中有助于改善患者症状,降低细胞免疫水平,并未增加药物不安全性,值得推广应用。
