腹部无辅助切口经直肠取出标本的完全腹腔镜下男性右半结肠癌根治术一例
2019-11-07包满都拉苏昊王鹏刘正关旭刘骞周志祥王锡山周海涛
包满都拉 苏昊 王鹏 刘正 关旭 刘骞 周志祥 王锡山 周海涛
随着国人饮食习惯的改变及预期寿命的延长,结直肠癌发病率逐年增加[1-2]。自1991年世界首例腹腔镜直肠癌手术开展以来,短短20年里以腹腔镜技术为代表的微创手术,在结直肠肿瘤的外科治疗中得到了快速的推广和发展[3]。越来越多的研究数据表明腹腔镜结直肠癌手术术后近期疗效优于传统开腹手术,同时也表现出相似的远期疗效,目前已成为结直肠癌手术的首选方式[4-6]。经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)是近年来腹腔镜结直肠外科手术的重大进展,改变了传统结直肠手术标本的取出方式,腹壁手术创伤更小,术后恢复更快,并具有更好的美容效果[7-10],已在我国获得广泛应用。但对于男性右半结肠癌经直肠取标本的NOSES术国内外仍无人报道。本团队完成1例行腹部无辅助切口经直肠取出标本的完全腹腔镜下男性右半结肠癌根治术,疗效良好,现报道如下。
一、病例简介
患者男性,60岁,因“体检发现升结肠肿物1周余”就诊,患者结肠镜检查结果显示:升结肠内可见黏膜3.0 cm×4.0 cm片状充血,黏膜浅凹。查体腹部无阳性体征,BMI 21.2 kg/m2,活检病理示:腺癌。胸腹盆增强CT:肠腔未见明确增厚及肿物,未见肿大淋巴结,肝脏多发囊肿,双下肺肺大泡。2018年5月成功实施腹部无辅助切口经直肠取出标本的完全腹腔镜下右半结肠癌根治术。
二、手术步骤
(一)手术准备
全麻后患者取膀胱截石位。采用五孔法放置腹腔镜Trocar,包括脐孔下置12 mm Trocar作为观察孔,左侧上腹部与左侧下腹部分别放置5 mm、12 mm Trocar各一枚作为操作孔,右侧腹与左侧对称各放置5 mm Trocar作为辅助操作孔(图1)。

图1 五孔法放置戳卡
(二)右半结肠及其系膜的游离
常规探查腹腔内无腹水,无明显粘连,盆腔未见转移结节,肝脏可见多发囊肿,胆、胰、脾、胃未见异常。肿瘤位于升结肠近回盲部,直径约3 cm,未侵及浆膜,升结肠系膜内未见明显肿大淋巴结。沿肠系膜上静脉表面打开后腹膜,进入Toldt’s间隙,显露并结扎切断回结肠动静脉血管、右结肠动静脉血管、结肠中动脉动静脉右支,清扫相应血管根部淋巴脂肪组织。沿Toldt’s筋膜由内向外分离直至右侧结肠旁沟,注意保护右侧生殖血管、胰头及十二指肠,完整游离末段回肠系膜、升结肠系膜及右侧横结肠系膜。自回盲部沿右侧结肠旁沟打开侧腹膜直至结肠肝曲,由结肠外后方向内侧分离,直至与内侧分离区域会合。于横结肠中部打开胃结肠韧带,自胃网膜血管外离侧断胃结肠韧带;然后分离胆囊与结肠之粘连,离断肝结肠韧带,由头侧向尾侧游离横结肠、升结肠系膜直至与内侧游离区域会合。
(三)标本切除和消化道重建
距回盲部15 cm腹腔内直线切割闭合器离断回肠(图2A),另一腹腔内直线切割闭合器于横结肠中部离断结肠(图2B)。完整切除末端回肠、盲肠、升结肠、右半横结肠、部分大网膜,将肿物置于标本袋中。拉拢两侧肠管,并将末端回肠断端与距横结肠断端8 cm处肠管缝合固定,检查两侧肠管血运,估计两侧吻合口张力。分别于末端回肠断端对系膜侧与相应位置的横结肠对系膜侧做5 mm切口,酒精纱布消毒肠腔。于一侧肠腔内置入直线切割闭合器钉仓,暂时关闭钳口,抓取另一侧肠腔,松开钳口,将肠管套上钉砧,进行必要的调整后闭合对系膜侧肠管(图2C)。酒精棉球擦拭肠腔,检查无出血后,将两侧肠管断端缺口缝合3针固定,用直线切割闭合器闭合两侧肠管共同开口,完成吻合(图2D)。
(四)标本取出
碘伏水冲洗直肠,于直肠上段取长约3 cm横行切口(图3A),经12 mm Trocar孔腹腔置入保护套,经肛拖出保护套末端,卵圆钳经保护套钳夹标本经直肠取出(图3B),经肛拖出保护套,直线切割闭合器闭合直肠开口(图3C),完成标本取出(图3D)。蒸馏水冲洗腹腔,腹腔留置引流管一根。
三、术后恢复及病理情况
患者成功施行手术,未中转开腹,手术时间为120 min,术中出血量为50 mL。患者术后恢复良好,1 d下床活动,50 h肛门排气,疼痛感轻微,4 d拔出引流管,5 d顺利出院。术后病理检查结果:结肠息肉隆起型早期浸润性高-中分化腺癌,主要呈绒毛状管状腺瘤合并高级别上皮内瘤变(重度异型增生/原位癌)改变,提示来自宽基腺瘤基底部恶变;未见明确脉管瘤栓及神经侵犯。肿瘤主体位于黏膜层,小灶区域侵透黏膜肌层达黏膜下浅层,未累及肌层,未累及浆膜,未累及回肠。回场切缘及结肠切缘均未见癌,阑尾组织层慢性炎。淋巴结未见转移癌(0/29)。免疫组化结果显示:BRAF-V600E(-),C-MET(3+),HER2(1+),MLH1(+),MSH2(+),MSH6(+),PMS2(+)。Desmin及SMA染色显示黏膜肌层中断。
随访6个月,患者未出现腹腔或吻合口出血、切口感染/裂开/愈合延迟、盆腔/腹腔脓肿、吻合口漏、肠梗阻、肺部感染、腹腔淋巴漏、心脑血管意外等并发症,消化道功能恢复良好。随访期间,患者排便和控制排便功能正常,吻合口及腹部戳孔愈合良好(图4)。
四、讨论
随着微创理念的深入人心以及微创技术的迅猛发展,微创手术已经成为结直肠肿瘤治疗的主要手段,而NOSES术作为微创技术的新星,在外科领域越来越多地受到国内外学者的青睐和推崇,其相关研究和报道也在与日俱增[11]。
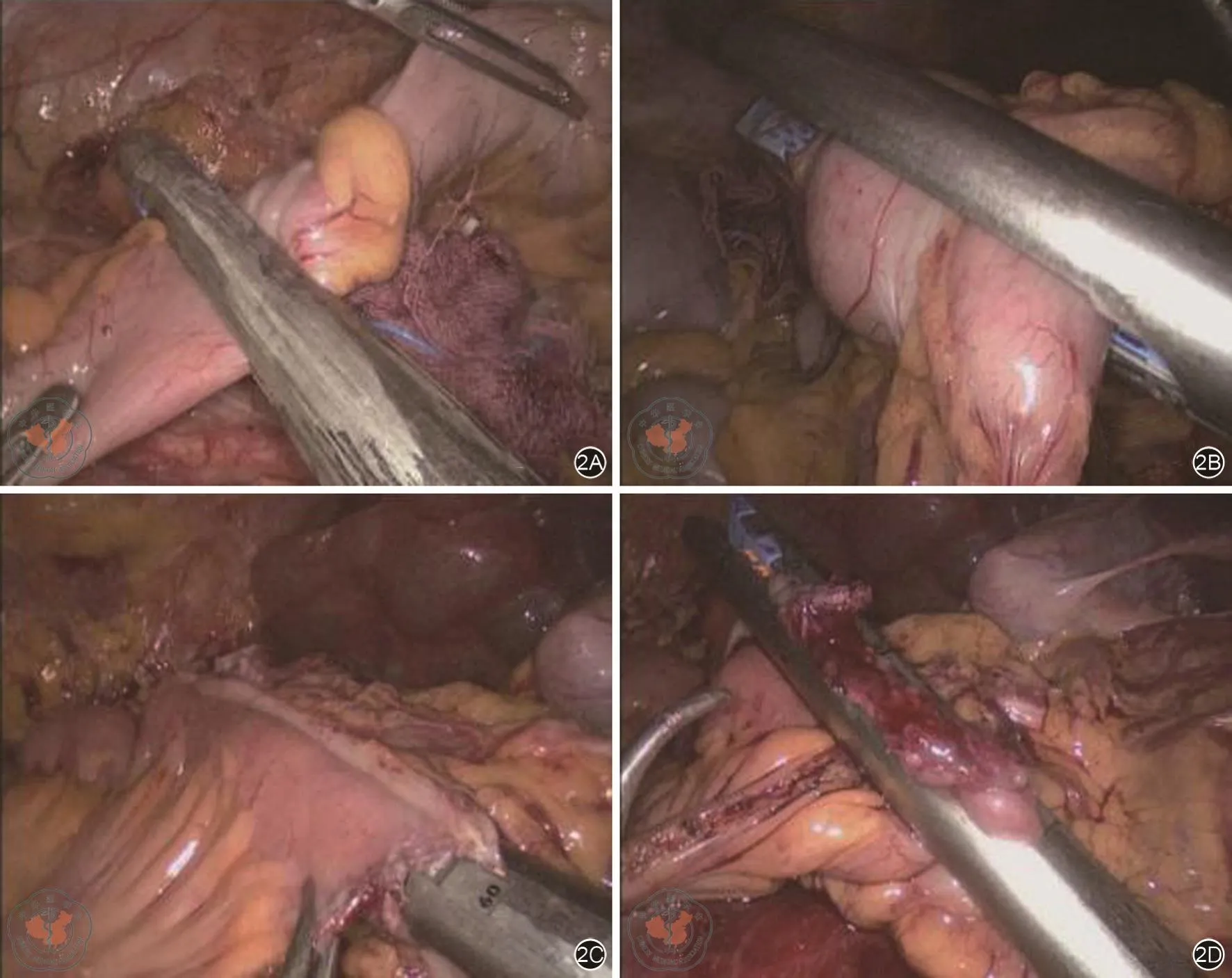
图2 标本切除和消化道重建。2A:距回盲部15 cm腹腔内直线切割闭合器离断回肠;2B:腹腔内直线切割闭合器于横结肠中部断结肠;2C:闭合对系膜侧肠管;2D:回肠断端与横结肠断端进行重叠式三角吻合
根据取标本的不同途径,NOSES术主要分为两大类,即经肛门取标本的NOSES术和经阴道取标本的NOSES术[7]。经肛门取标本的NOSES术主要适用于肿瘤较小、标本容易取出的患者;而经阴道取标本的NOSES术主要适用于肿瘤体积较大,肠系膜肥厚,标本无法经肛门取出的女性患者。右半结肠恶性肿瘤患者由于多数患者发现时肿瘤较大,无法实现经肛门取出,多适合经阴道取出。根据中国NOSES联盟,中国医师协会结直肠肿瘤委员会NOSES专委会,结直肠肿瘤经自然腔道取标本手术专家共识(2017)定义,右半结肠恶性肿瘤的NOSES术属于NOSES Ⅷ式,仅有经阴道取出一类[7],而并无经直肠取出类型。但经阴道标本取标本通路其不可克服的缺点是仅适用于女性患者。而且,经阴道取标本的另一个潜在的缺点是可能增加性交困难,盆腔感染,邻近结构创伤和阴道瘘等并发症的发病率[12]。本例病例证实对于肿瘤体积小的右半结肠恶性肿瘤的男性患者可进行经直肠NOSES术是可行的。
进行这种手术时我们的体会是:(1)严格把握适用证:肿瘤浸润深度以T2~T3为宜,经直肠NOSES术的标本环周直径<3 cm为宜;(2)围手术期严格掌握无菌及无瘤原则。与一切NOSES手术一样,术前充分做好肠道准备,切开直肠前应用稀碘伏水充分清洗直肠,闭合直肠后充分冲洗腹腔是防止腹腔感染的主要的措施,而术中避免过多接触和挤压肿瘤部位是无瘤原则的关键。此外,我们将保护套置入的途径由经直肠肛门改为经由左下腹12 mm的Trocar置入,然后顺行经直肠牵拉引出,有效避免了保护套置入过程中带来的污染机会;(3)横向切开直肠对系膜侧肠壁要充分,以免牵拉标本时可因为直肠开口小而出现肠壁撕裂可能。本例患者考虑到肿瘤较小,直肠纵向切开,有延纵轴撕裂的可能,故选择横向切开;(4)经肛取出标本后再度闭合直肠,会损失1~2 cm宽的直肠肠壁[13],相对应的,系膜侧直肠肠壁会多出1~2 cm肠壁,进行闭合直肠开口时应避免夹闭系膜侧肠壁组织并切除。我们的做法是经直肠开口前后及中间各应用缝合线腔内缝合一针,直线切割闭合器夹闭直肠开口时尽量牵拉缝线以使开口远离对侧肠壁,夹闭后检查对侧肠壁;(5)由于右半结肠切除术中切除的肠管较长,切除标本内积气和肠内容物较多,当经直肠牵拉时可因为挤压可能会聚集于腔内侧肠管内而影响标本的拖出。我们可以在拖出部分的肠管切开小切口,并放置吸引器吸出积气和肠内容物,以利标本顺利被拖出;(6)与经阴道取标本,将阴道后穹窿切开一样,本例病例需要切开直肠肠壁,有可能增加手术时间以及术后相关并发症的发生率。所以对女性患者来说,经直肠取标本的右半结肠恶性肿瘤NOSES术与经阴道取标本相比并无优势,但对于男性右半结肠恶性肿瘤患者却开辟了新的腹腔镜微创治疗方法。
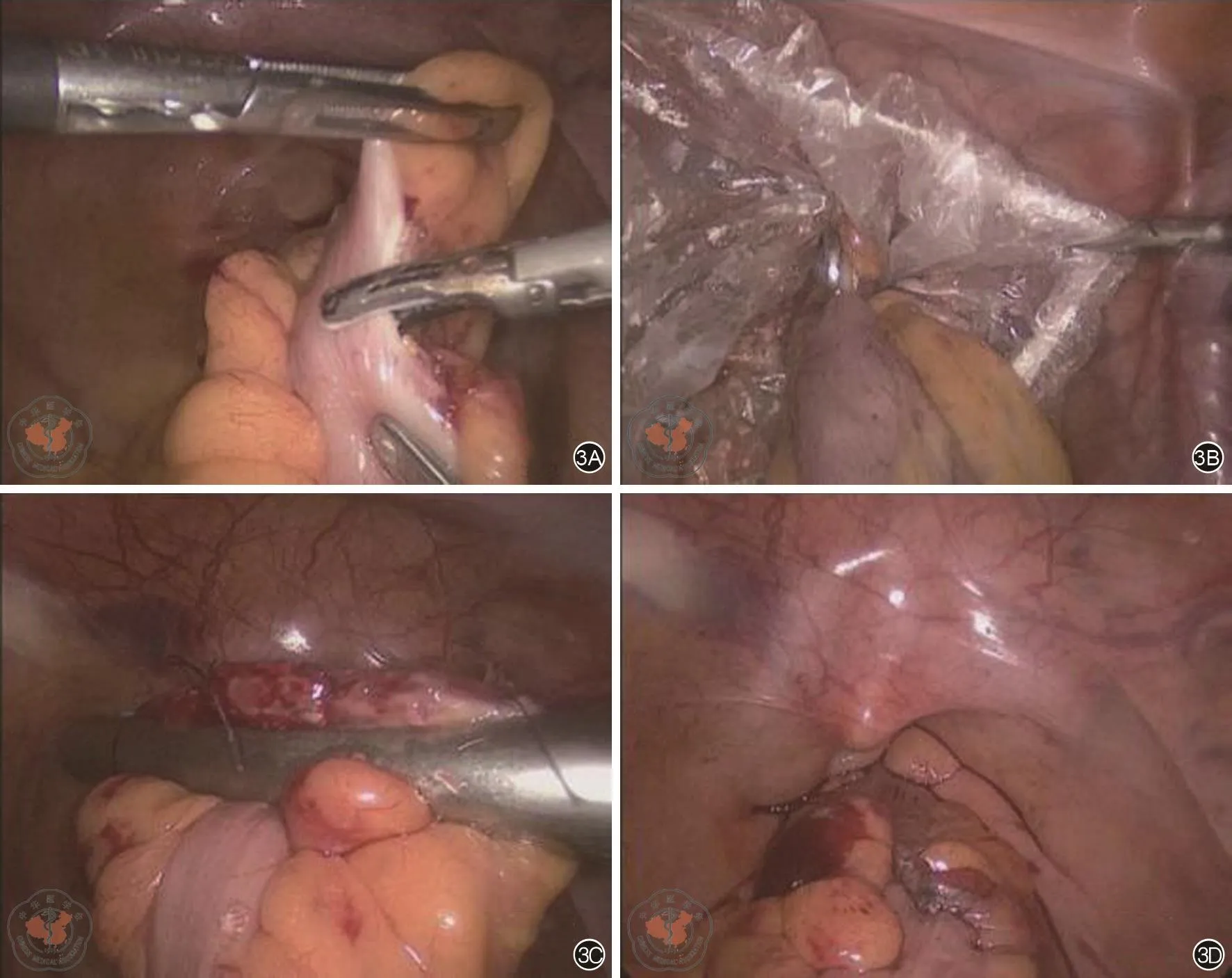
图3 标本取出。3A:直肠上段取长约3 cm横行切口;3B:卵圆钳经保护套钳夹标本经直肠拖出;3C:直线切割闭合器闭合直肠开口;3D:完成标本取出
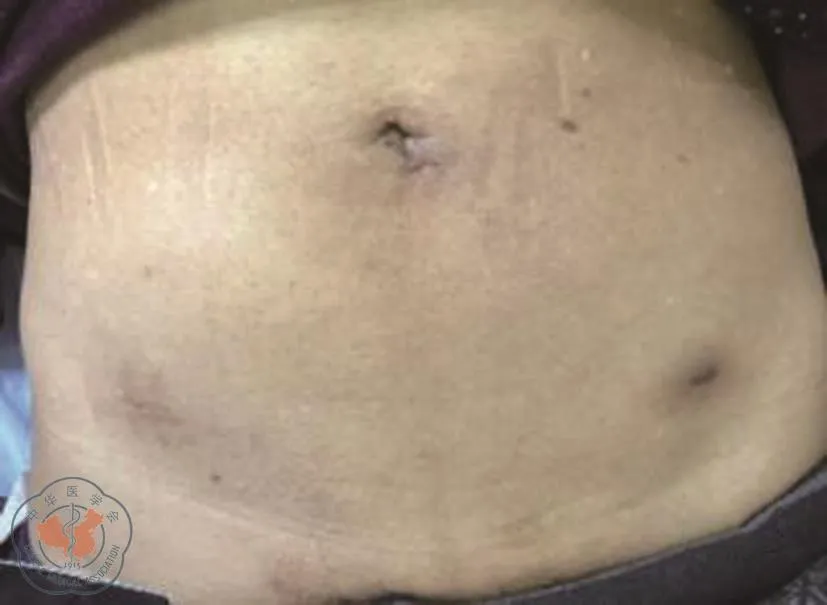
图4 术后吻合口及腹部戳孔愈合良好
综上,右半结肠癌经直肠取标本的NOSES术是可行的,并有着显著的微创及美观效果。我们相信,随着人们防癌抗癌、早诊早治意识的提高,越来越多的右半结肠恶性肿瘤患者会被早期发现,从而使适合本例手术适应证的患者数量逐年增加,但在男性患者中,经直肠取标本的腹部无辅助切口腹腔镜右半结肠切除术对术后近期疗效和远期疗效的影响还有待于进一步大规模的临床研究来明确。
