北京地区健康绝经期前女性骨转换标志物P1NP和β-CTX的参考区间分析
2018-08-02张然星李汉莲魏戌高景华谢雁鸣韩艳史颖红游珂
张然星 李汉莲 魏戌 高景华 谢雁鸣 韩艳 史颖红 游珂
1.中国中医科学院望京医院,北京 100102 2.中国中医科学院中医临床基础医学研究所,北京 100700
骨的重建是破骨细胞吸收旧骨与成骨细胞合成新骨的动态偶联过程,骨组织受激素信号、旁分泌和自分泌因子及物理压力的刺激,在基本多细胞单位中完成吸收与合成的相互转换,从而保证其矿化平衡与结构完整,并通过精确有序的调节机制维持其正常骨量和生理功能[1-3]。在此过程中的代谢产物以不同浓度和结构方式分布于骨骼、血液、尿液或其他体液中,因此,临床上可以通过检测血液或尿液中的骨代谢产物和相关激素,间接推断骨骼的各种代谢状态。这些可被检测的骨代谢产物与相关激素统称为骨代谢生化标志物或骨代谢标志物,其中能反映骨转换状态的指标称为骨转换标志物(bone turnover markers,BTMs)[4]。大量临床试验已证实,BTMs在骨质疏松性骨折的风险预测及抗骨质疏松药物的疗效监测等方面具有潜在的重要价值[4-5]。国际骨质疏松基金会(IOF)和国际临床化学联合会(IFCC)的骨标志物标准化工作组推荐血清I型原胶原氨基端前肽(procollagen type 1 N-terminal propeptide, P1NP)和I型胶原羧基端肽交联(β cross-linked C-telopeptide of type 1 collagen, β-CTX)作为骨转换参考性标志物,强调需要对两者建立国际参考标准,协调不同检测方法及研究结果的一致性,从而更好地评估其临床应用效能,扩大其在相关领域的应用经验[4]。
研究表明,在骨质疏松症的药物疗效监测中,作为“金标准”的骨密度(bone mineral density, BMD)对药物干预作用的响应不及BTMs敏感。在骨质疏松性骨折风险预测中,BTMs水平的变化可叠加或独立于BMD测量,提高风险评估的可信度[6-8]。然而,由于BTMs检测易受到显著的分析前和分析变异,以及个体内生物学变异的影响[9],加之其检测系统尚缺乏统一的国际标准[4],这都极大地限制了其在临床中的广泛应用[10]。在BTMs参考标准的建立过程中,如何确定不同人群的生物学参考区间无疑是一个核心问题[11]。绝经后女性是原发性骨质疏松症的高危人群,在对这部分人群骨质疏松的防治和管理过程中,需要健康绝经前女性BTMs的参考区间作为参照标准和评价依据。目前,BTMs水平在不同年龄阶段呈现不同程度的变化和分布趋势已成为共识[12-21],因此建立健康绝经期前女性BTMs参考区间的关键首先是要准确界定其变化和分布趋势趋于相对稳定的特异年龄阶段,再以此特异年龄阶段的健康人群作为参考人群,筛选参考个体,形成参考样本组,获得参考值,最终得到参考分布,参考限和参考区间。另外,研究显示[15,17,20],BTMs水平在不同种族、不同生活方式的国家和地区人群及不同检测系统之间都可能表现出显著差异。而目前国内临床实验室在开展BTMs检测过程中,检测项目的参考区间多由试剂厂商依据国外相关研究提供,近几年虽陆续有符合中国人群特征参考区间建立的报道,但罕见有北京地区健康女性绝经期前参考区间的研究[22-25]。
鉴于此,本研究选择北京地区健康绝经期前女性体检人群作为研究对象,通过观察不同年龄组血清BTMs水平的分布趋势差异,确定参考人群的特异年龄阶段,并初步建立北京地区健康绝经期前女性骨转换标志物P1NP和β-CTX罗氏电化学发光法检测系统的参考区间,进而为临床实验室如何建立骨转换标志物的参考区间提供经验与借鉴。
1 资料和方法
1.1 研究对象
选择2015年8月至2016年8月在中国中医科学院望京医院体检中心体检的健康绝经前女性作为招募对象,经调查问卷及体检筛查,确定符合入选标准的272名北京地区健康绝经前女性作为研究对象,每位入选受试者至少在京居住5年。纳入标准:(1)30~54岁月经周期正常女性;(2)愿意接受研究方案,并同意进行有关检查(如骨密度、血清骨转换标志物、肝肾功能、血糖等);(3)自愿签署知情同意书。排除标准:(1)BMD经双能X线吸收测量法(DXA)测量,腰椎和髋部骨量异常,T值<-1;(2)患有全身代谢性骨骼疾病;(3)半年内用过影响骨代谢药物;(4)两年内有外伤引起的骨折;(5)患有影响骨代谢的慢性疾病如糖尿病、类风湿性关节炎、甲旁亢、甲亢及其他需要长期治疗的慢性疾病;(6)患有严重心、脑血管疾病;(7)肝肾功能异常;(8)患有慢性胃肠道疾病;(9)近期有急慢性感染过敏;(10)1年内应用避孕药或怀孕;(11)当前或3个月内在哺乳期;(12)有长期吸烟和饮酒习惯;(13)2~3天内有剧烈运动;(14)严重的器质性疾病、精神神经系统疾病和活动性骨关节病。
1.2 研究方法
1.2.1问卷调查:所有受试者签署知情同意书后,在医生协助下填写调查问卷。调查问卷的基本内容包括:受试者出生日期、身高(cm)、体重(kg)、体重指数=体重(kg)/身高(m)2、月经周期、生活方式、饮食习惯及相关体检结果资料。
1.2.2常规生化指标及骨转换标志物检测:每名受试者于体检当日清晨8:00~9:00空腹采集两个真空采血管(每管4 mL)的静脉血,离心3000 rpm,5 min,分离血清后,其中1管血清采用罗氏C702生化检测系统检测肝肾功能、血糖、血钙、血磷;另一管血清于-80 ℃冰箱冻存,全部样本收集结束后同一时间采用罗氏E602免疫检测系统测定血清P1NP与β-CTX。检测过程严格按照IOF/IFCC提出的骨转换标志物检测的相关要求,尽量减少可控变异因素以保证实验数据的准确性。检测所用试剂为罗氏E602免疫检测系统专用试剂盒,实验步骤按照试剂盒说明书进行。检测不精密度为:P1NP的日内CV:1.7%~3.2%,日间CV:2.3%~3.7%;β-CTX日内CV:1.2%~4.7%,日间CV:1.7%~5.7%。最低检测限为:P1NP:5 ng/mL;β-CTX:0.01 ng/mL。
1.2.3骨密度检测:应用美国GE公司双能X线(DXA)骨密度仪,测定正位腰椎(L2~L4)和双侧股骨近端,即股骨颈(Neck),Ward’s 三角区,大转子(Troch),获取以下参数:骨密度(g/cm2)、T-值评分、Z-值评分。仪器精度1%,重复测量误差<1%。根据WHO推荐的骨量判断标准:T≥-1.0时,骨量正常;-2.5≤T<-1.0时,骨量减少;T<-2.5时,骨质疏松。
1.3 数据管理与统计分析
数据管理与统计分析均由第三方中国中医科学院中医临床基础医学研究所负责。应用Epidata3.0数据库对数据进行独立双人双录入,经一致性检验审核通过后锁定数据库,采用SPSS 20.0软件进行统计分析。所有的统计检验均采用双侧检验,P≤0.05被认为具有显著统计学差异,数据是否符合正态分布通过Kolmogorov-Smirnov检验来进行判断。运用局部加权回归散点平滑法(locally weighted scatterplot smoothing,LOWESS)描述P1NP与β-CTX水平随年龄变化的分布趋势,采用Kolmogorov-SmirnovZ检验比较不同年龄段间P1NP与β-CTX水平的分布差异,从而得出P1NP与β-CTX水平分布趋势相对平稳的特异年龄段。随后按照CLSI发布的C28-A3文件中关于医学实验室参考区间建立的具体要求,计算得出P1NP和β-CTX的参考限及参考限90%的可信区间。
1.4 伦理审查与临床研究注册
本项临床研究于2014年12月24日经中国中医科学院望京医院医学伦理委员会审查批准,同意该项研究的实施(批件号WJEC-KT-2014-026-P002)。调查对象按照自愿参加的原则,全部签署知情同意书。2015年5月10日在中国临床试验注册中心完成临床研究注册(注册号ChiCTR-DOC-15006377)。
2 结果
2.1 受试者筛选
根据受试者纳入与排除标准,636名体检的绝经期前女性参与筛选。427名受试者参与临床筛选,最终纳入健康绝经期前女性受试者272名。
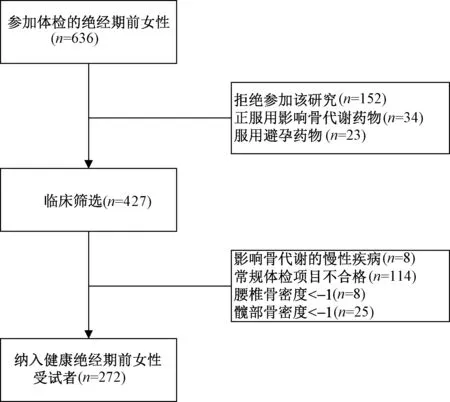
图1 受试者筛选流程图Fig.1 The flow-chart of the subject screening.
2.2 研究人群基本特征
共纳入北京地区健康绝经前女性272人,受试者年龄为(39.51±5.85)岁,身高为(161.97±4.48)cm,体重为(59.74±7.97)kg,体重指数为(22.77±2.86)kg/m2,血钙(2.27±0.12)mmol/L,血磷(1.11±0.16)mmol/L(表1)。

表1 研究人群基本特征(n=272)Table 1 The levels of P1NP and β-CTX in the study subjects (n=272)
2.3 研究人群P1NP与β-CTX水平
经Kolmogorov-Smirnov检验,总人群中P1NP与β-CTX水平均不符合正态分布(P=0.000)。P1NP水平的中位数为34.30 ng/mL(95%CI:32.94~35.74 ng/mL),β-CTX水平的中位数为0.24 ng/mL(95% CI:0.23~0.26 ng/mL)(表2)。

表2 研究人群P1NP与β-CTX水平(n=272)Table 2 The levels of P1NP and β-CTX in the study subjects (n=272)
2.4 P1NP与β-CTX水平随年龄变化趋势比较
运用LOWESS法绘制P1NP、β-CTX水平随年龄变化的拟合曲线图(图2~3),从图中大致可以看出35~45岁之间两种骨代谢标志物水平的分布趋势相对平稳。同时,运用Kolmogorov-SmirnovZ检验比较35~39岁与40~44岁的P1NP与β-CTX水平的分布趋势,无显著统计学差异(P>0.05),因此根据年龄分组情况将35~39岁与40~44岁两个年龄段进行合并,进一步采用Kolmogorov-SmirnovZ检验比较不同年龄段间P1NP与β-CTX水平的分布趋势。
结果显示β-CTX水平各年龄组比较,在30~34岁与35~44岁组有显著统计学差异(P=0.015<0.05),其余各组间比较无显著统计学差异(P>0.05);P1NP水平各年龄组比较,在45~49岁与35~44岁组有显著统计学差异(P=0.034<0.05),其余各组间比较无显著统计学差异(P>0.05)(表3)。
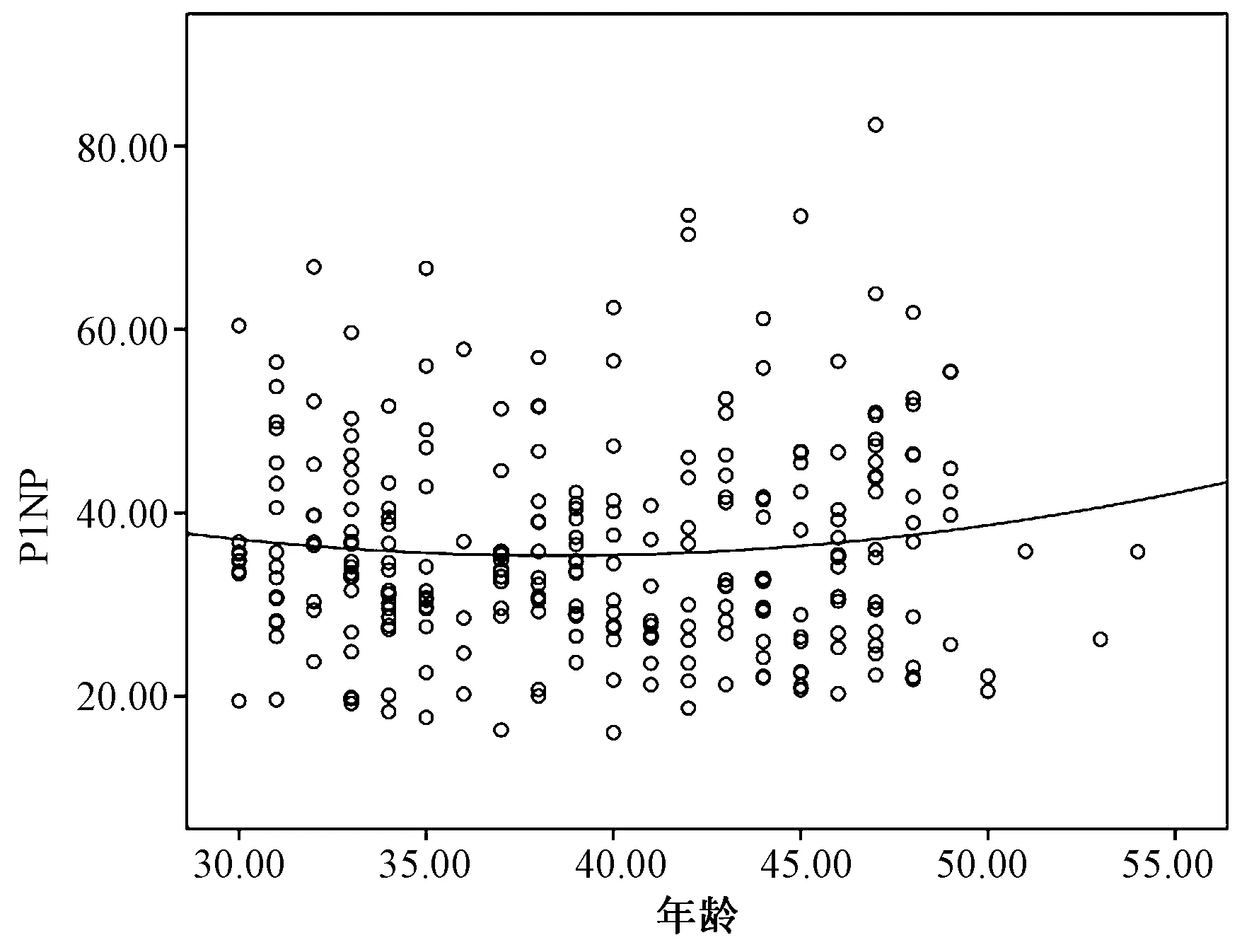
图2 P1NP水平随年龄变化的拟合曲线图Fig.2 Plot of P1NP level following the change of age
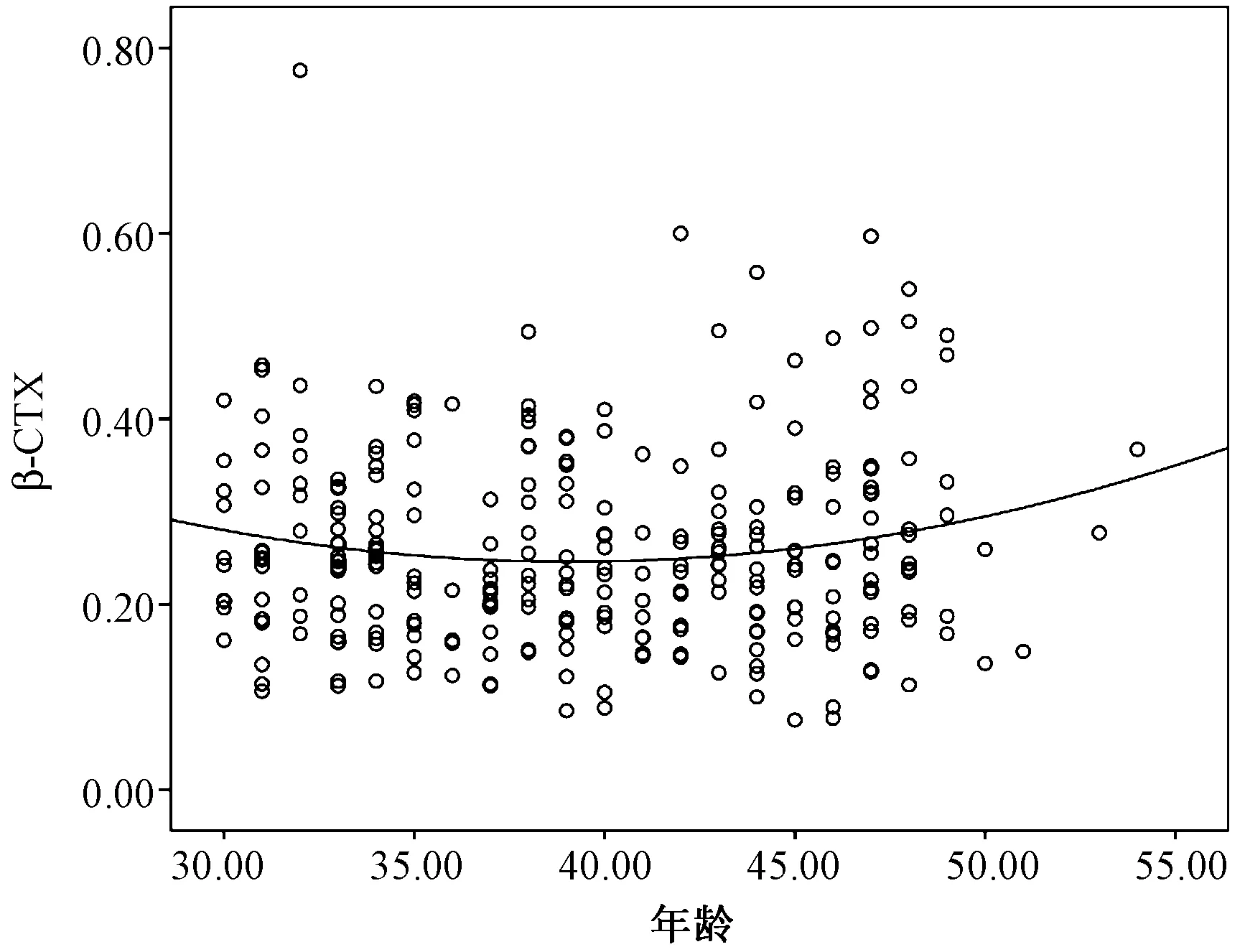
图3 β-CTX水平随年龄变化的拟合曲线图Fig.3 Plot of β-CTX level following the change of age
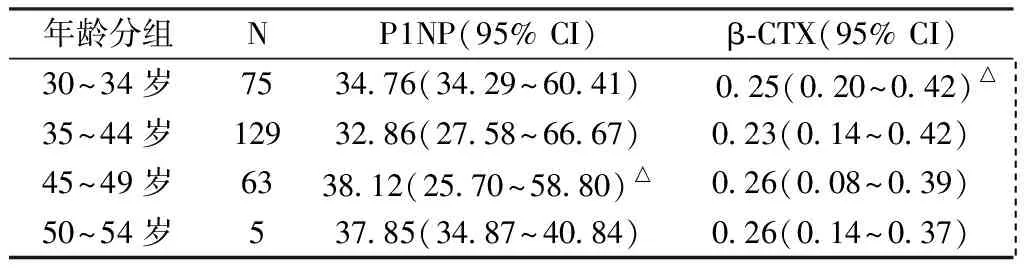
表3 不同年龄段P1NP与β-CTX水平比较Table 3 Comparison of P1NP and β-CTX among different age groups
注:与35~44岁相比,△P<0.05,其余P>0.05。
2.5 P1NP与β-CTX水平的参考限、参考限90%可信区间
根据上述结果,以35~44岁年龄组健康绝经期前女性作为参考人群,P1NP水平的参考区间为17.95~65.60 ng/mL,β-CTX水平的参考区间为0.10~0.49 ng/mL;P1NP与β-CTX水平的参考限、参考限90%可信区间见表4。
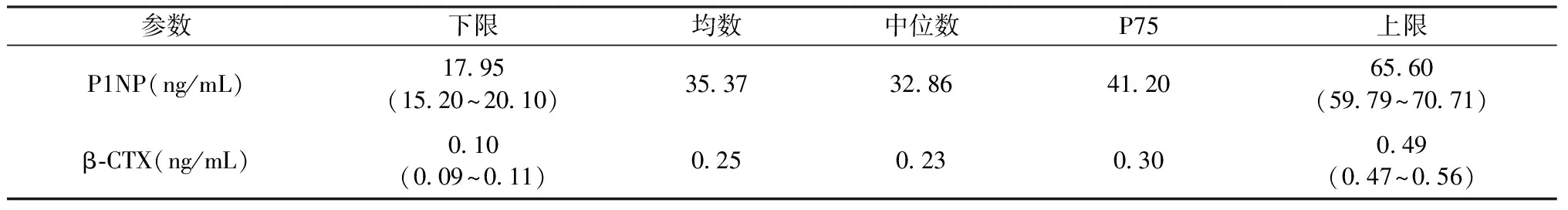
表4 P1NP与β-CTX水平的参考限、参考限90%可信区间Table 4 The reference interval value of P1NP and β-CTX (CI 90%)
3 讨论
参考区间是临床实验室解释检验报告的一个“决策支持工具”[26]。建立代表健康成年人BTMs真实表达水平的参考区间,对于推进BTMs的临床应用具有重要的现实意义。多数前瞻性队列研究证实,与健康绝经前女性BTMs参考区间的上限比较,绝经后女性非治疗者BTMs水平升高程度可预测远期发生骨折风险的大小[8]。绝经后骨质疏松症药物疗效监测的一个主要目标就是将患者BTMs水平降至健康绝经前女性参考区间的“下半段”,即低限值到均值之间的范围内[4]。
在参考区间的建立过程中,固有生物学变异对参考值的影响不容忽视,因为它决定了不同个体,甚至同一个体不同生理时期、不同生命阶段具有变异性[27]。对参考个体进行分组可有效减少个体间变异的影响,从而减少“受影响个体”与“正常个体”之间判别值的重叠,提高参考区间在实际应用中的参考价值[3]。女性在30岁之前可由骨骼发育尚未完全成熟而致BTMs的水平偏高,而在45岁之后开始进入围绝经期,雌激素水平的显著下降致破骨细胞活性增强,使BTMs的水平再次进入显著升高阶段[28-30]。因此,健康绝经前女性BTMs参考区间的建立是以年龄分组为前提的,IOF推荐其参考人群应为30~45岁之间BMD正常的人群[28]。由此可见,即使是在绝经期前,只有受变异因素影响最小的特异年龄段的健康人群,才适宜作为建立BTMs参考区间的参考人群。本研究应用IFCC推荐的前瞻性采样法,通过随机选择,按照纳入及排除标准筛选出272名符合条件的30到54岁的受试者,并以5岁为一个年龄阶段对受试者进行分组,这与国际相关研究的年龄分组方式相同,研究人群的基本特征代表了北京地区健康绝经期前女性的自然状态。同时,本研究选择了目前公认的具有较高灵敏度和特异性的电化学免疫分析技术来测定受试者血清P1NP与β-CTX水平,并通过严格的排除标准、分析前质量控制和标准化操作尽量减少导致BTMs水平出现变异的可控因素。结果显示,受试者血清P1NP与β-CTX整体水平的中位数分别为34.30(95% CI:32.94~35.74)ng/mL和0.24(95% CI:0.23~0.26)ng/mL。这与Li等[23]的研究结果存在差异,该研究报道的30岁至绝经前的中国五个地区健康女性人群血清P1NP与β-CTX整体水平的中位数分别为40.42(95% CI:17.1~102.15)ng/mL和0.26(95% CI:0.08~0.72)ng/mL。经分析,笔者认为上述差异可能来自于筛选受试者时所使用的纳入与排除标准的差异。
目前证实,骨量异常者和正常人群的BTMs水平具有显著的重叠性[31],这表明在确定参考人群年龄组过程中,更为准确的方法应该是通过比较各组BTMs水平的分布趋势来判断变异因素影响最小的年龄组,而不是只比较组间BTMs水平的均值/中位数是否存在差异[13,16,19,22]。因此,本研究通过LOWESS法绘制BTMs水平随年龄变化趋势的拟合曲线图,并应用Kolmogorov-SmirnovZ检验比较35~39岁与40~44岁年龄段及35~44岁年龄段与其他年龄段BTMs水平的分布趋势差异。结果显示,P1NP与β-CTX水平随年龄的增加均呈现出底部平缓的“波谷样”分布趋势,谷底的最低点均出现在40岁,位于35~44岁的中间位置。进一步与两者35~44岁的水平比较,P1NP与β-CTX水平具有统计学意义的分布趋势差异分别出现在30~34岁及45~49岁年龄组。由于骨重建是骨形成与骨吸收的动态偶联过程,因此,基本能够证明不论是骨形成标志物P1NP水平,还是骨吸收标志物β-CTX水平,35~44岁是两者分布趋势趋于相对平稳,受变异因素影响最小的年龄段,该年龄段的人群更适合作为建立健康绝经期前女性BTMs参考区间的参考人群,这一结论与Ardawi等[16]的研究结果相似,其报道的沙特绝经前女性参考人群年龄阶段为35~45岁。另外,Michelsen等[19]的研究虽然使用了不同于罗氏的检测系统,但其用于判断德国女性绝经前参考人群特异年龄段的方法、结论与本研究相同。
在计算参考区间时,由于大多数参考值不是正态分布,美国临床和实验室标准协会(CLSI)和IFCC均推荐使用非参数统计方法计算参考区间,定义参考区间为参考值数据95%的分布范围,即2.5%~97.5%位数所在的区间,并要求参考样本组至少包括120个参考数据, 这也是估计出参考上限和下限90%可信区间的最低保证[32]。本研究中,参考样本的选择遵循了上述方法和原则,经BTMs水平随年龄变化趋势分析,最终确定的参考样本组包含了129个P1NP和β-CTX的参考值。进而我们采用非参数方法并结合实际临床意义,建立两者的双侧95%参考区间。值得注意的是,在确定参考区间的参考限时,需要同时估计参考限的可信区间。这是因为,选择受试者样本进行参考限的计算,就是对研究人群相应百分数的评估,从同样人群中的其它抽样也许会得出稍微有些不同的参考限。因此,CLSI C28-A3指南中强调[32],一个非常有效的方法是通过计算样本中百分位数的可信区间,来识别和评定样本估算时的可变性。两个理由揭示了可信区间的必要性:首先,能够提示研究人员进行变异性评估并提供可变性评估的定量测定方法。其次,当采集的样本量增加时可信区间就会变窄。因此,研究人员可以采取增加参考个体的样本含量来提高评估的参考区间的精密度。本研究中,P1NP与β-CTX参考区间均值及其可信区间分别为35.37(95% CI:33.57~37.37)ng/mL,0.25(95% CI:0.23~0.27)ng/mL,这与Hu等[22]报道的上海地区健康绝经前女性参考区间的均值及可信区间相似,两者分别为:35.22(95% CI:30.67~40.10)ng/mL,0.242(95% CI:0.218~0.297)ng/mL。但本研究所建立的参考区间与试剂厂商提供的参考区间相差较大,试剂厂商提供的参考区间来自于OFELY研究[33-35]。这也再次证实,临床实验室在进行BTMs检测时需建立满足自身条件和符合本地人群特征的参考区间。
骨转换标志物能够成功应用于临床试验和实践需要最大程度提高其检测准确性、精确性和可比性。检测系统的标准化和协调化可使不同地区、不同时间、不同实验室的检测结果具有可比性。IOF和IFCC推荐在国际范围内建立BTMs的参考性检测系统,此过程中主要包括:制备初级和次级参考物,控制分析前变异因素,协调研究结果一致性,建立健康人群的参考区间及评价BTMs的临床应用价值等[4],这将有助于BTMs检测临床实践指南的制定与实施。Bauer等[11]指出,在健康年轻人群中建立更为稳健的参考区间极为必要,因为确定“非正常”范围首先要明确何为“正常”范围,来自于大样本的健康年轻人群的BTMs参考区间可以更好的解释骨转换标志物与临床评价的相关性。Morris等[5]回顾既往研究表明,在BTMs参考区间建立过程中不同的纳入与排除标准、不同的样本采集程序、不同的检测系统所致的研究结果存在一定差异。本研究的局限性在于:(1)在受试者体检筛查过程中,并未对甲状旁腺素与1,25-二羟维生素D3进行检测;(2)参考样本的数量为129例,仅能满足评估参考限90%可信区间的最低要求;(3)受试者主要来源于城市地区,农村地区的入选人数相对偏少。
本研究通过对北京地区30~54岁健康女性绝经期前血清骨转换标志物P1NP和β-CTX水平在不同年龄段分布趋势差异分析,证实了35~44岁为两者分布趋势趋于平稳且受变异因素影响最小的年龄段,进而以此年龄段健康女性为参考样本初步建立了血清P1NP和β-CTX的参考区间及其高、低限的可信区间。本研究可为北京地区女性骨质疏松症防治和管理提供参考依据,并为基层临床实验室建立骨转换标志物标准化检测程序提供借鉴。另外,如何协调BTMs参考区间在不同检测系统之间的一致性及如何提高其在骨质疏松症个体化治疗中的实际临床应用价值还有待于进一步的深入研究。
