不同钙源的羟基磷灰石的合成及表征
2017-04-27姚成立何艳娇李红英
姚成立,严 妍,何艳娇,李红英
(合肥师范学院 化学与化学工程学院,安徽 合肥 230601)
不同钙源的羟基磷灰石的合成及表征
姚成立*,严 妍,何艳娇,李红英
(合肥师范学院 化学与化学工程学院,安徽 合肥 230601)

羟基磷灰石;蛋壳粉;磷酸肌酸钠;水热反应
羟基磷灰石[Ca5(PO4)3(OH),HA]是天然骨的主要无机成份。在类型多样的磷酸盐中,羟基磷灰石是酸性条件下最为稳定的形态[1]。其中纳米羟基磷灰石具有很高的比表面积和独特的性能,使得仿生合成的纳米羟基磷灰石等在整形外科或骨替代物方面有着广泛的应用前景[2-4]。此外,羟基磷灰石还广泛用于药物载体[5-7]等。目前合成羟基磷灰石的过程中,高温热处理技术中的水热法倍受欢迎[8]。在水热条件下,有利于溶液的扩散,以及在一定程度上提高反应物活性,此外还可以通过控制反应条件,合成出一系列介稳结构、特殊凝聚态与聚集态的新物质、以及规则取向和晶形完美的晶体材料。肌酸磷酸二钠是一种含磷生物分子,在受热条件下可以水解释放出磷酸根并用于羟基磷灰石的矿化合成。与传统的磷酸盐相比,采用肌酸磷酸二钠作为磷源具有明显的优势:在受热条件下缓慢释放磷酸根可以避免磷酸钙、羟基磷灰石的快速成核和生长;通过控制肌酸磷酸二钠的水解速率可以控制产物的形貌、尺寸和结构;肌酸磷酸二钠及其水解产物具有良好的生物相容性,明显有益于诱导合成的磷酸钙、羟基磷灰石纳米颗粒的生物相容性[9-11]。鉴于鸡蛋壳主要由碳酸钙和有机质组成,利用蛋壳作为天然的绿色钙源合成HA粉体,可为蛋壳的高附加值产品的应用开发提供新的技术途径。目前已有文献报道了蛋壳制备HA生物材料的工艺技术,如微波合成、水热合成HA等,并分别就不同工艺参数对其热稳定性、形态特征、颗粒大小等的影响进行了对比研究,对合成产物的应用作了有益探讨[12-17]。
综合上述研究,不难发现多数研究通过煅烧蛋壳粉可获得纯度很高的CaO粉体,再用其与可溶性含磷无机盐来合成HA,虽然此方法可以成功合成HA,但该过程属于高能耗,又丧失了蛋壳生物性,无法体现蛋壳在合成中的双重作用:钙源和硬模板。为了考察供磷模式对羟基磷灰石结构和性能的影响,以磷酸肌酸二钠为磷源在水热条件下水解缓慢释放磷酸根合成HA,并对其结构性能进行表征。与传统的磷酸盐相比,采用肌酸磷酸二钠作为磷源具有明显优势:磷酸根缓慢供给可以避免磷酸钙、羟基磷灰石的快速成核和生长;通过控制肌酸磷酸二钠的水解速率可以控制产物的形貌、尺寸和结构;肌酸磷酸二钠及其水解产物具有良好的生物相容性,明显有益于诱导合成的磷酸钙、羟基磷灰石纳米颗粒的生物相容性。本文通过对上述研究的对比,从生物废弃物中获得钙源,并用作硬模板在水热条件下简便地获取了HA;同时利用磷酸肌酸二钠为磷源简易制备纯度较高的HA。此方法是比较可行的HA制备方法,并具备理想的预期应用效果,体现了环境友好和绿色化学理念。
1 实验部分
1.1 仪器与试剂
扫描电子显微镜(FESEM)测试通过日立S-1510扫描电镜(Hitachi公司)完成。产物的物相分析在XRD-6000型X射线衍射仪(日木岛津Shimadzu公司)上进行,采用Cu Kα(λ=0.154 18 nm),加速电压和电流分别为40 kV和30 mA,扫描速率(2θ)为10°/min,2θ角扫描范围为10°~80°。红外光谱测试在傅立叶变换红外光谱仪(NEXUS-870,美国尼高力仪器公司,频率范围:400~4 000 cm-1)上进行测定。
磷酸肌酸二钠盐(阿拉丁试剂(上海)有限公司)、无水氯化钙(分析纯)、无水乙醇(分析纯)、六亚甲基四胺(分析纯)、磷酸二氢钠(分析纯)、新鲜蛋壳若干。为了获得符合生成羟基磷灰石的Ca/P比,在设计实验方案时,反应物的Ca/P化学计量比均约为1.67。除特别说明外,所有在样品制备中使用的化学试剂均为分析级,使用前未做进一步的提纯。实验用水为去离子水。
1.2 实验方法
1.2.1 以CaCO3为钙源合成HA 小心剥离新鲜鸡蛋壳的内外层膜,利用水洗涤数次后在60 ℃下烘干,再用研钵研磨后以200目化学筛收集蛋壳粉,备用。取25 mL 0.1 mol/L NaH2PO4溶液置于有聚四氟乙烯内胆的高压反应釜内,向其中加入1.0 g蛋壳粉,搅拌后密封,在120 ℃条件下反应10 h后,搁置至室温。离心收集,水洗3次后,再用无水乙醇洗涤,60 ℃下烘干,备用,产物用HA-1表示。作为参比,利用商用碳酸钙粉末,在同样条件下制备了相应的产物,用HA-2表示。
1.2.2 以CaCO3为钙源、六亚甲基四胺为添加剂合成HA 在分别含有25 mL 0.1 mol/L NaH2PO4的标记A、B的100 mL烧杯中分别加入蛋壳粉、商用碳酸钙粉末1.0 g,再分别加入3 mmol的固体六亚甲基四胺粉末,磁力搅拌30 min后,转至装有聚四氟乙烯内胆的高压反应釜内,密封。反应条件和收集方法同“1.2.1”。在A和B烧杯得到的固体产物分别记为HA-3和HA-4。
1.2.3 以CaCl2为钙源,不同来源磷合成HA 在标记C和D的100 mL烧杯中分别放入25 mL 0.1 mol/L CaCl2(含3 mmol的固体六亚甲基四胺粉末)。然后向C烧杯中加入1.5 mmol肌酸磷酸二钠固体,向D烧杯中加入1.5 mmol NaH2PO4,分别磁力搅拌30 min后装入有聚四氟乙烯内胆的高压反应釜内,密封。反应条件和收集方法同“1.2.1”。在C和D烧杯得到的产物分别记为HA-5和HA-6。
2 结果与讨论
2.1 鸡蛋壳及商用碳酸钙的表征与分析
通过扫描电子显微镜测试发现,蛋壳上富含孔洞(图1A)。该孔洞具有非常重要的生物学作用,被称为气孔。气孔一般外大内小,是胚胎发育时与外界气体的交换通道;在鲜蛋存放过程中,蛋内水分通过气孔蒸发造成失重;同时微生物也可以通过气孔侵入蛋内,加速蛋的腐败;加工再制蛋时,料液通过气孔浸入[18]。由于蛋壳的主要无机成分是碳酸钙,在生物体内通过生物矿化缓慢形成,与商用碳酸钙相比,该碳酸钙缺乏明显的规则晶体形貌,而商用碳酸钙则呈现的是稳定菱形方解石(图1B)。使用蛋壳作为钙源水热合成碳羟基磷灰石,不仅利用了其含有的钙元素,同时多孔结构也为水热合成提供了有益的硬模板作用。


图2 鸡蛋壳(a)和商用碳酸钙(b)的XRD谱图Fig.2 XRD patterns of eggshell(a) and commercial calcium carbonate(b)
家禽的卵壳结构具有一定的种属特异性,且其结构特征在分类学上具有重要作用。鸡蛋壳粉末的X射线图谱如图2a所示,在(012),(104),(110),(113),(202),(018)和(116)衍射面有较强的衍射峰,说明蛋壳中的碳酸钙属方解石型晶体,与商用碳酸钙的主要衍射峰一致(图2b)。表明卵壳的矿物成分主要为方解石型碳酸钙,晶体层中方解石(110),(113)和(202)衍射面垂直外表面定向排列,这些研究结果对家禽卵壳的综合利用具有重要意义,为进一步研究家禽的微观结构提供了依据[19-20]。
2.2 不同条件下合成的HA的表征及分析



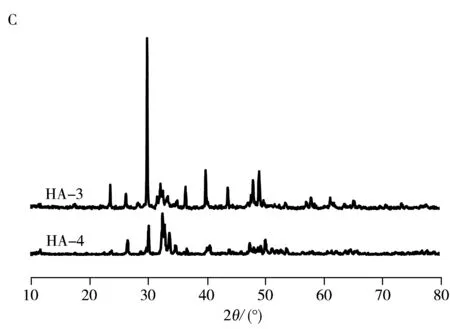
2.2.2 以蛋壳及商用CaCO3为钙源,六亚甲基四胺为添加剂制备HA 为了考察碱性环境对生成物成分和晶型的影响,在上述制备过程中,采用适量的六亚甲基四胺为添加剂参与合成。根据化学性质可知,六亚甲基四胺在120 ℃附近可以完全反应分解释放出NH3。由于反应体系属于高压密封体系,NH3不断生成但不易外漏,NaH2PO4不断电离,继而使得体系溶液的pH值增大,更有利于HA的生成。从图4的 SEM图可以看出,由蛋壳为钙源制备得到的产物花球状和未添加六亚甲基四胺时差异甚微(图4A,HA-3);而由商用碳酸钙为钙源所制备的产物在有六亚甲基四胺时,呈现多薄片层聚集(图4B,HA-4),与图3B相比差异很大。导致此种情形出现,可能与体系的pH值变化缓慢以及六亚甲基四胺参与反应有关。六亚甲基四胺受热缓慢分解与NaH2PO4侵蚀碳酸钙均停留在颗粒的表面,两者既抗衡又制约。蛋壳的多孔不仅被NaH2PO4渗透,同时也被六亚甲基四胺渗入,所以上述抗衡与制约对最终产物形貌的影响不大;但商用碳酸钙微粒内部无法渗透NaH2PO4和六亚甲基四胺,抗衡与制约仅停留在其表面,为HA晶核的生成和长大提供了位点和时间,所以形貌发生了不同的变化。虽然图4C依旧显示HA-3和HA-4产物中含有方解石型碳酸钙,但图4D显示,HA-3和HA-4中HA的特征吸收峰强度变得更大,表明含量增大。
2.2.3 以CaCl2为钙源,不同来源磷制备HA 在水热条件下,因肌酸磷酸二钠盐分解在溶液中缓慢释放出磷酸根,同时由于反应体系含有的六亚甲基四胺不断分解促成体系显碱性,磷酸根和Ca2+作用生成羟基磷灰石。这样肌酸磷酸二钠盐可以用于生物相容性磷酸盐源磷酸钙或HA材料的合成。图5A为以肌酸磷酸二钠盐为有机磷源,在120 ℃水热温度下反应10 h合成的HA扫描电镜图,从图中可以发现此时的颗粒整体上呈多孔珊瑚状,未出现片层,而是有诸多细小颗粒,可能是羟基磷灰石成核颗粒组成。而由CaCl2和NaH2PO4在碱性条件下直接沉淀生成的HA颗粒外形呈放射性花状,而且构成片层大小不均匀(图5B,HA-6)。通过XRD和FT-IR测试发现,HA-5和HA-6中不再出现碳酸钙的特征衍射峰,所制备的HA样品的XRD衍射峰位基本相同,其中2θ在30°和35°之间的有一较强衍射峰,分别对应HA的(211),(112)和(300)晶面,也是HA的主要特征峰(图5C)。而且图5D红外谱图中也未发现其他杂质峰,表明在该条件下制备的HA纯度较高。


上述研究表明:3种方法均可以制得羟基磷灰石粉体,但所制得的产品无论结构,还是纯度均有所差别。在以碳酸钙为钙源水热法制备HA时,对于碳酸钙在何种配料比时能完全转换成HA,后期仍需摸索,但蛋壳的废物利用值得进一步深入研究,同时蛋壳的特殊生物结构为其合理利用提供了便利。本文在以生物含磷分子肌酸钠为磷源水热合成高纯度的HA粉体方面进行了有益的尝试,为未来研究以羟基磷灰石为主体的骨替代品奠定了基础。
3 结 论
本文以蛋壳为生物钙源,磷酸二氢钠溶液为反应溶剂,采用水热合成工艺,可简单便捷地制备合适的HA粉体。研究结果表明,蛋壳不仅充当钙源,多孔结构还可合成HA的硬模板,合成的含碳羟基磷灰石可以用于药物缓释等方面。其中磷酸肌酸钠水热分解后可缓慢释放磷酸根,在合成高纯度生物功能的HA粉体中有着非常重要的应用前景。
[1] Wang L J,Nancollas G H.Chem.Rev.,2008,108:4628-4669.
[2] Fox K,Tran A,Tran N.ChemPhysChem,2012,13:2495-2506.
[3] Liu J,Chen W C,Zhao Z H,Xu H H K.Biomaterials,2013,34:7862-7872.
[4] Zakaria S M,Zein S H S,Othman M R,Yang F,Jansen J A.TissueEng.B,2013,19:431-441.
[5] Wu J,Liu L,Cai Y R,Yao J M.Mini-Rev.Med.Chem.,2013,13:1501-1507.
[6] Victor S P,Sharma C P.J.Biomater.TissueEng.,2012,2:269-279.
[7] Ginebra M P,Canal C,Espanol M,Pastorino D,Montufar E B.Adv.DrugDeliv.Rev.,2012,64:1090-1110.
[8] Sadat-Shojai M,Khorasani M T,Dinpanah-Khoshdargi E,Jamshidi A.ActaBiomater.,2013,9:7591-7621.
[9] Qi C,Zhu Y J,Zhao X Y,Lu B Q,Tang Q L,Zhao J,Chen F.Chem.Eur.J.,2013,19:981-987.
[10] Zhao X Y,Zhu Y J,Qi C,Chen F,Lu B Q,Zhao J,Wu J.Chem.AsianJ.,2013,8(6):1313-1320.
[11] Zhao J,Zhu Y J,Zheng J Q,Chen F,Wu J.MicroporousMesoporousMater.,2013,180:79-85.
[12] Ge D M,Sun F,Wang Z.J.HebeiNormalUniv.:Nat.Sci.Ed.(葛冬梅,孙峰,王震.河北师范大学学报:自然科学版),2013,1:60-64.
[13] Krishna D S R,Siddharthan A,Seshadri S K,Kumar T S S.J.Mater.Sci.:Mater.Med.,2007,18(9):1735-1743.[14] Rivera-Muoz E,Curiel R,Rodríguez R.Mater.Res.Innovations,2003,7(2):85-90.
[15] Tang S,Zeng R Y,Li C L,Liu H S,Wang Y P.J.HengyangNormalUniv.(唐松,曾荣英,李春莉,刘洪水,王尹鹏.衡阳师范学院学报),2010,31(6):169-171.
[16] Dong Y L,Wang Q L.Chin.J.Environ.Eng.(董衍林,王庆良.环境工程学报),2011,5(9):2156-2160.
[17] Chen X,Zhang Y,Zhao Y E.Chin.FoodAddit.(陈雪,张依,赵玉娥.中国食品添加剂),2010,1:191-194.
[18] Arias J L,Fink D J,Xiao S Q,Heuer A H,Caplan A I.Int.Rev.Cytol.,1993,145:217-250.
[19] Hu C X.Chin.J.LightScatter.(胡成西.光散射学报),2006,18(3):282-287.
[20] Fang J Z,Xu C F,Xi J.NingxiaEng.Technol.(房俊卓,徐崇福,郗军.宁夏工程技术),2007,6(4):358-360.
Synthesis and Characterization of Hydroxyapatite with Different Calcium Sources
YAO Cheng-li*,YAN Yan,HE Yan-jiao,LI Hong-ying
(School of Chemistry and Chemical Engineering,Hefei Normal University,Hefei 230601,China)
Synthesis methods of hydroxyapatite with different calcium sources under hydrothermal conditions were compared.From SEM,XRD and FT-IR results,it is concluded that the eggshell could be used as an effective source of Ca2+,and its porous structures could also be selected as a hard template in the formation of flower-like hydroxyapatite.Sodium dihydrogen phosphate was used as the sources ofto corrode the CaCO3to hydroxyapatite.The result indicated that the sodium phosphocreatine would have a wide application prospect in the synthesis of high purity hydroxyapatite by hydrothermal decomposition.
hydroxyapatite;eggshell;sodium phosphocreatine;hydrothermal reaction
10.3969/j.issn.1004-4957.2017.04.018
2016-11-08;
2016-12-05
安徽省高校省级自然科学研究项目(KJ2015A287);安徽省高校优秀青年人才支持计划重点项目(2013SQRL067ZD,gxyqZD2016229);国家级大学生创新创业训练计划项目基金(20151409801);合肥师范学院开放实验项目(2015-2016);安徽省大学生创新创业训练计划项目基金(201614098031)
O657.3;P578.92
A
1004-4957(2017)04-0544-06
*通讯作者:姚成立,博士,高级实验师,研究方向:生物无机化学和材料化学,Tel:0551-63674145,E-mail:yaochengli@hfnu.edu.cn
